Диетическая коррекция метаболических нарушений микрофлоры кишечника при вирусных диареях у детей раннего возраста
СтатьиЛ. Н. Мазанкова, Л. В. Бегиашвили, Н. О. Ильина, О. А. Кондракова, А. М. Затевалов
ГОУ ДПО Российская медицинская академия последипломного образования Росздрава, кафедра детских инфекционных болезней,
НИФ «Ультрасан» ГУ МНИИ эпидемиологии им. Г. Н. Габричевского, Москва В работе представлены результаты клинико-лабораторной оценки влияния лечебно-питательной смеси «Хумана ЛП + СЦТ» на динамику клинических симптомов и состояние метаболической активности микрофлоры кишечника при вирусных диареях у детей раннего возраста. Под наблюдением находилось 18 детей в возрасте от 1 мес. до 1 года, получавших в качестве основного питания детскую смесь «Хумана ЛП + СЦТ». Установлено, что на фоне диетической коррекции при биохимическом исследовании кала по спектрам и уровням летучих жирных кислот имеет место положительный эффект стимуляции функциональной активности нормальной, в первую очередь сахаролитической микрофлоры, а также регулирующее влияние на процессы метаболизма углеводов и жиров. Клинический эффект заключался в быстром и стойком купировании основных проявлений заболевания. Ключевые слова: вирусные диареи, летучие жирные кислоты, дисбактериоз, лечебно-питательная смесь «Хумана ЛП + СЦТ»
Dietary correction of metabolic disorders of intestinal microflora at virus diarrhoea conditions in early-aged children
L. N. Mazankova, L. V. Begiash v i l i, Н. O. Ilyina, O. A. Kondrakova, A. M. Zatevalov
COB VPD Russian Medical Academy of Post-Graduate Education Ministry of Public Health of Russian Federation, Chair of Children Infectious Diseases, Ultrasan Research Corporation of GU (State Institution) of N. I. Gabrichevsky Scientific Research Institute of Epidemiology and Microbiology, Moscow The paper presents clinical laboratory assessment results of influence of therapeutic baby's formula «Humana HN (Therapeutic Diet) + MCT (Medium Chain Triglycerides)» on dynamics of clinical symptoms and gut microflora metabolic activity at virus diarrhoea conditions in early-aged children. There were observed 18 children aged from 1 month until 1 year, receiving as their main food baby's formula «Humana HN + MCT». It was found out that against the background of dietary -correction according to biochemical faeces exam in spectrums and volatile fatty acids levels there was positive effect of stimulating normal functional activity, first of all of saccharolytic microflora, and also controlling influence on carbohydrates and fats metabolism processes. The clinical effect was manifested in fast and persistent relief of major disease symptomatics. Key words: virus diarrhoeas, volatile fatty acids, dysbacteriosis, therapeutic baby's formula «Humana HN + MCT»
С современных позиций, одним из наиболее важных факторов, оказывающих влияние на течение острых кишечных инфекций, особенно у детей раннего возраста, является состояние кишечной микрофлоры. Роль нормальной микрофлоры при инфекционных диареях не ограничивается формированием колонизационной резистентности и антагонистической конкуренцией с патогенами за рецепторы слизистой кишечника, а определяется целым комплексом иммунорегуляторных функций, направленных на активацию системы комплемента, фагоцитоза, синтез лизоцима и интерферонов, выработку различных биологически активных соединений и цитокинов, воздействие на гуморальное звено и стимуляцию антителообразования. За последние годы достигнуты немалые успехи в изучении иммуномодулирующих свойств нормальной микрофлоры [1-4].
Кроме того, большое значение уделяется метаболическим эффектам индигенной флоры, связанным с синтезом летучих жирных кислот (ЛЖК). ЛЖК - это монокарбоновые кислоты с длиной цепи до 8 атомов углерода, поэтому в англоязычной литературе их еще называют «short certain fatty acids» (SCFA) - короткоцепочечными жирными кислотами. К ним относят уксусную (С2), пропионовую (С3), масляную (С4), изо-масляную (iC4), валериановую (С5), изо-валериановую (iC5), капроновую (С6), изо-капроновую (iC6) кислоты. При анаэробном брожении углеводов образуются неразветвленные ЛЖК (уксусная, пропионовая и масляная), тогда как метабо-лизация белков ведет к образованию разветвленных кислот: изо-масляной (из валина), и изо-валериановой (из лейцина) [4, 5]. Основными углеводными субстратами, доступными нормальной микрофлоре, служат пищевые волокна. Источником других углеводов, потенциально способных метаболизироваться микрофлорой, служит слизь.
ЛЖК играют особую роль и выполняют многочисленные функции в организме, направленные как на регуляцию кишечного микробиоценоза, так и на поддержание гомеостаза физико-химических параметров, и, в первую очередь, водно-электролитного баланса, они участвуют в энергообеспечении кишечного эпителия, углеводном и липидном обмене, оказывают регулирующее воздействие на моторику желудочно-кишечного тракта, обладают противовирусным, антибактериальным и иммуномодули-рующим действием [5, 6].
Установлено, что большую часть основных физиологических функций выполняет уксусная (С2), пропионовая (С3) и масляная (С4) кислоты.
Важнейшая роль масляной кислоты (С4) как энергетического субстрата заключается в энергообеспечении кишечного эпителия. Помимо этого, бутират является важным фактором регуляции пролиферации и диффе-ренцировки эпителия толстой кишки, обеспечивая антиканцерогенный эффект микрофлоры. Пропионовая кислота (С3) регулирует микроциркуляцию в слизистой оболочке и поддерживает в ней трофические процессы, участвует в глюконеогенезе и синтезе биогенных аминов, блокируя адгезию патогенов. Уксусная кислота (С2) участвует, главным образом, в липогенезе, регуляции местного иммунитета, а также уровня рН, моторной и секреторной активности кишечника [5, 6].
Однако доказано, что все эффекты нормальных и изо-форм ЛЖК концентрационнозависимы, и их гиперпродукция, также как и недостаток способны играть патофизиологическую роль в организме [5].
Изучению роли ЛЖК при различных физиологических и патофизиологических состояниях посвящены исследования многих отечественных и зарубежных ученых, позволяющих использовать их для диагностики целого ряда заболеваний в качестве биохимических маркеров [2, 3, 5, 6-8].
Установлено, что при острых кишечных инфекциях процесс образования всасывания и утилизации ЛЖК нарушается, поэтому концентрации и, особенно, соотношения отдельных ЛЖК в фекалиях меняются [2, 5].
В ходе изучения функционального состояния кишечной микрофлоры у детей в острый период инфекционных диарей было выявлено, что при всех кишечных инфекциях вне зависимости от этиологии отмечается угнетение и снижение метаболической активности микрофлоры, характеризующееся снижением уровня как отдельных летучих жирных кислот, так и их суммарного общего уровня. Однако более глубокие метаболические нарушения развиваются при бактериальных ОКИ, в то время как при вирусных диареях уровни ЛЖК снижаются незначительно, свидетельствуя тем самым об относительной стабильности функциональной активности кишечной микрофлоры [2].
Принимая во внимание механизмы формирования микроэкологических и метаболических нарушений, развивающихся в острый период инфекционных диарей различной этиологии, патогенетически оправдано наряду с устранением причин, вызвавших эти нарушения (этиотропная терапия), использование в комплексной терапии препаратов, влияющих на количественный, качественный состав микрофлоры и её функциональную активность (комбинированные пробиотики, пробиотики метаболитного типа) [6, 9, 10]. Однако это возможно лишь в том случае, если нормальная микрофлора в полной мере обеспечена необходимыми для её роста и развития нутриентами.
В последние годы увеличился интерес исследователей, нутрициологов и врачей общей практики к продуктам лечебного питания, использующимся в диетической коррекции различных патофизиологических состояний желудочно-кишечного тракта, особенно у детей раннего возраста, у которых в силу незрелости функциональных и барьерных систем не только образование, но и метаболизм продуктов жизнедеятельности микрофлоры несовершенны и во многом зависят от характера питания. Дальнейшее изучение влияния характера питания на функциональное состояние кишечной микрофлоры у детей представляется наиболее перспективным.
Целью исследования явилась оценка клинического эффекта лечебной смеси «Хумана ЛП + СЦТ» в острый период кишечных инфекций у детей раннего возраста и определение её влияния на метаболическую активность микрофлоры толстой кишки.
Материалы и методы исследования
Исследование проводилось на базе 4-го инфекционного отделения Тушинской детской городской больницы (зав. отделением Яковлева Г. Ю.). Под наблюдением находилось 18 детей в возрасте от 1 мес. до 1 года с острыми кишечными инфекциями вирусной этиологии, получавших в качестве основного питания лечебно-питательную смесь «Хумана ЛП + СЦТ». У большинства детей (83,3%) заболевание протекало в среднетяжёлой форме, в 2-х случаях имело место лёгкое течение заболевания, что составило 11,1%, у одного ребёнка (5,6%) тяжёлая форма ОКИ была обусловлена развитием токсикоза с эксикозом II степени. Топика поражения желудочно-кишечного тракта у всех детей была идентичной, с вовлечением в патологический процесс верхних отделов и развитием энтеритов и гастроэнтеритов.
Лечебно-питательная смесь «Хумана ЛП + СЦТ» назначалась всем детям в острый период диареи в объёме от 50 до 180 мл каждые 3-3,5 часа в течение 5 дней. Смесь «Хумана Л П + СЦТ» по своему ингредиентному составу представляет собой оригинальный нетрадиционный продукт лечебного питания, являющийся сбалансированным казеиндоминантным продуктом, обогащенным банановыми пищевыми волокнами, содержащими клетчатку, лигнин, целлюлозу, фруктоолигосахариды и т.д. Жировой компонент на 50% представлен среднецепочечными триглицеридами, углеводный компонент — смесью сиропа глюкозы и мальтодекстрина при низком содержании лактозы. «Хумана ЛП + СЦТ» обеспечивает пищевые потребности ребёнка в острый период диареи, а по химическому составу и показателям безопасности отвечает требованиям, предъявляемым к продуктам данного вида.
Помимо диетической коррекции все дети в острый период заболевания получали идентичную базисную терапию с применением сорбентов и ферментных препаратов в возрастных дозировках на фоне оральной или парентеральной регидратации, а также при необходимости симптоматическую терапию (антипиретики, спазмолитики, противорвотные препараты). Из исследования были исключены дети, получавшие антибактериальную терапию.
Эффективность лечения оценивалась по клиническим критериям: улучшению общего самочувствия, срокам исчезновения симптомов интоксикации, тошноты, рвоты, абдоминального и кишечного синдромов, купирования явлений метеоризма, признаков эксикоза. Лабораторные методы обследования, помимо стандартных общеклинических и бактериологических, включали биохимическое исследование кала по спектрам и уровням летучих жирных кислот методом газо-жидкостной хроматографии (ГЖХ-анализ) в комплексе с микробиологическим исследованием количественного состава кишечной микрофлоры по стандартным методикам. ГЖХ-анализ с последующей компьютерной обработкой хроматограмм проводился на базе НИФ «Ультрасан» ГУ МНИИЭ им. Г. Н. Габричевского.
Результаты и их обсуждение
Положительный клинический эффект использования для диетической коррекции в острый период вирусных диарей у детей раннего возраста лечебной смеси «Хумана ЛП + СЦТ» во всех случаях был обусловлен сокращением частоты стула, улучшением его характера и консистенции, а также быстрым купированием рвоты, что в совокупности способствовало более быстрому уменьшению выраженности эксикоза.
Симптомы интоксикации до начала лечения отмечались у 66,6% детей. Выраженность и продолжительность интоксикации коррелировала с тяжестью заболевания и чаше регистрировалась у детей с тяжёлой и среднетяжёлыми формами болезни. При этом к концу 2-х суток пребывания в стационаре на фоне терапии у всех детей отмечалось значительное улучшение в состоянии: они становились более активными, исчезали вялость и слабость, появлялся аппетит, снижалась температура тела.
Рвота в дебюте заболевания имела место у 10 детей (55,5%), выраженность её колебалась от 1 до 6 раз в сутки. К концу первых суток на фоне проводимого комплекса лечебных мероприятий, включающих диетическую коррекцию смесью «Хумана ЛП + СЦТ», отмечалось значительное сокращение частоты рвоты или полное её купирование.
Абдоминальный синдром различной степени выраженности у всех детей сопровождался явлениями метеоризма, характеризуясь беспокойством, вздутием живота, болезненностью и урчанием при пальпации по ходу кишечника. Продолжительность абдоминального синдрома не превышала 3-х суток.
Наиболее постоянным признаком, встречающимся у 100% детей, был кишечный синдром. Выраженность кишечного синдрома во многих случаях определяла тяжесть заболевания: при среднетяжёлых и тяжёлой формах кишечной инфекции частота стула была наибольшей, достигая 10-12 раз в сутки, а при лёгких формах - не превышала 6 раз. Во всех случаях, независимо от тяжести инфекции, регистрировалась диарея осмотического типа: стул носил водянистый характер, чаще был обильным «пенистым» жёлтого или желтовато-коричневого цвета. У 7 детей (38,9%) в стуле присутствовали непереваренные комочки пищи, а у 11 детей (61,1%) — прозрачная слизь. Продолжительность диареи на фоне использования лечебно-питательной смеси «Хумана ЛП + СЦТ» в комплексе с базисной терапией не превысила 5 суток, чаще колеблясь от 2 до 4 суток, что свидетельствует об эффективности использования данной лечебной схемы.
На фоне выраженных патологических потерь жидкости с испражнениями у 2-х детей (11,1%) отмечалось развитие токсикоза с эксикозом I-II степени, явления которого купировались к концу 2-х суток пребывания в стационаре при адекватном проведении регидратационной терапии на фоне диетической коррекции.
Продолжительность лечения и пребывания в стационаре детей исследуемой группы в основном определялась тяжестью заболевания и сроками купирования основных клинических синдромов, в среднем не превышая 4-5 суток.
По результатам микробиологического исследования кала до начала лечения в половине случаев (у 9 детей) регистрировались количественные нарушения в составе микрофлоры, соответствующие дисбактериозу I-II степени. На фоне использования в качестве лечебного питания смеси «Хумана ЛП + СЦТ» существенной динамики в составе как индигенной, так и условно-патогенной флоры выявлено не было, в то время как в ходе проведения биохимического исследования кала по спектрам и уровням летучих жирных кислот получены данные, свидетельствующие об изменениях метаболит-ного статуса микрофлоры на фоне диетической коррек-ции с использованием лечебной смеси «Хумана ЛП + + СЦТ» (рис. 1, 2). В таблице 1 представлены абсолютные концентрации отдельных ЛЖК в исследуемой группе до и после использования смеси «Хумана ЛП + СЦТ» относительно диапазона норм этих показателей для детей от 1 месяца до 1 года.
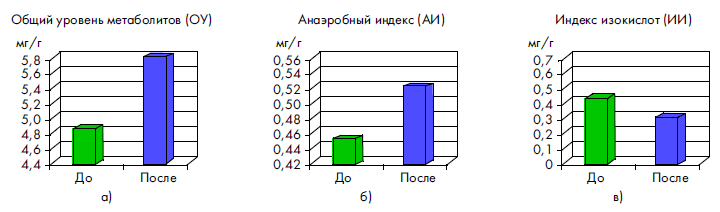
Установлено, что суммарный общий уровень метаболитов (ОУ) до назначения смеси «Хумана ЛП + СЦТ» был относительно снижен (Ме = 5,023 мг/мл [3,053 : 6,197]), что указывает в целом на угнетение метаболической ак-тивности нормальной микрофлоры кишечника в острый период инфекционной диареи и, вместе с тем, на дефицит пищевых субстратов на фоне ускоренного транзита кишечного содержимого. После применения лечебной смеси отмечалось повышение общего уровня ЛЖК (Ме = = 5,982 мг/мл [3,61 8 : 7,1 73]), свидетельствующее о положительном эффекте в плане нормализации функциональной активности кишечной микрофлоры (рис. 2а).
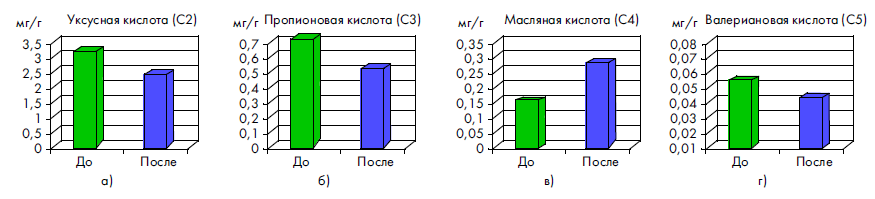
Повышенный уровень уксусной кислоты (С2) (Ме = = 3,368 мг/мл [1,642:4,531]) до лечения свидетельствовал о гиперколонизации аэробной, и, в том числе, условно-патогенной микрофлорой. В динамике на фоне лечебно-диетической коррекции концентрации уксусной кислоты приближались к норме (Ме = 2,569 мг/мл [1,830 : 5,007]), что можно расценить как восстановление структурного баланса аэробных и анаэробных популяций, и, вместе с тем, нормализацию процессов утилизации уксусной кислоты в качестве источника энергии в условиях восстановления нарушенного липидного обмена (табл. 1, рис. 1а).
Повышение содержания пропионовой кислоты (С3) в фекалиях (Ме = 0,780 мг/мл [0,236 : 1,422]) у большинства детей косвенно явилось отражением нарушений углеводного и липидного обмена, характерных для вирусных кишечных инфекций с осмотическим типом диареи. Тенденция к снижению и нормализации показателей пропионовой кислоты (Ме = 0,581 мг/мл [0,244: 1,862]) коррелировала с положительным клиническим эффектом, заключающимся в купировании абдоминального синдрома, явлений метеоризма и улучшения характера стула на фоне адекватной диетотерапии (табл. 1, рис. 1б).
Сниженные показатели масляной кислоты (С5) до лечения (Ме = 0,180 мг/мл [0,114:0,870]), являющейся одним из основных энергосубстратов для эпителиоцитов, свидетельствовали как об угнетении основных продуцентов этого метаболита (фузо-, эубактерии, бактероиды, клостридии, пептококки), так и о дефиците в рационе субстратов для сбраживания. Низкие концентрации бутирата часто коррелируют с гнилостным дисбактериозом. После применения смеси «Хумана ЛП + СЦТ» показатели масляной кислоты повышались, приближаясь к норме (Ме = = 0,319 мг/мл [0,092 : 0,772]), что явилось отражением положительного влияния лечебного питания на функциональную активность микроорганизмов-продуцентов этого метаболита и состояние слизистой оболочки кишечника (табл. 1, рис. 1в).
Отношение суммы ЛЖК (кроме уксусной) к уровню уксусной кислоты отражает анаэробный индекс (АИ). Повышение показателей анаэробного индекса (с Ме = = 0,459 мг/мл [0,187:0,922] до Ме = 0,529 мг/мл [0,288 : 0,972]) на фоне диетической коррекции смесью «Хумана ЛП + СЦТ» можно расценивать как повышение метаболической активности анаэробных популяций нормальной микрофлоры и стабилизации эубиоза (рис. 2б).
После применения лечебной смеси отмечалась нормализация значений индекса изо-кислот (ИИ) (Ме = = 0,324 мг/мл [0,160 : 0,667]), который отображает отношение суммы изо-масляной и изо-валериановой кислоты к сумме нормальных масляной и валериановой кислоты, свидетельствующего о восстановлении структурного и метаболического дисбаланса внутри анаэробных популяций микрофлоры (рис. 2в).
Уровни валериановой, изо-масляной и изо-валериановой кислот в динамике не претерпевали существенных изменений, а различия в их концентрациях были статистически недостоверны.
Рисунок 1. Динамика изменений спектров основных ЛЖК при вирусных диареях у детей на фоне использования лечебной смеси «Хумана ЛП + СЦТ»
Рисунок 2. Динамика изменений показателей суммарного уровня метаболитов, АИ, ИИ при вирусных диареях у детей на фоне использования лечебной смеси «Хумана ЛП + СЦТ»
Таблица 1. Концентрации ЛЖК (мг/мл) при вирусных диареях у детей раннего возраста на фоне использования лечебной смеси «Хумана ЛП + СЦТ» относительно диапазона возрастных норм
| ЛЖК | До, (n = 18) | После, (n = 18) | Диапазон норм для детей 1 мес. - 1 г. | ||||
|---|---|---|---|---|---|---|---|
| Me | – | + | Me | – | + | ||
| Уксусная (С2) | 3,368 | 1,642 | 4,531 | 2,569 | 1,830 | 5,007 | 3,023—3,550 |
| Пропионовая (С3) | 0,780 | 0,236 | 1,422 | 0,581 | 0,244 | 1,862 | 0,564—0,654 |
| Изо-масляная (iC4) | 0,041 | 0,023 | 0,136 | 0,044 | 0,036 | 0,064 | 0,027—0,046 |
| Масляная (С4) | 0,180 | 0,114 | 0,870 | 0,319 | 0,092 | 0,772 | 0,228—0,419 |
| Изо-валериановая (iC5) | 0,071 | 0,028 | 0,233 | 0,062 | 0,036 | 0,117 | 0,045—0,095 |
| Валериановая (С5) | 0,059 | 0,017 | 0,091 | 0,047 | 0,027 | 0,086 | 0,028 — 0,050 |
| Изо-капроновая (iC6) | 0 | — | — | 0 | — | — | 0 |
| Капроновая (С6) | 0 | — | — | 0 | — | — | 0 |
Таким образом, полученные результаты клинико-лабораторной оценки влияния лечебно-питательной смеси «Хумана ЛП + СЦТ» на клиническую картину и состояние микробиоценоза кишечника, позволили установить положительный эффект стимуляции функциональной активности нормальной, и, в первую очередь, сахаролитической микрофлоры (по стабилизации показателей уксусной, масляной и пропионовой кислот), а также регулирующее влияние на процессы метаболизма углеводов и жиров при вирусных диареях у детей раннего возраста. Клинический эффект заключался в быстром и стойком купировании основных проявлений болезни: рвоты, диареи, абдоминального синдрома и эксикоза, что наряду с хорошей переносимостью позволяет рекомендовать смесь «Хумана ЛП + СЦТ» для использования в качестве лечебного питания у детей раннего возраста в острый период кишечных инфекций вирусной этиологии.
Литература