Перфорации венозной стенки как ведущая причина болевого синдрома после эндовенозной лазерной облитерации
СтатьиОпубликовано в журнале:
Ангиология и сосудистая хирургия. Том 17 №3/2011
Мазайшвили К.В., Стойко Ю.М., Хлевтова Т.В., Кутидзе И.А., Моренко Д.Н.
ФГУ«Национальный медико-хирургический центр им. Н.И.Пирогова», Москва, Россия.
В данной статье освещена проблема возникновения перфораций венозной стенки в процессе эндовенозной лазерной облитерации (ЭВЛО). Показан синусоидальный характер болевого синдрома, обусловленный развитием перифлебита на 4-7 сутки после ЭВЛО. Выполнен ряд экспериментов на венах с использованием двух различных источников излучения. Показано, что про проведении тумесцентной анестезии вена обжимается вокруг световода, что приводит к образованию изолированных внутрипросветных лакун. При воздействии лазерного излучения на кровь, замкнутую в такой лакуне, происходит её выпаривание с выделением большого объема газа, что в свою очередь ведет к разрыву венозной стенки. Имевшееся ранее представление о перфорации венозной стенки раскаленным торцом световода подтверждения не получило.
Ключевые слова: эндовенозная лазерная облитерация, перфорации стенки вены, болевой синдром.
ВВЕДЕНИЕ
С момента появления в арсенале хирургии эндовенозной лазерной облитерации (ЭВЛО) прошло десять лет, в течение которых данный метод получил широкое распространение. Отсутствие необходимости госпитализации больного в стационар, отказ от выполнения разрезов и незначительное ограничение трудоспособности после вмешательства сделали ЭВЛО одним из самых популярных способов устранения стволового рефлюкса во многих странах.
Одним из основных осложнений ЭВЛО является образование перфораций венозной стенки в ходе процедуры, что приводит к возникновению явлений перифлебита и появлению болевого синдрома в послеоперационном периоде. Как правило, болевые ощущения уменьшаются на 2 сутки, затем вновь усиливаются к 4-5 суткам после вмешательства. Такой «синусоидальный» характер кривой интенсивности боли обусловлен развитием в эти сроки посткоагуляционных флебитических и перифлеби-тических явлений. Интенсивность воспалительного процесса связана с количеством перфораций стенки вены и объёмом термического повреждения параве-нозных структур во время ЭВЛО. Болевой синдром является практически единственным негативным фактором, ухудшающим качество жизни больного в раннем послеоперационном периоде. Снижение интенсивности болевого синдрома в послеоперационном периоде может быть достигнуто путем усовершенствования самой процедуры ЭВЛО, либо с помощью назначения противовоспалительной медикаментозной терапии. С целью купирования развивающегося воспаления перивенозных тканей. При этом должно быть решены задачи подавления чрезмерной лейкоцитарной агрессии, восстановление микроциркуляции и лимфатического дренажа в паравазальной зоне. С этой целью с давно и успешно применяются препараты на основе диосмина (флебодиа, детралекс, вазокет, венарус). «Флебодиа 600» блокирует выработку свободных радикалов, простагландинов и тромбоксана, улучшает микроциркуляцию, повышает резистентность капилляров и снижает их проницаемость, улучшает диффузию кислорода в ткани.
На перфорацию стенки вены во время ЭВЛО обращали внимание многие исследователи. Weiss R.A. [6], проводя сравнительные гистологические исследования последствий воздействия лазерного излучения с длиной волны 810 нм и РЧО на венах экспериментальных животных, выявил образование перфораций после ЭВЛО в 100% случаев. Kaspar S. [4] на сегментах БПВ изучали результаты ЭВЛО в зависимости от мощности излучения (8, 10, 12, 15 Вт) и скорости тракции световода (от 0,2 мм/с до 2мм/сек). Минимальное количество перфораций наблюдалось при использовании низкой или средней мощности (8 и 12 Вт), с увеличением этого показателя до 15 Вт количество перфораций увеличивалось.
Один из основоположников метода ЭВЛО Proeb-stle T.M. [5] главной причиной образования перфораций считал соприкосновение оптического волокна и венозной стенки при подаче лазерного импульса. При этом автор полагал, что максимальная температура во время ЭВЛО создаётся внутри пузырьков пара, и её значение должно составлять около 1000С. Однако Weiss R.A. и соавт. [6], в модели in vivo показали, что в просвете вены при ЭВЛО создаётся температура в 7290С, пиковые же значения температуры достигают 13340С. Disselhoff B. и соавт. [3], в экспериментальном исследовании (диодный лазер — 810 нм) отмечали создание на торце световода температуры до 1200оС.
На сегодняшний день уже устоялось мнение, что возникновение перфораций во время ЭВЛО обусловлено карбонизацией торца световода, который разогреваясь до высоких температур, «прожигает» стенку вены [1]. Между тем, гистологические исследования показывают, что перфорационные отверстия в стенке вены часто бывают значительных размеров, и никак не могут являться следствием прямого контакта со световодом, диаметр которого несоизмеримо мал по сравнению с диаметром перфорационного отверстия. Как показали исследования Amzayyb M. и соавт. [2], разогрев торца световода при проведении ЭВЛО действительно происходит за счет образованием тонкого слоя нагара. Нагар интенсивно поглощает энергию излучения, благодаря чему разогревается до экстремально высоких температур. Однако при этом образование нагара и степень разогрева совершенно не зависят от того, какая длина волны используется (810 нм, 940 нм, 1470 нм). Если карбонизация и разогрев торца световода до сверхвысоких температур происходит одинаково при воздействии лазера 810 нм и 1470 нм, то почему существует значимая разница, как по количеству перфораций, так и по выраженности болевого синдрома, между ЭВЛО «гемоглобинпоглощаемыми» и «водопоглощаемыми» длинами волн? Логично предположить, что разогретый до температуры свыше 1000оС торец световода должен одинаково «прожигать» стенку вены в обоих случаях, вызывая одинаковое число перфораций вены и схожую клиническую картину. Противоречивые данные о причинах образования перфораций венозной стенки, а также условий их возникновения требуют детального изучения.
МАТЕРИАЛЫ И МЕТОДЫ
Для определения характера и динамики болевого синдрома в послеоперационном периоде была изучена его интенсивность у 20 больных (группа 1) с варикозной болезнью вен нижних конечностей (ВБВНК). Из них с клиническим классом С2 по классификации СЕАР было 12 человек, с классом С3 — 8 человек. Всем больным выполнялась ЭВЛО большой подкожной вены (БПВ) от сафено-фемо-рального соустья (СФС) до верхней трети голени диодным лазером с длиной волны 1030 нм. Операцию выполняли амбулаторно под тумесцентной анестезией 0,1% раствором лидокаина. Средняя длина обли-терированного сегмента БПВ составила 42,1±3,4 см. Линейная плотность потока энергии лазерного излучения составила в среднем 148±36 Дж/см вены. Максимальный диаметр БПВ у СФС составлял 10 мм. Болевой синдром оценивали при помощи визуально-аналоговой шкалы (ВАШ). При этом больного просили оценить интенсивность боли по шкале от 0 (нет боли) до 10 (нестерпимая боль). Исследование проводили в день операции (просили оценить максимальную боль во время операции) и далее ежедневно в течение 10 дней. В качестве контрольной группы оценивали болевой синдром у схожей группы из 9 больных (группа 2), которым в послеоперационном периоде был назначен Флебодиа 600 (1 таблетка в сутки) в комбинации с ибупрофеном (200 мг трижды в сутки). Показатели болевого синдрома также сравнивали с группой из 18 больных, которым выполнялась комбинированная флебэктомия под спинномозговой анестезией (группа 3).
Для подробного изучения условий возникновения перфораций вены была проведена серия опытов на удалённых отрезках вен. Для этого вену, удалённую при операции, разрезали на отдельные участки длиной 2 см. Участки вены рассекались продольно и укладывались интимой наружу.
В первой серии опытов производили прямое воздействие лазерного излучения на стенку вены, смоченную физиологическим раствором. При этом угол падения луча по отношению к интиме составлял от 45 до 90 градусов. Поток энергии излучения составил 60 Дж на точку для лазера с длиной волны 1030 нм и столько же для лазера с длиной волны 1470 нм.
Во второй серии опытов производили прямое воздействие лазерного излучения на стенку вены, с нанесенной на интиму кровью. Поток энергии составил 60 Дж на точку для лазера с длиной волны 1030 нм и столько же для лазера 1470 нм.
В третьей серии опытов, производили прямое воздействие лазерного излучения на стенку вены, при этом кровь наносили на подложку, на которой лежала вена. Поток энергии составил 60 Дж на точку для лазера длиной воны 1030 нм и столько же для лазера 1470 нм.
В качестве контроля изучалось повреждение интимы вены раскалённой в пламени стальной иглой. Для этого, игла раскалялась до красного каления (температура составляла примерно 1000оС) и прижималась к интиме. Время контакта составляло от 1 до 6 секунд.
Все участки вен, участвующие в приведенных опытах изучались макроскопически и затем из них готовились гистологические препараты.
При создании вокруг вены давления за счет введения раствора анестетика, опорно-механический каркас венозной стенки, приспособленный к изменениям просвета, сокращается, а интима, не имея сократительных элементов должна образовывать складки, увеличивающие толщину венозной стенки. Логично предположить, что вены с большим диаметром при тумесценции уменьшаются в сечении, но при этом площадь поверхности внутренней оболочки вены должна оставаться неизменной за счет образования складок.
Для проверки этой гипотезы в эксперименте на нефиксированных трупах было произведено моделирование тумесцентной анестезии. Под ультразвуковым контролем проводилось введение раствора желатина по ходу БПВ в её фасциальный футляр на бедре. Таким образом, достигалась полная имитация тумесцентной анестезии. После застывания раствора желатина БПВ иссекали единым блоком с окружающими тканями и кожей. На поперечных срезах полученного препарата исследовали характер расположения интимы венозной стенки. У части трупов после создания имитации тумесцентной анестезии проводили ЭВЛО с разными параметрами излучения с целью изучения условий образования перфораций.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Проведенное исследование показало, что после ЭВЛО характер болевого синдрома имеет специфическую динамику. Прежде всего, отмечается снижение болей в первые дни после вмешательства и отчётливое усиление болевого синдрома на 4-7 сутки. У всех пациентов боли локализовались вдоль коагулированной БПВ, больше — в нижней трети бедра. Учитывая, что именно эти сроки являются классическими для послеоперационных воспалительных осложнений, усиление болей, по нашему мнению, обусловлено развитием посткоагуляционных флебитических и перифлебитических явлений. Динамика интенсивности болевого синдрома в послеоперационном периоде представлена на рисунке1.
Рис. 1. Динамика интенсивности болевого синдрома в послеоперационном периоде.
В первые сутки больные первой и второй групп указывали максимальную боль, возникшую непосредственно во время операции (выполнения анестезии).
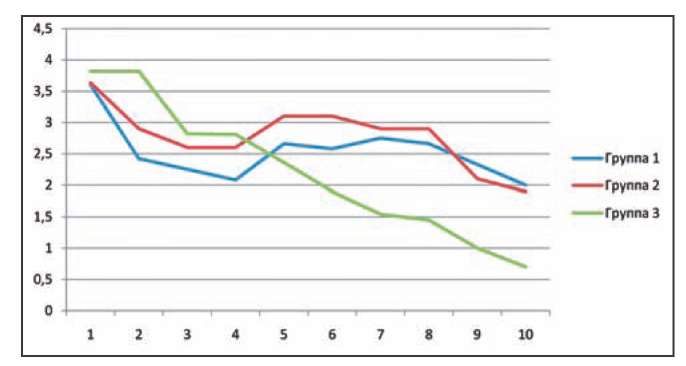
Более выраженный болевой синдром отмечался у больных первой группы. При этом максимальное значение болевого синдрома отмечалось на 5-6 сутки после ЭВЛО и было, в среднем, 3,1±0,5 баллов по ВАШ. Во второй группе пациентов, принимавших флеботропный препарат Флебодиа 600 в комбинации с ибупрофеном, динамика интенсивности болей имела схожий характер, однако абсолютные показатели болевых ощущений пациентов были ниже. У больных после комбинированной флебэктомии, выполненной под спинномозговой анестезией, динамика интенсивности болей была несколько иного характера. Как видно из графика, максимальная боль отмечалась в 1-2 сутки после вмешательства, а далее её интенсивность снижалась практически линейно. Через неделю после операции больные отмечали боль в среднем на 1,6±0,2 балла по ВАШ, в то время как после ЭВЛО этот показатель составлял, в среднем, 2,7±0,3. Таким образом, болевой синдром после ЭВЛО, характерный для «гемоглобинпоглощающих» длин волн лазера, остаётся серьезной проблемой, требующей своего решения.
В первой серии опытов на изолированных отрезках вен прямое воздействие лазера на лишенную крови вену было значительно более выражено для лазера с длиной волны 1470 нм. Перфораций венозной стенки ни в одном случае выявлено не было (Рис. 2).
Рис. 2. а - Воздействие излучения лазера с длиной волны 1030 нм на интиму вены, смоченную физиологическим раствором.
Локальная коагуляция в месте прямого воздействия лазерного излучения, без повреждения венозной стенки на протяжении. б - Воздействие излучения лазера с длиной волны 1470 нм на интиму вены, смоченную физиологическим раствором. Локальная коагуляция в месте прямого воздействия лазерного излучения и сморщивание отрезка вены на большом протяжении.
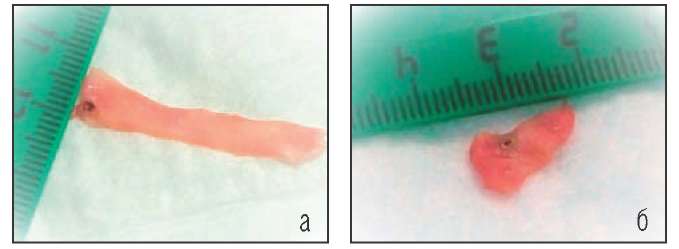
Излучение лазера с длиной волны 1030 нм вызывало локальную коагуляцию, сопоставимую с площадью сечения световода. Ткани вокруг оставались интактными. При воздействии излучения с длиной волны 1470 нм тепловое воздействие распространялось к периферии от участка коагуляции и вызывало контракцию коллагена венозной стенки, что выразилось в сморщивании исследуемого участка вены.
Во второй серии опытов, когда производили воздействие лазера на вену с нанесенной на интиму кровью, термическое действие было выражено примерно одинаково для обоих типов лазеров. При воздействии лазера с длиной волны 1030 нм, в 20% случаев возникали перфорации, тогда как при применении лазера с длиной волны 1470 нм перфораций венозной стенки ни в одном случае отмечено не было (Рис. 3).
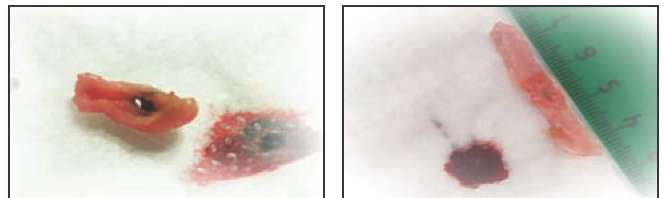
В третьей серии опытов мы попытались создать модель паравазальной гематомы, часто возникающей при тумесцентной анестезии. Воздействие лазера осуществляли на вену, уложенную на подложку с нанесенной каплей крови. Воздействие лазерного излучения с длиной волны 1030 нм в таких условиях приводило к мгновенному разогреву крови за стенкой вены. При этом в 100% случаев возникали перфорации стенки вены, с диаметром отверстия не менее 1 мм (Рис. 4-а), отрезок вены разогревался, что приводило к значительному его сокращению. Для лазера с длиной волны 1470 нм перфораций венозной стенки ни в одном случае выявлено не было и разогрева крови с газообразованием не наблюдалось.
Рис. 3. а - Воздействие излучения лазера длиной волны 1030 нм на интиму вены, смоченную кровью.
Получена локальная коагуляция большего диаметра, отмечено сморщивание венозной стенки на небольшом удалении от места приложения энергии. б - Воздействие излучения лазера длиной волны 1470 нм на интиму вены, смоченную кровью. Принципиального отличия от первого опыта не получено, результат аналогичен.
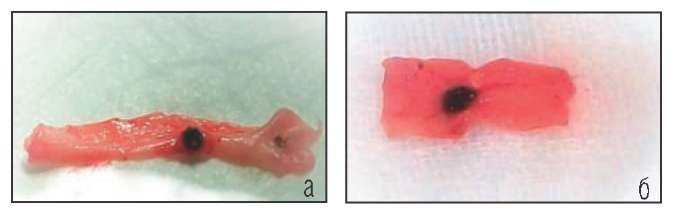
Рисунок 4. а - Воздействие излучения лазера с длиной волны 1030 нм на интиму вены с образованием перфорации.
Кровь находилась за стенкой вены (модель паравазальной гематомы). б - Воздействие излучения лазера с длиной волны 1470 нм на интиму вены.
Из результатов описанной серии опытов можно сделать важный вывод: для лазерного излучения длиной волны 1030 нм стенка вены практически прозрачна. Максимальное число и размер перфораций, возникает при попадании крови за пределы вены. У больных такая ситуация может возникать при создании тумесцентной анестезии, когда иглой случайно прокалывается стенка вены и кровь попадает в паравазальное пространство.
Как показали эксперименты на трупах, при проведении тумесцентной анестезии, внутренняя оболочка вены действительно образует складки, причем эти складки настолько выражены, что смыкаясь, образуют замкнутые лакуны, содержащие кровь. При гистологическом исследовании обнаружено, что просвет такой вены имеет вид щели сложной конфигурации, а интима образует большое число складок, которые контактируя друг с другом, создают замкнутые лакуны, просвет которых может не сообщаться с главным просветом вены (Рис. 5). Когда вена обжимается вокруг световода раствором анестетика, её интима, при этом, контактирует со световодом на очень незначительной площади (Рис. 6).
Увеличение в 160 раз. Окраска гематоксилин-эозин.
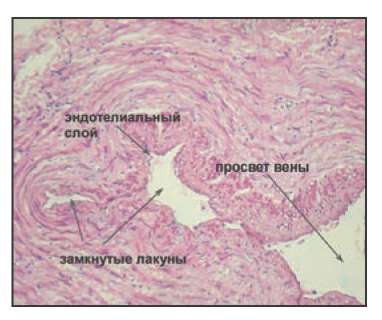
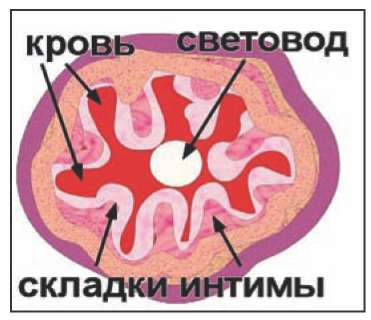
Рис. 6. Схематичное изображение вены, «обжатой» раствором анестетика вокруг световода.
Видны складки и лакуны, заполненные кровью.
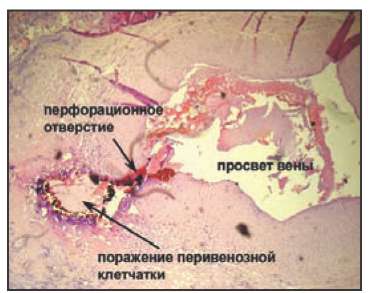
Интима практически прозрачна для лазера с «гемоглобинпоглощаемой» длиной волны. Поэтому разогрев гемоглобина происходит в этих лакунах независимо от его разогрева в просвете вены. При этом мгновенное выделение газа с внезапным повышением давления в замкнутой лакуне, ограниченной со всех сторон складками, является своего рода «микровзрывом» и, служит, по нашему мнению, основной причиной возникновения перфораций венозной стенки. Эта гипотеза объясняет, каким образом может произойти повреждение структур, расположенных вблизи вены. Кровь, содержащаяся в паравазальной клетчатке, поглощает энергию лазерного излучения, при этом образовавшийся из «сгоревшей» крови горячий газ, мгновенно расширяется, разрывает ткань и вызывая её повреждение. Подтверждение данной гипотезе мы нашли, изучая гистологические срезы, полученные в описанном эксперименте. На рисунке 7 представлена вена, имеющая небольшое перфорационное отверстие своей стенке и обширное повреждение паравазальной клетчатки.
Рис. 7. Вена с узким перфорационным отверстием в стенке и обширным повреждением окружающей ткани.
Окраска гематоксилин-эозин.
Контрольный эксперимент, во время которого интиму вены «прижигали» раскалённой иглой, показал, что получить таким способом перфорационное отверстие стенки сосуда практически невозможно. При коротком контакте (1-2 секунды) возникала точечная коагуляция в месте прикосновения раскалённой иглы. Если контакт был более длительным (3-6 секунд), то происходило сморщивание вены без образования перфорационного отверстия. Гистологически в этой ситуации выявлялась только поверхностная коагуляция интимы, в большинстве случаев с обугливанием.
ВЫВОДЫ
1. ЭВЛО имеет характерную динамику болевого синдрома в послеоперационном периоде. Она характеризуется усилением болей на 5-8 сутки после вмешательства. Для купирования болевого синдрома и воспалительных проявлений после ЭВЛО целесообразно с первого дня назначать нестероидные противовоспалительные препараты, а также флебопротекторы, в частности, высокоочищенный диосмин (Флебодиа 600).
2. Попадание крови в паравенозное пространство при проведении анестезии приводит появлению перфораций стенки вены во время ЭВЛО за счет мгновенного разогрева крови в этом пространстве. Выделение при этом продуктов сгорания в виде газа, приводит к резкому повышению давления и повреждению окружающих тканей (эффект микровзрыва).
3. При создании тумесцентной анестезии вена «обжимается» вокруг световода, при этом её внутренняя оболочка образует многочисленные складки. Это приводит к появлению в складках замкнутых лакун, заполненных кровью и не сообщающихся с главным просветом вены. Резкое повышение давления в такой лакуне за счет поглощения кровью излучения лазера с последующим сгоранием и газообразованием - ещё одна причина образования сквозных повреждений стенки вены.
4. Гипотеза образования перфорационных отверстий в венозной стенке за счет контакта с разогретым свыше 1000оС торцом световода не получила экспериментального подтверждения.
5. В эксперименте лазерное излучение длиной волны 1470 нм не вызывает сквозных перфораций стенки вены. Это указывает на перспективность лазерных аппаратов «водопоглощаемыми» с длинами волн.
ЛИТЕРАТУРА/REFERENCES
1. Соколов А.Л., Лядов К.В., Луценко М.М., Лавренко С.В., Любимова А.А., Вербицкая Г.О., Минаев В.П. применение лазерного излучения 1,56 мкм для эндовазальной лазерной облитерации вен в лечении варикозной болезни. Ангиология и сосудистая хирургия. 2009; 15: 1: 69-75.
2. Amzayyb M., van der Bos R.RR., Kodach V.M. et al. Carbonized blood deposited on fibres during 810, 940 and 1470 nm endovenous laser ablation: thickness and absorption by optical coherence tomography. Lasers Med. Sci. 2010; 25: 439-447.
3. Disselhoff B.C., Rem A.I., Verdaasdonk., Kinderen D.J., Moll F.L. Endovenous laser ablation: an experimental study on the mechanism of action. Phlebology. 2008; 23: 69-76.
4. Kaspar S, Siller J, Cervinkova Z, Danek T. Standardisation of Parameters during Endovenous Laser Therapy of Truncal Varicose Veins - Experimental Ex-vivo Study. Eur. J .Vasc Endovasc Surg. 2007; Aug: 4: 2: 224-228.
5. Proebstle T.M., Lehr H.A., KarglA., Espinola-Klein C., Rot-her W., Bethge S., Knop J. Endovenous treatment of the greater saphenous vein with a 940-nm diode laser: throm-botic occlusion after endoluminal thermal damage by laser-generated steam bubbles. J Vasc Surg. 2002.-№ 35-V.4-R729-36.
6. Weiss R.A.Comparison of endovenous radiofrequency versus 810 nm diode laser occlusion of large veins in an animal model. Dermatol Surg 2002 Jan.-№28-V.1-R56-61


