Остеоартроз как фактор риска кардиоваскулярных катастроф
Статьи Опубликовано в журнале:«РУССКИЙ МЕДИЦИНСКИЙ ЖУРНАЛ»; Неврология; ТОМ 15; № 23; 2007; стр. 1-5.
к.м.н. О.И. Мендель, к.м.н. А.В. Наумов1, д.м.н. Л.И. Алексеева2, профессор А.Л. Вёрткин1, к.м.н. М.М. Шамуилова1
2НИИ ревматологии РАМН, Москва
В структуре смертности населения РФ ведущее место занимают болезни системы органов кровообращения - 57% (рис. 1). Сердечно-сосудистые заболевания (ССЗ), в основе которых лежит атеросклероз, справедливо называют эпидемией ХХ-ХХI в. Ежегодно от ССЗ в России погибает более 1 200 000 человек, в том числе и лица трудоспособного возраста. Болезни сердечно-сосудистой системы составляют более 50% всех случаев инвалидизации. В то же время одной из лидирующих причин функциональной недостаточности и потери трудоспособности у взрослых является остеоартроз (ОА) -самое известное и частое в мире заболевание суставов с возраст-ассоциированной распространенностью. Например, в США более чем у половины людей в возрасте старше 65 лет и практически у каждого старше 75 лет диагностируется ОА. Ряд исследователей считает, что к 2020 г ОА будет страдать 71% населения в возрасте старше 65 лет [Oliveria S.A. et al., 1995]. В РФ также возрастает заболеваемость ОА. Об этом свидетельствуют данные статистики обращаемости в лечебно-профилактические учреждения (ЛПУ) по поводу клинических проявлений ОА. Так, в 1999 г в ЛПУ обратились 1 400 000 больных ОА, а в 2007 г - вдвое больше, 3 131 000 человек [В.А. Насонова, 2009].
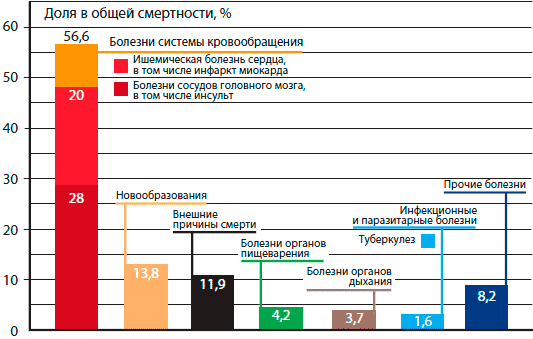
Рис. 1. Причины смертности населения России, 2007 г.
В медицинских публикациях последних лет все чаще появляются данные о том, что люди, страдающие ОА, имеют более высокий риск развития ССЗ и более высокий уровень общей смертности по сравнению с популяцией. Повышенная специфическая смертность при ОА главным образом регистрировалась в исследованиях, включающих кардиоваскулярные и желудочно-кишечные заболевания. Первое исследование по изучению причин смертности у пациентов с ОА в США опубликовано Monson и Hall в 1976 г, где были проанализированы уровень и причины смерти у 617 пациентов с ОА в сравнении с белой популяцией аналогичного возраста и пола. Авторами установлено, что смертность пациентов с ОА в 40% случаев была обусловлена атеросклерозом сосудов сердца (стандартизированный уровень смертности составил 156) и заболеваниями желудочно-кишечного тракта (ЖКТ) (6% случаев смертности). При этом стандартизированный уровень смертности от заболеваний ЖКТ у пациентов с ОА был в два раза выше, чем в популяции и составил - 239. Lawrence et al., 1990 г., изучив смертность среди 2384 лиц в возрасте от 55 до 74 лет с рентгенологическими признаками ОА коленных суставов в сопоставлении с аналогичной группой лиц без рентгенологических изменений, установили, что уровень смертности у них был выше - 38,9% у мужчин и 30% у женщин - чем у лиц без рентгенологических признаков ОА - 31,6 и 17,7% соответственно. Haara et al., 2003, нашли, что ОА суставов кистей ассоциирован с повышенной смертностью от ССЗ у мужчин. Дальнейшие исследования в этой области позволили определить факторы риска смертности у пациентов с ОА: тяжесть заболевания, пожилой возраст и наличие коморбидных заболеваний [M.C. Hochberg, 2008]. Более высокий уровень смертности у людей с ОА объясняют уменьшением физической активности пациентов на фоне поражения суставов нижних конечностей и наличием коморбидных заболеваний, в том числе, обусловленных отрицательным действием лекарственных препаратов, направленных на симптоматическое лечение ОА.
Под коморбидностью (полиморбидностью, мульти-морбидностью) принято подразумевать наличие двух и/или более синдромов или заболеваний у одного и того же пациента, патогенетически взаимосвязанных между собой или совпадающих по времени. Установлено, что ОА относится к болезням с высокой коморбидностью [Schellevis et al., 1993; Kadam U.T. et al., 2004; Caporali R.t al., 2005]. Как правило, у больного с ОА в возрасте старше 50 лет одновременно сосуществует более 5 болезней и практически не встречаются лица с первичным ОА, не имеющие сопутствующих соматических заболеваний [Kadam et al., 2004]. Коморбидность -достаточно частое состояние в общей популяции (30%), однако изучение этой проблемы показало, что ревматические болезни в структуре коморбидности - не простое дополнение к другим заболеваниям. E. Loza et al., 2009, проведя анализ данных 2192 рандомизированно выбранных пациентов (всего изучено 972 545 человек населения Испании) с использованием короткой формы обзора здоровья (SF-12) и опросника качества жизни (HRQoL), установили, что у пациентов с коморбидностью, включающей ревматические болезни, отмечаются худшие показатели качества жизни и дневной функции, чем у пациентов без ревматических заболеваний. По имеющимся данным, ОА наиболее часто сочетается с артериальной гипертензией (АГ) и другими ССЗ (атеросклерозом, ИБС), ожирением, сахарным диабетом (ОД), хроническими обструктивными заболеваниями легких, заболеваниями ЖКТ. ССЗ наблюдаются у более, чем у 50% пациентов с ОА. Анализ публикаций в Medline с 1966 по 2004 г показал, что сочетание ОА с АГ встречается у 48-65% пациентов с ОА в популяции и у более 65% пациентов с ОА в возрасте старше 80 лет, нуждающихся в артропластике коленных суставов [Loy и соавт., 2005].
Общие факторы риска ОА и ССЗ
Общие факторы риска для первичного ОА и ССЗ: возраст, избыточный вес, наследственность, метаболические нарушения (повышенный уровень холестерина, толерантность к глюкозе, сахарный диабет).
Возраст - основное условие для развития первичного ОА и ССЗ, которые рассматриваются как возраст- ассоциированные заболевания. С возрастом в различных тканях человека происходит накопление гликолизированных продуктов коллагена, играющих немалую роль в патогенезе как атеросклероза, так и ОА [Gibson G.J. et al., Saudek D.M et al., 2003]. Внеклеточное накопление AGE-продуктов изменяет структуру и функциональные свойства как матрикса, так и матрикс-клеточных взаимодействий. Артериальные сосуды в первую очередь подвергаются воздействию AGE-продуктов, которые ковалентно взаимодействуют с коллагеном I типа, а он в свою очередь, взаимодействует с растворимыми белками плазмы (липопротеинами низкой плотности - ЛПНП, -иммуноглобулином G и др.). Образование AGE-продуктов на белках базальной мембраны сосудистой стенки (коллаген IV типа, ламинин, гепарансульфат протеогликан и др.) приводит к утолщению базальной мембраны, сужению просвета капилляров и нарушению их функции (снижение адгезии эндотелиальных клеток, снижение пролиферации ретинальных перицитов, повышение пролиферации ретинальных эндотелиальных клеток и др.). Эти нарушения внеклеточного матрикса изменяют структуру и функцию сосудов: снижение эластичности сосудистой стенки, изменение ответа на сосудорасширяющее действие NO и др. и способствуют ускоренному развитию атеросклеротического процесса. AGE-продукты также специфически накапливаются и в хрящевой ткани человека. Они атакуют долгоживущие белки, преимущественно коллаген, связываются с ними и повреждают их, нарушая функциональные свойства. Более того, они являются триггерами воспаления - могут активировать клетки, стимулируя образование провоспалительных цитокинов и активных форм кислорода. AGE-продукты оказывают отрицательное воздействие на метаболизм хряща и его механические свойства, ставя под угрозу целостность матрикса. Предполагают, что AGE-продукты влияют на метаболическую активность хондроцитов и что сигнальные молекулы RAGE (рецепторы гликозилированных продуктов) хондроцита могут играть роль в патогенезе ОА. В норме суставные хондроциты экспрессируют функциональные RAGE. AGE-продукты вызывают быстрое увеличение RAGE на хондроцитах (экспериментально установлено, что в остеоартритическом хряще уровень RAGE намного выше, чем в контроле), которые усиливают свою метаболическую деятельность, приводя к деградации хряща. Лиганды RAGE стимулируют продукцию хондроцитами медиаторов воспаления и MMP-13.
Ожирение - первичный фактор риска как для ОА, так и для ССЗ. К заболеваниям, ассоциированным с ожирением, относят сахарный диабет 2-го типа, дислипидемии, АГ, коронарную болезнь сердца, сердечную недостаточность, цереброваскулярные заболевания (повышенный риск инсультов), остеоартроз, респираторные заболевания (синдром апноэ во сне, астма), холелитиаз и неалкогольный цирроз печени [Malnick et Knobler, 2006]. Установлено, что у людей с индексом массы тела (ИМТ) свыше 30 кг/м2 риск развития ОА коленных суставов в 4 раза выше, чем у лиц с ИМТ 25 кг/м2. Ожирение при варусном положении коленного сустава способствует перенесению оси тяжести тела и выраженному поражению медиальных тибио-феморальных сочленений [Sharma et al., 2000]. Исследование Hart et al., 1992, включившее 1000 женщин, выявило, что относительный риск развития одностороннего и двустороннего ОА коленных суставов, по данным рентгенологического исследования, был 6,2 для ИМТ<23,4 кг/м2 и 18 для ИМТ >26,4 кг/м2. Когда ИМТ <23,4 kg/м2 сравнили с ИМТ - 23,4-26,4 кг/м2, относительный риск ОА был выше в 2,9 раза для коленного сустава, в 1,7 раза для карпометакарпальных суставов и в 1,2 раза для проксимальных межфаланговых суставов. Двойное контролируемое исследование показало, что увеличение веса тела на каждый килограмм увеличивает риск рентгенологических признаков ОА коленных и карпометокарпальных суставов [Cicuttini F.M. et al., 1996]. Установлено, что не только повышенный вес ассоциирован с увеличением риска развития ОА, но и снижение веса ассоциировано со снижением риска ОА. В исследовании, включившем 800 женщин, было продемонстрировано, что уменьшение ИМТ на 2 кг/м2 на протяжении 10 лет снизило риск развития ОА более, чем на 50% [Felson DT, et al., 1992]. Систематический обзор литературы, посвященной изучению лиц с ожирением и диагностированным ОА коленных суставов, установил, что нетрудоспоспособность, обусловленная ОА, может быть значительно снижена с уменьшением массы тела на 5,1% [Christensen R. et al., 2007]. Какова же взаимосвязь между ОА и ожирением? Современные научные данные позволяют оценивать роль ожирения как фактора риска ОА и других хронических состояний гораздо шире, чем просто увеличение ИМТ Несомненно, сама по себе повышенная масса жировой ткани увеличивает нагрузку на скелет и приводит к повреждению костно-мышечной ткани. Эффект увеличенной нагрузки на суставной хрящ у людей с повышенным весом может объяснить возрастание риска ОА коленных суставов. Однако тот факт, что ОА часто развивается в суставах, не имеющих отношения к повышенному весу, позволяет предположить, что имеются какие-то другие механизмы, связанные с ожирением, способные изменить метаболизм хрящевой и костной ткани и привести к развитию заболевания. В последнее время показано, что жировая ткань не является пассивным накопителем энергии и значимость жировой ткани как эндокринного органа не вызывает сегодня сомнений. Новые данные позволили выдвинуть гипотезу, что ОА - системное заболевание, при котором дисрегуляция липидного гомеостаза может быть одним из лидирующих патофизиологических механизмов, приводящих к развитию ОА [Aspden R., 2001].
Роль воспаления в патогенезе ОА и ССЗ
По мнению ряда исследователей, связь ОА с ССЗ может быть обусловлена как общими патогенетическими механизмами, так и другими внешними факторами. В патогенезе атеросклероза и ОА немалую роль играет неспецифическое воспаление.
Атеросклероз относят к воспалительным заболеваниям, при которых воспаление связано с дислипидемией и хронической иммунной дисрегуляцией. Предполагаемыми факторами риска и маркерами атеросклероза являются С-реактивный протеин (СРП), фибриноген, тканевой активатор плазминогена, фосфолипаза А2, цитокины (интерлейкины, α-фактор некроза опухоли) и внутриклеточные сигнальные полипептиды [Kullo I.J. et al., 2000, Ridker P.M. et al., 2001]. Цитокины и сигнальные полипептиды, которые могут образовываться в сердце, сосудистых клетках, макрофагах и жировой ткани, стимулируют продукцию острофазных белков в печени как при острых, так и хронических воспалительных процессах [Gabay C., Kushner I., 1999]. Установлено, что одним из основных элементов атеротромбоза является увеличение синтеза провоспалительных цитокинов. Так, у больных ИБС по сравнению со здоровыми лицами обнаружено существенное повышение уровней интерлейкинов IL-2, IL-4, IL-6, IL-12 и IL-18, причем уровень IL-6 был выше у пациентов с инфарктом миокарда (ИМ) [Martins T.B. et al., 2006]. Повышенные уровни матриксной металлопротеазы-9 (MMP-9) вносят значимый вклад в разрыв фиброзной капсулы атеросклеротической бляшки, а повышенные уровни ингибитора-1 активатора плазминогена (PAI-1) играют большую роль в процессах тромбообразования. Как установлено, ММР оказывают влияние на ремоделирование сосудов и снижение эластичности артерий с возрастом [Page-McCaw A. et al., 2007]. ММР-3 ассоциирована с опасными, гладкими, липидосодержащими структурами артериосклеротических бляшек. Генотип MMP-3 может быть важной детерминантой ремоделирования сосудов и ригидности артериальных сосудов, связанной с возрастом. Исследование, проведенное Berg et al., 2009, показало, что у пациентов с ИБС уровни ММР-2 и ММР-9 оказались достоверно выше по сравнению с пациентами, не страдающими ИБС. Кроме того, активность ММР-2 достоверно ассоциировалась с уровнями С-реактивного белка, а также с уровнями атерогенного аполипопротеина В.
В патогенезе ОА также немалую роль играет неспецифическое воспаление [Pelletier J.P. et al., 2001]. При ОА отсутствуют классические макроскопические признаки воспаления, нет выраженной инфильтрации воспалительными клетками тканей сустава, однако провоспалительные цитокины, такие как IL, в частности, IL-1β, а также фактор некроза опухоли-α (ФНО-α) выявляются в синовиальной жидкости больных ОА в повышенных количествах. Под воздействием IL-1 хондроциты резко усиливают синтез ММР, прекращают синтез протеогликанов и коллагенов хряща. В ответ на стимуляцию IL-1β хондроциты синтезируют ферменты, необходимые для образования оксида азота (NO) (индуцибельную синтазу NO -ИСОА) и простагландинов (ЦОГ-2). Сложная сеть взаимодействий цитокинов, ферментов, свободных радикалов и продуктов распада матрикса приводит к уменьшению содержания протеогликанов в хряще, нарушению архитектоники матрикса, появлению микротрещин и надрывам хряща. Обнаружено значимое увеличение уровня MMP-3, как в синовиальной жидкости, так в крови пациентов с ОА коленных и тазобедренных суставов. Установлено, что ММР-3 продуцируется хондроцитами и клетками синовиальной мембраны [Pelletier J.P., et al., 2001]. Содержание MMP-3 корреллирует с активностью болезни или тяжестью ОА: уровень сывороточных MMР-3 и MMР-9 значительно повышен у пациентов с деструктивным ОА бедра по сравнению с пациентами с менее тяжелым ОА бедра. Таким образом, уровень MMP может служить быть диагностическим маркером быстро прогрессирующего ОА [Garnero P., 2007].
Нельзя не учитывать роль хронического болевого синдрома в патогенезе кардиоваскулярных осложнений при ОА. Хронический болевой синдром, вызывая нейроэндокринный ответ, нередко является причиной развития осложнений имеющихся у пациента ССЗ. Pincus et al. (2005) выявлено, что сокращение продолжительности жизни пожилых людей в большой степени зависит от выраженности болевого синдрома. Проведенная ими оценка выживаемости 1525 пациентов, среди которых 24% - 370 человек страдали ОА, 16% - 246 человек ССЗ, ОА и ССЗ - 109, показала, что относительный риск смерти был выше у пациентов с ОА с интенсивностью боли >40 мм по ВАШ (по сравнению с теми, у кого интенсивность боли была <40 мм при отсутствии различий по возрасту и полу). Помимо этого важным фактором, усугубляющим течение ССЗ, является ограничение физической активности пациентов, страдающих ОА.
Особенности терапии ОА у пациентов с ССЗ
Тот факт, что у больного с ОА, как правило, одновременно имеют место несколько соматических заболеваний, в первую очередь ССЗ, диктует необходимость жесткой оценки предполагаемой пользы и возможного риска от назначаемой противоартрозной терапии. На фоне коморбидности избыточное и нерациональное назначение лекарств без учета особенностей их взаимодействия приводит к резкому возрастанию вероятности развития нежелательных эффектов терапии и усугублению течения заболеваний.
Немедикаментозные методы лечения
Для пациента с ОА и ССЗ в случае повышенного ИМТ или ожирения проведение мероприятий по снижению веса является первоочередной задачей. Грамотная коррекция веса позволит уменьшить интенсивность болевого синдрома в пораженных суставах (коленных), будет способствовать замедлению прогрессирования ОА, а также значительно снизит риск сердечно-сосудистых осложнений. Регулярные занятия лечебной физкультурой (ЛФК) и правильный двигательный режим являются обязательным компонентом немедикаментозной терапии ОА. Позитивное влияние занятий ЛФК на снижение болевого синдрома в суставах при ОА установлено в ряде исследований. Комплекс ЛФК должен побираться индивидуально с учетом имеющейся ССП и ее степени тяжести.
Медикаментозные методы лечения
В международных рекомендациях по лечению ОА (EULAR, 2003, OARSI, 2008) НПВП указаны как препараты выбора для купирования болевого синдрома при ОА (в случае неэффективности парацетамола). НПВП, как неселективные, так и селективные, обладают выраженным противовоспалительным и обезболивающим эффектом, однако на пациентов с ОА и риском развития, а тем более страдающих ССЗ, они могут оказывать целый ряд побочных эффектов, отягощающих течение кардиоваскулярной патологии. Повышение риска кардиоваскулярных катастроф (инфаркта миокарда, инсульта и внезапной коронарной смерти) может рассматриваться как класс-специфический побочный эффект для всех НПВП [Насонов Е.Л., Каратеев А.Е., 2003, 2006, Antman E.M. et al., 2007]. Прием НПВП может приводить к дестабилизации АГ и прогрессированию сердечной недостаточности (СН). Установлено, что прием НПВП пациентами с заболеваниями сердца в анамнезе увеличивает в 10 раз вероятность (0R=10,5) госпитализации по поводу СН по сравнению с пациентами, не принимающими НПВП (OR=1,6). Также следует иметь в виду, что НПВП способны снижать эффективность препаратов, использующихся в стандартной терапии ССЗ (β-блокаторов, диуретиков, ингибиторов АПФ и в меньшей степени антагонистов кальция).
Как основные лечебные свойства всех НПВП, так и вызываемые ими нежелательные эффекты напрямую связаны с их механизмом действия - подавлением активности фермента циклооксигеназы (ЦОГ), что в результате приводит к угнетению синтеза простагландинов (ПГ), простациклинов и тромбоксанов. Существуют две изоформы ЦОГ: структурный изофермент (ЦОГ-1), регулирующий продукцию ПГ, участвующих в обеспечении нормальной (физиологической) функциональной активности клеток, и индуцируемый изофермент (ЦОГ-2), экспрессия которого регулируется иммунными медиаторами (цитокинами), принимающими участие в развитии иммунного ответа и воспаления. Принято считать, что противовоспалительное, анальгетическое и жаропонижающее действие НПВП преимущественно связано с их способностью ингибировать ЦОГ-2, в то время как наиболее часто встречающиеся побочные эффекты (поражение ЖКТ, почек, нарушение агрегации тромбоцитов) связаны с подавлением активности ЦОГ-1.
В настоящее время все более значимое место в терапии ОА занимают симптоматические препараты медленного действия с возможной структурно-модифицирующей активностью (SYSODOA). Они так же, как и НПВП, включены в рекомендации EULAR (2003, 2005, 2006) и OARSI (2008) по лечению ОА. К ним относят глюкозамин (ГА) и хондроитин сульфат (ХС), диацериин, препараты гиалуроновой кислоты для внутрисуставных инъекций и экстракты авокадо и сои. Наибольшие доказательства в отношении эффективности при лечении ОА получены для ХС и ГА. Суммируя результаты клинических исследований, проведенных с препаратами ХС и ГА, можно сделать заключение, что характерными для них являются противовоспалительный эффект, сравнимый с НПВП и позволяющий снизить дозу последних, возможность сочетания с парацетамолом и НПВП, длительное сохранение лечебного эффекта, высокая безопасность и отсутствие серьезных побочных эффектов. При этом они способствуют замедлению прогрессирования ОА (по данным рентгенологических исследований).
Механизм лечебного действия ХС и ГА при ОА связан с их способностью подавлять катаболические (дегенеративные) и активировать анаболические (восстановительные) процессы в хрящевой ткани, оказывать собственное противовоспалительное и обезболивающее действие. При этом установлено, что ХС и ГА оказывают не совсем идентичное фармакологическое действие: они дополняют и усиливают эффекты друг друга, что определяет перспективность их совместного применения в лечении ОА. Так, ХС зависимым от дозы образом подавляет стимулированный IL-1 синтез ПГ синовиальными фибробластами, отменяет зависимую от IL-1 ингибицию синтеза гиалуроновой кислоты, ингибирует зависимый от IL-1 синтез коллагеназы и активность аггреканазы, что свидетельствует о способности ХС уменьшать коллагенолитическую активность и увеличивать продукцию компонентов матрикса, способен подавлять синтез агрессивных ММР и активировать синтез ингибиторов ММР, что помогает восстановлению равновесия между анаболическими и катаболическими процессами в матриксе хряща. Помимо этого ХС подавляет NО-индуцированный апоптоз хондроцитов, улучшает микроцируляцию субхондральной кости за счет ингибиции синтеза липидов, связывания Е-селектина, мобилизации фибрина, липидов и холестерина в кровеносных сосудах субхондральной кости. ГА купирует провоспалительное и сосудоразрушающее действие IL— 1, подавляет активацию пути ядерного фактора (NF)-kB. Благодаря этому механизму ГА может подавлять экспрессию генов и синтез белков ЦОГ-2, избирательно через ЦОГ-1, таким образом предупреждая высвобождение простагландина PGE2 в питательной среде. Действие (NF)-kB подавляется ГА на уровне, как хондроцитов, так и синовиоцитов, при этом обеспечивается параллельное снижение синтеза белков ЦОГ-2, высвобождение (PGE2 и, в хондроцитах, высвобождение NO. Кроме того, ГА последовательно снижает обусловленный IL-1 синтез ММР в клетках обоих типов [Alvarez-Soria М.А. et al., 2001]. В эксперименте подтверждено усиление и дополнение фармакологических эффектов ХС и ГА в случае их совместного применения. Так комбинация ХС и ГА подавляла синтез некоторых медиаторов дегенерации хряща, в частности уменьшала желатинолитическую активность ММР-9, способствовала уменьшению концентрации протеина ММ-13 и уменьшению уровня кератан сульфата в тканях. В другом исследовании комбинированная терапия ХС и ГА увеличивала продукцию глюкозамино-гликанов хондроцитами на 96,6% по сравнению с 32% на монотерапии, а поражение хряща было менее тяжелым [Lippielo L.et al., 1999]. В недавнем двойном слепом плацебо-контролируемом исследовании «Glucosamine/Chondroitin Arthritis Intervention Trial (GAIT)» при оценке влияния различных схем лечения на боль (WOMAC) через 6 мес. терапии было установлено, что у больных ОА с сильными болями в коленных суставах (WOMAC 301-400 мм) эффективность терапии комбинацией ХС и ГГ была достоверно выше (79,2% , р=0,002 против плацебо ), чем в случае использования монотерапии ХС или ГГ [Clegg et al., 2006].
Учитывая доказанную клиническую эффективность, высокую безопасность и хорошую переносимость препаратов ХС и ГА, можно рассматривать их в качестве наиболее предпочтительных средств для лечения клинических проявлений ОА у больных с ССЗ. Проведенное нами исследование подтвердило эффективность и высокую безопасность комбинированного препарата АРТРА® (в 1 таблетке содержит 500 мг ХС и 500 мг глюкозамина гидрохлорида) в лечении ОА у больных с соматической патологией. В исследование были включены 60 больных в возрасте 62,3±4,7 года с ОА коленных суставов II-III стадии и сопутствующей соматической патологией, из которых 60% страдали АГ и 19% ИБС. Пациенты были рандомизированно разделены на 2 группы, сопоставимые по полу, возрасту, тяжести ОА (интенсивности болевого синдрома и степени функциональных ограничений) и сопутствующей терапевтической патологии (по 30 пациентов каждая). Пациенты основной группы получали АРТРА® совместно с НПВП, пациенты контрольной группы - только НПВП. По ходу лечения НПВП отменялись при отсутствии болевого синдрома и не рецидивировании последнего без терапии НПВП. Длительность терапии составила 6 мес., оценка эффективности проводилась: клиническая - через 3 и 6, МРТ - через 9 мес. В динамике оценивались: влияние терапии на боль (индексы ВАШ, WOMAC), отмену или снижение дозы принимаемых НПВП, функциональное состояние (WOMAC, быстрота ходьбы на 15 м), прогрессирование заболевания (МРТ коленных суставов), состояние сердечно-сосудистой системы и желудочно-кишечного тракта.
Оценка динамики болевого синдрома (WOMAC боли) продемонстрировала, что у пациентов, принимавших АРТРА®, уже через 3 мес. от начала терапии наблюдался более выраженный регресс болевого синдрома по сравнению с группой контроля. Через 6 мес. терапии у пациентов основной группы уровень интенсивности болевого синдрома был достоверно ниже, чем у пациентов контрольной группы, 178,3±37,2 против 287,4±42,8 соответственно (р=0,02). Оценка функциональной недостаточности по шкале WOMAC на старте исследования не выявила значимых различий между группами наблюдения. Через 6 мес. терапии в обеих группах мы наблюдали достоверное снижение функциональной недостаточности, однако в первой группе средний балл составил 427,3, во 2-й - 658,9 (р=0,002). Таким образом, у пациентов, получающих АРТРА®, после окончания запланированного срока наблюдения отмечалась достоверно большая динамика нивелирования болевого синдрома и улучшения функциональной способности. Визуальная оценка состояния коленных суставов сустав, проведенная врачом МРТ, до лечения и через 9 мес. терапии установила улучшение визуализации суставного хряща у 60% пациентов основной группы, в то время как у 63,3% пациентов контрольной группы отмечалась отрицательная динамика. Таким образом, больший положительный эффект терапии в группе пациентов, получавших АРТРА®, с точки зрения клинической картины подтвержден данными объективного метода исследования - МРТ. С целью изучения влияния терапии на состояние сердечно-сосудистой системы у пациентов с ОА и соматической патологией оценивались динамика САД (систолического АД) и частота БИ (болевой ишемии) и ББИ (безболевой ишемии) миокарда по данным холтеровского исследования (вначале и через 6 мес. исследования). Установлено, что на фоне лечения у пациентов, получавших АРТРА®, наблюдалась большая положительная динамика уровня САД. Разница среднесуточного САД до начала терапии и через 6 мес. наблюдения составила в основной группе 7,3 мм рт.ст (р<0,05), в то время как в контрольной группе - 3,6 мм рт.ст (р>0,05). По данным холтеровского мониторирования, у пациентов основной группы было отмечено меньшее число эпизодов как БИ, так и ББИ миокарда, чем у пациентов контрольной группы. Положительное влияние АРТРА® у больных с ОА и соматической патологией на состояние сердечно-сосудистой системы обусловлено, по-видимому, более эффективным купированием болевого синдрома в суставах и улучшением функционального состояния, снижением дозы принимаемых больным НПВП и связанным с этим снижением риска развития, вызываемых ими побочных эффектов. Исследование также продемонстрировало и выгодность применения препаратов ХС и ГА в лечении пациентов с ОА и соматической патологией с фармакоэкономической точки зрения. На фоне лечения препаратом АРТРА® у больных ОА уменьшилось число повторных госпитализаций по поводу обострений соматических заболеваний: в основной группе, получавшей АРТРА®, в течение последующих 9 мес. наблюдения повторно госпитализировались 43% пациентов (13 человек), тогда как во 2-й группе, получавшей только НПВП, повторные госпитализации были у 76% пациентов (23 человека). Общее число госпитализаций на 1 больного составило 1,2 в 1-й группе и 1,7 -во 2-й группе.
Заключение
Таким образом, терапия клинических проявлений ОА у больных с сердечно-сосудистой патологией (или ее высоким риском) должна быть тщательно продуманна врачом. При формировании схемы лечения должны быть выявлены и по возможности устранены имеющиеся у больного факторы риска сердечно-сосудистых заболеваний. Большое внимание следует уделять не медикаментозным методам лечения - ЛФК, диете, направленной на снижение ИМТ, организации режима труда и отдыха. На протяжении всего курса лечения необходим жесткий контроль уровня АД, ЭКГ Что касается медикаментозной терапии, то больным с АГ и высоким риском кардиоваскулярных осложнений НПВП следует назначать с большой осторожностью, соблюдая принятые рекомендации (в сочетании с низкими дозами спирина). Больным с СН НПВП лучше не назначать. Учитывая доказанную клиническую эффективность, высокую безопасность (сопоставимую с плацебо) и хорошую переносимость препаратов ХС и ГА, их можно рассматривать в качестве наиболее предпочтительных для лечения клинических проявлений ОА у больных с ССЗ.
