Флюдитек в лечении воспалительных заболевании верхних дыхательных путей
СтатьиОпубликовано в журнале:
«Российская оториноларингология», №6(19), 2005, с. 77-81
Г.Д. Тарасова*, Т.В. Иванова**, П.Г. Протасов*
* ФГУ «Научно-клинический центр оториноларингологии Росздрава» (Директор - проф. НА. Дайхес)
** Детский пульмонологический санаторий «Кратово» Московской области (Гл. врач -засл. врач РФ Н.В. Шарапов)
Одним из основных барьеров защиты слизистой оболочки является наличие мукоцилиарного клиренса и секреция мерцательным эпителием лактоферрина, секреторного иммуноглобулина А и лизоцима.
Вся поверхность дыхательных путей покрыта мерцательным эпителием за исключением носовых ходов и тех частей носоглотки, глотки и гортани, которые покрыты многослойным плоским эпителием. Эпителиальные клетки подразделяют на базальные и клетки, выстилающие просвет дыхательных путей. Эти клетки бывают реснитчатыми или секреторными железистыми клетками. Реснитчатые, или цилиарные клетки, ответственны за движение слизи и секрецию мукозной субстанции. Секреторные клетки продуцируют слизь, им присуща абсорбционная функция.
Эпителий респираторного тракта формирует двухфазную структуру слизи, состоящую из слоя водянистого золя - перицилиарный слой, в котором реснички сокращаются и расслабляются, и более поверхностного слоя геля, который лежит над ресничками. Золь действует как вспомогательная смазка, координирующая движение ресничек, которые транспортируют слой геля [4, 10, 11].
Существует оптимальная концентрация молекул муцина в отделяемом респираторного тракта, необходимая для полноценного выполнения транспортной, увлажняющей, фильтрационной и антибактериальной функций.
Физико-химические свойства секрета зависят от соотношения кислых и нейтральных муцинов в его составе. При снижении продукции кислых и повышении синтеза нейтральных муцинов происходит повышение вязкости секрета. При воспалительном процессе, как правило, происходит повышение вязкости секрета. Этому способствует возникновение дисульфидных и водородных связей между молекулами муцина, что ведет к преобладанию геля над золем [3, 8, 14].
Изменение реологических и физических свойств слизи является основным объяснением большинства нарушений при воспалительных заболеваниях полости носа и околоносовых пазухах, приводящих к ее застою вследствие нарушения экспекторации (свободного отделения).
Процесс слизеобразования, являясь физиологическим, способствует поддержанию биоценоза слизистой оболочки верхних дыхательных путей (ВДП). Кашель и мукоцилиарный клиренс относят к механизмам, способствующим поддержанию этого состояния. При гиперсекреции кашель может давать очищение более чем на 50%, компенсируя этим возможные нарушения мукоцилиарного транспорта.
С увеличением вязкости слизи, происходящим во второй фазе воспалительного процесса, уменьшается эффективность очищения с помощью кашля. При небольшом увеличении вязкости улучшается мукоцилиарный клиренс, но до определенного предела, а затем выключаются и клиренс и кашель, то есть механизмы собственной защиты [3, 4, 8, 12].
Инфекционный процесс, представляющий вариант взаимодействия между бактерией и слизистой оболочкой, сопровождается адгезией и инвазией бактерий в слизистую оболочку. При этом на 60-80% уменьшается или останавливается мукоцилиарный транспорт. Этот процесс сопровождается снижением продукции 81§ А, препятствующего проникновению бактерий в организм, тормозя их адгезию и способствуя их фагоцитозу, что особенно важно при хроническом воспалении [4, 5, 8-10, 14].
Регуляция гидратации слизи необходима для увлажнения вдыхаемого воздуха и для эффективности микоцилиарного клиренса. Ионный состав, рН и осмолярность контролируют гидратацию слизи. Степень диффузии или всасывающая способность слизистой оболочки поддерживает ее эффективность как фильтрационного барьера против бактерий и контаминирующих агентов. Некоторые гликопротеины, содержащиеся в слизи, обладают выраженными бактериостатическими и бактерицидными способностями.
В то же время, адгезия к эпителию, снижение мукоцилиарного клиренса - мукостаз и продукция экскреторных энзимов помогают бактериям противостоять мукоцилиарному клиренсу. Так называемые адгезины находятся на поверхности бактерии и обеспечивают их сцепление со слизистой оболочкой. Затем патогены размножаются и «запускают» местную воспалительную реакцию.
Патофизиологические процессы, происходящие при воспалительных заболеваниях ЛОР-органов, особенно хронические, сопровождаются нарушением мукорегуляции. При этом происходит нарушение не только продукции слизи, ее состава, но и функции и структуры ресничек эпителия. Вырабатываемую при этом слизь с нарушенными реологическими свойствами (деструктурированную) организм не в состоянии выводить самостоятельно, что приводит к ее застою и скоплению в полостях организма и, прежде всего, при ЛОР-заболеваниях: в полостях околоносовых пазух и среднем ухе [1, 2, 13, 15].
Большинство респираторных патогенов продуцируют экзотоксины, нарушающие функцию различных защитных механизмов, и, в первую очередь, мукоцилиарный клиренс. Как известно, наиболее частыми патогенами, вызывающими до 50% всех воспалительных заболеваний ЛОРорганов в мире являются Str. pneumoniae и Н. influenzае. Так, пневмококк замедляет цилиарные колебания, вызывает некроз клеток эпителия и приводит к травмированию их стенок. Гемофильная палочка также вызывает замедление цилиарных колебаний и слущивание эпителия.
Доказано, что инфекционное воспаление способствует сенсибилизации организма и более тяжелому течению аллергических заболеваний и, в частности, широко распространенного в настоящее время аллергического ринита (АР).
Многолетним опытом лечения воспалительных заболеваний околоносовых пазух и среднего уха доказана целесообразность включения в комплексную терапию муколитических препаратов. В настоящее время эта группа препаратов внесена в разработанный стандарт лечения синусита в России. В задачи муколитической терапии входят:
- стимуляция выведения слизи,
- разжижение слизи,
- уменьшение внутриклеточного образования слизи,
- регидротация.
В оториноларингологии используют несколько групп мукоактивных препаратов, обладающих различными механизмами действия [1,2,5,7, 15]. Мы предлагаем их рабочую классификацию (Табл. 1).
Таблица 1. Классификация мукоактивных препаратов по механизму действия.
|
Прямое действие |
||
| Препараты, разрывающие полимеры секрета | Тиолитики – производные цистеина | Ацетилцистеин, цистеин, месна, метилцистеин, этилцистеин, L-цистеин, гуайфенезин, имозимаза, террилитин |
| Производные алколоида визина (бензиламины) | Бромгексин, амброксол, лазолван | |
| Протеолитические ферменты | Трипсин, химотрипсин, химопсин, рибонуклеаза, дезоксирибонуклеаза | |
| Препараты, способствующие регидратации секрета | Неорганический йод, соли натрия и калия, гипертонические солевые растворы | |
|
Непрямое действие |
||
| Препараты, стимулирующие гастропульмональный рефлекс | Фитопрепараты | Препараты термопсиса, алтея, солодки, истода, эфирные масла |
| Синтетические соединения | терпингидрат, ликорин | |
| Препараты, регулирующие выработку секрета | Производные карбоцистеина | Карбоцистеина лизиновая соль, карбоцистеин |
Подбирая индивидуально муколитический препарат следует руководствоваться присущими ему особенностями действия. Так, производные алколоида визицина (бензиламины) — бромгексин, амброксол - лишь разжижают и уменьшают вязкость секрета. Муколитические ферменты -трипсин, химотрипсин, рибонуклеаза, дезоксирибонуклеаза имеют ряд выраженных побочных эффектов и в детстве не используются [2, 7, 8].
Препараты резорбтивного действия (способствующие регидратации) — соли натрия и калия (йодиды), гидрокарбонат натрия, гипохлорид аммония (нашатырно-анисовые капли), аммония хлорид — стимулируют бронхиальную секрецию, разжижают мокроту, усиливают перистальтику мерцательного эпителия, но их эффект почти не проявляется на уровне полости носа и околоносовых пазух.
Синтетические соединения, такие как терпингидрат и ликорин, действуют посредством гастропульмонального рефлекса через рвотный центр продолговатого мозга вызывают рефлекторную стимуляцию секреции бронхиальных и слюнных желез. Усиливают перистальтику мерцательного эпителия. У детей их следует применять с осторожностью, так как избыточная стимуляция рвотного и кашлевого центров может привести к рвоте и аспирации. В связи с этим препараты этой группы имеют ограниченное применение [7].
Существуют также препараты, активизирующие механизмы мерцательного эпителия. Это симпатомиметики - стимуляторы b2-адренорецепторов (b2-агонисты)—тербуталин, теофиллин, но их чаще применяют при воспалительных заболеваниях бронхов и бронхиальной астме.
Кроме того, применяют фитопрепараты, обладающие секретолитическим действием, изготавливаемые из термопсиса, алтея, солодки, истода, а также и эфирные масла и препараты на их основе (Геломиртол). Ограничение их использования обусловлено широким распространением пациентов, страдающих аллергией.
Существуют также комбинированные препараты-Терпинкод, Аскорил Экспекторанте, Алекс плюс, Эреспал, Трайфед, бронхотуссин, и комбинированные фитопрепараты — Синупрет и Проспан.
Муколитики прямого действия - это, прежде всего, носители сульфгидрильных групп (препараты, разрывающие полимеры секрета) - ацетилцистеин и месна. В нашей стране их достаточно широко используют, что определяется тем, что в основе действия производных ацетилцистеина лежит восстановление свойств слизи, путем разрыва дисульфидных связей мукополисахаридов мокроты - молекулы деполимеризуются и мокрота становится менее вязкой и адгезивной. Однако, одновременно происходит разрушение и молекулы 51§А, являющегося первой линией защиты слизистой оболочки от патогенов. Тем самым наблюдается усугубление снижения местного иммунитета, развивающееся на фоне воспалительного процесса. Это может неблагоприятно сказаться на течении заболевания, а также способствовать переходу воспаления в хроническую форму. Кроме того, им присущи множественные побочные реакции, развивающиеся как при местном, так и при системном их применении.
К препаратам непрямого действия относят производные карбоцистеина- карбоцистеин, карбоцистеина лизиновая соль.
Механизм действия карбоцистеина связан с активацией сиаловой трансферазы - фермента бокаловидных клеток слизистой оболочки. Он нормализует количественное соотношение кислых и нейтральных гликопептидов, что восстанавливает вязкость и эластичность слизи, то есть происходит замещение патологической слизи реструкторизованной, которая располагается между патологической слизью и слизистой оболочкой. При этом патологическая слизь как бы приподнимается, а пульсация ресничек осуществляется уже в контакте с физиологической слизью.
В таблице 2 мы представили сравнительную характеристику основных представителей мукоактивных препаратов: производных ацетилцистеина и карбоцистенина.
Таблица 2. Сравнительная характеристика действия производных ацетилцистеина и карбоцистеина
| Действие | Ацетилцистеин | Карбоцистеин |
| Совместимость с антибиотиками | Инактивирует действие (пенициллины, цефалоспорины, тетрациклины) | Совместим |
| Продукция Sig А | Снижает | Восстанавливает |
| Продукция лизоцима | Снижает | Восстанавливает |
| Вязкость слизи | Уменьшает | Нормализует |
| Состояние слизистой оболочки | Не влияет | Восстанавливает |
Учитывая вышеизложенное, целью нашего исследования явилось установление терапевтической эффективности Флюдитека влечении воспалительных заболеваний ВДП в детском возрасте в условиях пульмонологического санатория.
Объектом исследования были 58 детей в возрасте с 3 до 8 лет, находящиеся на санаторном этапе реабилитации. Основным критерием включения было наличие клиники инфекционного ринита с сопутствующим хроническим аденоидитом. Основную группу составили 36 детей, в комплекс лечения которых был включен препарат Флюдитек в возрастной дозировке, курсом от 8 до 10 дней. Контрольная группа включала 22 ребенка, комплекс терапии которых был традиционным и состоял из ирригации полости носа антибактериальными растворами и ингаляционной терапии (Табл. 3).
Таблица 3. Распределение по полу и возрасту обследованных пациентов
| Пол | 3-6 лет | 7-8 лет | Всего: | |||
| Основная | Контрольная | Основная | Контрольная | Основная | Контрольная | |
| Мальчики | 7 | 5 | 13 | 7 | 20 | 12 |
| Девочки | 5 | 4 | 11 | 6 | 16 | 10 |
| ИТОГО: | 12 | 9 | 14 | 13 | 36 | 22 |
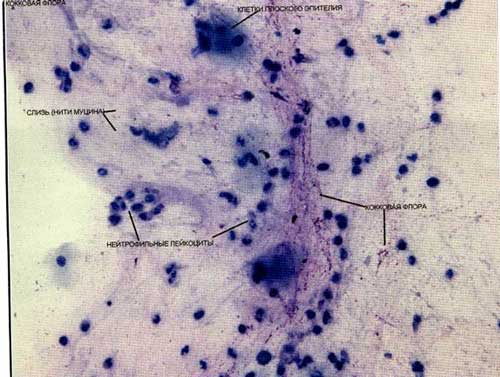
Методы: сбор и анализ данных анамнеза, оториноларингологический осмотр, эксфолиативная цитология назального секрета. Цитологическое исследование назального секрета основывали на подсчете общего относительного (%) количества клеточных элементов на 200 клеток с количественной оценкой фона (слизи) и микрофлоры.
Результаты. При оценке состояния пациента до лечения учитывали наличие и степень затруднения носового дыхания, характер и количество выделений из полости носа, наличие и характер кашля. У всех пациентов в той или иной степени имело место затруднение носового дыхания и выделения из полости носа. Кашель отмечен приблизительно у половины детей.
В результате проведенного исследования было выявлено более раннее выздоровление детей в основной по сравнению с контрольной группой. Это выражалось ранним купированием кашля, более быстрым улучшением носового дыхания и уменьшением отечности слизистой оболочки.
Особые различия у больных этих групп проявились в количестве, длительности и характере отделяемого. Если в основной группе на 2-3-й день от начала терапии у большинства детей увеличилось количество отделяемого, а с 3-4-го дня стал меняться его видимый характер, и наблюдали уменьшение его количества. Выделения становились менее густыми и лучше удалялись при отсмаркивании и при промывании. На рисунке 1 отражен наиболее характерный вид назального секрета до лечения.
Рис. 1. Назальный секрет (гнойный характер) у ребенка с хроническим инфекционным ринитом (до лечения).
Кашель почти у всех детей (у 88,2%) этой группы купировался к 7 дню лечения. В контрольной группе характер отделяемого видимо стал меняться лишь на 5-6 день от начала лечения. Уменьшение же его интенсивности наблюдали с 6-7 дня.
При эксфолиативной цитологии назального секрета у большинства больных до лечения было выявлено:
- низкий цитоз реснитчатого эпителия,
- превалирование плоского эпителия,
- высокие цифры нейтрофиллов,
- большое количество слизи,
- наличие в большом количестве разнообразной микрофлоры, преимущественно кокковой.
Эксфолиативные цитограммы по окончании лечения у 64,7% детей в основной группе свидетельствовали об урегулировании процесса фагоцитоза и отсутствии подавления экссудации с одновременным уменьшением количества микроорганизмов. В контрольной группе подобные изменения имели место лишь у 36,4% пациентов и были менее выраженными. Через 14 дней от начала лечения всем пациентам также делали забор назального секрета и его цитологическое исследование (Табл. 4).
Таблица 4. Результаты терапии в основной и контрольной группах
| Симптом | Основная группа | Контрольная группа |
| Нормализация дыхания | 61,8% | 54,5 % |
| Отсутствие выделений | 70,6 % | 63,6 % |
| Отечность сохранялась | 26,4 % | 40,9 % |
| Кашель сохранялся | 20,0 % | 40,0 % |
Полученные результаты свидетельствуют об эффективности использования препарата Флюдитек в комплексном лечении воспалительных заболеваний ВДП, а также рациональности включения его в комплекс лечения детей, находящихся на санаторном этапе реабилитации. Терапевтическую эффективность применения мукоактивных препаратов целесообразно оценивать на основании результатов методики эксфолиативной цитологии назального секрета.
Мукоцилиарный транспорт является сложным процессом, в котором задействованы различные механизмы, поэтому с целью его реактивации следует использовать мукоактивные препараты, и прежде всего препарат системного действия из группы карбоцистеина (Флюдитек).
ЛИТЕРАТУРА
1. Гаращенко Т.И. Мукоактивные препараты в лечении заболеваний верхних дыхательных путей /Т.И. Гаращенко, М.Р Богомильский // Рос. ринол.-2002.-№2.-С. 28-39.
2. Зайцева О.В. Лечение кашля у детей и подростков: рациональный выбор терапии / О.В. Зайцева // Сonsilium-medicum.-2003.-Т.5, №4.-С 204-207.
3. Овчаренко СИ. Муколитические (мукорегуляторные) препараты в лечении хронической обструктивной болезни легких / С.И.Овчаренко / Рос. мед. журн.-2002.-Т 10, №4.-С. 153-157.
4. Полевщиков А. В. Риносинуситы: механизмы развития воспаления слизистых оболочек и пути воздействия на него / А.В. Полевщиков // Матер. XVI съезда оториноларингологов РФ, СП6.-2001.-С.
5. Рязанцев СВ. Роль муколитических, секретолитических и секретомоторных препаратов в лечении острых и хронических синуситов у детей / СВ. Рязанцев // Новости оторинолар. и логопатол.-2002.-№1(29).-С 129-132.
6. Рязанцев СВ. Современные аспекты муколитической терапии синуситов / СВ. Рязанцев // Рос. оторинолар -2003.-№1(4).-С. 165-168.
7. Самсыгина Г.А. Бронхиты у детей. Отхаркиывающая и муколитическая терапия / Г.А. Самсыгина, О.В. Зайцева // Пособие для врачей.-М., 1999.-36 с.
8. Синопальников А.И. Место муколитических препаратов в комплексной терапии болезней органов дыхания / А.И. Синопальников, И.Л. Клячкина// Рос. мед. вести.-1997.-Т2, №4.-С. 9-18.
9. Тарасова Г.Д. Клиника и лечение иммунопрепаратами гайморита у детей: Автореф. дис.... канд. мед. наук / Г.Д. Тарасова -М., 1983.-21 с.
10 Aimay epithelium as an effector- of inflammation E molecular regulation of secondary media.tors I L. D. Martin, L.G. Rochelle, B.M. Fisher et a[. II Eur. Respir. J.-1997.—Vol,10.—P. 2139-2146.
11. Bals R. Cells types of respiratory epithelium: morphology, molecularbiolou and clinical significance/ R. Bals // Pneumologie — 1997.—Vol. 51.-13. 142-149
12 . Bron J. Relative biovailability of carbocysteine from three dosage forms, Investigated in healthy volunteers I J. Bron Biopharin Drug Disposit.-1988. Vol.9.—P. 97—111.
13. Catalano G.B. La carbocisteina nclla patologia flogisticacronica rinosin Lisa 1 e / G.B. Catalano, N. Mallanino, A. Serra // Otorinolaringologia.-1981.—V01.31.—P. 1-11.
14. Changes in Ig A Levels in nasal mucus after upper respiratory tract diseases in infant treated with carbo-cysteine/ A. Henocq, C. Moreau, E. Mallet et al, // Ann Otolaryngol Chir Cervicofac — 1985 —Vol.102.—P. 373-375.
15. Mucolitic agents for acute respiratory tract infections in infants: a pharmaco-epiderniologic problem? / M. Chalumeau, G. Cheron, R. Assathiany et al. //Arch Pediatr.-2002.—Vol.9 — P. 1128-1136.
