Применение препарата «Ливарол», вагинальные суппозитории, для купирования рецидива хронического рецидивирующего кандидоза гениталий, обусловленного не-albicans Candida spp.
СтатьиОпубликовано в сборнике статей:
«Опыт клинического применения суппозиториев вагинальных Ливарол® при остром и хроническом вульвовагинальном кандидозе» c.20-26
А. К. Мирзабалаева, Ю. В. Долго-Сабурова, О. Н. Жорж, И. А. Босак, И. В. Выборнова, Н.Н. Климко
Кафедра клинической микологии, аллергологии и иммунологии, НИИ медицинской микологии им. П. Н. Кашкина ГОУ ДПО «Санкт-Петербургская медицинская академия последипломного образования Федерального агентства по здравоохранению и медицинскому образованию»
Хронический рецидивирующий кандидоз гениталий (ХРКГ) является актуальной проблемой, этим заболеванием страдают 5–15% женщин репродуктивного возраста. Основной возбудитель ХРКГ – C.albicans, но в последние годы стали чаще выявлять ХРКГ, обусловленный другими видами Candida spp. [5, 11, 21]. Клиническое значение заболеваний, обусловленных не-albicans Candida spp., связано со сниженной эффективностью антимикотической терапии. Известно, что чувствительность возбудителя к антимикотикам in vitro зависит от его вида. Например, практически все штаммы C.krusei первично устойчивы к флуконазолу in vitro, а большинство изолятов C.glabrata отличается дозозависимой чувствительностью или резистентны к флуконазолу и итраконазолу. Понятно, что подобные варианты ХРКГ могут быть рефрактерны к «обычной» антимикотической терапии [1, 7, 12].
Методы лечения ХРКГ, обусловленного не-albicans Candida spp., не разработаны. Одним из вариантов лечения может быть применение интравагинальных лекарственных препаратов, при котором возникает высокая концентрация действующего вещества в очаге инфекции, что может привести к преодолению резистентности возбудителей ХРКГ к антимикотикам [21]. Данные об эффективности применения интравагинальных препаратов группы азолов для лечения этой категории больных отсутствуют.
В микологической клинике СПб МАПО с сентября 2006 г. по июнь 2007 г. провели проспективное клиническое открытое несравнительное исследование эффективности и безопасности применения вагинальных суппозиториев «Ливарол®» (производство фармацевтической компании ОАО «Нижфарм», Россия), содержащих 400 мг кетоконазола, для купирования рецидива ХРКГ, обусловленного не-albicans Candida spp.
Методы исследования, характеристика больных
В открытое несравнительное исследование включили 30 больных ХРКГ, обусловленным не-albicans Candida spp.
Критерии включения: возраст старше 18 лет; наличие не менее четырех лабораторно подтвержденных рецидивов кандидоза гениталий в течение года; возбудитель, не относящийся к виду Сandida albicans.
Критерии исключения: наличие острых и хронических (в фазе обострения) заболеваний органов малого таза, инфекций, передаваемых половым путем (ИППП), индивидуальная непереносимость компонентов препарата, психические заболевания, алкоголизм, наркозависимость, а также беременность и кормление грудью.
Возраст больных варьировал от 18 до 59 лет, средний возраст составил 33,8±8,7 года. У 77% больных длительность заболевания была от 1 до 5 лет, у 23% – от 6 до 17 лет. Частота рецидивов в среднем составила 8,6±3,3 в год. У 60% больных частота рецидивов составила 4–6 раз в год, у 40% обследованных (преимущественно у больных с эндокринопатиями – сахарный диабет, гипотиреоз, аутоиммунный тиреоидит) обострения кандидоза происходили практически ежемесячно, 9–12 раз в год.
Всех больных обследовали с целью выявления фоновой генитальной и экстрагенитальной патологии. Средний возраст менархе составил 13,2±0,2 года. У 32% женщин были выявлены нарушения менструальной функции (альгодисменорея, гипо-, гиперменоррея, предменструальный синдром). Средний возраст полового дебюта – 18,1±0,3 года. Репродуктивная функция была реализована у 60% пациенток. 7% женщин использовали современные методы контрацепции (комбинированные эстроген-гестагенные препараты), остальные пациентки эпизодически использовали барьерные и спермицидные средства контрацепции, календарный метод Огино-Кнауса.
При анализе особенностей менструальной (возраст менархе, ритм и объем менструальных кровотечений), сексуальной (возраст полового дебюта, количество половых партнеров), репродуктивной (количество беременностей, родов, искусственных и самопроизвольных абортов) функций, особенностей контрацепции у больных ХРКГ существенных отличий по сравнению с показателями в общей популяции женщин не выявлено.
Применение антибактериальных препаратов (преимущественно макролидов и полусинтетических пенициллинов в течение 7–10 дней), назначенных по поводу соматической и гинекологической патологии (инфекции ЛОР-органов, мочевыводящих путей, ИППП) отмечено у 13,3% обследованных женщин. Эндокринная патология (сахарный диабет II типа, аутоиммунный тиреоидит, гипотиреоз) выявлена у 13,3% женщин.
Всех больных обследовали в соответствии с протоколом исследования: сбор анамнеза, учет жалоб (зуд, жжение, выделения из половых путей, дизурические явления, диспареуния), клинических проявлений ХРКГ (отечность, гиперемия слизистых оболочек вульвы влагалища, экто- и эндоцервикса, губок уретры, наличие эрозий и трещин слизистых оболочек вульвы, вагины, различные по интенсивности выделения из половых путей).
Во всех случаях диагноз был установлен на основании стандартных критериев: наличие характерных клинических признаков в сочетании с выявлением почкующихся дрожжевых клеток и/или псевдомицелия при микроскопии окрашенных по Граму мазков, взятых из пораженных участков слизистых оболочек нижнего отдела полового тракта, а также выявление Candida spp. при посеве исследуемого материала [1, 7].
Микологическое исследование включало выделение культуры Candida spp. из исследуемого материала, определение вида и чувствительности возбудителей к флуконазолу in vitro. Материал из пораженных участков слизистых облочек полового тракта засевали на среду Сабуро с последующим количественным учетом колоний Candida spp. Идентификацию C.albicans проводили с помощью экспресс-теста на образование ростковых трубок в сыворотке крови. Далее биохимические тесты выполняли с культурами Candida spp., неспособными к образованию ростковых трубок. С этой целью использовали тест-системы Auxacolor-2 и Fungiscreen-4h (BIO RAD).
Определение чувствительности выделенных изолятов грибов к флуконазолу in vitro проводили диско-диффузионным методом согласно протоколу CLSI M-44A. Использовали стандартные диски производства компании Becton Dickinson (США), содержащие 25 мкг флуконазола. Учет результатов проводили после инкубации путем считывания диаметра зоны подавления роста грибов с помощью прибора BIOMIC Vision. Чувствительность оценивали на основании эквивалентности диаметра зон подавления роста (ЗПР) Candida spp. и минимальных ингибирующих концентраций (МИК) антимикотичеких препаратов. Штаммы Candida spp. считали чувствительными, если ЗПР составляла ≥ 19 мм для флуконазола (МИК ≤ 8 мкг/мл). Штаммы обладали дозозависимой чувствительностью к флуконазолу, если ЗПР составляли 15–18 мм, а МИК 16–32 мкг/мл. Резистентными считали штаммы, для которых ЗПР и МИК для флуконазола составили ≤ 14 мм, ≥ 64 мкг/мл соответственно [1, 7, 16].
После клинико-лабораторного подтверждения диагноза обострения ХРКГ пациенткам был назначен «Ливарол®» по 1 свече на ночь интравагинально в течение 10 дней.
В период наблюдения пациентки не получали других антимикотических и антибактериальных препаратов. Больные были предупреждены о необходимости применения контрацептивных средств на период проведения лечения.
Первый контрольный осмотр с целью оценки клинической эффективности и переносимости лечения проводили через 5 дней от начала применения «Ливарол®». Эффективность десятидневного курса лечения рецидива ХРКГ оценивали через 7 дней после окончания терапии на основании данных клинического и лабораторного обследования пролеченных больных.
Для определения эффективности лечения использовали следующие критерии:
- хороший эффект - отсутствие субъективной симптоматики (зуд, жжение, боль); отсутствие клинических проявлений воспаления (гиперемия, отек) и лабораторных признаков кандидоза гениталий;
- удовлетворительный эффект - отсутствие лабораторных признаков кандидоза гениталий, положительная динамика субъективной и объективной симптоматики, недостаточная для отнесения эффекта к категории «хороший эффект»;
- неудовлетворительный эффект - отсутствие эффекта от лечения или ухудшение субъективной и объективной симптоматики, или нежелательные явления, требующие отмены препарата. Для определения безопасности лечения учитывали нежелательные явления.
Результаты исследования
У всех пациенток, включенных в данное исследование, диагноз ХРКГ, обусловленного не-albicans Candida spp,. был установлен на основании сочетания жалоб, результатов гинекологического осмотра (осмотр слизистых влагалища и шейки матки в зеркалах, бимануальное исследование) и лабораторных признаков кандидоза (табл. 1).
Таблица 1. Клинические симптомы ХРВК
| Жалобы и клинические признаки | % | |
| Творожистые выделения из влагалища | 36,7 | Выраженные |
| 40 | Умеренные | |
| 23,3 | Незначительные | |
| Зуд наружных гениталий | 16,7 | Выраженный |
| 40 | Умеренный | |
| 23,3 | Незначительный | |
| 16,7 | Отсутствует | |
| Жжение наружных гениталий | 20 | Выраженное |
| 26,7 | Умеренное | |
| 23,3 | Незначительное | |
| 30 | Отсутствует | |
| Болезненность наружных гениталий | 3,3 | Выраженная |
| 10 | Умеренная | |
| 36,7 | Незначительная | |
| 46,7 | Отсутствует | |
| Отечность слизистых оболочек | 0 | Выраженная |
| 26,7 | Умеренная | |
| 43,3 | Незначительная | |
| 26,7 | Отсутствует | |
| Гиперемия слизистых оболочек | 16,7 | Выраженная |
| 33,3 | Умеренная | |
| 13,3 | Незначительная | |
| 30 | Отсутствует | |
Более чем у половины обследованных пациенток отмечены умеренные или незначительные клинические проявления воспалительного процесса, что, характерно для ХРКГ, обусловленного не-albicans Candida spp. [3, 4]. У 60% женщин клинические признаки заболевания появлялись во II фазу менструального цикла, у остальных пациенток не имели четкой связи с менструальным циклом.
Во всех случаях диагноз кандидоза был верифицирован на основании стандартных лабораторных диагностических критериев [1, 7]. Возбудителями ХРКГ у обследованных больных были C.tropicalis (27%), C.krusei (26%) и C.glabrata (20%), реже – C.dubliniens, C.papapsilosis и C.kefyr (рис. 1).
Рисунок 1. Возбудители хронического рецидивирующего кандидоза гениталий
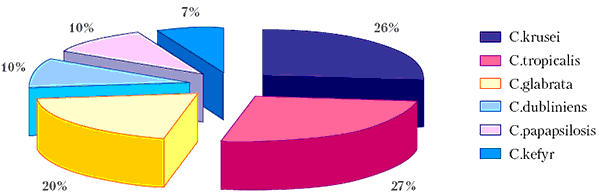
Чувствительны к флуконазолу in vitro были 63,3% возбудителей, в том числе все штаммы C.tropicalis, C.dubliniensis и C.parapsilosis, 66,7% изолятов C.glabrata, а также 50% изолятов C.kefyr. Сниженную чувствительность к флуконазолу in vitro выявляли у 36,7% изолятов, из них 26,7% штаммов были резистентны к флуконазолу (C.krusei – 100%), а 10% были чувствительными – дозозависимыми (C.glabrata – 33,3%, C.kefyr – 50%) (табл. 2).
Таблица 2. Чувствительность возбудителей хронического рецидивирующего кандидоза гениталий у обследованных больных к флуконазолу in vitro (n = 30)
| Оценка чувствительности штаммов | % |
| Чувствительные (S) | 63,3 |
| Чувствительные дозозависимые (SDD) | 10 |
| Резистентные (R) | 26,7 |
Эффективность препарата
Клинико-лабораторную эффективность купирования рецидива ХРКГ, обусловленного не-albicans Candida spp., оценивали по результатам клинико-лабораторного обследования через 7 дней после окончания лечения.
У 96,7% больных результат лечения рецидива ХРКГ оценили как «хороший», у 3,3% больных – как «неудовлетворительный» (табл. 3). Лечение сочли неэффективным у больной ХРКГ, обусловленным C.glabrata. Через 7 дней после окончания лечения при микологическом исследовании выделили C.glabrata в количестве 103 КОЕ/мл. При этом было отмечено улучшение состояния пациентки (уменьшение выделений из половых путей, исчезновение зуда и жжения наружных гениталий).
Таблица 3. Жалобы и клинические проявления у больных ХРКГ, обусловленным не-albicans Candida spp., через семь дней после окончания лечения (n=30)
| Жалобы и клинические признаки | % | |
| Творожистые выделения из влагалища | 0 | Выраженные |
| 0 | Умеренные | |
| 0 | Незначительные | |
| 100 | Отсутствуют | |
| Зуд наружных гениталий | 0 | Выраженный |
| 0 | Умеренный | |
| 3,3 | Незначительный | |
| 96,7 | Отсутствует | |
| Жжение наружных гениталий | 0 | Выраженное |
| 0 | Умеренное | |
| 0 | Незначительное | |
| 100 | Отсутствует | |
| Болезненность наружных гениталий | 0 | Выраженная |
| 0 | Умеренная | |
| 0 | Незначительная | |
| 100 | Отсутствует | |
| Отечность слизистых оболочек | 0 | Выраженная |
| 0 | Умеренная | |
| 0 | Незначительная | |
| 100 | Отсутствует | |
| Гиперемия слизистых оболочек | 0 | Выраженная |
| 0 | Умеренная | |
| 0 | Незначительная | |
| 100 | Отсутствует | |
Все больные отмечали хорошую переносимость препарата и удобство применения. Только у одной пациентки (3,3%) были отмечены нежелательные явления в виде покраснения и зуда нижних конечностей на восьмой день лечения. Связь с исследуемым препаратом возможна, степень тяжести – легкая. Указанные нежелательные явления не потребовали отмены препарата, антифунгальная терапия была выполнена в полном объеме.
Таким образом, клинико-лабораторная эффективность купирования рецидива ХРКГ, обусловленного не-albicans Candida spp., составила 96,7%.
Обсуждение
Хронический рецидивирующий генитальный кандидоз остается актуальной проблемой. Это связано как с увеличением частоты заболевания, так и с появлением рефрактерных к стандартной антимикотической терапии клинических случаев заболевания.
Хронический рецидивирующий генитальный кандидоз – особая форма кандидоза гениталий, предполагающая наличие не менее четырех рецидивов в течение года. Основной причиной хронического рецидивирующего течения заболевания является дефицит компонентов местного иммунитета [13, 19]. Определенное значение в патогенезе кандидоза гениталий представляют факторы, снижающие сопротивляемость макроорганизма, например дисбиотические процессы на уровне вагинального эпителия, применение половых стероидов [12, 18, 19]. Увеличение частоты ХРКГ связывают с применением антибактериальных препаратов широкого спектра действия, распространенностью эндокринопатий (сахарный диабет, снижение функциональной активности щитовидной железы), использованием иммуносупрессивной терапии. Кроме того, отмечена тенденция к возрастанию частоты ХРКГ у женщин старшей возрастной группы в связи с применением местной и системной заместительной терапии эстрогенами [7, 12, 15, 23].
Данные о частоте ХРКГ, обусловленного не-albicans Candida spp., разноречивы как в отечественной, так и в зарубежной литературе. По результатам различных исследований частота выделения Candida spp., не относящихся к виду Candida albicans, у больных ХРКГ составляет от 8% до 69% [5, 6, 14, 22]. При изучении этиологии ХРКГ у 251 женщины, находившихся в клинике НИИ медицинской микологии им. П. Н. Каш-кина, частота выделения не-albicans Candida spp. составила 17% [4].
Известна связь вида возбудителя и его чувствительности к флуконазолу in vitro. Ранее мы установили, что 98% изолятов C. albicans, выделенных от больных ХРКГ, чувствительны к флуконазолу in vitro. Вместе с тем 42% возбудителей ХРКГ, не относящихся к виду C.albicans, были резистентны к флуконазолу in vitro [3, 4]. Поэтому случаи ХРКГ, обусловленные не-albicans Candida spp., могут быть рефрактерны к «стандартной» терапии.
Лечение ХРКГ включает купирование обострения и последующую профилактику рецидива. С этой целью обычно используют как системные, так и интравагинальные антимикотические препараты (вагинальные свечи, таблетки, кремы). Методы лечения ХРКГ, обусловленного не-albicans Candida spp., не разработаны. Одним из вариантов лечения может быть применение интравагинальных лекарственных препаратов. Предполагается, что высокие концентрации действующего вещества в очаге инфекции способны преодолеть резистентность возбудителей ХРКГ к азолам [7, 9, 11, 23].
Для ответа на этот вопрос мы провели проспективное клиническое исследование по изучению эффективности и безопасности купирования рецидива ХРКГ, обусловленным не-albicans Candida spp., с помощью вагинальных суппозиториев «Ливарол®», содержащих 400 мг кетоко-назола. Кетоконазол является азольным антимикотиком. Азолы обладают преимущественно фунгистатическим эффектом, который связан с ингибированием цитохром Р-450-зависимой 14α-деметилазы, катализирующей превращение ланостерола в эргостерол – основной структурный компонент клеточной стенки грибов. Кетоконазол активен в отношении дрожжей (Candida spp., Malassezia spp.), дерматомицетов (Trichophyton spp., Epidermophyton flocossum, Microsporum spp.), а также некоторых грамположительных кокков и коринебактерий. Известно, что длительное использование кетоконазола в качестве системного препарата может сопровождаться токсичностью, в связи с чем был разработан препарат «Ливарол®» для интравагинального применения.
В состав вагинальных суппозиториев «Ливарол®» помимо кетоконазола входит полиэтиленоксидная основа, которая способствует увлажнению слизистых оболочек и улучшает взаимодействие активного компонента препарата с вагинальными эпителиоцитами.
Ранее препарат «Ливарол®» успешно примяли для лечения острого кандидоза гениталий. По результатам проспективного открытого клинического исследования клинико-лабораторная излеченность через 7 дней после окончания лечения составила 100%, через 30 дней после окончания лечения – 96% [10].
Наиболее частыми возбудителями ХРКГ у обследованных больных были C.tropicalis (27%), C.krusei (26%), хотя в многочисленных исследованиях наиболее частый возбудитель среди не-albicans Candida spp. – C.glabrata [11, 14]. Чувствительны к флуконазолу in vitro были 63% возбудителей, резистенты - 26,7% изолятов (в том числе, все изоляты C.krusei), чувствительными дозозависимыми оказались 10% штаммов.
Клинико-лабораторную эффективность купирования рецидива ХРКГ, обусловленного не-albicans Candida spp., оценивали по результатам клинико-лабораторного обследования через 7 дней после окончания лечения.
Применение препарата «Ливарол®» для лечения рецидива ХРКГ, обусловленного не-albicans Candida spp., было эффективным у 96,7% обследованных больных, несмотря на то, что чувствительность к флуконазолу in vitro была снижена у 37% возбудителей. Отмечена хорошая переносимость препарата: не потребовавшие отмены препарата нежелательные явления в виде покраснения и зуда нижних конечностей были выявлены у 3,3% пациентов.
Исследование показало, что вагинальные суппозитории «Ливарол®» являются эффективным и безопасным препаратом для лечения рецидива хронического рецидивирующего кандидоза гениталий, обусловленного не-albicans Candida spp.
Выводы
- Возбудителями хронического рецидивирующего генитального кандидоза у обследованных больных были C.tropicalis (27%), Ckrusei (26%), Cglabrata (20%), C.parapsilosis (10%), C.dubliniensis (10%) и C.kefir (7%).
- Чувствительны к флуконазолу in vitro были 63% возбудителей (C.tropicalis, C.dubliniensis и C.parapsilosis – 100%, C.glabrata – 67%, C.kefyr – 50%). Чувствительность к флуконазолу была снижена у 37% изолятов, из них 27% были резистентны (C.krusеi – 100%), а 10% -чувствительны-дозозависимы (C.kefyr – 50%, C.glabrata – 33%).
- Эффективность применения препарата «Ливарол®» (кетоконазол 400 мг) для лечения рецидива хронического рецидивирующего генитального кандидоза, обусловленного не-albicans Candida spp., составила 96,7%.
- Применение препарата «Ливарол®» было безопасным: не потребовавшие отмены препарата нежелательные явления были отмечены у 3,3% пациентов.
ЛИТЕРАТУРА
1. Аравийский Р.А., Климко Н.Н., Васильева Н.В. Диагностика микозов. – СПб. 2004; 185 с.
2. Букетова А.Б., Шурпицкая О.А., Выборнова И.В., Мирзабалаева А.К., Климко Н.Н. Клинико-лабораторные особенности кандидоза у ВИЧ-инфицированных женщин.// Проблемы мед. микологии. – 2007. – Т. 9. - № 1. – c. 12-15.
3. Долго-Сабурова Ю.В., Мирзабалаева А.К.,Васильева Н.В., Богомолова Т.С., Выборнова И.В., Колб З.К., Шурпицкая О.А., Климко Н.Н. Клинико-лабораторные особенности хронического рецидивирующего кандидоза гениталий у женщин.// Проблемы мед. микологии. – 2005. – Т. 7. - № 3. – c.12-15.
4. Долго-Сабурова Ю.В. Клинико-лабораторные особенности хронического рецидивирующего кандидоза гениталий у женщин.// Автореферат диссертации на соискание ученой степени к.м.н. – СПб, 2006, 22 с.
5. Захарова Т.П. Вульвовагинальный кандидоз. Проблемы и решения.// Consilium medicum. Экстра выпуск. – Симпозиум «Микозы. Рациональная фармакотерапия» – 2004. – с. 10-14.
6. Кисина В.И. Рецидивирующий кандидозный вульвовагинит: перспективы лечения орунгалом (итраконазолом) //Consilium medicum-Дерматология и венерология. – 2002. – Т. 6. - № 2. – с. 5-9.
7. Климко Н.Н. Микозы: диагностика и лечение. Руководство для врачей. – Москва, 2007, 335 с.
8. Мирзабалаева А.К., Долго-Сабурова Ю.В., Кандидоз гениталий и бактериальный вагиноз в практике акушера-гинеколога // Проблемы мед. микологии. – 2004. – Т. 6. – № 3. – c. 18-24.
9. Мирзабалаева А.К. Инфекционные вульвовагиниты: клиническая проблема и пути ее решения. // Акуш. и гинек. – 2005. – № 6. – c. 51-55
10. Мирзабалаева А.К., Долго-Сабурова Ю.В., Колб З.К., Шурпицкая О.А. Климко Н.Н. Опыт применения вагинальных суппозиториев «Ливарол» у больных острым кандидозным вульвовагинитом. //Гинекология, Т. 8, № 2, 2006, с. 11-14
11. Прилепская В.Н. Отчет о клиническом исследовании препарата «Ливарол». – М, 2006.
12. Тихомиров А.Л., Олейник Ч.Г. Пробиотики в комплексном лечении кандидозного вульвовагинита.// Эффективная фармакотерапия в акушерстве и гинекологии – 2007. – № 4, с. 13-17
13. Шабашова Н.В.,Фролова Е.В. Особенности иммунитета слизистых оболочек полости рта и женской половой сферы при кандидозе // Проблемы мед. микологии. – 2005 – Т. 7, № 2. – с. 70.
14. Asticcioli S., Migliavacca R., Nucleo E. et al. Reccurent vulvovaginal candidiasis: prevalens antifungal susceptibility patterns and genotyping of different species. Clinical Мicrobiology and Infection, 2004, vol.10 (suppl. 3) p. 266 -71.
15. Eschenbach D.A., Chronic Vulvovaginal Candidiasis // N Еngl J Med 2004; 351; 911-7.
16. Jilek P., Spasek J., et al. Factors associated with reccurent vulvovaginal candidiasis dietary intake, cloting, sexual activities, personal hygiene, antibiotic use and allergies.// 3rd Trends in Medical Mycology. – 2007. – Turin., р. 99
17. Mardh P.A., Rodrigues A.G., Genc N., et al. Facts and myths on recurrent vulvovaginal candidosis – a review on epidemiology, clinical manifestations, diagnosis, pathogenesis and therapy //Int J. of STD &AIDS – 2002. – № 13 – р. 522-539.
18. Patel D.A., Gillespie B., Sobel J.D. et al. Risk factors for recurrent vulvovaginal candidiasis in women receiving maintenance antifungal therapy: results of a prospective cohort study //Am. J. Obstet and Gynecol. – 2004. – 190(3) – р. 644-653.
19. Fidel P.L., Immunity in vaginal candidiasis.// Current Opinion in Infectious Diseases 2005, 18:107-111
20. Sobel J. D. Mucocutaneous candidiasis in Infectious diseases. – 2000. – New York.
21. Sobel J.D., Zervos M., Reed B.D. et al. Fluconasol susceptibility of vaginal isolates obtained from women with complicated Cand. vaginitis: clinical implications //Antimicrob. Agents Chemother. – 2003. – Т. 47. – № 1. – р. 34-38.
22. Sobel J.D. Recurrent vulvovaginal candidiasis advances in patogenesis and treatment.//3rd Trends in Medical Mycology. – 2007. – Turin.
23. Spasek J., Buchta V., Jilek P., et al. Gestagens in the management of reccurent vulvovaginal candidiasis.// 3rd Trends in Medical Mycology. – 2007. – Turin., р. 101
