Межпозвонковые суставы и боли в спине
СтатьиОпубликовано в журнале:
«Справочник поликлинического врача», 2013, №5, с. 34-40 Р.А.Алтунбаев
Казанский государственный медицинский университет
Боль в поясничной области является одной из основных инвалидизирующих причин. Она отмечается примерно с одинаковой частотой в разных этнических популяциях, значительно снижая качество жизни и работоспособность, и остается ведущей причиной обращения за медицинской помощью. Не всегда удается выявить конкретные причины возникновения боли в спине. В подавляющем большинстве случаев алгический феномен обусловлен неспецифическими изменениями, является самоограничивающимся и в большинстве случаев регрессирует в течение 3 мес. В 20% случаев у пациентов трудоспособного возраста острая боль в спине трансформируется в хроническую. Эта группа больных характеризуется неблагоприятным прогнозом для выздоровления, что обусловливает значительные затраты здравоохранения на их лечение.
Рекомендации по лечению болевого синдрома включают в себя купирование боли, улучшение функции и повышение качества жизни.
Адекватная терапевтическая тактика должна учитывать особенности клинической картины, получившие обобщение в клинической феноменологической классификации поясничной боли.
Нужно иметь ввиду, что поясничные боли (ПБ) могут быть вторичными и иметь отраженный или локальный характер. Наиболее ответственной и требующей достаточной общей врачебной эрудиции задачей является исключение отраженного генеза ПБ при заболеваниях внутренних органов. Отраженные боли – по сути своей вторичные – могут возникать, например, при следующих заболеваниях: аневризма, тромбоз грудного или брюшного отдела аорты, патология забрюшинного пространства, урологическая, гастроинтестинальная, гинекологическая и другие патологии.
Другая категория вторичных ПБ связана с наличием вертебрального локального фокуса при некоторых общих соматических заболеваниях. В этих случаях патологические явления локализуются в самом позвоночном столбе: в его опорных образованиях (чаще костно-хрящевых, суставных, связочных), моторных (мышцах с фасциями, сухожилиях) и невральных структурах (спинном мозге и менингеальных оболочках, корешках спинномозговых нервов и образованных ими периферических нервов). Такие вторичные локальные боли могут сопровождать, к примеру, следующие болезни: бактериальный или туберкулезный спондилит, дисцит, паравертебральный, эпидуральный абсцесс, первичные опухоли и метастазы в позвоночник, остеопороз, гиперпаратиреоз, болезнь Педжета, болезнь Бехтерева, миозиты.
Иная категория ПБ – первичные боли, не связанные с патологией внутренних органов и соматическими заболеваниями с вертебральным патологическим локусом. Можно принять следующее определение первичных ПБ. Первичные поясничные боли – это острое или хроническое заболевание, имеющее определяющий патологический фокус (дисфункциональный, дистрофический, неинфекционно-воспалительный) в опорных и моторных структурах позвоночного столба и проявляющееся болевыми и другими нарушениями в области поясницы, таза и ног. Причины первичных ПБ разнообразны и имеют вертебральные, паравертебральные и экстравертебральные локусы, нередко патогенетически взаимодействующие. Этиологическое разнообразие (мультифакторность) ПБ не дает возможности найти ей морфологическую или патологическую «прописку»: в части случаев это суставы с их дистрофическими изменениями (спондилоартроз – СА, фасеточный синдром); в других – мышцы с болезненными локальными уплотнениями (триггеры при миофасциальных болях, фибромиалгии), активизирующимися среди прочих обстоятельств при изменении функционального состояния нервной системы, хронической усталости; в третьих – межпозвонковые диски (МПД) с их дистрофическими и грыжевыми изменениями, часто оказывающими патологическое воздействие на спинномозговые нервы или спинной мозг и нарушающие их функции и т.д. При этом для ПБ как нозологии часто невозможно установить ранг важности определенных анатомических образований и их патологических изменений, как и их патогенетическую очередность. Это положение оказывается справедливым и при лечении конкретных пациентов, когда терапевтическое воздействие имеет неспецифический характер или направлено на несколько патогенетических элементов. Существовавшая долгие годы парадигма остеохондроза позвоночника, рассматривающая его в качестве универсальной схемы вертеброгенных поражений нервной системы, не смогла определить наиболее полно общие типы ПБ и люмбоишиалгий (ЛИ), характеризующие их течение, клиническое неврологическое наполнение, изменения функциональных возможностей. Вместе с тем в общей врачебной и неврологической практике имеется потребность в представлении таких типов, это позволило бы разделить больных по тяжести их состояния и особенностям клинических проявлений, что способствовало бы в целом адекватному диагностическому, лечебно-организационному и экспертному выбору.
Тип 1. Острое люмбаго
Тип 1А. Острая ПБ с быстрым регрессом без выраженных двигательных дисадаптаций. (ПБ возникают неожиданно, интенсивные, быстро достигают максимума, сочетаются с непродолжительными умеренными двигательными расстройствами, относительно быстро регрессируют.)
Тип 1Б. Острая ПБ с быстрым регрессом с выраженными двигательными дисадаптациями. (ПБ возникают неожиданно, интенсивные, быстро достигают максимума, сочетаются с непродолжительными выраженными двигательными расстройствами, относительно быстро регрессируют.)
Тип 2. Люмбалгия с медленным регрессом
Тип 2А. Подострая ПБ с медленным регрессом с нарушением сгибания в пояснице. (ПБ чаще появляются после неадекватного физического усилия, нарастают в течение нескольких дней, сохраняются относительно продолжительно, сочетаются с торпидными нарушениями позвоночной статики и преимущественным нарушением сгибания в пояснице.)
Тип 2Б. Подострая ПБ с медленным регрессом с нарушением разгибания в пояснице. (ПБ чаще появляется после перетруживания, переохлаждения, нарастает подостро, сохраняется продолжительно, сочетается с торпидными нарушениями позвоночной статики с преимущественным нарушением разгибания в пояснице и вторичными миалгическими зонами в спине.)
Тип 3. Нерадикулярная ЛИ
Тип 3А. Острая или подострая ЛИ без признаков поражения спинномозговых корешков. (ПБ длительно сохраняется, сочетается с торпидными болевыми миофасциальными нарушениями в ноге).
Тип 3Б. Острая или подострая ишиалгия без признаков поражения спинномозговых корешков. (Ишиалгия – доминирующая локализация болей, длительно сохраняется, сочетается с торпидными болевыми миофасциальными нарушениями в ноге.)
Тип 4. Радикулярная «доброкачественная» ЛИ
Тип 4А. Острая или подострая ЛИ с радикулярным поражением с благоприятным течением. (Равномерно протекающая ЛИ, сочетающаяся с корешковым расстройством в поясничном и/или крестцовом дерматомиотоме.)
Тип 4Б. Острая или подострая ишиалгия с радикулярным поражением с благоприятным течением. (Равномерно протекающая ЛИ сочетающаяся с корешковым расстройством в поясничном или крестцовом дерматомиотоме и преимущественной локализацией боли в ноге.)
Тип 5. Тяжелая радикулярная ЛИ
Тип 5А. Радикулярная ЛИ с выраженным торпидными расстройствами вертебральной статикодинамики и/или двигательными дисадаптациями. (Тяжело протекающая ЛИ, сочетающаяся с выраженным моно- или бирадикулярными расстройствами в пояснично-крестцовых дерматомиотомах, требующая, как правило, нейрохирургического лечения.)
Тип 5Б. Радикулярная или полирадикулярная ЛИ с выраженным двигательными нарушениями в ноге, тазовыми нарушениями, двигательными дезадаптациями. (Тяжело протекающая ЛИ, сочетающаяся с выраженным би- или полирадикулярными (в том числе двусторонними) расстройствами в дерматомиотомах конского хвоста, тазовыми расстройствами, требующими нейрохирургического лечения.)
Тип 6. Люмбалгия с доминированием психических и поведенческих нарушений
Тип 6А. ПБ как проявление депрессии или других нарушений психики. (ПБ или ЛИ без актуальной органической причины, сочетающаяся с изменениями психики и не поддающаяся лечению непсихотропными средствами).
Тип 6Б. ПБ как проявление симуляции или аггравации (рентного поведения). (Длительно протекающая неремиттирующая ПБ или ЛИ как осознанная пациентом форма приобретения социальных выгод).
Не всегда заключение о типе ПБ у конкретного пациента можно сделать в начальных этапах обострения. Это связано с тем, что, проявившись одним типом, по мере течения болезнь приобретает новое лицо. При этом смена варианта ПБ идет от первых типов к последующим. Данное обстоятельство учтено в предложенном делении вариантов ПБ, где с увеличением нумерации связано утяжеление клинических проявлений.
Концепция вертеброгенности болей в спине построена на парадигме вертебрального трехсуставного комплекса, включающего МПД и пару дугоотростчатых суставов. Дистрофическо-дегенеративное поражение трехсуставного комплекса заключено в каскад последовательных событий, начинающихся с дистрофии хрящевых структур диска и межпозвонковых суставов, приводящих к гипермобильности и завершающихся гиперостозной стабилизацией. Каскад изменений в МПД включает разрывы фиброзного кольца, спондилолистез, появление спондилезных остеофитов, стенозирование центральной и латеральной частей позвоночного канала. Каскад изменений в межпозвонковых суставах включает синовиальную реакцию, дегенерацию хряща, капсулярную разболтанность, подвывихи, формирование остеофитов и гипертрофию фасеток.
В рамках дегенеративного каскада могут развиваться разные варианты болевого синдрома, ассоциированные как с формированием грыжи МПД, так и с поражением фасеточных суставов. Преимущественное поражение передних отделов трехсуставного комплекса (МПД) характеризуется появлением или усилением боли при наклоне вперед (флексии поясничного отдела), что соответствует 2А клиническому типу ПБ (см. выше). Преимущественное поражение задних отделов трехсуставного комплекса (межпозвонковых суставов) характеризуется появлением или усилением боли при наклоне назад (экстензии поясничного отдела), что соответствует 2Б клиническому типу ПБ. Формированию этого типа болей способствуют анатомические особенности строения межпозвонковых суставов: наличие излишней округлости формы суставной щели в нижнепоясничных сегментах (рис. 1), нарушение суставного тропизма (сагиттальность суставной щели) в пояснично-крестцовом переходе (рис. 2).
Рис. 1. Округлая и плоская форма межпозвонковых суставов.
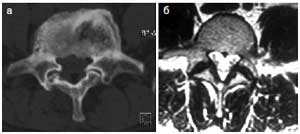
Рис 2. Нарушение суставного тропизма (стрелками показано разное направление суставной щели).
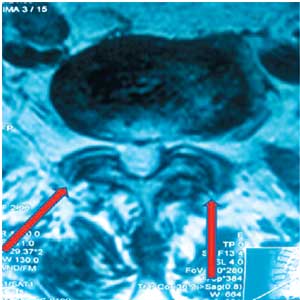
Болевые проявления при комплектном поражении трехсуставного комплекса характеризуются симметричным характером боли, утренней скованностью и/или тугоподвижностью в пояснице, ощущением хруста при разгибании, усилением болей при разгибании и стоянии, облегчением болей при ходьбе и сидении, а также хронизацией течения.
Развитию хронического болевого синдрома, формированию рецидивирующих болевых ощущений способствует образование спаек в эпидуральном пространстве на фоне грыжевых выпячиваний диска и реактивного синовита дугоотростчатых суставов (СА–артрита) на фоне функциональных и органических блокировок межпозвонковых суставов.
СА представляет собой локальное проявление дистрофическо-дегенеративного процесса в межпозвонковых синовиальных гиалиновых суставах. Некоторые исследователи считают, что СА – одна из самых частых причин болей в пояснице, особенно у пожилых лиц. При артрозе фасеточных суставов боль обычно двусторонняя, локализуется латерализованно от средней линии, усиливается при разгибании, длительном стоянии, а уменьшается при разминке, ходьбе и сидении.
В основе СА лежит дегенерация и деструкция суставного хряща, происходящая из-за несоответствия между механическим (часто ударным) воздействием на суставную поверхность хряща и его способностью (складывающуюся из генетических и средовых факторов) выдерживать это воздействие Существенные патоморфологические изменения при СА разворачиваются в хрящевом матриксе, вызывая эрозию хряща, разрушение коллагеновых волокон и деградацию протеогликана – белковополисахаридных комплексов, обеспечивающих стабильность структуры коллагеновой сети хрящевого матрикса.
В инициальной стадии СА в местах наибольшей нагрузки образуются зоны размягчения хряща, на более поздних стадиях происходит его фрагментация с образованием вертикальных трещин, фрагментов, которые попадают в полость сустава в виде детрита.
Клиническая картина и диагностика СА
Среди разнообразных клинических проявлений СА основными можно считать боль, болезненность и ограничение подвижности в том или ином отделе позвоночника, а подчас и в каждом из них. Причины формирования болевых феноменов имеют разнообразные патологические и патофизиологические механизмы: так фактор воспаления связан с поражением энтезисов, субхондральной кости, синовиальной оболочки и суставной капсулы; механическое растяжение связок и суставной капсулы, а также воздействие со стороны остеофитов провоцирует раздражение болевых рецепторов; в самой субхондральной кости болезненные явления могут быть связаны с медуллярной гипертензией; продолжительное иммобилизирующее напряжение околосуставных мышц достаточно быстро становится автономным источником боли.
Клиническая характеристика болей при СА также разнообразна как по продолжительности, так и обстоятельствам их проявлений. Различают кратковременные – до 30 мин, «стартовые боли», возникающие после периодов покоя, проходящие на фоне «разминки» и обусловленные трением суставных поверхностей, на которых оседает детрит – фрагменты хрящевой и костной деструкции. При повторных движениях в суставе детрит выталкивается в завороты суставной сумки, и движения облегчаются. Вечерние механические боли возникают под влиянием дневной физической нагрузки и стихают после ночного отдыха; такие боли связаны со снижением амортизационных качеств хряща субхондральной кости. Ночные продолжительные тупые боли связаны с венозным стазом в субхондральной кости и повышением внутрикостного давления. Постоянные продолжительные перемежающиеся боли обусловлены развитием реактивного синовита, а также рефлекторным спазмом прилежащих мышц.
На разных стадиях течения СА преимущественное патогенетическое значение имеют разные механизмы: на начальных стадиях, при явлениях синовита, боли в спине возникают как при движении, так и в покое, отмечаются утренняя скованность, ощущение припухлости в области позвоночника. По мере прогрессирования заболевания развиваются деформация и тугоподвижность позвоночника за счет фиброзно-склеротических и дистрофических изменений параартикулярных тканей. Функциональные вертебральные нарушения на ранней стадии СА обусловлены болевым синдромом и ограничивающим болезненные движения спазмом мышц. На более поздних стадиях болезни развиваются сухожильно-мышечные контрактуры, гиперостозы и нарушение конгруэнтности суставных поверхностей, что ведет к усугублению ограничения подвижности.
Патофизиологические механизмы формирования болевых синдромов в области позвоночника разнообразны: ноцицептивные боли связаны с раздражением ноцицепторов в капсулах суставов, связок, мышцах позвоночника, в периосте позвонков, в наружной трети фиброзного кольца МПД. Мышечный спазм приводит к накоплению эргических метаболитов, отеку, гипоксии мышечной ткани. Нейропатические боли вызваны механическим и воспалительным повреждением корешков спинномозговых нервов, а также неврогенным асептическим воспалением при периферической сенситизации хронизирующихся болей. Дисфункциональные боли обусловлены центральной сенситизацией при хроническом мышечном спазме и истощением центральных антиноцицептивных механизмов.
При доминировании роли межпозвонковых суставов в клинических болевых и невральных проявлениях нозографически выделяют фасеточный синдром. Клинические варианты фасеточного синдрома включают следующие проявления:
- Дорзалгия в форме локальных проявлений: цервикалгия, торакалгия, люмбалгия, сакралгия, люмбалгия, сакралгия с ишиалгией.
- Радикулопатия на фоне фораминального стеноза.
- Радикулопатия (радикулоалгия) верхней суставной фасетки (синдром Эпштейна).
- Синдром клаудикации (перемежающейся хромоты).
Дорзалгические варианты фасеточного синдрома характеризуются усилением боли при разгибании, усилением их при статических нагрузках, локальной асимметричной болезненностью при пальпации.
Фораминальный стеноз и связанное с ним повреждение корешка развиваются в верхнем этаже рецессуса позвоночного канала (рис. 3).
Рис. 3. Этажи латерального рецессуса позвоночного канала.
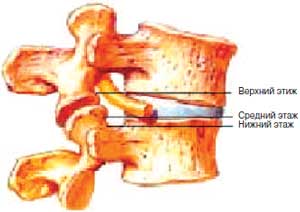
Травматизация корешка в виде продолжительного стабильного воздействия возможна: гипертрофированной нижней фасеткой, подвывихом нижней фасетки, остеофитами фасеток, остеофитами тела позвонка.
Клинические проявления повреждения корешка при латеральном стенозе позвоночного канала характеризуются:
- монорадикулярным синдромом с типичной соматотопической иррадиацией;
- отрицательным симптомом Ласега и другими симптомами натяжения;
- малой эффективностью консервативного лечения, в особенности нестероидными противовоспалительными препаратами (НПВП).
Радикулопатия (радикулоалгия) верхней суставной фасетки (синдром Эпштейна) представляет собой ишиалгию, вызванную «ловушкой» нерва в латеральном рецессусе (рис. 4). При этом происходит проникновение верхнего суставного отростка нижележащего позвонка в верхний этаж бокового рецессуса (см. рис. 4, стрелка). Повреждение корешка также возможно при воздействии остеофита или подвывиха (сублюксации) верхнего суставного отростка нижележащего позвонка.
Рис. 4. Формирование синдрома Эпштейна (верхней суставной фасетки, по А.И.Продан, 1992): 1 – суставная щель, 2 – нижний суставной отросток вышележащего позвонка, 3 – хрящевая поверхность отростка, 4, 6 – элементы капсулы сустава, 5 – спинномозговой нерв (нерв Нажотта), 7 – желтая связка, 8 – верхний суставной отросток нижележащего позвонка, стрелкой показано направление его проникновения в верхний этаж (корешковый канал).
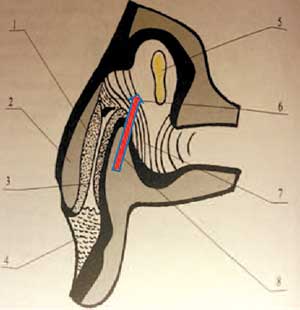
Синдром клаудикации (перемежающейся хромоты) при фасеточном синдроме развивается чаще у 50–60-летних мужчин. Больные предъявляют жалобы на онемение и слабость в ногах, проявляющиеся только при ходьбе или продолжительном стоянии. Болевые субъективные феномены характеризуются как «окоченение», «одеревенелость», «ватность ног». Примечательно, что для уменьшения болей при ходьбе пациенты используют остановки с легким сгибанием ног в тазобедренных и коленных суставах и наклоном тела вперед, иногда прибегая к сгибанию «калачиком». Иногда имеются легкие тазовые расстройства. При этом рутинное неврологическое обследование не выявляет объективных парезов и расстройств чувствительности. Предполагается, что причина такой клаудикации – динамическое усиление стеноза латеральной части позвоночного канала с нарушением венозного спинального оттока при дополнительных ротациях позвоночно-двигательного сегмента при ходьбе. Нельзя также исключить увеличение протрузии МПД с дополнительным воздействием на корешки при гиперэкстензии и уменьшение при вынужденном положении сгибания позвоночника. Рассматривается участие в проявлении перемежающейся хромоты сосудистых механизмов, связанных с усилением кровотока по радикулярным артерии и вене с их полнокровием и дополнительным воздействием на корешок при латеральном стенозе, а также с перемежающимся сдавлением радикуломедулярной артерии в стенозированном корешковом канале.
Существенным в диагностике СА является рентгенологическое исследование позвоночника. В настоящее время выделяют:
а) облигатные рентгенологические признаки: сужение суставной щели, остеофиты, субхондральный остеосклероз (рис. 5);
Рис. 5. Облигатные признаки СА.
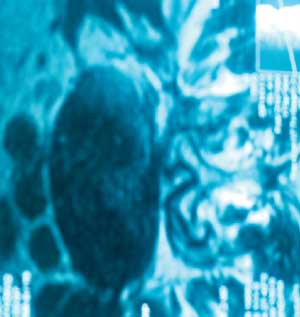
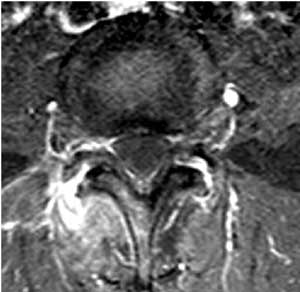
б) дополнительные рентгенологические признаки: околосуставной краевой дефект костной ткани, субхондральные кисты, внутрисуставные обызвествленные хондромы, периартикулярные воспалительные реакции (рис. 6).
Рис. 6. Периартикулярные воспалительные реакции.
Клиническая картина СА определяется локализацией суставов, вовлеченных в патологический процесс, и часто сочетается с остеоартрозом суставов конечностей, часто с коксартрозом и гонартрозом.
Симптоматическое и патогенетическое лечение СА объединяет немедикаментозные и медикаментозные подходы. Немедикаментозное воздействие использует:
- двигательную активность – обучение в «школе здоровой спины», лечебная физкультула, йога, пилатес, фитнес, ортезы, корсеты;
- экстероцептивную стимуляцию – иглорефлексотерапия, физиотерапия.
Медикаментозное воздействие использует: ноцицептивное обезболивание (НПВП), нейропатическое обезболивание (антиконвульсанты, антидепрессанты), миорелаксанты, стимуляторы нейромышечной активности, метаболические активаторы (витамины, нейропептиды), лечение остеопороза (Са, D3, бисфосфонаты), а также структурно-модифицирующее лечение (хондропротекторы: глюкозамин + хондроитин).
Патогенетические препараты замедленного действия для лечения СА (symptomatic slow acting drug in osteoarthritis – SYSADOA) – собирательное название группы лекарственных средств, включающей глюкозамина сульфат и его производные, хондроитина сульфат и диацерин, неомыляемые соединения авокадо и сои. Исследования, подтверждающие эффективность глюкозамина сульфата и хондроитина сульфата (ХС), отнесены к высокой 1А категории доказательности.
ХС относится к соединениям, классифицируемым как гликозаминогликаны (ГАГ). ХС сформирован на основе объединения чередующихся остатков сульфатированных и/или несульфатированных остатков глюкуроновой кислоты и N-ацетилгалактозамина в полисахаридные цепи. Из-за биохимического разнообразия дисахаридов, включенных в первичную структуру цепи полисахарида, ХС рассматривают как гетерогенную группу соединений, имеющих разную молекулярную массу и удельный вес. ХС обеспечивает субстрат для синтеза протеогликанов и способствует увеличению ГАГ во внеклеточном матриксе хряща, ингибирует деградацию протеогликанов и стимулирует регенерацию хряща после его повреждения.
Препарат Артра, содержащий 0,5 г ХС и 0,5 г глюкозамина гидрохлорида, представляет оптимальное средство для лечения остеоартроза и, в частности, СА. Эффекты Артры по влиянию на хрящ представлены в таблице.
Эффекты по влиянию на хрящ препарата Артра
| Особенности влияния на хрящ | ХС | Глюкозамин |
| Анаболические эффекты |
|
|
| Антикатаболические эффекты | Ингибирует гиалуронидазу, а также ИЛ-1-зависимый синтез коллагеназы и активность агреканазы | Ингибирует коллагеназу, фосфолипазу А2, стромелизин и агреканазу |
Примечание. ПГ – простагландин, ИЛ – интерлейкин.
Широкомасштабное отечественное исследование эффективности и безопасности Артра в лечении неспецифических пояснично-крестцовых болей охватило 2344 пациентов (В.В.Алексеев, Л.И.Алексеева, 2013). В процессе лечения Артрой за 3 мес боль в покое с 5,2 балла (по визуальной аналоговой шкале – ВАШ) в исходном состоянии снизилась до 1,4 балла. Боль при движении достоверно уменьшилась с 6,7 до 2,3 балла. Индекс инвалидизации значимо уменьшился у 75% больных. Потребность в НПВП снизилась с 63,5 до 6,7% пациентов. Полученные результаты указывают на то, что хондропротекторы, в частности артра, помимо их доказанной активности в отношении симптомов остеоартроза, также оказываются высокоэффективными и при терапии хронической пояснично-крестцовой боли.
При использовании Артры важен режим дозирования: приступая к лечению, мы рекомендуем прием по 1 таблетке 2 раза в день в течение 1 мес, затем по 1 таблетке в день 2 мес. Согласно инструкции по медицинскому применению, непрерывный прием препарата должен составлять 6 мес, однако наш опыт показывает, что нередко бывает достаточно и трех. В последующем после 3-месячного перерыва рекомендуем прием по 1 таблетке (или по 2 таблетки в зависимости от массы тела и тяжести остеоартроза) в день 3 мес, чередуя в последующем 3-месячные периоды приема препарата и лекарственных «каникул».
Последующая стратегия длительности использования Артры основывается на оценке эффективности и комплаенса. При этом необходимо иметь ввиду и акцентировать внимание пациента на признании положительного эффекта уже при стабилизации (непрогрессировании) клинических проявлений.
