Грандаксин как возможная альтернатива заместительной гормональной терапии
СтатьиОпубликовано в журнале, Вестник, 2000;3:67-69 А.Н. Стрижаков, Н.М. Подзолкова, О.Л. Глазкова, Е.Н. Романова
Кафедра акушерства и гинекологии №2 лечебного факультета Московской медицинской академии им. И.М. Сеченова
Медицинские и социальные аспекты естественной и искусственной менопаузы являются одними из основных тем медицинских публикаций последних лет. Это обусловлено рядом факторов, и прежде всего- широкой распространенностью климактерического синдрома и синдрома удаленных яичников, а также их выраженным негативным влиянием на основные показатели качества жизни больных [6]. Общепризнано, что не только хирургическое выключение функций яичников, но и возрастные инволютивные процессы являются мощными стрессовыми факторами, которые неизбежно запускают адаптивные реакции различных органов и систем организма - адекватные у здоровых женщин и патологические у больных. Помимо эндокринных сдвигов обязательными компонентами этих реакций становятся вегетативные и психоэмоциональные расстройства, центральным координатором и морфологической основой которых являются структуры лимбико-ретикулярного комплекса [5]. Многообразные и на первый взгляд разнородные клинические проявления климактерического и посткастрационного синдромов, такие как приливы жара, гипергидроз, ознобы, сердцебиение, нарушения сна, депрессия, немотивированная слабость и др., в настоящее время объединяют термином "синдром вегетативной дистонии", который, по мнению A.M. Вейна и соавт. [2,3], включает в себя проявление всех форм вегетативной дизрегуляции.
На протяжении последних 10 лет "золотым стандартом" в лечении климактерического синдрома и синдрома удаленных яичников по праву считают заместительную гормональную терапию, эффективность которой при длительном курсовом применении чрезвычайно высока [5]. Тем не менее, известно, что абсолютно все гормональные препараты, рекомендованные женщинам в пре- и постменопаузальный периоды, имеют достаточно большое число противопоказаний и побочных эффектов. Кроме того, сознательный отказ женщины от их применения может быть мотивирован материально-финансовыми проблемами, страхом перед онкологическими заболеваниями, увеличением массы тела и, наконец, реальной возможностью появления нерегулярных маточных кровотечений, крайне нежелательных для больной.
Поэтому абсолютно оправданно стремление врачей из всего многообразия существующих лекарственных средств выбрать те, которые по своей безопасности, эффективности и доступности могли бы конкурировать с препаратами для гормональной заместительной терапии, а следовательно, рассматриваться в качестве разумной ее альтернативы. Мы полагаем, что одним из таких лекарственных средств является тофизопам, или Грандаксин (фирма "Эгис", Венгрия). По своему фармакологическому действию он занимает промежуточное положение между "малыми транквилизаторами" и слабыми психоэнергетическими препаратами. Оказывая селективное анксиолитическое действие и обладая выраженной вегетокорригирующей и психостимулирующей активностью, Грандаксин эффективно купирует основные проявления синдрома "вегетативной дистонии" [4], который является неотъемлемой составляющей и своеобразной "визитной карточкой" климактерического и посткастрационного синдромов. Мы обследовали 30 женщин в возрасте от 40 до 50 лет, 13 из них - в постменопаузе с выраженными проявлениями климактерического синдрома и 17- после тотальной или субтотальной гистерэктомии с одно- или двусторонней аднексэктомией, произведенной более 6 мес назад по поводу миомы матки и/или аденомиоза. Тяжесть течения посткастрационного и климактерического синдромов определяли на основании подсчета менопаузального индекса Куппермана. Тонус вегетативной нервной системы оценивали с помощью "Схемы исследования для выявления вегетативной дисфункции" [2]. Личностную и реактивную тревожность изучали по шкале Спилбергера в модификации Ю.Л. Ханина (1976). Динамику состояния здоровья женщины на фоне терапии исследовали с помощью визуально-аналоговых шкал (ВАШ). Все показатели регистрировали дважды - до и непосредственно после курса лечения Грандаксином. Оценку эффективности терапии проводили по следующим критериям: "хорошо" (уменьшение индекса Куппермана более чем на 40%), "удовлетворительно" (уменьшение индекса на 15-30%), "без эффекта" (уменьшение не более чем на 10%), "хуже" (увеличение балльной оценки). Полученные в процессе исследования цифровые данные обработаны на компьютере типа IBM PC/AT с помощью стандартных статистических программ в соответствии с общепринятыми для медицинских исследований критериями.
При фоновом исследовании у всех женщин выявлены различного рода нейровегетативные и психоэмоциональные нарушения. В клинической картине заболевания доминировали жалобы на выраженную эмоциональную лабильность (100%), снижение работоспособности (80%), неполноценный прерывистый сон (100%), немотивированную тревогу или даже страх (70%). Большинство обследованных (80%) выражали сильное беспокойство состоянием своего здоровья, каждая 5-я (20%) женщина указывала на полную апатию, объясняя ее плохим самочувствием (80%), семейными неурядицами (67%), неудовлетворенностью половой жизнью (83%). Исходные значения индекса Куппермана у 9 (30%) больных в среднем составили 15,3 балла, у 12 (40%) - 26,0 баллов и у 9 (30%) - 31,3 балла, что позволило оценить тяжесть течения климактерического синдрома в соответствии с общепринятой градацией как легкую, средней тяжести и тяжелую.
Наиболее выраженные нейровегетативные и психоэмоциональные нарушения, а также повышенный уровень тревожности отмечены у женщин пременопаузального возраста после хирургического вмешательства в объеме пангистэктомии (более 80% по схеме A.M. Вейна и 8,2 балла по шкале Спилбергера). У пациенток с климактерическим синдромом эти показатели, соответственно, 30% и 6,8 балла. Очевидно, временное совпадение радикального хирургического вмешательства с естественной возрастной инволюцией усугубляет биологическую трансформацию организма, приводя к срыву хорошо налаженных защитно-приспособительных механизмов и как следствие - к нарастанию тяжести нейровегетативных и психоэмоциональных нарушений.
Всем 30 больным с диагностированным климактерическим или посткастрационным синдромом назначали стандартизованную монотерапию Грандаксином по 50 мг 2 раза в день непрерывно в течение одного месяца. Контрольные исследования подтвердили высокую терапевтическую эффективность препарата в отношении синдрома вегетативной дистонии, обусловленного эстрогенной недостаточностью. Так, хорошие и удовлетворительные результаты лечения отмечены, соответственно, у 67 и 31% обследованных: лечение было неэффективным только в 2% наблюдений. При оценке степени редукции отдельных симптомов климактерического и посткастрационного синдромов (рис.1) наилучшие результаты получены в отношении эмоциональной лабильности (на 80%), нарушений сна (на 75%), матеозависимости (на 30%).
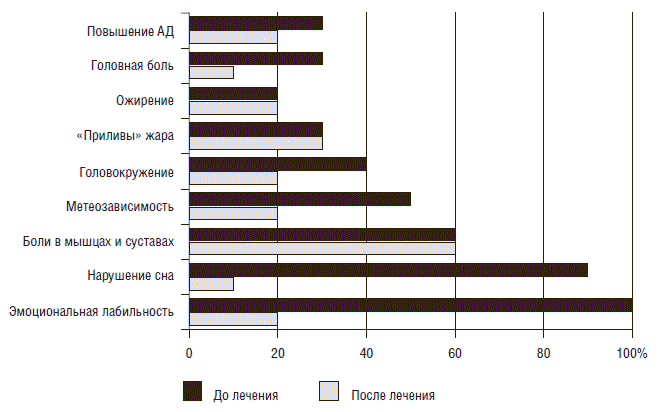
Рис. 1. Динамика основных клинических проявлений климактерического и посткастрационного синдромов на фоне монотерапии Грандаксином
Вместе с тем, Грандаксин практически не оказал влияния на частоту "приливов", однако уменьшил их интенсивность и существенно нивелировал эмоционально-негативное их восприятие. Суммарная оценка менопаузального индекса Куппермана после лечения снизилась более чем на 50%, прежде всего за счет купирования (частичного или полного) нейровегетативных и психоэмоциональных нарушений (рис.2).
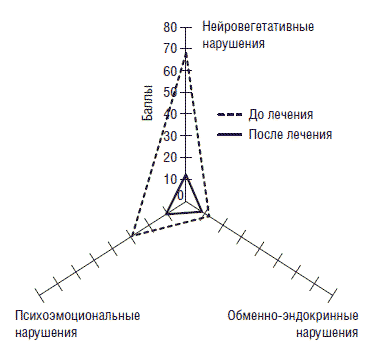
Рис. 2. Влияние монотерапии Грандаксином на степень тяжести климактерического посткастрационного синдрома (динамика индекса Куппермана)
По нашим данным, уже через 10 дней от начала лечения достоверно снизились показатели личностной и реактивной тревожности (по тесту Спилбергера), возрастала субъективная оценка состояния здоровья (по ВАШ). К окончанию месячного курса терапии наметившаяся положительная тенденция не только сохранилась, но и прогрессировала: в частности более чем на 40% снизился уровень тревожности больных (рис. 3), практически в 2 раза улучшилась оценка состояния здоровья (рис. 4), уменьшилась степень выраженности и сузился спектр разнообразных вегетативных нарушений (рис.5).
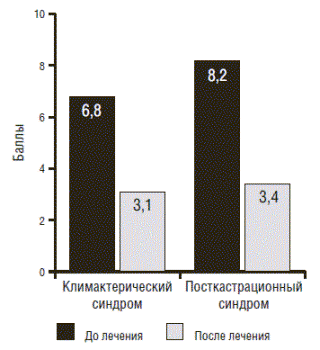
Рис. 3. Динамика уровня тревожности у больных с климактерическим и посткастрационным синдромом под влиянием монотерапии Грандаксином
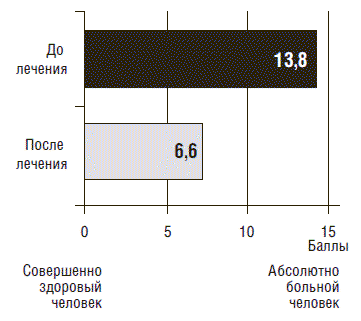
Рис. 4. Динамика состояния здоровья при лечении Грандаксином (визуально-аналоговые шкалы)
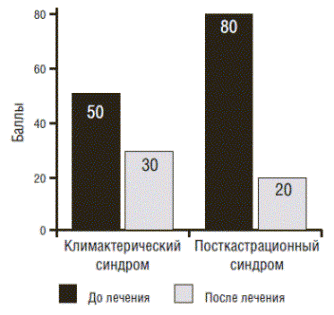
Рис. 5. Динамика суммарной балльной оценки вегетативных расстройств при терапии Грандаксином
Отдельно следует отметить хорошую переносимость препарата. Ни в одном из наших наблюдений не выявлено побочных эффектов Грандаксина, которые существенно ограничили бы привычный ритм жизни больных, послужили бы поводом к немедленной отмене или снижению дозы препарата. Однако необходимо обратить внимание на то, что эффективность лечения в целом зависит от продолжительности климактерического и посткастрационного синдромов. Оптимальные результаты монотерапии Грандаксином нами отмечены при длительности заболевания не более 3 лет и преобладании в клинической картине эмоционального характера. Вероятно, при более длительном анамнезе (более 3 лет) постепенно нивелируется грань между функциональными и органическими нарушениями, вследствие чего большинство клинических компонентов синдрома вегетативной дистонии со временем становятся типичными симптомами вполне конкретных соматических заболеваний: артериальной гипертензии, ишемической болезни сердца, атеросклероза и т.д. Бесспорно, эффективное лечение любого из этих заболеваний возможно только по средством комплексной патогенетической терапии, одним из компонентов которой может стать Грандаксин [1].
Таким образом, проведенные исследования показали высокую эффективность монотерапии Грандаксином нейровегетативных и психоэмоциональных нарушений у больных пременопаузального возраста с клинической картиной климактерического или посткастрационного синдрома. Оптимальные результаты лечения получены у женщин с длительностью заболевания менее 3 лет и преобладанием в клинической картине вегетативно-эмоциональных нарушений перманентного или пароксизмального характера. Отсутствие у Грандаксина побочных эффектов и способности вызывать лекарственную зависимость позволяет рекомендовать его для применения в амбулаторных условиях.
Литература
1. Александровский Ю.А., Аведисова А.С., Павлова М.С.Тер. Арх. 1998;70(10):76-78.
2. Вейн A.M. и др. Руководство по заболеваниям вегетативной системы. М, 1991.223 с.
3. Вейн A.M. и др. Вегетативные расстройства: клиника, диагностика, лечение. М, 1998.176 с.
4. Вейн А.М; Артеменко А.Р., Окнин В.Ю., Поморцева И.В. Фармакотерапия. 1999;(6):41 -45.
5. Сметник В.П., Тумилович Л.Г. Неоперативная гинекология. М, 1997. с. 592.6. Стрижаков А.Н. и др. Анн.Хир. 1998(94)56-60.


