Диеногест и трипторелин одинаково эффективны в лечении эндометриоза после лапароскопической операции: результаты проспективного многоцентрового рандомизированного исследования
СтатьиОпубликовано в журнале
Fertility and sterility, Vol. 77, No. 4, April 2002
Michel Cosson, M.D.,a Denis Querleu, M.D.,a Jacques Donnez, M.D.,b Patrick Madelenat, M.D.,c Philippe Koninckx, M.D.,dAlain Audebert, M.D.,e HubertManhes, M.D.f
Department of Gynecologic Surgery, Maternite Jeanne de Flandres, Лилль, Франция; HJniversite Catholique de Louvain, Clinique Universitaire St. Luc, Service de Gynecologie Obstetrique, Брюссель, Бельгия; cService Gynecologie Obstetrique, Hopital Bichat-Claude Bernard, Париж, Франция; d Gasthuisberg University Hospital, Левен, Бельгия; e Centre Hospitalier Bordeaux, Service Gynecologie, Бородо, Франция; f Service Gynecologie Obstetrique, Clinique de la Pergola, Виши, Франция.
Цель.
Сравнение эффективности Диеногеста и Декапептила® в дозе 3,75 мг в комплексной терапии послеоперационного лечения эндометриоза.
Структура исследования.
Многоцентровое открытое рандомизированное клиническое исследование параллельных групп.
Участники.
Добровольцы в научно-исследовательском окружении.
Пациенты.
Женщины с эндометриозом 2, 3 и 4 (≤70) степени, выявленным при начальной лапароскопии.
Лечение.
В течение 16 недель женщины получали Диеногест (по 1 таблетке ежедневно) или Декапептил® (3,75 мг в/м каждые 4 недели).
Оценка исходов.
Изменение степени эндометриоза по данным лапароскопии после лечения в соответствии с пересмотренной классификацией Американского общества фертильности.
Результаты.
С июня 1994 по июль 1998 года к исследованию привлекались 142 пациентки. После исключения некоторых из них из-за значительных нарушений протокола, группа, получающая Диеногест, насчитывала 59, а группа, получавшая Декапептил - 61 женщину. Обе группы были сравнимы по исходным показателям - демографическим и клиническим характеристикам, средней продолжительности эндометриоза, его степени по пересмотренной шкале Американского общества фертильности и интенсивности боли по визуально-аналоговой шкале (ВАШ). Статистические различия в эффективности лечения между группами отсутствовали. Побочные эффекты отмечали 87,7% женщин группы Диеногеста и 85,1% группы Декапептила®. Оба препарата не влияли ни на вес тела, ни на жизненно важные показатели.
Заключение.
Диеногест столь же эффективен, как Декапептил®, в консолидационной терапии после хирургического лечения эндометриоза. Профили безопасности Диеногеста и Декапептила® (3,75 мг) различны. Диеногест составляет альтернативу аналогам ГнРГ. (Fertil Steril 2002;77:684 -92. ©2002 by American Society for Reproductive Medicine.)
Ключевые слова:
рандомизированное исследование, эндометриоз, агонист ГнРГ, прогестины.
Эндометриозом страдают 2-3% всего женского населения и до 15-30% женщин с первичным или вторичным бесплодием (1). Гипоэстрогения или гиперандрогения способствует регрессии эндометриозных очагов (2,3). Поэтому при эндометриозе применяют ряд антигонадотропных и антиэстрогенных препаратов. Вместо Данатрола® и прогестинов, обладающих анаболической и андрогенной активностью, в настоящее время используют аналоги ГнРГ (4-7). Недавно предложены прогестины с минимальной андрогенной активностью (7), но их сравнение с аналогами ГнРГ в рандомизированном исследовании не проводилось. Диеногест (17ɑ-цианометил-17β-гидроксиэстра-4,9-диен-3-он), выпускаемый компанией Schering, представляет собой синтетический прогестин - производное 19-норстероидов. Его фармакологический профиль сходен с таковым производных прогестерона (17-гидрокси- или 19-нор-прогестерона). Цель нашего исследования - сравнение эффективности Диеногеста и аналога ГнРГ в консолидационной терапии после оперативной лапароскопии. В качестве аналога ГнРГ использовался трипторелин (Декапептил®) 3,75 мг - широко применяемый эффективный и безопасный препарат (8,9).
Методы
Данное иссследование является III фазой многоцентрового открытого рандомизированного исследования больных эндометриозом 2-4 степени по пересмотренной классификации Американского общества фертильности (rAFS) (≤70 баллов), которым производили оперативную лапароскопию. Пациенткам основной группы было предписано принимать внутрь Диеногест по 1 мг дважды в сутки в течение 16 недель. Пациенткам контрольной группы каждые 4 недели на протяжении того же периода в/м вводили трипторелин в дозе 3,75 мг. Эффективность послеоперационной консолидационной терапии оценивали клинически и по данным контрольной лапароскопии.
Критериями включения в исследование служили возраст от 18 до 40 лет и наличие эндометриоза, подтвержденного при диагностической лапароскопии (Лап. 0) независимо от исходных симптомов. Согласно rAFS, у больных имелся эндометриоз 2 (6-15 баллов), 3 (16-40 баллов) или 4-й степени (16-40 или ≤70 баллов). Пациентки не должны были получать никакой гормональной терапии как минимум в течение 3 месяцев до включения в исследование.
Из исследования исключались больные с какими-либо противопоказаниями к лапароскопии или лечению синтетическими прогестинами (тромбофлебит, инфаркт миокарда, нарушения мозгового кровообращения, гепатит, сахарный диабет или дислипидемия в анамнезе, текущая беременность или маточные кровотечения неясной этиологии).
В течение 3 месяцев до диагностической лапароскопии не разрешалось использовать гормональные препараты, будь то природные или синтетические эстрогены, за исключением местного применения эстрогенов. Не разрешалось применять Даназол, аналоги ГнРГ или комбинированные пероральные контрацептивы (эстрогены/прогестины). В случаях, когда пациентки ранее принимали пероральные контрацептивы, у них до начальной лапароскопии должны были иметь место по меньшей мере два регулярных спонтанных цикла. О тяжелых побочных эффектах требовалось немедленно сообщать исследователю. Эффективность терапии оценивали по данным повторного клинического обследования (изменение интенсивности боли и общего самочувствия) и повторной лапароскопии (число баллов по rAFS и ВАШ). ВАШ - это визуально-аналоговая шкала, учитывающая распространенность очагов эндометриоза, наличие спаек, подвижность маточных труб и воспалительные изменения. Безопасность лечения оценивали по клиническим показателям и анализам крови.
Подготовка к исследованию проходила три стадии (рис. 1): клиническую (V1), на которой пациенток с подозрением на эндометриоз проверяли на соответствие критериям включения; лапароскопическую и стадию анализов крови. Лапароскопическая стадия включала диагностический этап (Лап. 0) для определения степени эндометриозных повреждений по rAFS (rAFS 0) и ВАШ (ВАШ 0) и лечебный этап (Лап. 1).
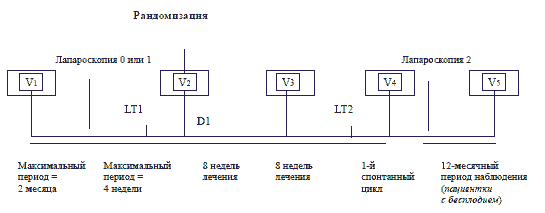
V1 - отборочный визит; Лап. 1 - диагностическая лапароскопия (rAFS 0) + (ВАШ 0) + лечебная лапароскопия (rAFS 1); LT1 -анализы крови (в клинике);
V2 - визит, при котором у пациенток с нормальными лабораторными показателями получали информированное согласие и включали их в исследование (рандомизация); D1 - первый день менструаций (цикл после лапароскопии) - начало медикаментозной терапии;
V3 - визит на втором месяце; LT2 - проверка лабораторных анализов (в клинике);
V4 - визит на четвертом месяце (оценка общего состояния пациета); Лап. 2 - контрольная лапароскопия (rAFS 2, ВАШ 1) и общая оценка исследователями;
V5 - визит через 12 месяцев после отмены медикаментозного лечения (для ранее бесплодных пациенток).
Группа 1: Диеногест (по 1 таблетке утром и вечером) 16 недель
Группа 2: Декапептил® 3,75 (одна в/м инъекция каждые 4 недели) 4 инъекции
Тяжесть эндометриоза после операции (rAFS 1) служила исходным показателем до начала любого терапевтического вмешательства. Анализы крови позволяли убедиться в отсутствии противопоказаний к исследованию у пациентов, удовлетворяющих клиническим и лапароскопическим критериям включения.
На втором визите (V2) больных случайным образом распределяли по группам терапии. Рандомизация производилась централизованно, лечебным центрам присваивались номера от 1 до 8. Исследователь и пациентка узнавали о виде лечения только после принятия решения о включении. Диеногест выдавали больным по 1 мг в покрытых пленкой таблетках, а Декапептил® - в шприцах для в/м инъекций (содержащих по 3,75 мг трипторелина). Предписывалось принимать Диеногест внутрь по две 1-мг таблетки ежедневно (одну утром и одну вечером) в течение 16 недель, а Декапептил® - по одной в/м инъекции (3,75 мг) каждые 28 дней на протяжении 16 недель (всего 4 инъекции).
Пациентки группы Диеногеста начинали лечение на 1 и 2-й день цикла после лапароскопии. Больным группы Декапептила® инъекции производились амбулаторно квалифицированными медсестрами. Первую инъекцию Декапептила® пациентки получали на 1 и 2-й день цикла после лапароскопии, или начиная с 24-го дня цикла после лапароскопии, согласно решению исследователя (рис. 2).
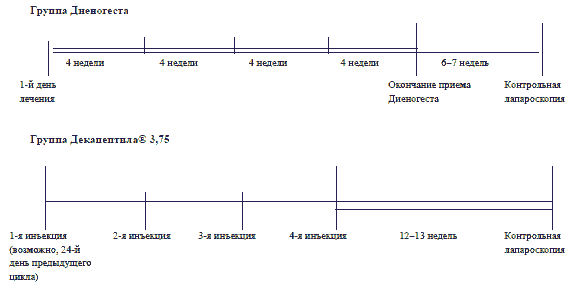
Общая интенсивность боли оценивалась на 3 и 4-х визитах (V3 и V4). Проводилось повторное тазовое обследование для выявления любых изменений в положении, чувствительности, подвижности, размеров матки и придатков, болезненности в области дугласова пространства или маточно-крестцовых связок. До начала лечения и через 16 недель в крови определяли липидный профиль (общий холестерин, триглицериды, холестерин липопротеинов высокой и низкой плотности), уровень глюкозы натощак, сывороточные трансаминазы (АСТ, АЛТ), γ-ГТ и щелочную фосфатазу.
По окончании лечения в фолликулярную фазу следующего спонтанного цикла производили контрольную лапароскопию (Лап. 2). Вновь регистрировали степень повреждений по тем же классификациям, что и до лечения (rAFS 2 и ВАШ 1). После контрольной лапароскопии оценивали общее состояние каждой больной по всем изучаемым показателям. Для бесплодных женщин в течение 12 месяцев после окончания лечения фиксировали репродуктивные исходы.
В соответствии с представленными данными положительный эффект означал бы, что Диеногест по использованным критериям превосходит Декапептил®. Степень эффекта оценивали ранговым методом Ходжеса-Лемана (11). Для проверки гипотезы, что Диеногест, по меньшей мере, "не хуже" Декапептила®, истинный эффект рассчитывали по 90% и 95%-му доверительным интервалам, принимая за порог уменьшение эндометриозных имплантантов на 4 пункта. Иными словами, если этот порог в абсолютных показателях оказывался ниже 4 пунктов, то гипотезу "не хуже" можно было считать статистически доказанной с 5% вероятностью ошибки (односторонний критерий). Существование каких-либо различий между группами оценивали с помощью непараметрического теста Вилкоксона, соответствующему 95%-му доверительному интервалу истинного эффекта. Протокол исследования был одобрен этическим комитетом и наблюдательным советом Лилльского университета 5 апреля 1994 года.
Результаты
С 28 июня 1994 по 8 декабря 1997 года в 17 центрах в исследование были включены 142 пациентки: 74 в группу Диеногеста и 68 - в группу Декапептила® (рис. 3).
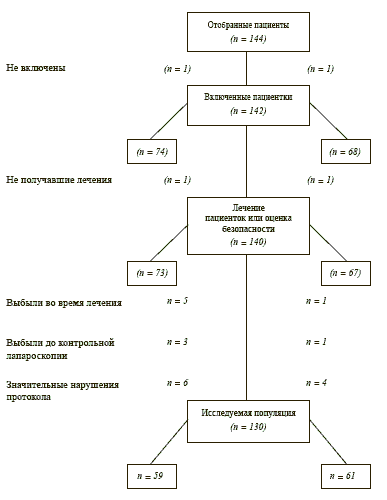
Двенадцать из них были исключены: 9 (12,3%) из группы Диеногеста и 3 (4,5%) из группы Декапептила®. Двое выбыли до начала лечения: одна - по совету лечащего врача, а другая - из-за спонтанной беременности. Пятеро из группы Диеногеста были исключены по одной из следующих причин: сахарный диабет, метроррагия, мигрень, боли в желудке и отказ от участия. Из группы Декапептила® выбыла одна женщина с жалобами на головную боль и приливы. В период между окончанием лечения и контрольной лапароскопией одна женщина выбыла из-за беременности и одна - из-за развившегося гипотиреоза. Одна из группы Декапептила® прекратила лечение из-за самопроизвольного аборта.
Из-за серьезных нарушений протокола исследования после рандомизации и контрольной лапароскопии были исключены 10 пациентов (6 из группы Диеногеста и 4 из группы Декапептила®). Нарушения были сходными в обеих группах. Таким образом, окончательный анализ проведен с учетом оставшихся 120 пациенток, прошедших рандомизацию, полностью завершивших исследование, которым была проведена контрольная лапароскопия.
Средний возраст и вес пациенток группы Диеногеста и Декапептила® были практическими одинаковыми (28,5 ± 4,9 vs. 30,3 ± 5,1 лет и 58,4 ± 9,9 vs. 57,2 ± 9,5 кг соответственно). Основные показатели (систолическое и диастолическое артериальное давление и частота сердечных сокращений) находились в нормальных пределах и были сравнимыми у пациенток обеих групп. У 32% женщин эндометриоз был диагностирован ранее, и средний срок (медиана) его существования (668 дней) в обеих группах был сходным (табл. 1).
Таблица 1 Пациентки с ранее диагностированным эндометриозом
| Общая популяция (n = 35) | Диеногест (n = 13) | Декапептил® (n = 22) | |||
| Длительность болезни (дни) | |||||
| 668 | 802 | 595,5 | |||
| 349; 1731 | 349; 1137 | 368; 1731 | |||
| 92-4238 | 190-4238 | 92-3416 | |||
| Предшествующее медикаментозное лечение n (%) | |||||
| 30 (85,7) | 13 (100,0) | 17 (77,3) | |||
| Предшествующая лечебная лапароскопия n (%) | |||||
| 28 (80) | 12 (92,3) | 16 (72,7) | |||
Большинство этих пациенток ранее получали медикаментозное (85,7%) или лапароскопическое лечение (80%). Статистически значимые различия между группами по этим показателям отсутствовали.
Симптомы и признаки заболевания в группах Диеногеста и Декапептила® были сходными и включали боль (83,1% vs. 85,2%), дисменорею (83,6% vs. 91,5%), диспаурению (66,7% vs. 66,1%), бесплодие (более половины пациенток в обеих группах) или бесплодие и боль (примерно 50% в каждой группе). Хотя на тазовые боли несколько чаще жаловались пациентки группы Декапептила® (67,8% vs. 47,5%; Р = 0,3), средняя продолжительность и интенсивность болей во время менструальных циклов в обеих группах были сходными.
Общий балл rAFS 0 в обеих группах был практически одинаковым, сходным образом распределялись и оценки отдельных компонентов этого показателя (гетеротопий, спаек, облитерации дугласова пространства) (табл. 2).
Таблица 2 Общий балл по пересмотренной классификации Американского общества фертильности
| Лапароскопия | Диеногест (n = 59) Медиана (1, 3-й квартили) | Декапептил® (n = 61) Медиана (1, 3-й квартили) | Эффект | 90% ДИ | 95% ДИ | Р |
| 38 | 38 | 0 | -8; 7 | -8; 8 | 0,96 | |
| 24; 61 | 24; 54 | |||||
| 4 | 4 | 0 | -2; 0 | -2; 0 | 0,61 | |
| 0; 12 | 0; 12 | |||||
| Изменение балла | -28 | -31 | -3 | -9; 2 | -10; 4 | 0,38 |
| -45; -8 | -44; -20 | |||||
| 16 | 12 | 0 | -6; 3 | -7; 4 | 0,85 | |
| 2;40 | 4;24 | |||||
| Изменение балла | 8 | 9 | 0 | -6; 4 | -6; 5 | 0,97 |
| -1; 26 | 1; 18 | |||||
Главным критерием служила оценка гетеротопий по классификации rAFS. Степень гетеротопий и спаек (табл. 3) рассчитывали на основании данных лапароскопии: диагностической лапароскопии при включении пациенток в исследование (Лап. 0), послеоперационной лапароскопии (Лап. 1) и контрольной лапароскопии после окончания лечения (Лап. 2) (табл. 2-4). Статистически значимая разница между оценками гетеротопий при Лап.2 отсутствовала (Р = 0,43).
Таблица 3 Балл гетеротопий по пересмотренной классификации Американского общества фертильности
| Лапароскопия | Диеногест (n = 59) Медиана (1, 3-й квартили) | Декапептил® (n = 61) Медиана (1, 3-й квартили) | Эффект | 90% ДИ | 95% ДИ | Р |
| 20 | 22 | 2 | 0; 5 | 0; 6 | 0,19 | |
| 8; 24 | 16; 26 | |||||
| 0 | 1 | 0 | 0; 0 | 0;0 | 0,34 | |
| 0; 4 | 0; 8 | |||||
| Изменение балла | -16 | -20 | -1 | -4; 2 | -5; 2 | 0,47 |
| -24; -4 | -24; -6 | |||||
| 2 | 2 | 0 | -1; 0 | -2; 0 | 0,43 | |
| 0;16 | 0;4 | |||||
| Изменение балла | 0 | 0 | 0 | -2; 0 | -2; 0 | 0,31 |
| 0; 4 | -2; 2 | |||||
Квартильный анализ показал, что по меньшей мере у 75% пациенток группы Диеногеста этот балл был меньше 16, а в группе Декапептила® - меньше 4. Не менее чем у 25% пациенток каждой группы новые гетеротопии не появлялись (нулевой показатель). Средняя разница в баллах гетеротопий при послеоперационной и контрольной лапароскопии (Лап. 2 - Лап. 1) в обеих группах была одинаковой (медиана: 0).
Через 4 месяца лечения (при Лап. 2) степень повреждений изменилась в обеих группах практически одинаково. При 90%-х доверительных интервалах нижняя граница составляла -2, тогда как для опровержения гипотезы "не хуже" она должна была составлять - 4. Категориальный анализ изменений гетеротопий (ухудшение, стабильность, улучшение) не выявил статистически значимой разницы между видами лечения (Р = 0,25). При Лап. 2 у большего числа пациенток имели место более высокие показатели спаечного процесса или облитерации заднего дугласова пространства, чем при Лап. 1 (табл. 4). Полная облитерация обнаруживалась при Лап. 2 также у большего числа пациенток, чем при Лап. 1, но реже, чем при Лап. 0.
Таблица 4 Балл спаек по пересмотренной классификации Американского общества фертильности
| Лапароскопия | Диеногест (n = 59) Медиана (1, 3-й квартили) | Декапептил® (n = 61) Медиана (1, 3-й квартили) | Эффект | 90% ДИ | 95% ДИ | Р |
| 8 | 8 | 0 | -4; 1 | -4; 2 | 0,58 | |
| 4; 22 | 4; 16 | |||||
| 0 | 0 | 0 | 0; 0 | 0; 0 | 0,23 | |
| 0; 4 | 0; 0 | |||||
| Изменение балла | -8 | -8 | 0 | -2; 2 | -3; 3 | 0,83 |
| -17; -1 | -16; -2 | |||||
| 5 | 8 | 0 | -1; 4 | -1; 4 | 0,51 | |
| Изменение балла | 2 | 6 | 2 | 0; 4 | 0; 4 | 0,15 |
| 0; 2 | 1; 12 | |||||
Статистически значимые различия между группами при Лап. 2 отсутствовали (Р = 0,85).
За 4 месяца лечения (Лап. 2 - Лап. 1) баллы rAFS в двух группах изменились одинаково. Нижняя граница 90%-го доверительного интервала составляла -6. Диеногест оказался столь же эффективным, что и Декапептил®.
В группе Диеногеста 34,5% пациенток были "очень удовлетворены" и 51,7% - "удовлетворены" лечением; таким образом, удовлетворенность выразили 86,2% пациенток. В группе Декапептила® "очень удовлетворенными" были 30%, а просто "удовлетворенными" - 50% пациенток (всего - 80%). Судя по отношению шансов, распределение пациенток как функция реакции на лечение свидетельствует в пользу Диеногеста (отношение шансов = 1,35), но разница между группами не достигала степени статистической значимости (Р = 0,39).
В течение 12 месяцев после окончания лечения регистрировали частоту спонтанных беременностей у тех, у кого до начала исследования имело место бесплодие (45 женщин группы Диеногеста и 41 - группы Декапептила®). Спонтанная беременность наступила у 15 (33,3%) женщин из группы Диеногеста и у 12 (29,3%) - из группы Декапептила®, что статистически незначимо (Р = 0,71) (табл. 5).
Таблица 5 Частота и характеристика спонтанных беременностей
| Беременности | Диеногест (n= 45) | Декапептил® (n = 41) | ||
| n | % | n | % | |
| Всего спонтанных беременностей | 15 | 33,3 | 12 | 29,3а |
| Нормальное течение до родов | 13 | 28,9 | 9 | 22,0 |
| 12 | 26,7 | 9 | 22,0 | |
| Прерванные беременности | 2 | 4,4 | 4 | 7,3 |
| 3 | 4,4 | 3 | 7,3 | |
| 0 | 0,0 | 0 | 0,0 | |
аР = 0,71
При анализах крови выявлены статистически значимые различия в следующих показателях.
Общий холестерин: среднее увеличение за время лечения в группе Декапептила® составило 0,15 г/л (Р < 0,01), а в группе Диеногеста - 0,05 г/л (Р = 0,03) (Р между группами = 0,02).
Холестерин ЛПВП: за время лечения в группе Диеногеста увеличился на 0,03 г/л (Р = 0,04), а в группе Декапептила® - на 0,09 г/л (Р Щелочная фосфатаза: за время лечения в группе Диеногеста увеличилась на 1,0 МЕ/л (статистически незначимо), а в группе Декапептила® - на 11 МЕ/л (Р < 0,01) (Р между группами < 0,01).
По меньшей мере один побочный эффект отмечали 92% пациенток (разница между группами отсутствовала), но тяжелые побочные эффекты имели место только у 23% из них. Профиль безопасности обоих препаратов был одинаковым, за тем лишь исключением, что кровянистые выделения из влагалища чаще отмечались в группе Диеногеста (61,6% vs. 25,4%), а приливы - в группе Декапептила® (61,2% vs. 9,6%).
Клиническая безопасность лечения нашла отражение в общей удовлетворенности пациентов: 85% из группы Дие-ногеста и 80% из группы Декапептила®. Биологическая безопасность Диеногеста была высокой: он не изменял уровня глюкозы в крови и увеличивал уровень общего холестерина в меньшей степени, чем Декапептил®. Наконец, Декапептил® повышал активность щелочной фосфатазы, тогда как Диеногест - нет (Р между группами <0,01).
Обсуждение
Сочетание центрального ингибиторного эффекта прогестинов с их периферическим действием обеспечивает полное исчезновение эндометриозных повреждений в 50% и частичное - в 13% случаев (12). Однако используемые соединения (в основном медроксипрогестерон ацетат, линестренол, этинодрел или норэтистерон) обладают значительными побочными метаболическими эффектами (13, 14).
Поиски более эффективных антиандрогенных соединений привели к синтезу даназола и гестринона. Некоторое время именно даназол служил основным средством лечения эндометриоза, хотя и обладал побочным андрогенным действием. В настоящее время такими средствами являются аналоги ГнРГ, обладающие не меньшей активностью, чем даназол, но лишенные андрогенных и метаболических побочных эффектов.
В данной статье приведены результаты многоцентрового открытого рандомизированного контролируемого клинического исследования, в котором сравнивались эффективность и безопасность использования гестагена Диеногеста и аналога ГнРГ Декапептила® в лечении эндометриоза. Применение плацебо было этически неоправданным, поскольку польза медикаментозного лечения эндометриоза 2-4 степени по классификации rAFS надежно установлена (15).
Наконец, исследование было открытым, так как скрыть разницу между инъекциями и приемом таблеток было невозможно.
Учитывая характер проводимого сравнения (новый препарат против референсного), требовалось сравнить эффективность Диегеноста и Декапептила®. Эффективность лечения эндометриоза можно оценить по анатомическим изменениям повреждений, и поэтому необходимо было проводить лапароскопию до и после лечения. Повторная лапароскопия оправдывалась тяжестью заболевания (2-4 степень по классификации rAFS). В этих случаях медикаментозное лечение дополняло хирургическое.
По данным литературы, средняя продолжительность лечения аналогами ГнРГ составляет 6 месяцев. В настоящее время эти средства стремятся применять не больше 3-4 месяцев, так как они влияют на костную ткань. Три месяца - слишком короткий срок для оценки лечебного эффекта гестагена, тогда как четыре - представляется разумным компромиссом. Только анатомические критерии (баллы, регистрируемые при лапароскопии) позволяют объективно оценить эволюцию заболевания. Основным критерием в протоколе исследования служило изменение балла rAFS (rAFS 2 - rAFS 1). При этом учитывали степень облитерации дугласова пространства, число и размер гетеротопий и выраженность спаечного процесса; эффективность медикаментозного лечения лучше всего оценивать по степени распространенности гетеротопий, которая является самым специфическим критерием, поэтому именно она служила основным показателем.
Не было выявлено существенной разницы в гетеротопиях или спайках трубной или яичниковой локализации, в общей степени процесса или степени отдельных компонентов оценки эндометриоза. Эти результаты позволяют утверждать, что Диеногест столь же эффективен, что и Декапептил®. Гипотеза о превосходстве одного из препаратов оказалась несостоятельной (нулевой положительный эффект; Р = 0,31). Диеногест действовал "не хуже" и у женщин с тяжелым эндометриозом (балл гетеротопий ≥15 при диагностической лапароскопии). По данным Evers (16), наиболее адекватной является оценка тяжести эндометриоза после возобновления менструаций.
Сравнение тяжести эндометриоза (гетеротопии и спайки) до и после медикаментозной терапии обнаружило улучшение общего показателя у 20% пациенток обеих групп. Отсутствие изменений зарегистрировано у 53% пациенток, получавших Диеногест, и у 60%, получавших Декапептил®. Можно заключить, таким образом, что суммарно в обеих группах удовлетворительные результаты достигнуты в 70-80% случаев, и это соответствует данным, ранее полученным при использовании Даназола, как в сравнительных (17), так и в плацебо-контролируемых (13) исследованиях. Аналогичный успех достигался и при использовании Декапептила® (8,9) и других аналогов ГнРГ (18). Кроме того, судя по показателям ВАШ, статистически значимая разница между группами отсутствовала и в отношение воспалительного статуса.
При обоих видах терапии интенсивность болей уменьшалась у пациенток обеих групп в равной степени. Среди наших пациенток 86 предъявляли жалобы на бесплодие (45 в группе Диеногеста и 41 в группе Декапептила®). В группе Диеногеста беременность наступила в 33% случаев и завер шилась родами у 13 из 15 женщин. В группе Декапептила® забеременели 29% пациентов и родили 9 из 12. Общая частота родов в группе Диеногеста составила 29%, а в группе Декапептила® - 22%. Разница между группами свидетельствует в пользу Диеногеста, но была статистически недостоверной. Таким образом, и в случаях бесплодия Диеногест не уступает Декапептилу®; он не увеличивает риск бесплодности или самопроизвольных абортов.
Что касается клинической безопасности препаратов, то симптомы у пациенток, получавших лечение, были связаны в основном с нарушениями вегетативной нервной системы. Поскольку аналоги ГнРГ индуцируют химическую менопаузу, при их применении обычно развивается климактерический синдром. Приливы у женщин, получавших аналоги ГнРГ, отмечались в 61% случаев (тяжелые - у 31%), а у получавших гестогены - в 11% случаев. Наиболее частым осложнением терапии Диеногестом были влагалищные кровотечения (в 61,6% случаев), тогда как у пациенток, получавших аналоги ГнРГ, они наблюдались в 25,4% случаев. Обычно это были лишь мажущие выделения, что часто имеет место в первые месяцы после гормональной терапии (заместительной гормональной терапии или применения пероральных контрацептивов, особенно в низких дозах).
Пациентки хорошо переносили медикаментозную терапию, о чем свидетельствует общая частота удовлетворенности лечением. В отличие от эффектов при лечении классическими гестагенами или даназолом, пациентки не жаловались на такие проявления андрогенных эффектов, как прибавка в весе, угревая сыпь, алопеция или вирилизация (гирсутизм). Это подтверждает предыдущие сообщения об отсутствии у Диеногеста андрогенных свойств (19).
О безопасности и эффективности обоих видов терапии с точки зрения пациенток и врачей свидетельствуют показатели общей удовлетворенности лечением: 85,5% женщин, получавших Диеногест, и 80%, получавших Декапептил®, были удовлетворены или очень удовлетворены терапией. Отсутствие у Диеногеста андрогенной активности подтверждается на биологическом уровне. Основным биохимическим сдвигом стало увеличение щелочной фосфатазы в группе Декапептила®, что может отражать активизацию обмена костной ткани. В группе Диеногеста этого не наблюдалось. Липидный профиль (в частности, уровень холестерина ЛПВП) и уровень глюкозы в крови у пациентов обеих групп оставались сходными.
Заключение
Диеногест является терапевтической альтернативой аналогам ГнРГ в лечении эндометриоза. В данном исследовании 4-месячное послеоперационное лечение эндометриоза Диеногестом было столь же эффективным, что и терапия Декапептилом®; Диеногест не обладает андрогенными эффектами.
Благодарности.
Авторы признательны д-ру Pennehouat (Париж, Франция), д-ру Cusumano (Льеж, Бельгия), д-ру Pettemans (Брюссель, Бельгия), Pr. Tran (Ницца, Франция) и Pr. Raudrant (Лион, Франция) за помощь в проведении исследования, а также Afchine Fazel, M.D., и Yukio Sonoda, M.D. за существенную редакторскую помощь.
Список литературы:
1. Muse KN, Wilson EA. How does mild endometriosis cause infertility? Fertil Steril 1982;38:145-52.
2. Bur ME, Greene GL, Press MF. Estrogen receptor localization in formalin-fixed paraffin embedded endometrium and endometriotic tissues. Int J Gynecol Pathol 1987;6:140-51.
3. Barbieri RL. Hormone treatment of endometriosis: the estrogen threshold hypothesis. Am J Gynecol 1992;166:740-5.
4. Donnez J, Nisolle M, Grandjean P, Gillerot S, Clerckx F. La place des agonistes de la GnRH dans le traitement par voies endoscopiques de l'endome'triose et des fibromyomes. Contracep Fertil Sex 1993;21:59-62.
5. Henzl MR, Cordon SL, Moghissi K, Buttram VC, Berqvist C, Jacobson J. Administration of nasal nafarelin as compared with oral danazol for endometriosis. A multicenter double-blind comparative clinical trial.N Engl J Med 1998;318:485-9.
6. Wheeler JM, Knittle JD. Depot leuprolide versus danazol in treatment of women with symptomatic endometriosis. Efficacy results. Am J Obstet Gynecol 1992;167:1367-71.
7. Dorangeon P, Buvat-Herbaut M, Buvat J, Thomas JL. Traitement de l'endome'triose par l'ace'tate de nome'gestrol. Gynecologie 1993;1:139-43.
8. Meldrum DR, Chang RJ, Lu J, Valt W, Rivier J, Judd HL. "Medical oophorectomy" using a long-acting GnRH agonist-a possible new approach to the treatment of endometriosis. J Clin Endocrinol Metab 1982;54:1081-3.
9. Zorn JR, Tanger C, Roger M, Grenier J, Comaru-Schally AM, Schally AV. Therapeutic hypogonadism induced by a delayed-release preparation of microcapsules of D-Tr-6-luteinizing hormone releasing hormone: a preliminary study in eight women with endometriosis. Int J Fertil 1986;31:11-27.
10. The American Fertility Society. Revised American Fertility Society classification of endometriosis, 1985. Fertil Steril 1985;43:351-2.
11. Hodges JL, Lehmann EL. Estimates of location based on rank tests. Ann Math Stat 1963;34:598-611.
12. Bruhat MA, Canis M. Diagnostic et traitement actuel de l'endome'triose externe. Contracep Fertil Sex 1986;14:617-27.
13. Telimaa S, Ronnberg L, Kauppila A. A placebo-controlled comparison of danazol and high-dose medroxyprogesterone acetate in treatment of endometriosis after comparative surgery. Gynecol Endocrinol 1987;1: 363-71.
14. Acosta AA. Medical treatment of endometriosis. In: Hedon B, Bringer J, Mares P, eds. Proceedings of the 15th World Congress on Fertility and Sterility, Montpellier, France, September 17-22, 1995. New York: Parthenon, 1995:43-57.
15. Hornsteins MD, Hemmings R, Yuzpe AA, Heinrichs WL. Use of nafarelin versus placebo after reductive laparoscopy surgery of endometriosis. Fertil Steril 1997;68:860-4.
16. Evers JLH. Endometriosis does not exist; all women have endometriosis. Hum Reprod 1994;9:2206-8.
17. Barbieri RL, Evans S, Kister RW. Danazol in the treatment of endometriosis: analysis of 100 cases with a 4-year follow-up. Fertil Steril 1982;37:737-46.
18. Lemay A, Maheux R, Huot C, Blanchet J, Faure N. Efficacy of intranasal or subcutaneous luteinizing hormone-releasing hormone agonist inhibition of ovarian function in the treatment of endometriosis. Am J Obstet Gynecol 1988;158:233-6.
19. Kohler G, Brackmann K. Modification des parame'tres du me'tabolisme lipidique sous traitement de l'endome'triose par dienogest. N Klin Med 1987;42:2103-5. 692
Комментарии
ПРАКТИКА ПЕДИАТРА
