Влияние нарушения функции яичников у женщин репродуктивного возраста на состояние минеральной плотности костной ткани
СтатьиО.Ф.Серова, В.У.Торчинов
Московский областной НИИ акушерства и гинекологии (директор – член-корр. РАМН, проф.В.И.Краснопольский)
Остеопороз - системное метаболическое заболевание скелета, характеризующееся уменьшением массы костной ткани в единице объема по отношению к нормальному показателю у лиц соответствующего пола и нарушением микроархитектоники костной ткани с последующим повышением хрупкости костей и учащением риска переломов. Являясь широко распространенным обменным заболеванием костей, остеопороз имеет огромное медико-социальное и экономическое значение. Следует отметить, что остеопороз развивается постепенно и долгое время может оставаться незамеченным. Проявление характерных его симптомов достигает максимума приблизительно через 10-15 лет существования остеопенического синдрома.
Несмотря на то, что исследования последних лет направлены преимущественно на изучение костной ткани в перименопаузальном периоде, в настоящее время обсуждается тот факт, что истоки остеопороза лежат в детстве.
В работах многих авторов указывается на взаимосвязь развития постменопаузального остеопороза с возрастом менархе, гормональным дисбалансом и сопутствующими нарушениями менструального цикла у девочек в подростковом периоде (Байдак М.М., 1994; Вихляева Е.М., 1997). Доказано, что риск развития остеопороза у человека зависит от уровня его пиковой костной ткани, которая достигается в возрасте между 20 и 30 годами. Роль половых гормонов и их дефицита в развитии остопороза и остеопении особенно важна в пубертатном и репродуктивном периодах.
В пубертатном периоде возрастает продукция половых гормонов и скелет становится мишенью их действия. Особенности формирования скелета в значительной степени зависят от преобладания женских или мужских половых гормонов. Активация костного обмена проявляется в прогрессирующем увеличении костной массы. Как преждевременное половое созревание, так и его задержка влияют на формирование скелета посредством замедления или ускорения костного обмена.
Между процессами резорбции и формирования кости существует тесная контролируемая гормонами взаиморегуляция, которая осуществляется на тканевом уровне. Гормоны наряду с физической активностью и полноценным питанием входят в число основных факторов, определяющих массу кости и качество костной ткани.
Наиболее распространенная классификация остеопороза учитывает возраст его развития и основные этиологические факторы:
- Первичный остеопороз
- постменопаузальный,
- сенильный,
- ювенильный,
- идиопатический.
- Вторичный остеопороз (составляет менее 15 % случаев остеопороза), возникает в результате:
- ревматических заболеваний,
- эндокринных болезней,
- болезней крови,
- болезней органов пищеварения (особенно тех, которые характеризуются нарушением всасывания в кишечнике),
- болезней печени,
- болезней почек,
- приема лекарственных препаратов.
В настоящее время отмечается рост заболеваемости ювенильным остеопорозом, наблюдающимся у молодых людей, костная масса которых не достигла своего пикового значения.
В основе жизнедеятельности костной системы лежат два взаимосвязанных и взаимозамещающих процесса: процесс созидания, образования новой кости и процесс разрушения – резорбции старой (ремоделирование кости).
Выделяют следующие периоды возрастных изменений костного скелета:
- С момента рождения до закрытия эпифиза (к 20-25 годам) - достижение пиковой костной массы - прогрессивное увеличение объема костной ткани за счет эндохондрального и периостального окостенения.
- К 30-35 годам начинается потеря костной массы до 1% в год от пиковой массы.
- До 40-45 лет процессы костной формации и резорбции происходят с одинаковой интенсивностью.
- После 45 лет процессы резорбции превалируют над процессами костеобразования.
Вероятность развития остеопороза у взрослого человека определяют стартовая минеральная плотность костной ткани (МПКТ) и скорость потери костного вещества, а также нарушение процессов ремоделирования.
Факторы, контролирующие и инициирующие костную перестройку, условно можно разделить на 4 группы:
- Гормоны, регулирующие обмен кальция: паратгормон, активный метаболит витамина D – кальцитриол, кальцитонин.
- Системные гормоны: глюкокортикоиды, тироксин, инсулин, гормон роста, половые гормоны.
- Факторы роста: белковые факторы плазмы, тромбоцитов и костной ткани;
- Местные факторы, продуцируемые самими костными клетками: простагландины Е, оказывающие активирующие влияние на остеокласты
Развитию остеопороза могут способствовать многие причины: генетические (наследственная предрасположенность), гормональные (позднее начало менструации, аменорея, бесплодие, ранняя менопауза), экстрагенитальные заболевания, особенности питания, низкая физическая активность, недостаточное потребление кальция, дефицит витамина Д, курение, алкоголизм, значительное употребления кофе, длительное применение некоторых лекарств (глюкокортикоиды, антикоагулянты, антиконвульсанты, тиреоидные препараты и др).
В костном ремоделировании порядок событий четко запрограммирован. Под влиянием определенных стимулов группа остеокластов резорбирует костную ткань на глубину около 50мкм. Пространство резорбированной кости покрывается остеобластами, которые формируют новообразованную костную ткань с остеоцитами, погруженными в зрелую кость. Процесс ремоделирования кости осуществляется с разной скоростью практически всю жизнь, что проявляется костной перестройкой. Ежегодно перестраивается от 2-4 % до 10% костной ткани, то есть за 10-20 лет обновляется половина скелета.
Основным субстратом для минерализации костной ткани является кальций, который играет значимую роль в формировании скелета. Достаточное потребление кальция в детском и подростковом периодах необходимо для достижения оптимального пика костной ткани. В теле взрослого человека содержится около 1200г кальция, из которого 98,9% приходится на скелет. Недостаток кальция приводит к увеличению синтеза паратгормона, в результате чего происходит активное вымывание кальция из костной ткани, снижение МПКТ, развитие остеопении и остеопороза. В условиях гипокальциемии ослабляется и стимулирующее влияние кальцитонина на остеобласты.
Механизмы влияния половых гормонов на костную ткань чрезвычайно важны и до конца не изучены. Однако после открытия специфических рецепторов на остеобластах к эстрогенам, андрогенам, гормону роста и тиреоидным гормонам стало очевидно, что губчатое вещество костной ткани является своеобразным органом-мишенью для половых гормонов. Наиболее значимое влияние на костно-минеральный обмен оказывают эстрогены, так как они активизируют остеобласты, подавляют продукцию интерлейкинов, активируя апоптоз остеокластов, способствуют торможению костной резорбции, снижают чувствительность костной ткани к рассасывающему влиянию паратгормона, повышают чувствительность костной ткани к витамину D3, стимулируют синтез кальцитонина, регулируют процессы всасывания и выделения Са, активируют апоптоз остеокластов. Снижение уровня эстрогенов ведет к ускорению костного обмена и потере костного вещества. Тестостерон активизирует анаболические процессы в костях. Прогестерон оказывает антирезорбтивное действие за счет прямого стимулирующего действия на остеобласты или опосредованно путем блокады рецепторов этих клеток к глюкокортикоидам, активирующим апоптоз остеобластов, а также может самостоятельно активировать апоптоз остеокластов.Глюкокортикоиды ингибируют всасывание кальция в кишечнике и повышают экскрецию его с мочой, приводят к снижению процесса превращения витамина D в активные метаболиты. Тиреоидные гормоны активируют остеокласты Пролактин регулирует процесс костеобразования, степень снижения которого зависит от уровня повышения пролактина. Инсулин стимулирует активность остеобластов. Соматотропный гормон стимулирует синтез кальцитриола, который увеличивает всасывание кальция в кишечнике.
Методы определения МПКТ
- Однофотонная денситометрия - для сринингового измерения МПКТ кисти, дистальных отделов костей предплечья или голени.
- Двухфотонная рентгеновская денситометрия - для исследования любой кости или всего скелета в двух и более проекциях.
- Количественная компьютерная томография - для получения трехмерного изображения, что позволяет произвести прямое определение плотности и пространственного отделения трабекулярной кости от кортикальной.
- Ультразвуковая денситометрия - для скриннингового исследования (пяточная кость, надколенник, большеберцовая кость, фаланги пальцев кисти).
- Исследование биохимических маркеров (остеокальцин -ОК, щелочная фосфатаза -ЩФ, Са, Р и др. проколлагеновые пропептиды).
С целью выснения влияния нарушения функции яичников на МПКТ было проведено комплексное обследование и лечение 100 пациенток репродуктивного возраста до 35 лет. Определение МПКТ проводилось с помощью двухэнергетической ренгеновской абсорбциометрии (DPA) на денситометре «Delphi N» компании «Hologic». В зависимости от особенностей гормональных нарушений все обследованные были разделены на 5 групп:
I группа - 48 женщин, гормональные изменения у которых соответствовали синдрому поликистозных яичников (СПКЯ).
II группа - 11 пациенток с функциональной гиперпролактинемией.
III группа - 20 пациенток с врожденной дисфункцией коры надпочечников (ВДКН).
IV группа - 9 пациенток с гипогонадотропной гипофункцией яичников.
V группа - 12 пациенток с гипергонадотропной гипофункцией яичников. Из них 8 пациенток с дисгенезей гонад и 4 - с синдромом истощения яичников (СИЯ).
Мы провели анализ основных клинических характеристик, которые могут влиять на формирование костной ткани. Ожирение II- III степени чаще всего наблюдалось у пациенток с СПКЯ и гиперпролактинемией ( 68,5% и 27,3% соответственно). У пациенток с ВДКН, гипо- и гипергонадотропными состояниями чаще отмечался дефицит массы тела ( 55,5%; 15,0% и 15,0% соответственно). Первичная аменорея наблюдалась чаще у пациенток V группы (66,6%), IV группы (55,5%) и III группы (35,0%) , вторичная аменорея - у пациенток II, IV и V групп (63,6%; 44,4% и 33,3% соответственно).
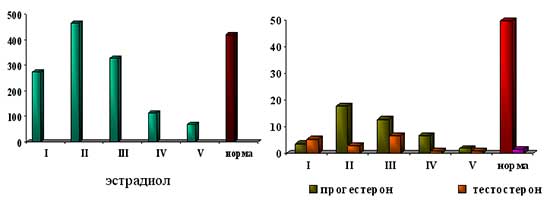
Исследование сывороточных уровней яичниковых гормонов показало, что наиболее низкие показатели эстрадиола, прогестерона и тестостерона также определялись у пациенток с гипо- и гипергонадотропными состояниями, гиперандрогения была выявлена у всех пациенток с ВДКН и у большинства женщин с СПКЯ (рис. 1).
Рис. 1. Содержание эстрадиола (пмоль/л), прогестерона (нмоль/л) и тестостерона (нмоль/л) у обследованных пациенток
Оценка результатов двухэнергетической ренгеновской абсорбциометрии проводилась только по Z-критерию, оценивающего МПКТ относительно возрастной нормы. Мы не учитывали значения Т-критерия, который сравнивает полученную МПКТ с пиковой костной массой, поскольку большинство обследованных пациенток были в возрасте до 30 лет, т.е. до достижения пика костной массы.
Поскольку остеопоротические изменения развиваются неравномерно в различных отделах скелета, нами проанализированы данные денситометрического исследования поясничных позвонков (L2–L4), состоящих преимущественно из трабекулярной ткани, и проксимального отдела бедра, представленного в основном кортикальной тканью.
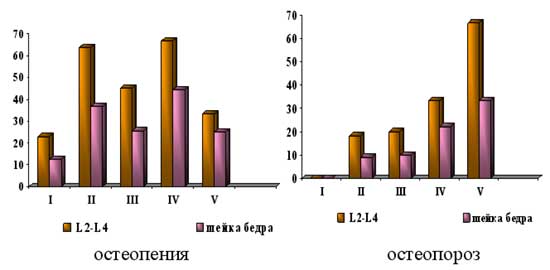
Частота выявления остеопении и остеопороза у наблюдаемых пациенток в поясничном отделе позвоночника была почти в 2 раза больше, чем в шейке бедра, Снижение МПКТ выявлено более, чем у половины (54,0%) женщин: остеопения - в 37%, остеопороз - в 17% случаев. При этом, снижение МПКТ наблюдалось у всех пациенток с гипо- и гипергонадотропными состояниями (рис. 2). Средние значения Z-критерия в этих группах были самыми низкими (-3,1±0,3 и –3,5±0,5 соответственно). По-видимому это объясняется низким содержанием эстрогенов и прогестерона в сыворотке крови и, соответственно, отсутствием их участия в процессах ремоделирования кости.
Рис. 2. Частота выявления остеопении и остеопороза у пациенток с дисфункцией яичников
Исследование биохимических показателей фосфорно–кальциевого обмена (уровня ионизированного кальция и фосфора, а также показателей активности процессов костеобразования - ОК, ЩФ) показало, что их достоверного изменения у пациенток всех групп не наблюдалось.
При сопоставлении результатов рентгенологической денситометрии с клиническими и лабораторными данными выявлено, что степень снижения МПКТ зависит от:
- веса пациенток - она была более выражена при низкой массе тела, при которой усиливается негативное влияние дефицита эстрогенов на костную ткань. Избыток массы тела может отчасти защищать костную ткань, вероятно за счет экстрагонадного синтеза эстрогенов. Поэтому у пациенток с СПКЯ, больше половины которых страдали ожирением, снижение МПКТ было минимальным;
- от длительности аменореи - степень снижения МПКТ была максимальной у пациенток с первичной или вторичной аменореей длительностью более 1 года;
- от гормонального гомеостаза - степень снижения МПКТ прямо пропорциональна сывороточному содержанию тестостерона и пролактина и обратно пропорциональна содержанию эстрогенов и прогестерона;
Всем пациенткам в течение года проводилась дифференцированная гормональная терапия в зависимости от характера и степени нарушения функции яичников. Пациенткам с СПКЯ назначались гестаген-эстрогенные препараты (Диане-35, Регулон). При функциональной гиперпролактинемии применяли бромкриптин в индивидуально подобранных дозах. После нормализации уровня пролактина этим пациенткам назначали Регулон. Пациенткам с ВДКН назначали Диане-35 в виде монотерапии или в сочетании с андрокуром. Следует отметить, что длительное назначение глюкокортикоидов этим пациенткам нецелесообразно ввиду негативного влияния их на состояние МПКТ.
Пациенткам с гипогонадотропной гипофункцией яичников назначалась циклическая гормональная терапия Эстрожелем и Утрожестаном, так как в этих случаях целесообразно применение натуральных гормонов.
Эстрожель – гель для наружного применения, содержащий 17β-эстрадиол. Одна доза (2,5г/сут) препарата достаточна для поддержания МПКТ. Эстрожель создает оптимальную стабильную концентрацию эстрадиола в плазме, которая анологична средней фолликулярной фазе, позволяет избежать первичного печеночного метаболизма и метаболических нарушений (повышения триглицеридов и ЛПНП), в меньшей степени влияет на коагуляционный потенциал крови. Утрожестан – натуральный прогестерон физиологично дополняет эстрогены в защитном действии на костную ткань. Благодаря “естественным” связям c рецепторами во всех органах и тканях при его применении не происходит удлинения времени взаимодействия с рецепторным аппаратом. Кроме того, он восполняет дефицит эндогенного прогестерона, обеспечивая адекватную секреторную трансформацию эндометрия и нормализацию менструального цикла.
Пациенткам с гипергонадотропной гипофункцией яичников проводилась заместительная гормональная терапия препаратом Фемостон 2/10.
Контрольное обследование , проведенное через 6 месяцев и 1 год, показало, что на фоне гормональной терапии отмечалось восстановление менструального цикла через 6 месяцев у 93% пациенток, через 1 год – у 96%. Лишь у 4 пациенток с дисгенезией гонад менструальноподобной реакции в течение года наблюдения не было в связи с выраженными анатомическими изменениями матки.
Особого внимания заслуживает факт значительного уменьшения частоты остеопении и особенно остеопороза на фоне лечения. Так, если до лечения остеопения выявлялась у 37 пациенток , а остеопороз – у 17, то через 6 месяцев после лечения – у 12 и 5 соответственно, а через 1 год – лишь у 6 (6,0%) и 1 (1,0%) соответственно. Наиболее выраженное увеличение МПКТ было отмечено у женщин с гиперпролактинемией. Явления остеопороза сохранялись лишь при гипергонадотропных состояниях.
В нашем исследовании была проведена также оценка эффективности применения препарата кальция Натекаль Д3 для восстановления МПКТ в комплексном лечении пациенток с дисфункцией яичников. Для этого 54 пациентки с нарушением МПКТ были разделены на 2 группы: 1-я группа – 27 пациенток, которые в комплексе с гормональной терапией получали Н Натекаль Д3 в течение 6 месяцев, 2-я группа – 27 пациенток, которые получали только гормональную терапию. Средние значения Z-критерия в обеих группа были идентичны (-2,4± 0,6 и -2,3± 0,7 соответственно).
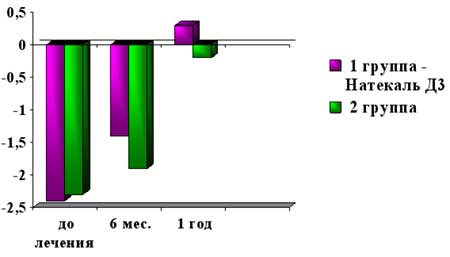
Динамическое определение МПКТ убедительно показало, что на фоне применения препаратов кальция в комплексной терапии дисфункции яичников у пациенток основной группы наблюдается более быстрое и выраженное восстановление МПКТ (рис. 3).
Рис. 3. Динамика восстановления костной ткани у пациенток с дисфункцией яичников (Z-критерий)
Таким образом, проведенные исследования показали наличие изменений костно-минерального метаболизма у молодых пациенток с нарушением менструального цикла по типу олигоменореи, а также возможность восстановления МПКТ до достижения пика костной массы в отличие от постменопаузального периода, в котором можно лишь существенно уменьшить скорость и степень ее снижения.
