Комплексный подход в терапии опийного абстинентного синдрома
СтатьиОпубликовано в журнале «Врач» №7, 2008
Н. Иванец, член-корреспондент РАМН, профессор, М. Винникова, ММА им. И. М. Сеченова, ННЦ наркологии МЗСР РФ
Наиболее распространенным видом наркотической зависимости в России является зависимость, формирующаяся при употреблении опия, его алкалоидов и синтетических производных (к ним относятся: опий-сырец, героин, так называемый метадон и некоторые другие наркотики). Зависимость от опиатов относится к наиболее тяжелым, так как клинические проявления основополагающих симптомокомплексов выражены в крайней степени; зависимость с трудом поддается терапии, получение положительного результата (стойкая ремиссия), по мнению многих авторов, сомнительно [1–3, 7–11].
Важное диагностическое значение наряду с синдромом патологического влечения принадлежит абстинентному синдрому. К клиническим особенностям проявлений абстинентного синдрома при употреблении различных производных опия относится смещение некоторых акцентов. Так, при героиновой зависимости значительно сильнее выражены психопатологические, в частности аффективные, психопатоподобные и диссомнические нарушения. Болевой симптомокомплекс тяжелый, однако редуцирован во времени (в условиях терапии его редукция происходит к 4–5-му дню). При употреблении кустарно приготовленных дериватов опия и натуральных опиатов ведущее место в клинической картине занимает выраженная болевая симптоматика, которая сопровождается также значительно выраженной вегетативной дисфункцией. При использовании метадона болевой симптомокомплекс по степени тяжести приравнивается к возникающему при применении кустарно приготовленных опиатов, но растянут во времени (его длительность иногда достигает 2 нед). При злоупотреблении трамалом болевой симптомокомплекс протекает с преобладанием сенестопатических ощущений, очень тягостных для больного. Особенности течения абстинентного синдрома объясняются различиями в фармакокинетике и фармакодинамике перечисленных наркотических препаратов.
Знание особенностей течения опийного абстинентного синдрома (ОАС) необходимо для выбора адекватного терапевтического подхода. Для успешного проведения лечения важно использовать комплексные подходы и мероприятия [4, 5, 12]. В настоящее время в терапии болевых расстройств при ОАС все чаще применяются нестероидные противовоспалительные препараты (НПВП).
В нашем Центре уже проводились клинические исследования представителя данного класса НПВП – кетанова [6]. В связи с тем что были получены хорошие результаты, возникла необходимость в продолжении клинических исследований кетанова и расширении границ его применения у больных с зависимостью от различных дериватов опия.
Целью настоящего исследования было изучение влияния кетанова на болевой симптомокомплекс при опиатной зависимости (опий-сырец, метадон, трамал).
В открытое контролируемое сравнительное исследование было включено 36 пациентов (все – мужчины), которые находились на стационарном лечении в отделениях клиники ННЦ наркологии МЗСР РФ. В исследование не включали больных с сочетанной зависимостью от других групп наркотиков; острыми психотическими состояниями; хроническими соматическими заболеваниями в стадии обострения; язвенной болезнью желудка и двенадцатиперстной кишки, желудочно-кишечными кровотечениями в анамнезе; выраженным нарушением функции почек; нарушениями свертываемости крови; гиперчувствительностью к препарату.
Диагностика осевых синдромов зависимости проводилась по МКБ-10. У всех больных была сформирована клиническая картина зависимости от опиатов, включавшая психическую зависимость, сформированный ОАС, высокую толерантность, соматические и социальные последствия, связанные с употреблением наркотика.
Из числа обследованных 18 пациентов употребляли кустарно приготовленный опий-сырец (1-я группа), 12 – метадон1 (2-я группа), у 6 пациентов диагностирована зависимость от трамала (3-я группа). В связи с разнородностью выборки основные клинико-динамические параметры будут рассмотрены в сравнении.
Начальный период приобщения к наркотикам чаще приходился на возраст 15–17 лет и был сравнительно коротким (не превышал 3–6 мес). Начало приема наркотиков опийной группы относилось к возрасту 15–18 лет. По срокам становления заболевания значимых отличий между группами не наблюдалось: формирование систематического приема опиатов происходило в течение 1–3 мес; развитие ОАС после начала систематического употребления в большинстве случаев занимало от 2 нед до 3 мес. Симптоматика ОАС включала специфические соматоневрологические, болевые и психопатологические нарушения.
Группы различались по длительности развития заболевания и тяжести клинических проявлений.
Так, в 1-й группе (зависимость от опия-сырца) длительность заболевания была наибольшей (от 6 до 8 лет); заболевание отличалось тяжестью всех проявлений зависимости. В клинической картине ОАС болевые расстройства занимали ведущее место. Степень тяжести ОАС была расценена как тяжелая у 14 (78%) пациентов, средняя – у 4 (22%). Кроме того, у всех пациентов отмечались соматические последствия употребления наркотика – в основном токсическое поражение печени и сердца. Личностные изменения в преобладающем большинстве случаев протекали по психоорганическому типу. Толерантность на момент обследования была высокой (табл. 1).
Таблица 1
Распределение толерантности на момент обследования
| Толерантность | 1-я группа | 2-я группа | ||
|---|---|---|---|---|
| абс. | % | абс. | % | |
| Низкая | – | – | 1 | 8 |
| Средняя | 6 | 33 | 3 | 25 |
| Высокая | 12 | 67 | 8 | 67 |
| Всего | 18 | 100 | 12 | 100 |
Эти пациенты 2-й группы (зависимость от метадона) начинали употребление наркотиков с героина, однако при прогрессировании заболевания, учащении неудачных попыток самолечения переходили на употребление так называемого метадона (в большинстве случаев они употребляли кустарно изготовленный метадон). При переходе на употребление метадона наблюдалась трансформация клинической картины заболевания. Абстинентный синдром был растянут во времени, болевая симптоматика имела тенденцию к нарастанию в течение 3–5 дней, на высоте болевых расстройств становились выраженными и психопатологические нарушения, преобладали поведенческие расстройства психопатоподобного регистра. Тяжесть абстинентного синдрома была выраженной у 7 (58%) пациентов и средней степени – у 5 (42%). Длительность заболевания составляла от 4 до 6 лет. Соматическая отягощенность также наблюдалась у всех пациентов; преобладало поражение печени вирусной или смешанной этиологии. Личностные изменения проявлялись по эндоформному или психоорганическому типу.
У пациентов 3-й группы (зависимость от трамала) изначально была сформирована зависимость от героина, однако в связи с различными внешними факторами (невозможность достать наркотик, преследование правоохранительными органами и пр.) они переходили на прием наиболее доступного для них морфинсодержащего препарата. Установление диагноза «зависимость от трамала» было возможно лишь в том случае, если наблюдалось систематическое употребление препарата в течение не менее 6 мес и сопровождалось клиническими проявлениями синдрома зависимости (патологическое влечение, абстинентный сидром и др.). Дозы употребляемого трамала варьировали в широких пределах (от 20 до 40 таблеток в сутки). Особенности клинических проявлений заключались в болевой симптоматике средней (у 4) или тяжелой (у 2) степени с превалированием сенестопатических жалоб,а также умеренной выраженности вегетативных расстройств. Личностные изменения – по психоорганическому типу. Значительная соматическая отягощенность: преобладание поражений печени токсического, вирусного или смешанного генеза, заметное снижение памяти, больше на текущие и недавно происшедшие события.
Особенности проявлений компонентов ОАС по группам представлены в табл. 2.
Таблица 2
Динамика и балльная оценка ОАС в группах
| Группа | Проявления | Продолжительность ОАС, дни | ||
|---|---|---|---|---|
| вегетативные | алгические | психопатологические | ||
| баллы, M+m | ||||
| 1-я | 2,6±0,2 | 2,8±0,1 | 2,4±0,2 | 5–6 |
| 2-я | 2,4±0,1 | 2,6±0,4 | 2,6±0,4 | 6–12 |
| 3-я | 1,8±0,1 | 1,6±0,3 | 2,2±0,1 | 5–6 |
Первично госпитализированных было 16 (44%) пациентов, повторно госпитализированных – 20 (66%).
Пациенты поступали в клинику в основном с начальными проявлениями абстинентных нарушений. Развитие абстинентных расстройств было индивидуальным и зависело от вида употребляемого наркотического вещества. Начальные проявления были представлены специфическими соматовегетативными нарушениями. Затем присоединялись характерные болевые ощущения в мышцах и суставах верхних и нижних конечностей, спине. С усилением болевой симптоматики было связано и нарастание психопатологических нарушений, пациенты жаловались на осознанное влечение к наркотику; у них усиливались беспокойство, раздражительность, напряженность, проявлялась тревога, в некоторых случаях доходившая до степени ажитации; практически постоянно присутствовали расстройства сна.
Основными методами исследования являлись клиникопсихопатологический, статистический. Клиническое исследование препарата проводилось с использованием специально разработанного протокола, максимально отвечающего международным требованиям GCP (качественная клиническая практика). Для определения терапевтической эффективности препарата использовались специально разработанные в отделении клинической психофармакологии шкалы оценки соматовегетативных и психопатологических проявлений в структуре абстинентного синдрома, а также шкала оценки интенсивности боли и шкала общего клинического впечатления. Для статистического анализа полученных результатов были использованы компьютерные программы Microsoft Excel 2000. Проводилось внутри- и межгрупповое сравнение по параметру редукции боли. Использовался параметрический t-критерий Стьюдента для уровня значимости <0,05.
Лечение абстинентного синдрома было комплексным, применялись антиконвульсанты, агонисты α2-адренорецепторов, антипсихотики, транквилизаторы, общеукрепляющая терапия.
Психотропная терапия в группах не отличалась, дозы препаратов подбирали индивидуально, лечение было направлено на купирование психопатологической симптоматики: патологического влечения к наркотику, связанных с ним поведенческих, аффективных расстройств, нарушений сна.
При назначении обезболивающей терапии применялась следующая тактика. В 1-й и 2-й группах проводилось сравнительное открытое исследование. Предварительно каждая из них была разделена на 2 подгруппы: основную и контрольную2. В контрольных группах в качестве обезболивающего средства применялся трамал в дозе 400–800 мг/сут.
Кетанов применяли в плановом порядке по схеме (1-я группа – 120 мг, 2-я – 9–120 мг, 3-я – 60–90 мг внутримышечно), причем 1-ю дозу вводили профилактически при поступлении больного в отделение с дальнейшим продолжением базовой терапии в течение 4–5 дней, когда выраженность болевой симптоматики была наиболее высокой.
Кетанов назначали в средней суточной дозе 90 мг, в более тяжелых случаях дозу увеличивали до 120 мг. В первые 4–5 дней препарат назначался в инъекциях (по 1,0 мл 3–4 раза в сутки). В дальнейшем препарат назначался внутрь в средней суточной дозе 60 мг, максимальная доза составляла 90 мг – до полного купирования болевой симптоматики. Общая длительность применения препарата не превышала 10 дней (в 1-й и 3-й группах – 5–7 дней, во 2-й – до 14 дней). Больных обследовали в день поступления (0 день), в дальнейшем – ежедневно до купирования болевого симптомокомплекса.
Эффект признавали хорошим, если достигалась редукция болевой симптоматики по шкале оценки интенсивности боли на 50% к 3-му дню лечения, а показатели шкалы общего клинического впечатления не превышали 2 баллов на 7-й день исследования.
Клинические исследования препарата кетанов позволили сделать ряд выводов.
- При болевом симптомокомплексе средней степени выраженности (у больных 1-й и 2-й групп) кетанов обладал достаточно выраженной обезболивающей активностью. При внутримышечном введении разовой дозы (30 мг) действие препарата начиналось через 15–20 мин, длительность обезболивающего эффекта составляла в среднем 4–6 ч. В некоторых случаях использовалось разовое введение двойной дозы 60 мг, тогда обезболивающая эффективность усиливалась, хотя длительность анальгетического действия не изменялась. При сравнительном анализе обезболивающего терапевтического эффекта кетанова и трамала (рис. 1) статистически достоверных различий не обнаружено.
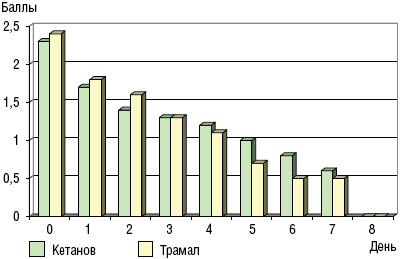 Рис. 1Рис. 1. Оценка эффективности кетанова средней степени выраженности
Рис. 1Рис. 1. Оценка эффективности кетанова средней степени выраженности - При болевом симптомокомплексе тяжелой степени (больные 1-й и 2-й групп, 21 человек) действия одного кетанова было недостаточно, поэтому в базовые схемы добавляли трамал. Таким образом, мы имели возможность сравнить терапевтическое действие 2 препаратов изолированно и при их сочетании (рис. 2). Видно, что наибольшая обезболивающая активность наблюдалась при сочетанном применении кетанова и трамала.
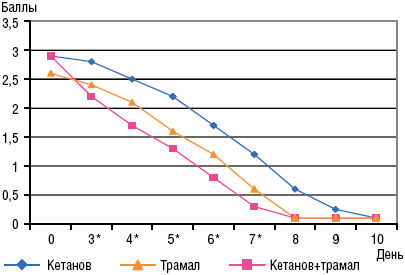 Рис. 2Рис. 2. Сравнительная оценка изолированного применения кетанова и трамала и их сочетания при выраженной степени болевого синдрома
Рис. 2Рис. 2. Сравнительная оценка изолированного применения кетанова и трамала и их сочетания при выраженной степени болевого синдрома
Примечание. * – достоверные различия между группами на 3–7-й день терапии (р<0,05). Отдельно следует отметить, что суточная доза трамала при таком сочетанном применении препаратов не превышала 200 мг (при монотерапии трамалом суточная доза достигает 400–600 мг). Снижение доз антагонистов-агонистов являлось положительным моментом, так как снижался риск побочных эффектов и привыкания к препарату. Базовое применение кетанова позволяло не только снизить суточные дозы трамала, но и уменьшить длительность его применения до 3–4 дней (табл. 3). Таблица 3
Сочетанное использование НПВП (кетанов) и антагонистов-агонистов (трамал)
Кетанов вводили внутримышечно лишь в первые 4–5 дней, в последующем пациентов переводили на таблетированную форму препарата с учетом адекватной терапевтической дозы. Трамал применяли только на высоте развития болевой симптоматики, в связи с чем осуществлялось только парентеральное (внутримышечное) его введение; таблетированные формы препарата не применялись. При сочетанном применении кетанова и трамала наблюдалось потенцирование анальгетического действия, что, в свою очередь, оказывало положительное влияние на общее состояние пациентов: они становились спокойнее, достаточно быстро засыпали при плановых назначениях, сон был продолжительным, глубоким, без пробуждений в течение ночи и без возобновления болевых ощущений. Таким образом, адекватные терапевтические мероприятия, направленные на снижение болевой симптоматики, позволяли опосредованно улучшать и психическое состояние пациентов, что во многом определяло успешность проводимого лечения.Препарат Дни лечения 1 2 3 4 5 6 7 8 9 10 Кетанов
(90–120 мг/сут)+ + + + + + + + +/- +/ Трамал
(200–400 мг/сут)+ + + + - У больных со сформированной зависимостью от трамала кетанов являлся препаратом первого выбора. Его достаточно выраженная анальгетическая активность позволяла с высокой степенью безопасности проводить терапию у данного контингента пациентов. В этом случае принципиальным являлся вопрос о применяемой дозе. При средней степени выраженности болевой симптоматики действие кетанова было достаточным в средней терапевтической дозе (90 мг/сут), при тяжелых проявлениях применялась высшая терапевтическая доза (120 мг), при недостаточности обезболивающего эффекта в терапевтические схемы добавляли другие анальгетики или нейролептики. Немаловажен в наркологической практике вопрос о развитии постинъекционных инфильтратов после введения определенных групп препаратов или их больших количеств. При использовании кетанова таких осложнений не наблюдалось, при внутримышечном введении препарат быстро всасывался, не отмечено и местно-раздражающего его действие. На протяжении всего периода применения кетанова каких-либо побочных действий или осложнений не наблюдалось. Возможно, это связано с коротким курсом назначения препарата. Случаев привыкания к кетанову также не отмечено. При взаимодействии кетанова с другими психотропными препаратами не было ни усиления, ни ослабления действия последних. Использование шкалы общего клинического впечатления позволило подтвердить значительный терапевтический эффект кетанова (рис. 3, 4).
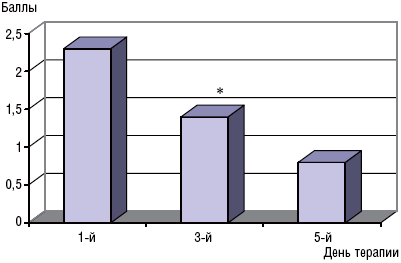 Рис. 3
Рис. 3
Рис. 3. Шкала общего клинического впечатления от терапевтической эффективности кетанова при лечении больных с опиатной зависимостью (общая выборка, средний балл)
Примечание. Терапевтическую эффективность оценивали, только принимая в расчет влияние препарата; * – р<0,05.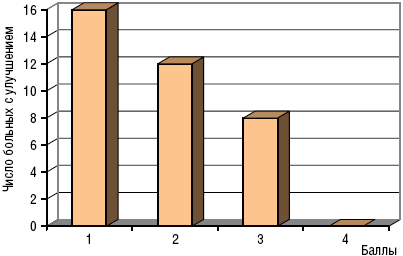 Рис. 4
Рис. 4
Рис. 4. Шкала общего клинического впечатления («общее улучшение
Примечание. Баллы отражают терапевтический эффект через 5 дней применения кетанова: 1 – существенное улучшение; 2 – умеренное улучшение; 3 – незначительное улучшение; 4 – изменений нет или ухудшение.
Итак, кетанов оказывает достаточное обезболивающее действие при болевом синдроме средней степени выраженности, при тяжелых проявлениях абстинентного синдрома может применяться как базовое средство в сочетании с традиционными антагонистами-агонистами (трамалом). Кетанов обладает высокой безопасностью в дозах, необходимых для достижения полноценного обезболивающего эффекта; осложнений, побочных явлений, нежелательного взаимодействия с другими препаратами, случаев привыкания к кетанову не наблюдалось. При наличии зависимости от трамала является препаратом первого выбора.
Полученные результаты расширяют терапевтические возможности врачей психиатров-наркологов, позволяют рекомендовать включение кетанова в комплексные программы лечения опиатной зависимости.
1 В данном случае было трудно определить, использовался метадон, изготовленный промышленным или кустарным способом. В отношении этого факта специальная дифференциация группы не проводилась.
2 В связи с малым объемом выборки применялась простая рандомизация с использованием таблицы случайных чисел.
Литература
- Бабаян Э. А., Булаев В. М. Фармакологические аспекты лечения наркоманий, вызываемых морфиноподобными средствами // Журнал невропатологии и психиатрии им. С. С. Корсакова. – 1989; 88 (1): 134–139.
- Буйков В. А., Хамидулин Э. И. Биологические методы терапии в лечении больных опийными наркоманиями и барбитуровыми токсикоманиями // 6-й Всероссийский съезд психиатров. – Томск, 1990; 2: 202–203.
- Воронин К. Э., Рохлина М. Л., Петракова Л. Б. Клинические проявления и патогенетические методы лечения опийного абстинентного синдрома // Актуальные проблемы медико-социальной реабилитации больных алкоголизмом и наркоманиями. – М., 1994; 125–129.
- Иванец Н. Н., Анохина И. П., Стрелец Н. В. Современное состояние проблемы наркоманий в России // Вопросы наркологии. – 1997; 3: 3–12.
- Иванец Н. Н., Винникова М. А. Героиновая наркомания (постабстинентное состояние: клиника и лечение). – М.: Медпрактика, 2000. – 121 с.
- Иванец Н. Н., Винникова М. А. Кетанов в терапии абстинентного синдрома у больных с опийной (героиновой) зависимостью: пособие для врачей. – М., 2003. – 16 с.
- МКБ-10.
- Погосов А. В. Некоторые клинико-динамические особенности опийного абстинентного синдрома: сб. научн. трудов. Тезисы работ. – Душанбе, 1992; 19–22.
- Рохлина М. Л. и соавт. Принципы фармакотерапии наркоманий: пособие для врачей психиатров-наркологов. – М., 1997. – С. 18.
- Adelekan M., Green A. et al. // Drug and Alcohol Review. – 1996; 15 (3): 261–270.
- Meyer R. E., Mirin S. M. The heroin stimulus. – New-York, 1979. – Р. 231–245; 93–118; 215–230.
- Shuckit M. A. Opiates and other analgesics // Drug and alcohol abuse. – 1989; 118–142, 307.
