Факторы, определяющие правильность и эффективность лечения детей с железодефицитной анемией
Статьи И.С.Тарасова, В.М.Чернов / Вопросы практической педиатрии, 2011, т. 6, №3И.С.Тарасова, В.М.Чернов
Федеральный научно-клинический центр детской гематологии, онкологии и иммунологии Минздравсоцразвития России, Москва
Лекция посвящена лечению железодефицитной анемии у детей. Подробно рассмотрены: расчет оптимальной дозы пероральных препаратов железа; выбор современного препарата железа; применение наиболее эффективного терапевтического плана; контроль эффективности лечения и его стоимость. Обсуждены недостатки и достоинства основных препаратов железа. Доказана высокая эффективность нового терапевтического плана лечения железодефицитной анемии с применением 100% дозы препарата железа в течение всего курса. Расчеты, учитывающие количество элементарного железа в одной таблетке, количество таблеток в упаковке и потребности в препарате на курс лечения показали, что стоимость курса лечения железодефицитной анемии с использованием препаратов трехвалентного железа на основе гидроксид-полимальтозного комплекса выше, чем при применении солевых препаратов железа. Однако эта разница не так велика, как это может показаться при сравнении стоимости одной упаковки препаратов. Более высокая стоимость не должна служить основанием для отказа от использования препаратов трехвалентного железа на основе гидроксид-полимальтозного комплекса, поскольку их хорошая переносимость и отсутствие нежелательных явлений обусловливают высокую приверженность больного к терапии, что, в конечном итоге, определяет ее успех.
Ключевые слова: дети, железодефицитная анемия, препараты железа, дозы, терапевтический план, эффективность, стоимость лечения, Мальтофер
Factors determining correctness and effectiveness of treating children with iron-deficiency anemia
I.S.Tarasova, V.M.Chernov
Federal Scientific and Clinical Center of Pediatric Hematology, Oncology and Immunology, Ministry of Public Health and Social Development of the Russian Federation, Moscow;
The lecture deals with treatment of iron deficiency anemia in children. A detailed account is given of calculating optimal doses of peroral iron drugs; choice of a modern iron drug; use of the most effective therapeutic treatment plan; control of effectiveness of treatment and its cost. Shortcomings and benefits of the main iron drugs are discussed. High effectiveness of a new therapeutic treatment plan for iron deficiency anemia with using a 100% dose of iron medication during the whole course has been proven. Calculations taking into account the amount of elemental iron in a tablet, the number of tablets in a package and drug requirements for a course of treatment showed that the cost of the course of treatment of iron deficiency anemia with using ferric (III) hydroxide polymaltose complexes is higher than in using iron salt drugs. However, this difference is not so great as it might seem as compared to the cost of one drug package. A higher cost should not be the reason to reject the use of ferric iron drugs based on hydroxide-polymaltose complex, since their good tolerance and absence of adverse effects ensure high adherence of a patient to therapy, which, in the long run, conditions its success. Key words: iron-deficiency anemia, iron drugs, doses, therapeutic plan, effectiveness, cost of treatment, Maltofer
Приступая к лечению железодефицитной анемии (ЖДА), необходимо еще раз проверить, правильно ли установлен диагноз. В детской практике 90% всех анемий являются железодефицитными [1]. Остальные 10% - это анемии, сопровождающие хронические заболевания, ранняя анемия недоношенных, наследственные и приобретенные гемолитические и апластические анемии. При этих анемиях препараты железа не только неэффективны, но при некоторых из них противопоказаны.
Расчет дозы препарата железа
В России лечение ЖДА определяется протоколом, утвержденным Минздравсоцразвития России 22 октября 2004 г. - «Протокол ведения больных. Железодефицитная анемия» [2]. Создание этого протокола группой ведущих специалистов нашей страны явилось значительным движением вперед, поскольку «вооружило» врачей единым пониманием проблемы дефицита железа, критериями его диагностики, принципами лечения, ведения больных ЖДА, оценки качества их жизни.
С точки зрения врача-педиатра, лечение ЖДА у детей имеет некоторые особенности, которые следует учитывать в лечебном протоколе. Прежде всего, применение у детей в возрасте до 3 лет солевых препаратов двухвалентного железа в дозе 5-8 мг/кг массы тела в сутки, как это рекомендовано в «Протоколе», вызывает проявления токсичности у многих больных и не оправдано с терапевтической точки зрения.
При расчете доз солевых препаратов железа мы используем рекомендации Всемирной организации здравоохранения (ВОЗ) [3, 4] (табл. 1). Аналогичная доза солевых препаратов железа (3 мг/кг массы тела в сутки) для детей в возрасте до 3 лет указана и в пособии для врачей, утвержденном Департаментом здравоохранения Москвы в 2004 г. [5].
|
Таблица 1. Возрастные терапевтические дозы пероральных солевых препаратов железа для лечения железодефицитной анемии у детей (ВОЗ, 1998) [3] |
|
|
Возраст |
Суточная доза элементарного железа |
|
До 3 лет |
3 мг/кг массы тела |
|
Старше 3 лет |
45-60 мг |
|
Подростки |
До 120 мг |
Различный возраст детей (от периода новорожденности до старшего подросткового периода) и, соответственно, различная масса тела (3,2-70 кг и более) делают необходимым индивидуальный расчет дозы препарата железа для каждого ребенка.
В «Протоколе» рекомендуют рассчитывать дозу препарата на основе гидроксидполимальтозного комплекса (ГПК) трехвалентного железа, ориентируясь на возраст детей, а не на массу их тела. Мы считаем, что в детской практике доза препаратов железа (III) на основе ГПК должна составлять 5 мг/кг массы тела в сутки независимо от возраста; именно эту дозу рекомендует упомянутое выше пособие для врачей [5].
Выбор препарата железа
Выбор препарата железа для лечения ЖДА является задачей лечащего врача. Врач назначает препарат с учетом собственного опыта, информации о новых препаратах, полученной на выставках, из медицинских журналов или Интернета, материальных возможностей родителей больного ребенка (приобретение препарата на весь курс лечения). Вместе с тем, нельзя игнорировать тот факт, что в мировой практике наметилась тенденция смены солевых препаратов двухвалентного железа на менее токсичные препараты железа (III) на основе ГПК.
Многие годы в лечении ЖДА у детей и взрослых применяли солевые препараты железа, а назначение сульфата железа считали «золотым стандартом» терапии, поэтому не случайно, что большинство солевых препаратов железа представлено именно этим соединением (табл. 2). Кроме того, самой высокой всасываемостью обладает сульфат железа, затем - по мере уменьшения этого качества - следуют глюконат, хлорид и фумарат железа.
|
Таблица 2. Некоторые современные пероральные препараты железа |
|
|
Соль/соединение железа |
Препарат |
|
Сульфат железа |
Актиферрин |
|
Глюконат железа |
Тотема |
|
Хлорид железа |
Гемофер |
|
Фумарат железа |
Ферретаб комп. Железа фумарат Железа фумарат 200 Ферронат |
|
Гидроксид-полимальтозный комплекс |
Мальтофер Феррум Лек Орофер |
Однако применение солевых препаратов железа сопряжено со многими проблемами и нежелательными явлениями [6, 7]:
• возможность передозировки и даже отравлений вследствие неконтролируемого всасывания в желудочно-кишечном тракте (ЖКТ);
• взаимодействие с другими лекарственными препаратами и пищей;
• выраженный металлический привкус препаратов;
• окрашивание эмали зубов и десен, иногда стойкое;
• частый отказ пациентов от лечения (до 30-35% от начавших лечение), то есть низкая комплаентность.
Ситуация принципиально изменилась с разработкой препаратов железа (III) на основе ГПК. Особенности строения этого комплекса: высокая молекулярная масса, наличие ядра трехвалентной гидроокиси железа, состоящего из 260 атомов, высокое содержание железа в ядре (около 27%), полимальтозная оболочка. По строению и валентности молекула препарата железа (III) на основе ГПК похожа на молекулу ферритина.
Препараты железа (III) на основе ГПК обладают следующими основными свойствами и преимуществами [8]:
• высокая эффективность;
• высокая безопасность, отсутствие риска передозировки, интоксикации и отравлений;
• отсутствие потемнения десен и зубов;
• приятный вкус;
• отличная переносимость, определяющая высокую комплаентность;
• отсутствие взаимодействия с другими лекарственными препаратами и пищей;
• наличие антиоксидантных свойств.
Причины неэффективности лечения препаратами железа:
• применение низких доз;
• сокращение длительности курса лечения по вине больного или врача;
• нарушение всасываемости;
• лечение хронической постгеморрагической анемии без выявления и/или без устранения источника кровопотери.
Крайне редко не удается достичь излечения ЖДА с помощью стандартной терапии препаратами железа. Недавно американские ученые установили, что хроническое течение
заболевания и отсутствие ответа на лечение препаратами железа при ЖДА обусловлены наличием различных мутаций в гене TMPRSS6 [9]. Предполагается, что обнаруженные мутации приводят к избыточному синтезу гепцидина -белка, который регулирует в организме два важных процесса: всасывание железа в кишечнике и высвобождение его из макрофагов в процессе реутилизации [9, 10].
Терапевтический план лечения ЖДА
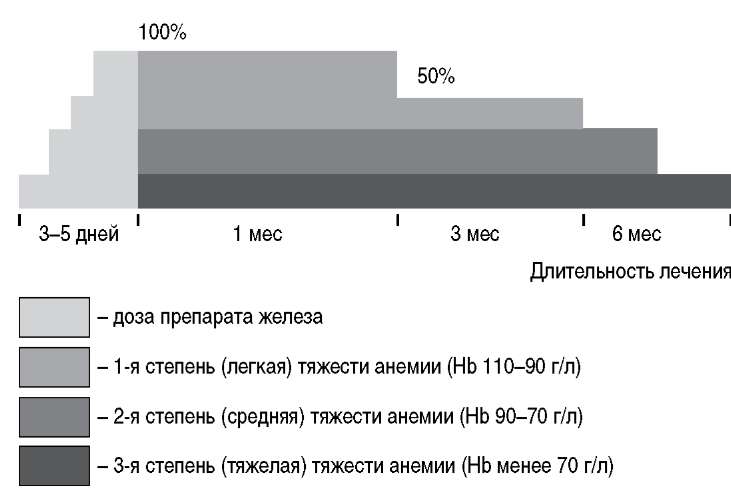
В российской педиатрической практике многие годы был принят так называемый «трапециевидный» терапевтический план лечения ЖДА у детей (рисунок). Этот план был рассчитан на солевые препараты железа, поскольку других тогда просто не существовало. В соответствии с этим планом в первые 3-5 дней дозу солевых препаратов железа постепенно повышали, чтобы не вызвать у больного раздражения слизистой оболочки ЖКТ. Полную (100%) дозу солевого препарата железа применяли в течение 1,5-3 мес в зависимости от степени тяжести анемии с последующим ее снижением до 50% к окончанию лечения. Этот план, как и большинство других, был разработан эмпирическим путем, и его эффективность никогда не была подтверждена рандомизированными исследованиями.
Появление препаратов железа (III) на основе ГПК заставило пересмотреть план лечения ЖДА.
Под руководством сотрудников Федерального научно-клинического центра детской гематологии, онкологии и иммунологии Минздравсоцразвития России было проведено рандомизированное исследование по сравнению эффективности двух планов лечения ЖДА различной степени тяжести у детей и подростков: традиционного «трапециевидного» и нового, предусматривающего прием 100% дозы препарата железа (III) на основе ГПК в течение всего периода лечения. Во время исследования оценивали переносимость препарата Мальтофер («Вифор Интернэшнл», Швейцария) и эффективность терапии в ранние (ретикулоцитарная реакция, прирост концентрации гемоглобина - Hb) и поздние сроки (нормализация концентрации Hb, сывороточного железа и сывороточного ферритина). Была доказана эффективность заместительной терапии у детей и подростков с ЖДА препаратом железа (III) на основе ГПК. После завершения курса лечения нормализация концентрации Hb была достигнута у 96,9%, сывороточного железа - у 73,4%, сывороточного ферритина - у 60,9% больных. Незначительное количество (6,3%) нежелательных явлений (запор в течение 1-го месяца лечения) и 100% приверженность пациентов к лечению позволили заключить, что препарат железа (III) на основе ГПК является оптимальным препаратом для терапии ЖДА у детей и подростков [11, 12].
Рисунок. Терапевтический «трапециевидный» план лечения ЖДА, используемый в России.
Также было доказано преимущество использования 100% дозы препарата железа (III) на основе ГПК в течение всего курса лечения: нормализация концентрации сывороточного железа была зафиксирована у 90,6%, сывороточного ферритина - у 75% детей и подростков. При использовании традиционного «трапециевидного» плана лечения эти цифры составили 56,3 и 46,9% соответственно [11, 12].
Об эффективности лечения ЖДА врач может судить по ряду критериев. Наиболее ранним критерием ответа, свидетельствующим о правильности установления диагноза и об эффективности лечения, является ретикулоцитарная реакция. Через 7-10 дней от начала применения препаратов железа повышается количество ретикулоцитов, обычно на 1-2% (10-20%о) по сравнению с исходным. Для оценки эффективности лечения ЖДА препаратами железа также можно использовать критерии, разработанные Центрами по контролю и профилактике заболеваний в США (Centers for Disease Control - CDC). Согласно этим критериям, к концу 4-й недели лечения ЖДА концентрация Hb должна повыситься на 10 г/л, а гематокрит - на 3% по сравнению с исходными значениями [13].
К поздним критериям эффективности лечения ЖДА следует отнести нормализацию концентрации Hb и сывороточного ферритина.
Излечением от ЖДА считают преодоление тканевой сидеропении и восстановление запасов железа в организме. На сегодняшний день признанным на международном уровне маркером запасов железа в организме является ферритин сыворотки крови, несмотря на некоторые существующие ограничения (белок острой фазы воспаления), необходимость забора крови из вены и относительно высокую стоимость его определения.
Стоимость лечения ЖДА у детей
По мнению некоторых врачей, единственным сдерживающим моментом для повсеместного и широкого внедрения препаратов железа (III) на основе ГПК является более высокая их стоимость (в 2-3 раза) по сравнению с солевыми препаратами. Мы рассчитали реальную стоимость курса лечения ЖДА с применением солевых препаратов железа и препарата железа (III) на основе ГПК (табл. 3) При расчетах были использованы средние розничные цены на препараты железа в московских аптеках на 30.01.2011. Оказалось, что с учетом количества элементарного железа, содержащегося в одной таблетке, количества таблеток в упаковке и потребности в препарате на курс лечения ЖДА стоимость последнего при использовании препарата железа (III) на основе ГПК выше, но не настолько, как это может показаться при сравнении стоимости одной упаковки препаратов. Более низкую стоимость одной упаковки солевого препарата железа и приобретение лекарства только по этому признаку мы назвали «синдромом аптечной стойки». Следует подчеркнуть, что более высокая стоимость не должна служить основанием для отказа от использования препаратов железа (III) на основе ГПК. Упомянутые ранее их преимущества, прежде всего, хорошая переносимость и отсутствие нежелательных явлений обусловливают высокую приверженность больного к терапии (комплаентность), что, в конечном итоге, определяет успех лечения.
|
Таблица 3. Основные характеристики различных препаратов железа для лечения железодефицитной анемии у детей |
||||
|
Характеристика |
Препарат |
|||
|
Актиферрин |
Тардиферон |
Ферроплекс |
Мальтофер |
|
|
Форма выпуска |
Капсулы; |
Таблетки, |
Драже; |
Жевательные таблетки; |
|
|
в блистере 10 капсул; 2 блистера в упаковке |
покрытые оболочкой; 10 таблеток в блистере; 3 блистера в упаковке |
100 штук в упаковке |
в блистере 10 таблеток; 3 блистера в упаковке |
|
Соединение железа |
Сульфат железа Fe2+ |
Сульфат железа Fe2+ |
Сульфат железа Fe2+ |
Гидроксидполимальтозный комплекс Fe3+ |
|
Содержание элементарного железа в 1 капсуле/таблетке, мг |
34,5 |
80 |
10 |
100 |
|
Содержание элементарного |
690 |
2400 |
1000 |
3000 |
|
железа в упаковке, мг |
|
|
|
|
|
Средняя розничная цена |
86 |
165 |
90 |
340 |
|
упаковки в аптеках Москвы |
|
|
|
|
|
на 30.01.2011, руб. |
|
|
|
|
|
Стоимость 1 мг элементарного |
0,12 |
0,07 |
0,09 |
0,11 |
|
железа, руб. |
|
|
|
|
|
Доза, мг/кг массы тела |
3 |
3 |
3 |
5 |
|
Стоимость курса лечения*, руб. |
972 |
567 |
729 |
1485 |
|
'Стоимость курса лечения железодефицитной анемии длительностью 90 дней рассчитана для ребенка с массой тела 30 кг. | ||||
Мы считаем, что практикующие врачи должны быть полностью ориентированы в экономической части вопроса и объяснять родителям преимущества лечения ЖДА с помощью препаратов железа (III) на основе ГПК.
Выполнение предложенных рекомендаций позволит врачампедиатрам улучшить результаты лечения ЖДА у детей и подростков, а широкое обсуждение проблемы позволит разработчикам «Протокола» внести в него необходимые изменения.
Литература
1. Хертл М. Дифференциальная диагностика в педиатрии. М.: Медицина, 1990; 2: 512.
2. Протокол ведения больных. Железодефицитная анемия. М.: Ньюдиамед, 2005; 76.
3. WHO, UNICEF, UNU. IDA: prevention, assessment and control: report of joint WHO/UNICEF/UNU consultation. Geneva, WHO; 1998.
4. World Health Organization. Iron deficiency anemia: assessment, prevention and control. A guide for programme managers. Geneva, 2001 (WHO/NHD/01.3): 132.
5. Румянцев А.Г., Коровина Н.А., Чернов В.М. и др. Диагностика и лечение железодефицитной анемии у детей. Методическое пособие для врачей. М.,2004; 45.
6. Самсыгина Г.А. Железодефицитные анемии у детей. Фармакологи и фармакокинетика современных ферропепаратов. В кн.: Дефицит железа и железодефицитная анемия / под ред. Н.С.Кисляк и др. М.: Славянский диалог, 2001; 108-13.
7. Дворецкий Л.И., Заспа Е.А. Железодефицитные анемии в практике акушера-гинеколога. Русский медицинский журнал 2008; 16(29): 1898-906.
8. Мальтофер. Монография по препарату. 3-е изд. М.: Мега Про, 2001; 96.
9. Finberg K., Heeney M., Campagna D., et al. Mutations in TMPRSS6 cause iron-refractory iron deficiency anemia (IRIDA). Nat Genet 2008; 40(5):569-71.
10. Маянский Н.А., Семикина Е.Л. Гепцидин: основной регулятор обмена железа и новый диагностический маркер. Вопросы диагностики в педиатрии 2009;1(1): 18-23.
11. Ожегов Е.А., Тарасова И.С., Ожегов А.М. и др. Сравнительная эффективность двух терапевтических планов лечения железодефицитной анемии у детей и подростков. Вопросы гематологии/онкологии и иммунопатологии в педиатрии 2005; 4(1): 14-9.
12. Ожегов Е.А. Оптимизация лечения железодефицитной анемии у детей и подростков. Автореф. дисс. ... канд. мед. наук. М., 2005; 23.
13. Recommendations to prevent and control iron deficiency in the United States. Centers for Disease Control and Prevention. MMWR Recomm Rep 1998; 47(RR-3): 1-29.
Комментарии
ПРАКТИКА ПЕДИАТРА
