Современные подходы к терапии ОРВИ у детей
Статьи Опубликовано в журнале:
« Сonsilium medicum - Педиатрия » экстравыпуск №3 А.Л.Заплатников
Острые респираторные инфекции вирусной этиологии (ОРВИ) продолжают занимать лидирующую позицию в структуре инфекционных заболеваний вне зависимости от возраста и характеризуются полиэтиологичностью. К сожалению, к подавляющему большинству возбудителей, вызывающих ОРВИ, нет вирулицидных препаратов с прямым действием. Только группа противогриппозных лекарственных средств является истинно противовирусной, все остальные препараты относятся к группе широкого спектра действия, но действуют опосредованно, через влияние на иммунные и неспецифические защитные системы самого организма. К сожалению, в обозримом будущем вряд ли в арсенале педиатров появятся экспресс-методы диагностики, которые позволят идентифицировать огромное количество респираторных вирусов-патогенов. Следовательно, каждый раз выбор терапии при ОРВИ – это обращение к клиническому опыту врача и эпидемиологическим сводкам, но нередко назначение осуществляется вслепую. При доказанной гриппозной этиологии, безусловно, препаратами выбора являются специфические противогриппозные препараты на основе озельтами-вира и занамивира. Однако следует подчеркнуть, что это хи-миопрепараты, а значит, их частое и необоснованное назначение приведет к возникновению и распространению резистентных штаммов.
С момента инфицирования параллельно нарастанию титров вирусов увеличиваются содержание и функциональная активность факторов врожденного иммунитета, в первую очередь, интерферонов (ИФН) и натуральных киллеров. Т-лимфоциты и В-лимфоциты начнут играть свою роль только после инициации иммунного ответа. На фоне взаимодействия антиген-презентирующих клеток и Т-хелперами в процесс начинает подключаться гуморальное и клеточное звенья адаптивного иммунитета – Т-и В-лимфоциты. Так, к концу недели, когда информация об антигенной структуре будет передана на В-лимфоциты, нужный клон В-лимфоцитов начнет вырабатывать антитела к различным мишеням возбудителя инфекции. При этом адекватно высокие (защитные) уровни антител будут достигнуты лишь через несколько недель после первичного инфицирования. Это еще раз подчеркивает роль врожденных факторов иммунитета в защите и уменьшении распространения возбудителя при первичном инфицировании.
Экспериментальные данные показывают, что у животных с искусственно выключенной системой ИФН наблюдаются увеличение продолжительности периода максимальной концентрации вирусов в организме и более длительный период их элиминации по сравнению с животными с полноценным иммунным ответом и адекватной работой системы ИФН. Поэтому, назначая препараты ИФН или их индукторы, мы вправе ожидать значимый лечебный эффект, но при условии, что терапия этими препаратами начинается в первые часы заболевания. Это не всегда достижимо, но стремиться к этому нужно.
При применении данной группы препаратов необходимо сделать выбор: применять заместительную терапию (природные или рекомбинантные ИФН) либо использовать индукторы ИФН? Конечно, есть четкие показания для назначения и тех и других препаратов. Так, у детей с низкой эффективностью выработки собственного ИФН в остром периоде заболевания могут быть эффективны заместительные препараты. В то же время, если система синтеза эндогенного ИФН несущественно повреждена, лучше использовать индукторы.
Известно, что, дети, склонные к реккурентным респираторным инфекциям, в большинстве случаев имеют поздний старт системы ИФН и сниженную продукцию в ответ на те или иные патогены. Вместе с тем, учитывая заболеваемости таких детей (нередко за один эпидсезон у них регистрируется 3-4 эпизода ОРВИ), при выборе индуктора ИФН следует учитывать необходимость назначения препаратов для лечения ОРВИ, в том числе индукторов ИФН, повторными курсами без развития ряда нежелательных явлений. В данном контексте имеются в виду не побочные эффекты, напрямую связанные с применением того или иного медикамента, а развитие резистентности и/или толерантности.
Развитие резистентности, связано в первую очередь, с применением специфических противогриппозных препаратов. По данной причине в течение нескольких последних лет Всемирная организация здравоохранения не рекомендует в качестве этиотропных средств любые производные ремантадина, так как более 70% эпидемических штаммов вирусов гриппа резистентно к этим препаратам. По данным прошедшего эпидсезона 2014–15 гг., 99,4% эпидемических штаммов вируса гриппа чувствительны к занамивиру и озельтамивиру, поэтому их надо оставить в качестве препаратов резерва, в частности для случаев истинно гриппозной инфекции, особенно тяжело протекающей. К сожалению, назначение этих препаратов вслепую – повальная беда в реальной клинической практике. Риск развития толерантности, а также явление гипореактивности после значительной стимуляции функций может быть связано с применением индукторов ИФН, кроме того, не следует забывать о возможных межлекарственных взаимодействиях, с развитием как потенцирующих, так и антагонистических эффектов.
В многочисленных исследованиях доказано, что на фоне применения Анаферона детского (индуктор ИФН избирательного действия на основе релиз-активных антител к ИФН-γ– Анаферон детский, являющийся по механизму действия модификатором естественной активности ИФН-γи его рецептора) быстро купируются основные общие симптомы ОРВИ: лихорадка, головная боль, недомогание, чувство озноба. В серии клинических работ было показано, что Анаферон может применяться повторными лечебными и профилактическими курсами без снижения эффективности и без развития нежелательных эффектов, включая изменения реактивности системы ИФН. Учитывая это, становится понятным, почему препараты на основе релиз-активных антител к ИФН-γ– единственные индукторы ИФН, которые разрешены к применению у детей в возрасте до 1 года (Анаферон детский – с 1-го месяца, Эргоферон – с 6 месяцев). Другие препараты, обладающие свойствами стимулировать продукцию ИФН, разрешены только начиная с 3-летнего (Арбидол, Кагоцел – с 3 лет, Циклоферон – с 4 лет, Амиксин – с 7 лет).
В связи с изложенным, не вызывает сомнений актуальность поиска, разработки и внедрения в клиническую практику новых эффективных и безопасных противовирусных лекарственных средств.
Одним из таких препаратов является новый препарат на основе антител к ИФН-γ в релиз-активной форме – Эргоферон. Препарат разрабатывался, прежде всего, для лечения вирусных инфекций и дополнительно в его в состав включены релиз-активные формы антител к CD4 и гистамину. Для того, чтобы понять идею создания этого препарата, надо вспомнить следующее.
После инфицирования вирусами для развитии адекватного противовирусного ответа очень важно, чтобы после включения первичных неспецифических реакций со стороны макрофагов и естественных киллеров под влиянием Т-лимфоцитов хелперов произошла активация иммунного ответа по Тh-первому типу с включением в первую очередь клеточного звена иммунитета (цитотоксические Т-лифоциты, несущие рецепторы к специфическим антигенам возбудителя инфекции), а несколько позже, с дополнительной активацией и гуморального специфического реагирования (продукция антител плазмоцитами).
Можно сказать, что ключевым звеном этого сложного механизма является процесс антиген-презентации с участием CD4+ клеток: макрофагов (дендритные клетки, например) и Т-лимфоцитов (Т-хелперы), который регулируется через активность ИФН-g. С учетом того, что релиз-активные формы антител способны напрямую модифицировать функциональную активность молекул-мишеней, становится понятным механизм действия Эргоферона. За счет синергидного влияния на активность двух сонаправленно действующих систем (ИФН и система распознавания антигенов возбудителя инфекции), Эргоферон оказывает усиленное противовирусное действие. Вместе с тем, за счет уменьшения выраженности гистамин-зависимых реакций (благодаря модифицирующему влиянию антител к гистамину) и восстановления баланса активности про-и противовоспалительных цитокинов (действие антител к ИФН-γи CD4) Эргофеорн позволяет подойти к решению проблемы полипрагмазии.
В рамках изучения течения ОРВИ у детей на фоне применения наиболее широко применяющихся препаратов, нами было проведено проспективное открытое рандомизированное исследование эффективности и переносимости Эргоферона, Кагоцела, Арбидола у детей старше 3 лет в условиях сезонных подъемов заболеваемости на протяжении двух эпид-сезонов (осень 2012 – весна 2013 г., осень 2013 – весна 2014 г.). Исследование проводилось в двух центрах – на базе Новосибирского медицинского университета и Российской медицинской академии последипломного образования. Для участия в исследовании отбирали детей от 3 до 9 лет, которые имели признаки ОРВИ, возникавшие не позднее 48 ч до включения в исследование/начала терапии: повышение аксиллярной температуры тела не ниже 37,8°C, катаральные симптомы (кашель, затруднение носового дыхания, выделения из носовых ходов, осиплость голоса, боль в горле) и симптомы интоксикации (миалгия, озноб/потливость, недомогание, слабость, головная боль и снижение аппетита).
Непременным условием было информированное согласие от родителя/представителя ребенка. Благодаря четкому мониторингу к итоговому обзору удалось подвести 152 из 167 включенных пациентов (часть пациентов не завершила исследование из-за несоблюдения графика визитов к врачу). Все пациенты методом рандомизации были распределены на 3 группы – Э, К и А: Эргоферон (n=67), Кагоцел (n=40) и Арбидол (n=45). Группы были сравнимы по полу, возрасту, срокам начала терапии, спектру сопутствующих заболеваний и тяжести исходного состояния, а также по клиническим характеристикам (выраженность интоксикационного и катарального синдромов), оцениваемым с помощью 4-х балльной шкалы (0-3).
В ходе статистического анализа было показано, что клиническая эффективность двух препаратов сравнения (Кагоцел и Арбидол) не имела значимых различий. Поэтому для оценки эффективности и переносимости Эргоферона, применяемого в рутинной амбулаторной педиатрической практике релиз-активных препаратов, и традиционных индукторов ИФН с помощью специального статистического анализа группы К и А были объединены в одну группу – группу 2. Группу 1 представляли пациенты, получавшие Эргоферон. Между скорректированными группами значимых различий демографических и клинических характеристик не было. При анализе данных, полученных на 2-м визите, была отмечена выраженная положительная динамика в группах 1 и 2. Между пациентами двух групп не было выявлено различий в быстроте купирования симптомов – как интоксикации, так и катаральных симптомов (рис. 1, 2).
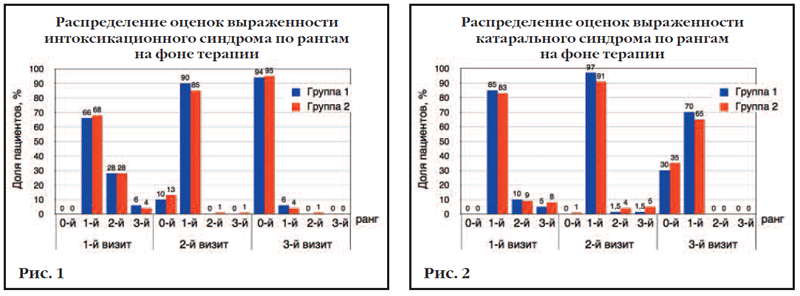
Вместе с тем, в группе детей, получавших Эргоферон, отмечался ряд значимых отличий. Прежде всего, это проявилось более высокими оценками эффективности и переносимости Эргоферона по сравнению с другими препаратами, применяемыми в исследовании. Кроме того, в ходе специального анализа было выявлено, что общее число назначений медикаментов в 1-й группе было в 1,4 раза меньшим, чем в группе сравнения (р=0,01), а доля детей, получавших более 5 медикаментов – в 1,8 раза меньшей, чем во 2-й группе (p=0,05). Применение Эргоферона для терапии ОРВИ в 1-й группе позволило уменьшить и количество назначаемых лекарственных препаратов, и длительность их использования, что снижает медикаментозную нагрузку на организм ребенка и позволяет решить фармакоэкономические проблемы терапии ОРВИ.
Таким образом, результаты проведенного исследования в целом свидетельствуют о сопоставимой клинической эффективности и переносимости применения исследованных схем терапии ОРВИ у детей. В ходе исследования не было зарегистрировано побочных эффектов, связанных с приемом тех или иных компонентов изучаемых схем терапии. При этом в группе детей, получавших Эргоферон, чаще регистрировались более высокие оценки качества терапии (эффективность и переносимость) как со стороны врачей, так и родителей. В группе Эргоферона было достоверно меньшее количество используемых препаратов, а также достоверно снижалась продолжительность применения антигистаминных препаратов.


