Агонисты дофаминовых рецепторов и проблема эквивалентности доз
СтатьиОпубликовано в журнале:
«Неврология/ревматология, приложение consilium medicum», 2010, № 2, с. 46-49
Е.А.Катунина
Кафедра неврологии и нейрохирургии лечебного факультета РГМу им. Н.И.Пирогова, Москва
Агонисты дофаминовых рецепторов (АДАР) используют в клинической практике для лечения болезни Паркинсона (БП) около 40 лет. За это время определены основные механизмы действия этой группы препаратов, уточнены показания к применению, накоплен значительный клинический опыт, касающийся эффективности и переносимости ДЦАР. На сегодняшний день это самая многочисленная группа противо-паркинсонических препаратов. Широкая распространенность АДАР обусловлена рядом преимуществ. В отличие от леводопы, механизм их действия связан со стимуляцией рецепторного аппарата, а не трансформацией веществ в условиях дегенерирующего нейрона черной субстанции. Важным преимуществом этой группы препаратов является отсутствие конкурентного всасывания с аминокислотами пищи в желудочно-кишечном тракте, длительный период полувыведения и, что очень важно, меньший риск развития моторных флуктуации и лекарственных дискинезий [1-17]. За счет стимуляции D2/D3-рецепторов мезолимбического и мезокортикального пути АДАР помимо противопаркинсонического эффекта обладают положительным влиянием на когнитивную и эмоционально-аффективную сферу. АДАР представлены различными лекарственными формами. Большинство - традиционно таблетированной формой (пирибедил, прамипексол, ропинерол, бромокриптин, перголид, карбеголин), накожным пластырем (ротиготин), подкожными инъекциями (апоморфин). Согласно рекомендациям Европейской федерации неврологов и Протокола ведения пациентов с БП, утвержденного Минздравсоцразвития РФ в 2005 г., АДАР рекомендованы в качестве препаратов выбора для лечения начальных стадий БП в виде монотерапии, а также в комбинации с леводопой с целью усиления эффективности применяемой терапии на развернутых стадиях болезни, коррекции моторных флуктуации и лекарственных дискинезий.
Нередко в процессе лечения АДАР возникает необходимость замены одного препарата другим. Это может быть связано с недостаточной изначальной эффективностью препарата, вторичным снижением эффекта или развитием побочных эффектов [18,19]. На сегодняшний день используют несколько вариантов перевода. Смена препарата может происходить постепенно с уменьшением дозы одного агониста и одновременным увеличением дозы другого либо в виде последовательной полной отмены одного препарата и последующим введением другого. Обсуждается и быстрый способ замены с назначением нового препарата сразу после ночного перерыва. Метод быстрой замены препарата продемонстрировал хорошую переносимость в ряде исследований и позволяет избежать периода ухудшения симптомов паркинсонизма [20, 21]. Вместе с тем, при переводе пациента с одного АДАР на другой встает вопрос об эквивалентности доз. Исследований, напрямую сравнивающих эффективность терапии при быстрой смене одного АДАР на другой, достаточно мало. Вместе с тем, имеется ряд исследований, посвященных эффективности и переносимости АДАР различных групп при добавлении их к терапии леводопой и последующим ретроспективным сравнением эффективных доз препаратов с вычислением коэффициента соотношения доз.
В данной статье приводится обзор литературы, проведенный S.Thobois с использованием поисковой системы MEDLINE и базы данных Кокрановской библиотеки и опубликованный в журнале «Clnincal Therapeutics» за 2006 г. [22].
Сравнение пирибедила и бромокриптина
В двойном слепом исследовании Parkinson-CONROL [23] сравнивали эффективность долгосрочной терапии бромокриптином и пирибедилом на фоне применения леводопы у пациентов с недостаточным контролем моторных функций. Участники бьши рандомизированы на 2 группы. В группе пирибедила (n=210) дозу увеличивали до 150 мг/сут, а в группе бромокриптина (n=215) - до 2 5 мг/сут. Группы пациентов на момент начала исследования бьши однородны по тяжести состояния (средний балл по III разделу шкалы UPDRS составил в группе пирибедила 23,8±9,3 и 24,1±10,6 - в группе бромокриптина). Через 12 мес терапии положительный эффект (снижение индекса по шкале UPDRS - унифицированная рейтинговая шкала оценки проявлений БП, S.Fahn, RElton, 1987) был зарегистрирован у 60,8% пациентов в группе пирибедила и у 58,196 - в группе бромокриптина, различие между группами было недостоверным [23]. Средняя доза леводопы/ингибитора дофамин декарбоксилазы (ДДК) составила 395/127 мг/сут в группе пирибедила и 391/122 мг/сут - в группе бромокриптина. Показатели частоты и тяжести побочных явлений не отличались между группами. Данное исследование было продолжено еще на 12 мес в группе из 27 человек, получавших пирибедил, и 25 человек, получавших бромокриптин [24]. Улучшение симптомов, достигнутое через 1 год лечения, сохранялось к концу 2-го года в 2 группах. Достоверных различий по шкале UPDRS не было, но в группе пирибедила суточная доза леводопы/ингибитора ДДК была достоверно меньше - 382/164 мг/сут (в группе бромокриптина - 434/151 мг/сут) [24]. Таким образом, фиксированные дозы 150 мг/сут пирибедила и 25 мг/сут бромокриптина приводили к сходному улучшению клинической симптоматики и одинаково переносились пациентами. Хотя исследование Parkinson-CONROL [23] не было предназначено для установления эквивалентности доз, проведенный ретроспективный анализ определил соотношение эквивалентных доз бромокриптина и пирибедила как 1:6.
Сравнение перголида и бромокриптина
G.Pezzolli и соавт [25] провели простое 12-недельное исследование, в котором сравнивали терапию бромокриптином и перголидом у 68 пациентов с БП, находящихся на монотерапии леводопой. В течение первого 12-недельного периода пациентам постепенно повышали дозу до 5 мг/сут для перголида и 50 мг/сут для бромокриптина. Для оценки эффективности использовали шкалу NYUPD (New York University Parkinson's Disease Scale). Через 12 нед снижение по использованной шкале было выявлено в группе бромокриптина и перголида, но перголид приводил к достоверно более выраженному улучшению (р=0,01). Достоверные различия имелись по подразделу шкалы NYUPD «Повседневная активность» (р=0,02) и по подразделу «Двигательная активность» (р=0,038). По шкале глобального клинического впечатления (CGI) достоверное уменьшение тяжести заболевания отмечались у 49,1% пациентов в группе перголида и 33,39° - в группе бромокриптина (р=0,001). Соответственно, улучшение симптоматики наблюдалось у 80,7% пациентов в группе перголида и у 63,2% - в группе бромокриптина (р=0,004). Побочные явления, в целом, чаще возникали в группе бромокриптина. Оптимальные дозы бромокриптина и перголида составили 24,2±8,4 и 2,3±0,8 мг/сут соответственно. Более чем у 50% пациентов в этом исследовании примерное соотношение доз бромокриптина и перголида составило 10:1 [25].
Сравнение ропинерола и бромокриптина
В двойном слепом исследовании AKorczyn и соавт. [26, 27] сравнивали долгосрочную эффективность и переносимость ропинерола и бромокриптина у пациентов на ранних стадиях БП, в редких случаях получавших дофаминергические препараты или леводопу Исследование носило долгосрочный характер - 3 года. Постепенно методом титрования с недельными интервалами 168 пациентам в группе ропинерола и 167 в группе бромокриптина увеличивали дозу в зависимости от терапевтического эффекта и переносимости. Максимально разрешенная доза для ропинерола составила 24 мг/сут, для бромокриптина - 40 мг/сут. Трехлетний период лечения завершили примерно 2/3 пациентов (115/168 в группе ропинерола и 110/167 в группе бромокриптина). Среди завершивших исследование улучшение по III разделу («Двигательная активность») шкалы UPDRS на 3196 было в группе ропинерола и на 2296 в группе бромокриптина (различия недостоверны). Улучшение по II разделу («Повседневная активность») шкалы UPDRS было более выраженным в группе ропинерола (р=0,009). В группе ропинерола чаще отмечалось возникновение тошноты (40,596 против 19,896 для бромокриптина), головокружения (22,696 против 19,896), рвоты (14,996 против 7,296), галлюцинаций (9,596 против 9,096) и спутанности сознания (7,796, против 5,496). Проведенный в этом исследовании ретроспективный анализ эквивалентности доз установил, что оптимальное соотношение суточных доз бромокриптина и ропинерола составило 10:5 [26, 27].
Сравнение прамипексола и бромокриптина
M.Guttmann [15] провел рандомизированное двойное слепое исследование оценки эффективности бромокриптина и прамипексола, в сравнении с плацебо, у больных с БП со снижением терапевтической эффективности леводопы. В исследование включили 247 пациентов, его продолжительность составила 9 мес. Длительность периода титрации бромокриптина и прамипексола составила 12 мес, шаг титрации 2 нед. Максимальные дозы составили 30 мг/сут для бромокриптина и 4,5 мг/сут для прамипексола. Снижение балла по III разделу шкалы UPDRS было достоверно более выраженным в группах лечения ДДАР по сравнению с группой плацебо: на 3496 для прамипексола (/К0,001), на 23,896 для бромокриптина (р=0,01) и на 5,796 для плацебо. По II разделу («Повседневная активность») шкалы UPDRS суммарный балл уменьшился на 26,796 для прамипексола (/К0,001), на 1496 для бромокриптина (р=0,02) и на 4,896 для плацебо. Достоверных различий по частоте побочных явлений между группами прамипексола и бромокриптина выявлено не было. Ретроспективный анализ установил коэффициент эквивалентной дозы бромокриптина к прамипексолу равный 10:1-1,5 [15].
Быстрая замена бромокриптина или перголида на прамипексол
Одно из немногих исследований, посвященных быстрой замене одного ДДАР на другой, было проведено CGoets и соавт. [20]. В нем оценивалась эффективность перехода от бромокриптина или перголида на прамипексол, проводившегося двумя способами: быстрым (замена на следующий день в эквивалентной дозе) и медленным (в течение 8 нед). Коэффициенты пересчета составили для прамипексола и бромокриптина 1:10, для прамипексола и перголида —1:1. Оценку эффективности по III разделу шкалы UPDRS проводили через 8 нед (исследование носило слепой характер). Степень улучшения и заключительная доза прамипексола были примерно одинаковы в 2 группах. Тем не менее, время до достижения улучшения моторного балла по III разделу шкалы UPDRS по сравнению с исходным уровнем было значительно меньше в группе с быстрым титрованием доз (2,1 против 5,3 нед;pБыстрая замена бромокриптина или перголида на ропинерол
Цель открытого краткосрочного (4 нед) исследования M.Canesi и соавт [21] заключалась в установлении доз при быстром переходе на ропинерол у пациентов, находившихся на моно- или комбинированной терапии перголидом (n=46) или бромокриптином (n=22). Первоначально использовали соотношение доз бромокриптина и ропинерола 10:6, а перголида и ропинерола - 1:3. Однако соотношение 1:3 для перголида и ропинерола было заменено на 1:6 после выбывания пациентов в связи с нарастанием моторных симптомов БП. Через 4 нед достоверных изменений по шкале UPDRS выявлено не было. Таким образом, результаты исследования показали, что соотношение эквивалентных доз перголид : ропинерол составляет 1:6, бромокриптин: ропинерол - 10:6 [21].
В другом исследовании (S.Gimenez-Roldan и соавт.) сравнивались три отношения эквивалентности доз (5:1, 3:1 и 2:1) при проведении замены бромокриптина на ропинерол [28]. В исследование вошли 23 пациента, получавших лечение бромокриптином и леводопой с недостаточной эффективностью. В течение 1-го месяца дозу бромокриптина постепенно уменьшали, вплоть до полной отмены. Одновременно увеличивали дозу ропинерола на 0,75 мг в неделю и затем корректировали ее по соотношению 5:1. Если эффект был недостаточный, дозу продолжали увеличивать до соотношения 3:1, при необходимости и далее до 2:1. Продолжительность исследования составила 12 нед. Достоверное улучшение по шкале UPDRS было установлено только для соотношения доз бромокриптин: ропинерол - 2:1. При использовании других соотношений у 44% пациентов не отмечалось изменений по шкале UPDRS, а у 37% зарегистрировано ухудшение [28].
Обсуждение
Проблема замены одного препарата на другой является весьма актуальной. Как показало исследование Goetz и соавт, метод быстрой замены (на следующий день после ночного перерыва) является безопасным и может иметь ряд преимуществ: отсутствие переходного периода, который может сопровождаться нарастанием симптомов паркинсонизма; снижение риска возникновения нежелательных явлений, связанных с временным назначением двух АДАР; такая стратегия является менее затратной и, кроме того, этот метод значительно проще как для врача, так и для пациента [20, 29]. Вместе с тем, данная методика еще требует отработки и подтверждения в крупных двойных слепых рандомизированных исследованиях.
При быстрой смене препарата очень важно перейти на адекватную дозу. Имеющиеся на сегодняшний день данные литературы позволяют использовать следующие соотношения: при переходе с бромокриптина на перголид - 10:1, при переходе с бромокриптина на пирибедил -1:6, при переходе с бромокриптина на ропинерол - 5:3, при переходе с бромокриптина на прамипексол -10:1—1,5, при переходе с перголида на ропинерол - 1:6 [29].
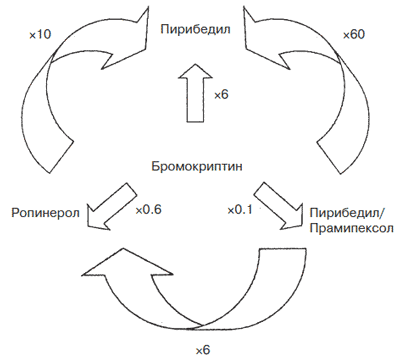
Примечание. Рекомендуемые коэффициенты пересчета для определения оптимальных суточных доз агонистов допаминовых рецепторов при быстрой смене вида терапии у пациентов с БП, основанное на данных литературы [15, 20, 26, 28]. От бромокриптина к прамипексолу точное соотношение доз от 10:1 до 10:1,5 в зависимости от исследования.
ЛИТЕРАТУРА
1. Thobois S, Delamarre-Damier F, Derkinderen P. Treatment of motor dysfunction in Parkinson’s disease: An overview. Clin Neurol Neurosurg 2005; 107: 269–81.
2. Rinne UK. Early combination of bromocriptine and levodopa in the treatment of Parkinson’s disease: A 5-year follow-up. Neurology 1987; 37: 826–8.
3. Montastruc JL, Rascol O, Senard JM, Rascol A. A randomised controlled study comparing bromocriptine to whtich levodops was leter added, with Parkinson’s disease: A 5-year follow-up. J Neurol Neurosurg Psychiatry 1994; 57: 1034–38.
4. Adler CH, Sethi KD, Hauser RA et al., for the Ropinirole Study Group. Ropinirole for the treatment of early Parkinson’s disease [published correction appears in Neurology. 1997; 49: 1484]. Neurology 1997; 49: 393–9.
5. Hely MA, Morris JG, Traficante R et al. The Sydney Multicentre Study of Parkinson’s disease: Progression and mortality at 10 years. J Neurol Neurosurg Psychiatry 1999; 67: 300–7.
6. Clarke CE, Deane KH. Ropinirole versus bromocriptine for levodopa- induced complications in Parkinson’s disease. Cochrane Database Syst Rev 2001; 1: CD001517.
7. Clarke CE, Speller JM. Pergolide versus bromocriptine for levodopa- induced motoer complications in Parkinson’s disease. Cochrane Database Syst Rev 2000; 2: CD000236.
8. Rinne UK, Bracco F, Chouza C et al., for the PKDS009 Study Group. Early treatment of Parkinson’s disease with cabergoline de;ays the onset of motor complications. Result of a double-bling levodopa controlled trial. Drugs 1998; 55 (Suppl. 1): 23–30.
9. Barone P, Bravi D, Bermejo-Pareja F et al., for the Pergolide Monotherapy Study Group. Pergolide monotherapy in the treatment of early PD. A ramdomized, controlled study. Neurology 1999; 53: 573–9.
10. Rascol O, Brooks DJ, Dorczyn AD et al., for the 056 Study Group. A five-year study of the incidence of dyskinesia in patients with early Parkinson’s disease who were treated with ropinirole or levodopa. N Engl J Med 2000; 342: 1484–91.
11. Leberman AN, Neophytides A, Leibowitz M et al. Comparative efficacy of pergolide and bromocriptine in patients with advanced Parkinson’s disease. Adv Neurol 1983; 37: 95–108.
12. Lieberman A, Olanow CW, Sethi K et al., for the Ropinirole Study Group. A multicenter trial of ropinirole as adjunct treatment for Parkinson’s disease [published correction appears in Neurology. 1999; 52: 435]. Neurology 1998; 51: 1057–62.
13. Pezzoli G, Martignoni E, pacchetti C et al. A crossover, controlled study comparing pergolide with bromocriptine as an adjunct to levodopa for the treatment of Parkinson’s disease. Neurology 1995; 45 (Suppl. 3): S22–7.
14. Inzelberg R, Nisipeanu P, Rabey JM et al. Double-blind comparison of cabergoline and bromocriptine in Parkinson’s disease patients with motor fluctuations. Neurology 1996; 47: 785–8.
15. Guttman M, for the International Pramipexole-Bromocriptine Study Group. Double-blind comparison of pramipexole and bromocriptine treatment with placebo in advanced Parkinson’s disease. Neurology 1997; 49: 1060–5.
16. Brunt ER, Brooks DJ, Korczyn AD et al. A six-month multicentre, double-blind, bromocriptine-controlled study of the safety and efficacy of ropinirole in the treatment of patients with Pardinson’s disease not optimally controlled by L-dopa. J Neural Transm 2002; 109: 489–502.
17. Ziegler M, Castro-Caldas A, Del Signore S, Rascol O. Efficacy of piribedil as early combination to levodopa in patients with stable Parkinson’s disease: A 6-month, randomized, placebo-controlled study. Mov Disord 2003; 18: 418–25.
18. Rascol O, Pathak A, Bagheri H, Montastruc JL. New concerns about old drugs: Valvular heart disease on ergot dervative dopamine agonists as an exemplary situation of pharmacovigilance. Mov Disord 2004; 19: 611–3.
19. Fsctor SA, Sanchez-Ramos JR, Weiner WJ. Parkinson’s disease: An open label trial of pergolide in patients failing bromocriptine therapy. J Neurol Neurosurg Psychiatry 1988; 51: 529–33.
20. Goetz CG, Blasucci L, Stebbins GT. Switching dopamine agonists in advanced Parkinson’s disease: il rapid titration preferable to slow? Neurology 1997; 52: 1227–9.
21. Canesi M, Antonini A, Mariani CB et al. An overnight switch to roinirole therapy in patients with Parkinson’s disease. J Neural Transm 199; 106: 925–9.
22. Thobois S. Proposed dose equivalence for rapid switch between dopamine receptor agonists in Parkinson’s disease: a review of the literature. Clinical Therapeutics 2006; 28: 1–12.
23. Castro-Caldas A, Delwaide P, Jost W et al. The Parkinson-CONTROL study: A 1-year randomized, double-blind trial comparing piribedil (150 mg/day) with bromocriptine (25 mg/day) in early combination with levodopa in Parkinson’s disease. Mov Disord. In press.
24. Aguilar M, Delwaide P, Linazasoro G et al. A double-blind 2-year extension of the Parkinson-CONTROL Study comparing fixed doses of piribedil (150 mg/day) an bromocriptine (25 mg/day) in early combination with L-dopa in Parkinson’s disease. Mov Disord. 2005; 20 (Suppl. 10): 259. Abstract.
25. Pezzoli G, Martignoni E, Pacchetti C et al. Pergolide compared with bromocriptine on Parkinson’s disease: A multicenter, crossover, controlled study. Mov Disord 1994; 9: 431–6.
26. Korczyn AD, Brooks DJ, Brunt ER et al., for the 053 Study Group. Ropinirole versus bromocriptine in the treatment of early Parkinson’s disease: A 6-month interim report of a 3-year study. Mov Disord 1998; 13: 46–51.
27. Korczyn AD, Brunt ER, Larsen JP et al., for the 053 Study Group. A 3-year randomized trial of ropinirole and bromocriptine in early Parkinson’s disease [publiched correction appear in Neurology. 1999; 53: 1162]. Neurology 1999; 53: 364–70.
28. Gimenez-Roldan S, Esteban EM, Mateo D. Switching form bromocriptine to ropinirole in patients with advanced Parkinson’s disease: Open-label pilot responses to three different doseratios. Clin Neuropharmacol 2001; 24: 346–51.
29. Olanow CW, Agid Y, Mizuno Y et al. Levodopa in the treatment of Parkinson’s disease: Current controversies [published correction appears in Mov Disord. 2005; 20: 645]. Mov Disord 2004; 19: 997–1005.
Комментарии
ПРАКТИКА ПЕДИАТРА
