Применение ацетилсалициловой кислоты для профилактики инсульта
Статьи Инструкция по применению |
CONSILIUM MEDICUM / ТОМ 11 / № 2 О.Д.Остроумова
Кафедра факультетской терапии и профболезней МГМСу, Москва
Внастоящее время инсульт - вторая после ишемической болезни сердца (ИБС) причина смертности в мире. В последние годы во всем мире отмечено увеличение заболеваемости и смертности от острого нарушения мозгового кровообращения (ОНМК), в том числе и в России. К сожалению, Россия находится на одном из первых мест по заболеваемости и смертности от инсультов. Проблема ОНМК имеет также большое социально-экономическое значение: стоимость лечения одного инсульта составляет 110 тыс. долларов США. Если учесть, что в год происходит около 500 тыс. ОНМК, то за это время общество тратит на лечение инсультов 53 млрд долларов.
Инсульт является также одной из основных причин инвалидности. Анализ годичных исходов ОНМК свидетельствует о том, что 33% из них имеют летальный исход, 22% приводят к стойкой инвалидности и лишь 45% больных реабилитируются.
Исходя из вышеизложенного становится понятной важность задачи профилактики инсультов. Различают первичную и вторичную (после уже произошедших ОНМК или транзиторной ишемической атаки - ТИА).
Одним из направлений первичной и вторичной профилактики ишемического инсульта (ИИ) является применение ацетилсалициловой кислоты (АСК).
АСК является одним из самых часто применяемых и хорошо изученных лекарственных средств. У пациентов с высоким риском развития осложнений назначение АСК позволяет снизить риск развития серьезных сердечно-сосудистых событий (нефатальный инфаркт миокарда (ИМ) + нефатальный инсульт + смертность от сердечно-сосудистых заболеваний) примерно на 25%. Это данные крупнейшего мета-анализа рандомизированных клинических исследований Antithrombotic Trialists' Collaboration (2002 г.), включившего результаты 287 исследований, в которых принимали участие 135 тыс. пациентов с высоким риском развития осложнений.
Первичная профилактика ИИ: каким группам пациентов необходимо назначать АСК
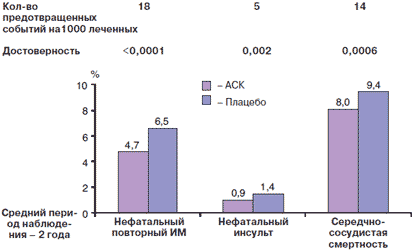
Пациенты с ИМ в анамнезе. В метаанализе Antithrombotic Trialists'-Collaboration охвачены 11 многоцентровых контролируемых плацебо исследований, в которых приняли участие в общей сложности 18 788 больных, а средний срок наблюдения составлял 27 мес. Полученные результаты с высокой степенью достоверности (p<0,0001) свидетельствуют о снижении риска сердечнососудистых событий (ИМ + инсульт + сердечно-сосудистая смертность) на фоне лечения АСК (рис. 1). Так, назначение АСК позволяет предотвратить 5 нефатальных инсультов на каждые 1000 леченых пациентов, а также 18 повторных нефатальных ИМ, 14 смертей от сердечно-сосудистых причин. Назначение АСК в течение длительного времени после перенесенного ИМ снижает частоту нефатального инсульта (на 42%), смертность (на 31%), частоту повторного нефатального ИМ (на 31%), поэтому все пациенты с инфарктом миокарда в анамнезе должны получать АСК в дозе 75-150 мг/сут.
Рис. 1. Снижение риска серьезных сердечно-сосудистых событий на фоне лечения АСК у больных с инфарктом миокарда в анамнезе.
Пациенты со стабильной стенокардией
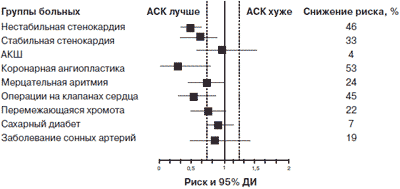
Согласно данным метаанализа Antithrombotic Trialist's Collaboration назначение АСК пациентам со стабильной стенокардией сопровождается выосокодостоверным (p=0,00004) 33% снижением риска серьезных сердечно-сосудистых событий (ИМ + инсульт + сердечно-сосудистая смертность; рис. 2). В данный метаанализ включены результаты 7 рандомизированных исследований, в которых принимали участие около 3 тыс. пациентов со стабильной стенокардией.
Рис. 2. Терапия АСК снижает риск серьезных сердечно-сосудистых событий у различных групп пациентов.
В шведском рандомизированном двойном слепом контролируемом плацебо исследовании SAPAT, включившем 2 035 больных со стабильной стенокардией, период наблюдения составил в среднем 50 мес. Все больные принимали β-блокатор соталол в средней дозе 160 мг, АСК назначали в дозе 75 мг/сут. В группе АСК по сравнению с плацебо частота сосудистой смерти, инсультов и общая смертность снизились на 22-32%, отмечено также достоверное снижение частоты ИМ и внезапной смерти на 34%.
Пациенты с мерцательной аритмией
Мерцательная аритмия является основной причиной тромбоэмболических осложнений и одной из основных причин инсульта у пожилых лиц. Фибрилляция предсердий - самая распространенная форма нарушений ритма сердца у взрослых. У лиц старше 60 лет она развивается в 2-4% случаев и отмечена практически у каждого шестого человека старше 75 лет. Однако вне зависимости от возраста мерцательная аритмия является причиной примерно 1 из 7 инсультов. У лиц старше 80 лет это отношение увеличивается до 1 из каждых 4 инсультов. Наиболее распространенной причиной фибрилляции предсердий является ИБС.
Последнее руководство, изданное "Национальной ассоциацией по инсультам" (National Stroke Association) в США (Gorelick и соавт., 1999) рекомендует прием АСК в качестве первичной профилактики инсультов пациентам старше 65 лет с фибрилляцией предсердий при отсутствии других факторов риска. Для пациентов в возрасте от 65 до 75 лет с фибрилляцией предсердий АСК рассматривается как альтернатива варфарину при отсутствии других факторов риска.
Результаты Antithrombotic Trialists' Collaboration суммируют результаты лечения АСК или плацебо 2770 пациентов с мерцательной аритмией (4 рандомизированных исследования). Показано, что назначение этой категории пациентов АСК приводит к снижению риска серьезных сердечно-сосудистых событий (нефатальный ИМ + нефатальный инсульт + смертность от сердечно-сосудистых причин) на 24% (рис. 2).
Имеются данные о том, что у больных с постоянной формой мерцательной аритмии назначение АСК в дозе 75 мг/сут привело к снижению риска развития ИИ на 18%, при увеличении дозы АСК до 325 мг/сут снижение риска развития ИИ составило 44%. В Великобритании 36% больных с мерцательной аритмией постоянно получают АСК.
Пациенты с хронической сердечной недостаточностью (ХСН)
ХСН - состояние, при котором возрастает риск тромбоэмболических осложнений и инсультов, особенно при наличии у пациентов мерцательной аритмии. Однако убедительных данных о целесообразности применения каких-либо антиагрегантов для лечения ХСН нет.
В настоящее время всего в 2 рандомизированных исследованиях, в которых участвовали лишь 134 пациента с ХСН (в подавляющем большинстве случаев ишемической этиологии), изучалось влияние АСК на прогноз при ХСН. В группе получавших АСК зафиксировано 4 серьезных сердечно-сосудистых события на 66 (6,1%) пациентов, а в группе плацебо - 7 (7,3%) осложнений у 68 человек.
Таким образом, вопрос о пользе назначения АСК у пациентов с ХСН остается открытым и требует дальнейших специальных исследований.
Пациенты с заболеваниями периферических артерий.
Еще более интенсивные научные исследования необходимы для получения ответа на вопрос, в какой степени АСК обладает положительным эффектом при облитерирующих заболеваниях периферических артерий. АСК рутинно назначается при этих заболеваниях из-за их сходства с кардиоваскулярными и цереброваскулярными расстройствами. Однако, несмотря на это, на сегодняшний день все еще недостаточно хорошо спланированных исследований, которые бы давали четкий ответ на вопрос о пользе назначения АСК этой категории пациентов.
Тем более ценными являются результаты метаанализа Antithrombotic trialists' Collaboratioin, в котором объединены результаты лечения 9 214 пациентов из 42 рандомизированных исследований. Снижение риска серьезных сердечно-сосудистых событий (нефатальный инсульт + нефатальный ИМ + смерть от сердечно-сосудистых причин) на фоне приема АСК составило 23% (p=0,004), при этом у больных с перемежающейся хромотой и у пациентов, перенесших хирургические операции на сосудах нижних конечностей, получен примерно одинаковый эффект (рис. 2).
Пациенты с сахарным диабетом
Сахарный диабет ассоциируется с повышенным риском развития сердечно-сосудистых событий. Поскольку это заболевание также сопровождается гиперактивностью тромбоцитов, значительно повышенным сывороточным уровнем тромбоксана А2, ускоренным обменом тромбоцитов, более быстрым развитием атеросклероза и повышенной частотой развития тромбо-эмболий, это предполагает, что больные сахарным диабетом с коронарными нарушениями в первую очередь могли бы получить пользу от приема АСК (см. таблицу).
Таблица 1. Риск летального исхода и абсолютные преимущества, связанные с приемом АСК при сахарном диабете
| Причина смерти | Риск смерти, % | |
| АСК | без АСК | |
| Среди пациентов с диабетом | (n=1220) | (n=1148) |
| 10,9 | 15,9 | |
| 1,2 | 1,9 | |
| 18,4 | 26,2 | |
| Среди пациентов без диабета: | (n=4801) | (n=3,785) |
| 4,8 | 6,9 | |
| 0,3 | 0,4 | |
| 9,3 | 13,4 | |
Результаты метаанализа
Antithrombotic Trialists' Collaboration (2002 г.), суммировавшие результаты лечения 4961 пациента с сахарным диабетом из 9 рандомизированных исследований, выявили, что применение АСК привело к снижению риска серьезных сердечно-сосудистых осложнений (нефатальный ИМ + нефатальный инсульт + смерть от сердечно-сосудистых причин) только на 7% (рис. 2).
Американская Диабетологическая ассоциация (ADA; 1999 г.) рекомендует для вторичной профилактики заболеваний крупных сосудов у больных диабетом прием АСК (в дозе от 81 до 325 мг в день). Более того, ADA рекомендует АСК в качестве препарата для первичной профилактики у пациентов с классическими факторами риска, такими как отягощенный семейный анамнез по ИБС, курение, высокое артериальное давление (АД), избыточная масса тела (>120% от идеальной массы тела -ИМТ, ИМТ >28 у женщин и >27,3 у мужчин), отклонение от нормы показателей липидов крови (холестерин (ХС) >200 мг%; ХС липопротеинов (ЛП) низкой плотности >130 мг%; ХС ЛП высокой плотности <40 мг%; триглицериды >250 мг%). Поскольку еще не накоплено достаточного опыта использования АСК у молодых лиц с сахарным диабетом, рекомендации ADA касаются только пациентов старше 30 лет.
Пациенты с поражением сонных артерий. Вопрос о пользе назначения АСК при поражении сонных артерий нуждается в дальнейшем изучении. Так, в метаанализ Antithrombotic Trialists' Collaboration удалось включить данные лишь 6 рандомизированных исследований, в которых участвовало менее 700 пациентов (5 исследований по эффективности АСК после оперативных вмешательств на сонных артериях и 1 - у пациентов с бессимптомным стенозом сонных артерий). Выявленное снижение риска серьезных сердечно-сосудистых событий (19%) на фоне применения АСК было недостоверным по сравнению с плацебо (рис. 2).
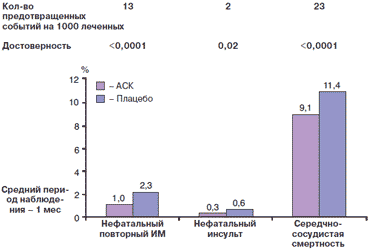
Результаты метаанализа Antithrombotic Trialists' Collaboration суммируют результаты лечения 19 288 больных острым ИМ в 15 многоцентровых рандомизированных исследованиях (средняя длительность лечения - 1 мес). Назначение АСК в остром периоде ИМ позволило достоверно (p<0,0001) снизить частоту сердечно-сосудистых событий на 38 на каждые 1000 леченых пациентов. Доказано, что если 1000 больных острым ИМ получают АСК, помимо достоверного снижения частоты повторных ИМ и сердечно-сосудистой смертности, достоверно (p<0,02) снижается и частота инсультов - по 2 на каждые 1000 пациентов, получавших АСК (рис. 3).
Рис. 3. Снижение риска серьезных сердечно-сосудистых событий на фоне лечения АСК у больных с острым инфарктом миокарда.
Пациенты с нестабильной стенокардией. Назначение АСК пациентам с нестабильной стенокардией сопровождается высокодостоверным (p<0,0001) снижением риска серьезных сердечно-сосудистых осложнений, в том числе инсультов, на 46% (метаанализ Antithrombotic Trialist's Collaboration; рис. 2). В метаанализ включены результаты 12 рандомизированных исследований, в которых принимали участие более 5 тыс. пациентов с нестабильной стенокардией.
Как известно, у пациентов с нестабильной стенокардией тромбоциты находятся в активированном состоянии, и регулярно высвобождаются вазоактивные медиаторы. Именно поэтому эффект АСК у данной категории пациентов выражен даже в большей степени, чем у пациентов со стабильной стенокардией.
Вторичная профилактика ИИ
Пациенты с инсультом и/или ТИА (преходящими нарушениями мозгового кровообращения) в анамнезе
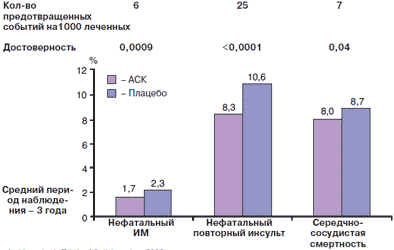
С 1990 г. резко увеличилось количество данных относительно пользы от применения АСК у этой группы больных. По данным Antithrombotic Trialists' Collaboration, среди 18 270 больных более чем из 20 многоцентровых рандомизированных исследований, средняя длительность наблюдения в которых составляла 29 мес, терапия АСК способствовала профилактике 26 случаев нефатального инсульта и 36 серьезных сердечно-сосудистых событий (p<0,0001; рис. 4). Кроме того, назначение АСК 1000 больным с инсультами и/или ТИА в анамнезе позволит предотвратить у них 6 нефатальных ИМ (p<0,0009). Полученные данные со всей очевидностью демонстрируют большую пользу от АСК для этой категории больных.
Рис. 4. Снижение риска серьезных сердечно-сосудистых событий на фоне лечения АСК у больных с инсультами и/или транзиторными ишемическими атаками в анамнезе.
Большая польза АСК у пациентов с нарушенным кровоснабжением головного мозга обусловлена тем, что это состояние сопровождается гиперактивностью тромбоцитов. Именно поэтому у пациентов с повышенным риском, обусловленным предшествующими ТИА или инсультом, применение АСК значительно уменьшает частоту возникновения ТИА, а также фатальных и нефатальных инсультов (Canadian Cooperative Study Group, 1978; ESPS Group, 1987; SALT Collaborative Group, 1991). Это положение особенно актуально для пожилых женщин, пациентов с повышенным АД и курильщиков.
При этом пациенты, которые на момент развития у них инсульта уже в течение некоторого времени принимали АСК, имеют в 2 раза больше шансов на выживание. Таким образом, АСК способна также смягчать течение инсультов.
Данные о высокой распространенности инсульта и сопровождающей его значительной инвалидизации больных обусловливают большую не только медико-социальную, но и экономическую значимость его профилактики. На основании данных исследования ESPS-2 были подсчитаны затраты на профилактику инсульта по сравнению с расходами на лечение. Так, показано, что применение АСК (в сравнении с плацебо) у 1 пациента в течение 2 лет позволяет сэкономить 923,39 (с учетом прямых затрат) или 982 (с учетом прямых и непрямых затрат) новозеландских доллара.
Оптимальные дозы АСК для профилактики, так же как и для лечения, цереброваскулярных заболеваний окончательно не определены: эффективность была одинакова, как при назначении 300 и 1200 мг, так для доз 30 и 285 мг/сут.
Таким образом, назначение АСК пациентам, перенесшим инсульт и/или ТИА, позволит снизить у них риск повторных инсультов, смертность, а также частоту развития ИМ.
Пациенты с острым инсультом
На сегодняшний день эффективность и безопасность АСК у данной категории больных не вызывает сомнений. Имеются результаты двух крупных исследований: одно из них открытое (international stroke trial, суточная доза АСК - 300 мг), другое контролируемое плацебо (Chinese acute stroke trial, суточная доза АСК - 160 мг). В каждом из этих исследований приняли участие около 20 000 пациентов с острым ИИ. Средняя продолжительность лечения составила всего 3 нед. Результаты метаанализа свидетельствуют о том, что назначение АСК позволяет предотвратить 9 серьезных сердечнососудистых осложнений на каждые 1000 леченых пациентов, в том числе 4 нефатальных инсультов и 5 смертей от сердечно-сосудистых причин (различия с плацебо достоверны; рис. 5). Возможно, эти результаты менее впечатляют, чем данные, полученные у пациентов с ишемией головного мозга в анамнезе (см. ниже), но ведь и период наблюдения был минимален - всего 3 нед в отличие от нескольких лет в исследованиях у больных с инсультами и/или ТИА в анамнезе.
Рис. 5. Снижение риска серьезных сердечно-сосудистых событий на фоне лечения АСК у больных с острым инсультом.
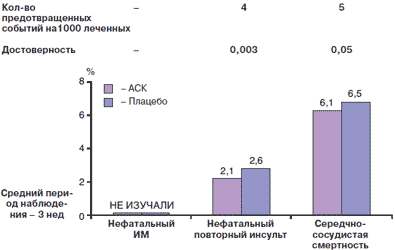
В 4 из этих 7 исследований, включенных в метаанализ Antithrombotic Trialists' Collaboration, проследили влияние терапии АСК на риск развития разных типов инсультов. Так, риск развития ИИ снизился на 6,9 на 1000 человек, а геморрагического -увеличился на 1,9 на 1000, что в сумме дало снижение риска инсультов в целом на 5,4 на каждые 1000 леченых пациентов.
Пациенты, которые на момент развития у них инсульта уже принимали АСК, имели в 2 раза больше шансов выжить.
Ценные свойства АСК при терапии цереброваскулярных расстройств могут включать не только ее антиагрегатное действие, но также, и клеточнопротективные эффекты. Нервные клетки, которые подвергались предварительной терапии АСК, лучше переживают последствия кислородного дефицита. Высокая температура тела ухудшает прогноз выживания после инсульта даже при других приемлемых условиях. Повышенная температура тела увеличивает скорость основного обмена и потребление кислорода, поэтому ткани, которые уже были повреждены патологическим процессом, имеют повышенную чувствительность к ишемии. Следовательно, жаропонижающее действие АСК (особенно в высоких дозах) может оказаться полезным и у пациентов с ИИ. Оптимальные дозы АСК для лечения цереброваскулярных заболеваний также окончательно не определены (эффективность была одинакова, как при назначении 300 и 1200 мг, так и 30 и 285 мг/сут).
Неотложная терапия АСК при остром инсульте в последующем должна быть продолжена приемом низких доз препарата (100 мг/сут АСК).
Таким образом, назначение АСК в остром периоде инсульта позволит снизить смертность и риск развития повторного инсульта в кратчайшие сроки. Предшествующий (до развития настоящего инсульта) прием АСК повышает выживаемость пациентов. В последующем (после инсульта) терапия АСК должна быть продолжена.
Оптимальные дозы АСК
Несмотря на то, что в некоторых рандомизированных исследованиях проведены сравнения эффективности АСК в дозах <75 и 75 мг, в них не выявлено достоверных различий между данными двумя режимами назначения АСК, эффективность АСК в дозах <75 мг все же гораздо менее изучена, чем эффективность АСК в дозе 75 мг. Поэтому вопрос о том, являются ли дозы АСК <75 мг так же эффективной, как и доза АСК 75 мг остается открытым. В то же время преимуществ назначения высоких (более 500 мг) доз АСК по сравнению с меньшими дозами не выявлено.
Так, по данным метаанализа Antithrombotic Trialists' Collaboration снижение риска сердечно-сосудистых осложнений на фоне применения АСК в дозе 500-1500 мг составило 19%, 160-325 мг - 26% и в дозе 75-150 мг - 32%. В то же время на фоне применения доз <75 мг АСК в сутки отмечен меньший эффект (снижение риска на 13%; p=0,05).
Результаты ряда исследований также подтвердили, что минимальная эффективная доза АСК при многих заболеваниях, являющихся показаниями к ее назначению, составляет 75 мг, причем ее повышение обычно не приводило к повышению эффективности. Главный недостаток приведенных данных заключается в том, что они не были получены в прямых сравнительных исследованиях. Тем не менее, существуют и прямые доказательства по крайней мере сопоставимой эффективности малых и более высоких доз АСК. Например, в исследовании Dutch TIA был сопоставлен эффект АСК в дозах 30 и 283 мг/сут у 3 131 больного, перенесшего ТИА или нетяжелый ИИ. Статистически достоверных различий частоты сосудистой смерти, инсульта или инфаркта миокарда между группами не выявлено. В исследовании ACE изучали эффективность 3-месячной терапии АСК в дозах 81, 325, 650 или 1300 мг/сут примерно у 3000 больных, перенесших эндартерэктомию, которая является мощным стимулом агрегации тромбоцитов, что теоретически обосновывает применение более высоких доз АСК. Тем не менее, частота инсультов, ИМ или смерти у больных, получавших АСК в дозах 81-325 мг/сут была даже ниже, чем у больных, принимавших этот препарат в дозах 650-1300 мг/сут (6,2 и 8,4% соответственно, p=0,03). При этом эффект АСК в дозах 81 или 325 мг/сут не отличался.
В то же время риск развития больших кровотечений был одинаков при приеме разных доз АСК (в пределах до 325 мг/сут): 1,7 для доз <75 мг, 1,5 - для доз 75-150 мг, и 1,4 для доз 160-325 мг (Antithrombotic Trialists' Collaboration, 2002 г.).
Повышение переносимости и безопасности лечения АСК: новые лекарственные формы
Помимо риска кровотечений, который повышен у пожилых пациентов, при одновременном приеме кортикостероидов, а также при наличии язвенной болезни в анамнезе, основной клинической проблемой назначения АСК являются частые побочные эффекты со стороны желудочно-кишечного тракта (ЖКТ) - прежде всего повышение частоты эрозивно-язвенных поражений ЖКТ и диспептические симптомы.
Возникновение эррозивно-язвенных поражений желудка на фоне приема АСК даже в дозах, применяемых в кардиологии, - общеизвестный факт. Эти язвы можно эффективно лечить теми же препаратами, что и язвенную болезнь. Как правило, рубцевание язвы происходит быстрее, если АСК отменена, при этом условии сроки рубцевания аналогичны срокам рубцевания при язвенной болезни - на 4-8-й неделе лечения. Однако если терапию АСК продолжать несмотря на выявленное эрозивно-язвенное поражение ЖКТ показатели рубцевания достаточно удовлетворительные: к 4-й неделе лечения рубцуются 60-75% язв.
Долгое время единственным и практически 100% решением этой проблемы многие считали применение кишечнорастворимых форм АСК. Однако ряд авторов отметили образование эрозий и язв желудка даже при применении таблеток АСК, покрытых кишечнорастворимой оболочкой. Более того, согласно результатам еще одного исследования, применение кишечнорастворимых форм АСК у пациентов с аспирининдуцированными язвами не вело к увеличению показателей рубцевания язв при терапии циметидином и антацидами; у 7 больных, получавших АСК в кишечнорастворимой оболочке, не было дос-тигнуто рубцевание язвы, тогда как у 90% больных после отмены этой формы АСК язвы зарубцевались.
Созданы новые лекарственные формы АСК, предлагающие другие способы защиты ЖКТ. Особый интерес представляет препарат Кардиомагнил, который представляет собой соединение АСК (в наиболее эффективных и безопасных дозах - 75 и 150 мг) с невсасывающимся антацидом - гидроокисью магния.
Невсасывающиеся антациды являются одними из наиболее часто используемых препаратов для лечения заболеваний желудка, в том числе и язвенной болезни. Свой положительный эффект они реализуют, адсорбируя соляную кислоту. Кроме того, невсасывающиеся антациды обладают и рядом других позитивных свойств. Они снижают протеолитическую активность желудочного сока (посредством адсорбции пепсина, повышения pH среды, в результате чего пепсин становится неактивным), обладают обволакивающими свойствами, связывают лизолецитин и желчные кислоты, оказывающие неблагоприятное воздействие на слизистую оболочку желудка.
Но, пожалуй, самым важным для профилактики аспирининдуцированных осложнений, являются дан-ные о цитопротективном действии антацидов. В частности, антациды способны предотвращать в экспериментальных и клинических условиях возникновение повреждений слизистой оболочки желудка при применении нестероидных противовоспалительных препаратов. Было установлено, что цитопротективный эффект антацидов обусловлен повышением простагландинов в стенке желудка (снижение простагландинов в стенке желудка - основной механизм язвообразования при применении АСК), усилением секреции бикарбонатов и увеличением гликопротеинов желудочной слизи.
Гидроокись магния, входящая в состав Кадиомагнила, кроме того, является наиболее быстродействующим антацидом, в отличие от гидроокиси алюминия. Это очень важный момент, поскольку АСК быстро всасывается из желудка: значимые концентрации в плазме достигаются всего через 15-20 мин. При этом результаты специально проведенных исследований показали, что гидроокись магния не влияет на всасываемость АСК.
Однако самым частым побочным эффектом АСК со стороны ЖКТ является диспепсия (по данным некоторых авторов, в 50% случаев и более), причем эзофагогастродуоденоскопия не выявляет эрозивно-язвенных и воспалительных изменений. Этот вроде бы безобидный симптомокомплекс на самом деле является наиболее частой причиной отказа пациента от приема АСК. Соединение АСК с гидроокисью магния (Кардиомагнил) позволит резко снизить частоту диспепсии и повысить приверженность пациентов лечению.
Литература
1. Collaborative meta-analysis of randomized trials of antiplatelet therapyfor prevention of death, myocardial infarction, arid stroke in high risk patients. BMJ2002; 324: 71-86.
2. Patrono C, Coller B, Dalenf et al. Platelet-active drugs: the relationships among dose, effectiveness, and side effects. Sixth ACCP Consensus Conference on Antithrombotic Therapy. Chest2001; 119: 39S-63S.
3. Taylor D, BarnettH, Haynes R et al. Low-dose and high-dose acetylsalicylic acidfor patients undergoing carotid endarterectomy: a randomized controlled trial. Lancet, 1999; 353:2179-84.
4. The Dutch TLA Trial Study Group.A comparison of two doses of aspirin (30 mg vs283 mg a day) in patients after a transient ischemic attack or minor ischemic stroke. NEnglJMed 1991; 325:1261-6.
5. Reilly LAG, FitzGerald GAAspirin in cardiovascular disease. 1988; 35: 154-76.
6. Cairns JA, Gent M, SingerJ et al.Aspirin, sulfinpyrasone, or both in unstable angina. Results of Canadian multicenter trial. N EnglJ Med 1985; 313: 1369-75.
7. Lewis H, DavisJ,Arhibald D et al. Protective effects of aspirin against acute myocardial infarction and death in men with unstable angina. Results of Veterans Administration Cooperative Study. N Engl J Med 1983; 309:396-403.
8.Antiplatelet Trialist' Collaboration. Collaborative overview of randomized trials of anplatelet therapy-1: prevention of death, myocardial infarction, and stroke by prolonged antiplatelet therapy in various categories ofpatients. BrMedJ 1994; 308: 81-106.
9. Risk of myocardial infarction and death during treatment with low dose aspirin and intravenous heparin in men with unstable coronary artery disease. The RISK Group. Lancet 1990; 336:827-30.
10. Management of acute coronary syndromes: acute coronary syndromes without persistent ST segment elevation. Recommendation of the Task Force of the European Society of Cardiology. Eur Heartf 2000; 21: 1406-32.
11. Randomised trial of intravenous streptokinase, oral aspirin, both, or neither among 17187 cases of suspected acute myocardial infarction: LSLS-2. LSLS-2 (Second International Study of Infarct Survival) Collaboration group. Lancet 1988; 8: 349-60.
12. Ridker PPM, MansonJE, GazianofM et al. Low-dose aspirin therapy for chronic stabile angina: a randomized, placebo controlled clinical trial. ANN. Intern Med 1991; 114:835-9.
13. Juul-Moller S, Edvardsson N, Jahnmatz B et al. Double-blind trial of aspirin in primary prevention of myocardial infarction in patients with stable chronic angina pectoris. Lancet 1992; 340: 1421-5.
14. Antiplatelet Trialist' Collaborative overview of randomized trials of anplatelet therapy-II: maintenance of vascular graft or arterial potency by antiplatelet therapy Br MedJ 1994; 308:159-68.
15. Warlow C. Secondary prevention of stroke. Lancet 1992; 339: 724-7.
16. McConnel H. Collaborative meta-analysis of randomized trials of antiplatelet therapyfor prevention of death, myocardial infarction, and stroke in high risk patients. Br MedJ2002; 324: 71-86.
17. Hansson L, ZanchettiA, Carruthers SG et al. Effects of intensive blood-pressure lowering and low dose aspirin in patients with hypertention; principal results of Hypertension Optimal Treatment (HOT) randomized trial. Lancet 1988; 351: 1766-72.
18. Hayden M, Pignone M, Phillips C, Mulrow C. Aspirin for the primary prevention of cardiovascular events: A summary of the evidencefor the US Pre-ventive Services Task Force. Ann Intern Med 2002; 136: 161-72.
19. US Preventive Services Task Force. Aspirin for the primary prevention of cardiovascular events: Recommendation and rationale. Ann Intern Med 2002; 136: 157-60.
20. Gum PA, Tramiilarasan M, Watanabe J et al. Aspirin use and all-cause mortality among patients being evaluated for known or suspected coronary artery disease: A propensity analysis. JAMA 2001; 286 (100): 1187-94.
21. Ridker PPM, MansonJE, BuringJE et al. The effect of chronic platelet inhibition with low-doses aspirin on atherosclerotic progression and acute thrombosis: clinical evidencejrom the Physicians' Health Study. Am Heartf 1991; 122 (6): 1588-92.
22. Medical Reseach Council. Randomized trial of low intensity oral anticoagulation with warfarin and low-dose aspirin in the primary prevention of ischaemic heart disease in men at increased risk: the Medical Research Council's General Practice Research Framework Thrombosis Prevention Trial. Lancet 1998; 351: 233-41.
23. MansonJE, StampferMJ, Colditz GA et al. A prospective study of aspirin use and primary prevention of cardiovascular disease in women. JAMA 1991; 266 (4): 521-27.
24. Sanmuganathan PS, Ghahramani Pfackson PR et al. Aspirin for the primary prevention of coronary heart disease: safety and absolute benefit related to coronary risk derived from meta-analysis of randomized trials. Heart 2001; 85 (3): 265-71.
25. Cairns J, Theroux P, Lewis D et al. Antithrombotic Agents in Coronary Artery Disease. Sixth ACCP Consensus Conference on Antithrombotic Therapy. Chest 2001; 119: 228S-252S.
26. Collins R, Baigent C, Sandercock P, Peto R. Antiplatelet therapy for thromboprophylaxis: the need for careful consideration of the evidence from randomized trials.Antiplatelet Trialists' Collaboration. BMJ 1994; 309 (6963): 1215-7.
27. Bousser MG. Antithrombotic strategy in stroke. Thromb Haemost 2001; 86: 1-7.
28. Swedish Aspirin Low-Dose Trial (SALT) of 75 mg aspirin as secondary prophylaxis after cerebrovascular ischemic events. The SALT Collaborative Group. Lancet 1991; 338 (8779): 1345-9.
29. MajeedA, Moser K, Carroll K. Trends in the prevalence and management of atrialfibrillation in general practice in England and Wales, 1994-1998: analysis of data from he generalpractice research database. Heart 2001; 86 (3): 284-8.
30. ColwellJA Treatment for theprocoagulant state in type 2 diabetes. Endocrinol. Metab. Clin North Am 2001; 30 (4): 1011-30.
31. Waeber B, Leonetti G, Kolloch R, McInnes GT. Compliance with aspirin or placebo in the Hypertention Optimal Treatment (HOT) study. J Hypertens 1999; 17: 1041-5.
32. VaneJ. R, Meade T. W. Second European Stroke prevention Study (ESPS2): clinical and pharmacological implications. J Neurol Sci 1997; 145 (2): 123-5.
33. Diener HC, Cunha L, Forbes C et al. European stroke prevention Study 2: dipyridamol and acetylsalicylic acid in the secondary revention of stroke.f Neurol Sci 1996; 143:1-13.
34. Scrutinio D, Cimminiello C, Marubini E et al. Tialopidine versus aspirin after myocardial infarction (STAMI) trial. Am Coll Cardiol 2001; 37 (5): 1259-65.
35. A randomized, blinded trial of clopidogrel versus aspirin in patients at risk of ischeamic events (CAPRIE). CAPRIE Steering Committee. Lancet 1996; 348: 9038, 1329-39.
36. Easton JD. Future perspectives for optmizing oral antiplatelet therapy. Cerebrovasc Dis 2001; 11: S223-8.
37. DammannHG, BurhardtF, Wolf N. Enteric coating of aspirin significantly decreases gastroduodenal mucosal lesions. Aliment Pharmacol. Ther. 1999; 13 (8): 1109-14.
38. Cole AT, Hudson N, Liew LC. et al. Protection of human gastric mucosa against aspirin-enteric coating or dose reduction? Aliment Pharmacol Ther 1999; 13 (22): 187-93.
39. Chan FK Chung SC, Suen BY et al. Preventing recurrent upper gastrointestinal bleeding in patients with Helicobacter pylori infection who are taking low-dose aspirin or naproxen. N EnglJ Med 2001; 344 (13): 967-73.
40. KellyfP,Kaufman DWJugelcon JM et al. Risk of aspirin-associated major upper-gastrointestinal bleeding with enteric-coated or buffered product. Lancet 1996; 348:1413-16.
41. Petroski D. Gastric safety and enteric-coated aspirin. Lancet 1997; 349.
42. Petroski D. Endoscopic comparison of three aspirin preparations and placebo. Clin Ther 1993; 15:314-20.
43. Petroski D. Endoscopic comparison of various preparations: gastric mucosal adaptability to aspirin restudied. Curr Ther Res 1989; 45: 345-54.
44. SavonJ,Allen /ML, DiMarino AJ. Gastrointestinal blood loss with low-dose (325 mg) plain and enteric-coated aspirin administration.Am J Gastrointerol 1995; 90:581-85.
45. Latini R, Santoro E, Masson S et al. Aspirin does not interact with ACE inhibitors when both are given early after acute myocardial infarction: results of the GISSI-3 Trial. Heart Dis 2000; 2 (3): 185-90.
46. ClelandfG,fohnf, Houghton T. Does aspirin attenuate the effect of angiotensin-converting enzyme inhibitors in hypertension or heart hailure? Curr OpinNephrolHypertens 2001; 10 (5): 625-31.
47. Mahe I, Meune C, Diemer M et al. Interaction between aspirin andACE inhibitors in patients with heartfailure. DrugSaf2001; 24 (3): 167-82.
48. Latini R, Tognoni G, Maggioni A et al. Clinical effect of early ACE inhibitor treatmentfor acute myocardial infarction are similar in the presence and absence of aspirin: meta-analysis of individual data from nearly 96000 randomizedpatients.J Am Coll Cardiol2000; 35:1801-7.
