Алгоритм коррекции анемии смешанного генеза у пациентов с изолированной острой почечной недостаточностью
СтатьиМ.А. Ямпольский, О.В. Арепьева, А.В. Бердникова, И.П. Яковлева, И.Б. Заболотских, А. Ф. Ямпольский
Кубанский государственный медицинский университет,
Краевой нефрологический центр, Краснодар
Цель исследования — обосновать необходимость применения эритропоэзстимулирующих препаратов (ЭСП) и внутривенных препаратов железа для коррекции анемии у больных с изолированной острой почечной недостаточностью (иОПН).
Материалы и методы: Обследовано 38 больных в возрасте от 24 до 67 лет, получавших интенсивную и заместительную/поддерживающую терапию. Пациенты разделены на три группы — по дозе препарата Эральфон (эпоэтин альфа).
Результаты: Выявлено достоверное влияние тяжести анемии на летальность больных с иОПН. Концентрация гемоглобина у выживших больных составила 96± 17г/л, а среди умерших — 79,5±11 г/л, р=0,0281. Используя сверхвысокие (140—150 МЕ/кг/36 часов) дозы Эральфона, удалось достичь приемлемых для больных с иОПН, значений гемоглобина через 48 часов. Показана необходимость введения сахарата железа каждые 36 часов, до достижения целевых значений показателей обмена железа. Предложен показатель эффективной транспортной концентрации трансферрина, прямо отражающий адекватность коррекции метаболизма железа на фоне применения ЭСП у уремических больных.
Заключение: Разработанный в данном исследовании алгоритм коррекции анемии у больных с иОПН позволяет решить проблему достижения целевых значений гемоглобина и, соответственно, снизить летальность и инвалидизацию этой группы пациентов.
Ключевые слова: острая почечная недостаточность, анемия, эритропоэзстимулирующий препарат.
ALGORITHM FOR MANAGEMENT OF MIXED GENESIS ANEMIA IN PATIENTS WITH ISOLATED ACUTE RENAL FAILURE
М.А. Yampolsky, О. V. Arepyeva, A.V. Berdnikova, I.P. Yakovleva, I.B. Zabolotskikh, A.F. Yampolsky
Kuban state medical university,
Regional center of nephrology, Krasnodar
Introduction: То estimate the need for erythropoiesis stimulating agents and intravenous iron for management of anemia in patients with isolated acute renal failure. Materials and methods: The study involved 38 patients aged from 24 to 67 years, who received intensive and replacement/supporting therapy. The patients were divided into three groups, only one criterion — the dose of Eralfon (epoetin alfa).
Results: A significant impact of the severity of anemia on mortality in patients with isolated acute renal failure. Hemoglobin concentration in the survivors was 96±17g/l, and among the dead — 79,5±11 g/l, p = 0,0281. Using ultra-high doses of erythropoietin (140—150 IU/kg/36 hours) failed to achieve acceptable for patients with isolated acute renal failure, hemoglobin values as early as the 48th hour of therapy. The necessity of introducing iron sucrose every 36 hours, before reaching the target values of iron metabolism. We proposed to measure the effective transport of transferrin concentration, directly reflects the possibility of correction of anemia erythropoiesis stimulating agents in uremic patients.
Conclusion: This study developed an algorithm for management of anemia, can completely solve the problem of achieving target levels of hemoglobin and, consequently, reduce mortality and disability of this pool of patients.
Key words: acute renal failure, anemia, erythropoiesis stimulating agent.
Введение. Существующая летальность до 10—15% при иОПН вынуждает сделать вывод о недостаточном акцентировании внимания исследователей на этом довольно часто встречающемся синдроме, а декомпенсированная анемия является независимым предиктором риска смерти у данной категории больных [1]. Лечение анемии у больных с иОПН является предметом дискуссий с 70-х годов прошлого века, когда появились убедительные сведения о достаточно частом развитии осложнений гемотрансфузий — инфицировании вирусными гепатитами, анафилактических реакциях и т.д.
Значительными шагами вперед были: применение декстранов, растворов на основе крахмала, появление перфторуглеродных соединений, рекомбинантных человеческих эритропоэтинов и, наконец, внутривенных препаратов железа. Тем не менее, широкое распространение новых лекарственных средств и методов лечения в нефрологии не получило столь же широкого развития в интенсивной терапии иОПН. Применение ЭСП у этого, достаточно большого пула пациентов уменьшает почечное повреждение и облегчает восстановление почечной функции, влияя на эритропоэз, и чем раньше начата терапия эритропоэтинами, тем лучший эффект будет достигнут [2]. Применение ЭСП способствует выживаемости и пролиферации эритроцитов. Протективный эффект ЭСП при иОПН доказан на модели животных, что связано, скорее всего, с антиапоптотическим цитопротективным действием [3]. Терапия ЭСП быстро и достоверно увеличивает уровень гемоглобина и гематокрита, что позволяет снизить смертность при ОПН [4]. Гемопоэтический фактор роста эритропоэтина является мультифункциональным цитокином, который играет ключевую роль при ишемии [5], и раннее назначение ЭСП при остром ишемическом почечном повреждении ингибирует апоптоз, улучшает канальцевую эпителиальную регенерацию и способствует функциональному восстановлению почки.
Результаты клинических исследований подтверждают, что ЭСП являются ренопротективными агентами для пациентов с риском ишемической ОПН или после перенесенного ишемического почечного инсульта [6].
Таким образом, адекватная коррекция закономерно возникающей анемии смешанного генеза позволяет снизить инвалидизацию и летальность пациентов с иОПН.
Цель исследования — обосновать необходимость применения ЭСП и внутривенных препаратов железа для коррекции анемии у больных с иОПН.
Материалы и методы. Для решения задач поставленных в работе обследованы 38 больных (11 женщин, 27 мужчин) в возрасте от 24 до 67 лет, получавших интенсивную и заместительную терапию в отделениях интенсивной терапии. Причиной иОПН были осложнения хирургических и гинекологических вмешательств — 11 больных, интерстициальный нефрит — 8, экзогенные отравления — 6, осложнения инфекционных заболеваний — 8 и обструкция мочевыводящих путей — 5.
Пациенты разделены на три группы по применяемой дозе препарата Эральфон (Сотекс, Россия). В первой группе — 12 больных (3 женщины, 9 мужчин) доза препарата составила 40—80 МЕ/кг/36 часов, во второй 15 пациентов (5 женщин, 10 мужчин) — 100—120 МЕ/кг/36 часов и в третьей 11 человек (3 женщины, 8 мужчин) — 140—150 МЕ/кг/36 часов. Все пациенты получали Венофер (Vifor, США) по 100 мг внутривенно каждые 36 часов, заместительную почечную терапию (ЗПТ) методом on-line гемодиафильтрации (ГДФ) с объемом конвекции 38—50 мл/кгхчас на аппаратах 4008S (Fresenius, Германия), с использованием гемодиафильтров: ВК — F 1,6 (Тоrау, Япония) и Hdf 100S (Fresenius, Германия). Объем возмещения потерь жидкости проводился с учетом степени гидратации пациента. Исследования проводились в олигоанурическом периоде иОПН на двух проводимых подряд процедурах ГДФ (2,3-я или 3,4-я от начала ЗПТ). Перерыв между процедурами колебался от 24 до 48 часов, продолжительность процедур составляла 300±30 мин. Во всех случаях использовался глюкозосодержащий концентрат (глюкоза — 5,5 ммоль/л, калий — 2,0 ммоль/л), поступление бикарбоната в диализирующий раствор осуществлялось через бикарбонатный картридж. Объемная скорость кровотока устанавливалась на уровне 250—300 мл/мин, поток диализирующей жидкости — 500 мл/мин. Регистрировались пульс, артериальное давление, масса тела, объем ультрафильтрации. Забор крови для определения уровня гемоглобина, концентраций эритропоэтина, сывороточного железа, ненасыщенной железосвязывающей способности (НЖСС) сыворотки, ферритина, трансферрина проводился перед началом ГДФ, через 5 минут, 1 час, 5 часов и 12 часов после введения эпоэтина альфа, а затем каждые 12 часов. Последнее исследование проводили через 84 часа от начала терапии ЭСП и внутривенным препаратом железа.
Параметры гемодинамики контролировались мониторами Dash 3000 («General Electric», США), уровень гемоглобина исследовался на гематологическом анализаторе KX-21N («Sysmex», Япония), параметры обмена железа на биохимическом анализаторе AU 640 («Olympus Corporation», Япония), концентрация эритропоэтина в крови с помощью иммунохимического анализатора ACCESS 2 («Beckman Coulter», США).
Статистическая обработка материала произведена с использованием программного обеспечения StatSoft Statistica Version 6.0 и Microsoft Excel. Производили вычисление медианы (Me) и персентилей (Р25, Р75). Достоверность различий полученных результатов проводилась с использованием непараметрических методов статистики. Для определения внутригрупповых изменений использован критерий Уилкоксона, а для сравнения между исследуемыми группами — Крускала-Уоллиса [7].
Результаты исследования и их обсуждение.
Достаточно высокая летальность у пациентов с иОПН показывает необходимость в разработке алгоритма консервативной терапии анемии смешанного генеза, как независимого предиктора риска смерти. Нам показалось важным выявить возможность использования всего комплекса коррекции анемии современными технологиями и лекарственными средствами у больных данной группы. В нашем исследовании выявлено достоверное влияние тяжести анемии на летальность больных с иОПН. Концентрация гемоглобина у выживших больных составила 96±17 г/л, а среди умерших — 79,5±11 г/л, р=0,0281
Как известно, точный выбор мембран, модальности ЗПТ позволяет исключить влияние грубой уремической интоксикации на развитие и прогрессирование анемии, поэтому, больные были разделены на группы только по дозе ЭСП. Динамика важнейших параметров, влияющих на коррекцию гемоглобина, приведена в табл. 1 и 2. Ранее считалось, что основным показателем, отражающим коррекцию обмена железа, является ферритин, что, однако, не подтверждается результатами нашего исследования. Как видно из табл. 2, введение сахарата железа каждые 36 часов по 100 мг не вызывало нарастания ферритина до сверхвысоких, опасных концентраций (более 800 мкг/л), медиана пиковых значений колебалась от 731 мкг/л до 796 мкг/л. В нашем исследовании, прямой зависимости между динамикой концентраций ферритина и гемоглобина выявлено не было, тем не менее, определение его концентрации сохраняет свое значение для профилактики передозировки препаратами железа. Существенно более важное значение имела сатурация трансферрина железом. Насыщение трансферрина железом возрастало буквально на «конце иглы», значительно и достоверно. Однако влияние этого параметра было ограничено концентрацией транспортного (для активного железа) белка трансферрина, 1,5—2-х кратный дефицит которого был наиболее существенным препятствием для коррекции активного железа, транспортируемого к рецепторам костного мозга. Несмотря на проводимую коррекцию препаратами незаменимых аминокислот, добиться коррекции этого показателя хотя бы до нижней границы нормы нам не удалось. Поэтому единственным средством увеличить доставку активного железа к рецепторам было достижение роста насыщения трансферрина железом. Как видно из табл. 2, процент насыщения трансферрина железом возрастал до рекомендуемых значений во всех случаях, причем, чем выше была доза ЭСП, тем быстрее снижался процент насыщения трансферрина, отражая быструю утилизацию активных запасов железа. Таким образом, два важнейших фактора, обеспечивающих коррекцию дефицита активного железа, в комплексе лечения комбинированной уремической анемии имели разную направленность и разные возможности компенсации современными методами терапии. Поэтому, в настоящей работе нами предлагается комбинированный показатель, отражающий «виртуальную» концентрацию трансферрина, насыщенную железом на 100%. Этот показатель, названный нами эффективная транспортная концентрация трансферрина (ЭТКТр), рассчитывается по формуле [8]:
ЭТКТр = (КтрхКж) / (Кж±НЖСС),
где: Ктр — концентрация трансферрина (г/л),
Кж — концентрация железа (мкмоль/л),
НЖСС — ненасыщенная железосвязывающая способность (мкмоль/л). Для эффективной коррекции обмена железа и, соответственно, обеспечения возможности достижения целевых значений гемоглобина с использованием ЭСП, ЭТКТр должна быть ≥0,65 г/л. Наблюдение динамики показателя прямо подсказывало необходимость введения очередной дозы венофера.
Таблица 1
Динамика медианных значений концентраций эритропоэтина и гемоглобина до, во время и после процедур ГДФ у пациентов исследованных групп
| Группа | Показатель/время | 0 | 5 мин | 1 час | 5 часов | 12 часов | 24 часа | 36 часов | 48 часов | 60 часов | 72 часа | 84 часа |
|
1 |
Эритропоэтин, мМЕ/д/л | 8,6 | 859 | 729 | 557 | 215 | 41 | 16 | 221 | 49 | 20,5 | 219 |
| Гемоглобин, г/л | 68 | 68 | 69 | 76 | 70 | 67 | 71 | 74* | 76* | 71 | 75* | |
|
2 |
Эритропоэтин, мМЕ/д/л | 15,1 | 1956 | 1302 | 889 | 266 | 75 | 20 | 272 | 78 | 24 | 279 |
| Гемоглобин, г/л | 74 | 74 | 75 | 78 | 75 | 78 | 83* | 89*1 | 87*1 | 91*1 | 95*1 | |
|
3 |
Эритропоэтин, мМЕ/д/л | 14,7 | 2522 | 1966 | 1136 | 311 | 106 | 34 | 349 | 112 | 42 | 361 |
| Гемоглобин, г/л | 75 | 75 | 77 | 81 | 85* | 88* | 94* | 98*1,2 | 100*1,2 | 99*1,2 | 104*1,2 |
* — р<0,05, достоверность отличий к исходному уровню гемоглобина в соответствующей группе.
1,2 — р<0,05, межгрупповые отличия достоверны.
Таблица 2
Динамика медианных значений концентраций параметров обмена железа до, во время и после процедур ГДФ в исследованных группах больных
| Группа | Показатель/время | 0 | 1 час | 5 часов | 12 часов | 24 часа | 36 часов | 48 часов | 60 часов | 72 часа | 84 часа |
|
1 | Ферритин, мкг/л | 89 | 632 | 694 | 708 | 656 | 591 | 729 | 711 | 688 | 796 |
| Трансферрин, г/л | 1,28 | 1,29 | 1,31 | 1,25 | 1,33 | 1,34 | 1,36 | 1,31 | 1,27 | 1,3 | |
| Сатурация трансферрина железом, % | 14,1 | 45,8 | 43,3 | 38,6 | 36,7 | 31,3 | 49,6 | 43,4 | 39,7 | 51,3 | |
| ЭТКТр, г/л | 0,17 | 0,58 | 0,58 | 0,47 | 0,50 | 0,41 | 0,69 | 0,55 | 0,51 | 0,68 | |
|
2 | Ферритин, мкг/л | 96 | 692 | 729 | 712 | 681 | 643 | 790 | 654 | 602 | 731 |
| Трансферрин, г/л | 1,35 | 1,35 | 1,37 | 1,31 | 1,31 | 1,24 | 1,32 | 1,27 | 1,29 | 1,33 | |
| Сатурация трансферрина железом, % | 12,8 | 47,8 | 43,6 | 35,1 | 30,3 | 27,1 | 50,3 | 44,1 | 36,4 | 52,2 | |
| ЭТКТр, г/л | 0,18 | 0,66 | 0,59 | 0,47 | 0,39 | 0,35 | 0,68 | 0,54 | 0,48 | 0,71 | |
|
3 | Ферритин, мкг/л | 91 | 613 | 657 | 641 | 623 | 605 | 725 | 710 | 655 | 763 |
| Трансферрин, г/л | 1,6 | 1,6 | 1,67 | 1,57 | 1,54 | 1,57 | 1,65 | 1,55 | 1,56 | 1,6 | |
| Сатурация трансферрина железом, % | 10,9 | 46,9 | 41,7 | 32,3 | 28,7 | 24,4 | 48,9 | 42,3 | 28,8 | 45,1 | |
| ЭТКТр, г/л | 0,16 | 0,74 | 0,69 | 0,53 | 0,45 | 0,37 | 0,73 | 0,67 | 0,47 | 0,73 |
Нами впервые исследованы концентрации эритропоэтина в динамике у больных с иОПН, получавших различные дозы ЭСП короткого действия. В целом, все три пула больных были в достаточной степени готовы к адекватному ответу на вводимые дозы ЭСП, результаты исследования концентраций которого показаны на рисунке. Как видно на рис., концентрация ЭСП уже через 5 минут после введения эральфона достигала высоких и сверхвысоких концентраций (медианные значения, соответственно, 859 мМЕ/л, 1956 мМЕ/л и 2522 мМЕ/л). Концентрации эритропоэтина достаточно быстро снижались уже к 5-ому, и еще более к 12-ому часу наблюдения, когда их концентрации выравнивались до значений, соответственно, 215 мМЕ/л, 266 мМЕ/л и 311 мМЕ/л. На графике (рис.) не показаны пики концентрации эритропоэтина после следующих введений ЭСП, а только концентрации через 12 часов после введения. Таким образом, при большей детализации графика, становятся заметными два радикальных отличия эффекта введения различных доз ЭПО. Первое — значительно большая суммарная площадь под кривой при введении более высоких доз ЭСП, и второе — существенно более высокие, почти в 2 раза, по сравнению с 2-мя первыми пулами больных, значения перед введением очередной дозы ЭСП. Это очень важно по двум причинам: первая — на всем протяжении лечения концентрация эритропоэтина превышает исходную более, чем в два раза, т.е. остается эффективной, и вторая — мы не получаем осцилляций гемоглобина, которые не только осложняют течение заболевания, но и обусловливают более высокую летальность, наряду с влиянием на летальность низких концентраций гемоглобина [9]. В целом, у больных 1-й группы отмечается лишь тенденция к росту гемоглобина, во 2-й — видна убедительная положительная динамика, не позволившая, однако, достигнуть целевых его значений. В то же время, у пациентов 3-ей группы, получавших сверхвысокие (140—150 МЕ/кг/36 часов) дозы ЭСП, удалось достичь приемлемых значений гемоглобина уже к 48-ому часу терапии.
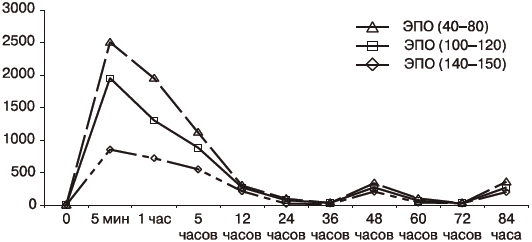
Рисунок. Динамика концентраций эритропоэтина в крови у больных исследованных групп.
Мы умышленно не использовали пролонгированные ЭСП, так как к моменту начала действия препарата пациент уже может быть переведен из отделения интенсивной терапии, либо выписан. Разработанный в данном исследовании комплекс коррекции анемии позволяет полностью решить проблему достижения целевых значений гемоглобина у больных с иОПН.
Таким образом, данные литературы и наши собственные исследования позволяют рекомендовать алгоритм лечения анемии смешанного генеза для больных с иОПН, который, по нашему мнению, выглядит следующим образом:
1. При уровне гемоглобина ≤70 г/л коррекция анемии включает трансфузию отмытых эритроцитов и/или перфторана/перфлюокарбона [10, 11, 12], раннее назначение ЭСП в дозе не менее 140 МЕ/кг 1 раз в 24—48 часов.
2. Вне зависимости от показателей обмена железа, для обеспечения полноценных возможностей коррекции анемии внутривенно медленно необходимо ввести 100 мг венофера (проведение пробы на переносимость обязательно), что обеспечит достижение целевых значений, буквально, «на конце иглы». При снижении ЭТКТр ниже целевых значений необходимо повторное введение железа через 12—24 часа.
3. Ежедневное применение внутривенных (лейковорин) или пероральных препаратов фолиевой кислоты до 5 мг/сутки.
4. Коррекция сниженных уровней плазменного альбумина, который достигается назначением специальных растворов аминокислот (аминостерил-нефро в дозе 250 мл/сутки) и концентрированных растворов альбумина (50—200 мл 20% раствора в сутки). Целевые значения параметров для коррекции анемии, представлены в табл. 3.
Таблица 3
Целевые значения параметров для коррекции анемии:
| Параметр | Целевой уровень |
| ЭТКТр (г/л) | ≥0,65 |
| Сатурация трансферрина железом (%) | ≥40 |
| Ферритин (мкг/мл) | 200-800 |
| Альбумин (г/л) | ≥40 |
| Гемоглобин (г/л) | ≥110 |
Выводы:
1. На всем протяжении лечения при использовании сверхвысоких доз (140—150 МЕ/кг) ЭСП концентрация эритропоэтина превышает исходную более чем в два раза, т.е. остается эффективной.
2. Мы не получили осцилляций гемоглобина, которые, не только осложняют течение заболевания, но и обусловливают более высокую летальность [13], как и низкая концентрация гемоглобина, являющаяся независимым предиктором риска смерти.
3. У больных с иОПН раннее назначение ЭСП и внутривенных препаратов железа, начиная со дня поступления пациента в отделение интенсивной терапии, обеспечивает достижение целевых значений параметров коррекции анемии.
4. Предлагаемый алгоритм лечения анемии при иОПН позволяет снизить инвалидизацию больных, уменьшить частоту первичных исходов в ХПН и 6-месячную летальность до приемлемых сегодня 3—6%.
ЛИТЕРАТУРА
1. Perelman R.L., Finkelstein F.O., Liu L., Roys E., Kiser М., Eisele G., Burrows-Hudson S., Messana J.M., Levin N., Rajagopalan S., Port F.K., Wolfe R.A., Saran R. Quality of life in chronic kidney disease a cross-sectional analysis in the Renal Research Institute-CKD study // American journal of kidney diseases. — 2005. —Vol. 45. — R 658—666.
2. Qian Y., Mehandru S.K., Gornish N., Frank E. The first description of serve anemia associated with acute kidney injury and adult minimal change disease: a case report //Journal of medical case reports. — 2009. — Vol. 3. — P. 20.
3. Spandou E., Tsouchnikas I., Karkavelas G., Dounousi E., Simeonidou C., Guiba — Tziampiri O., Tsakiris D. Erythropoietin attenuates renal injury in experimental acute renal failure ischaemic/reperfusion model // Nephrology dialysis transplantation. — 2006. — Vol. 21, № 2. — P. 330—336.
4. Nemoto T., Yokota N., Keane W.F., Rabb H. Recombinant erythropoietin rapidly treats anemia in ischemic acute renal failure //Kidney international. — 2001. — Vol. 59, № 1. — P. 246—251.
5. Sharpies E.J., Yaqoob M.M. Erythropoietin and acute renal failure // Seminars in nephrology. — 2006. — Vol. 26, № 4. — P. 325—331.
6. Johnson D. W., Pat B., Vesey D.A., Guan Endre Z, Gobe G.C. Delayed administration of darbepoetin or erythropoietin protects against ischemic acute renal injury and failure // Kidney international. — 2006. — Vol. 69, № 10. — P. 1806-1813.
7. С. Гланц. Медико-биологическая статистика. Пер. с англ. М.: Практика. — 1998. — Р. 459.
8. Ямпольский М.А., Ямпольский А.Ф., Еремеева Л.Ф., Бердникова А.В. Способ оценки эффективного транспорта железа у больного с почечной недостаточностью. Патент на изобретение № 2010141374 от 07.10.2010.
9. Gilbertson D. Т., Ebben J. P., Foley R. N., Weinhandl Е. D., Bradbury В., Collins A. J. Hemoglobin level variability: associations with mortality // Clinical journal of the American society of nephrology. — 2008. — Vol. 3. — P. 133-138.
10. Жибурт Е.Б, Иваницкий Г.P., Пушкин С.Ю. и соавт. Современная терапия острой массовой кровопотери. Тихоокенский медицинский журнал. — 2004. — № 4. — Р. 11—15.
11. А. М. Голубев, Ф. А. Тамаева. Коррекция метаболических нарушений в почках при острой массивной кровопотере (экспериментальное исследование) // Общая реаниматология. — 2007. — Т. 3, № 5—6, стр. 38—42.
12. Spiess B.D. Perfluocarbon Emulsions: Artificial Gas Transport Media in «Perioperative transfusion medicine», 2nd ed. / eds: Spiess B.D, Spence R.K., Shander A. —2006. — № 20. — P. 273—283.
13. D. T. Gilbertson, J. P. Ebben, R. N. Foley, E. D. Weinhandl, B. Bradbury and A. J. Collins. Hemoglobin level variability: associations with mortality // Clinical Journal of the American Society of Nephrology. — 2008. — № 3. — P. 133—138.


