Исследование эффективности, переносимости и безопасности препарата Хондрогард у пациентов с остеоартрозом
Статьи Опубликовано в журнале:«ФАРМАТЕКА»; № 7; 2013; стр. 60-64.
Л.И. Алексеева, С.Г. Аникин, Е.М. Зайцева, Н.Г. Кашеварова, Т.А. Короткова, Е.П. Шарапова, Н.В. Чичасова, Г.Р. Имаметдинова, Н.В. Бадокин, С.А. Колова
ФГБУ НИИР РАМН, Москва
Представлены результаты исследования по оценке эффективности, переносимости и безопасности внутримышечного введения хондроитина сульфата (ХС) больным остеоартрозом (ОА) коленных суставов. В 2-месячном проспективном исследовании приняли участие 70 человек, 67 (96 %) женщин и 3 (4 %) мужчины в возрасте 45-70 лет с первичным ОА коленных суставов II (79 %) и III (21 %) рентгенологических стадий по Kellgren-Lawrence, нуждавшихся в приеме нестероидных противовоспалительных средств (НПВС). Препарат ХС Хондрогарт вводили внутримышечно через день (всего 30 инъекций), исследование завершили 66 (94 %) человек. Результаты исследования показали, что терапевтический эффект наступал в среднем на 23-й день от начала лечения. Таким образом, Хондрогард обладает достоверным симптоматическим эффектом, уменьшая боль, скованность и улучшая функциональные показатели. Преимуществом препарата являются быстрое наступление эффекта, возможность отмены или снижения дозы НПВС на фоне лечения и хорошая переносимость. Препарат Хондрогард может быть рекомендован лицам, страдающим ОА, в качестве первого средства, дающего более быстрый эффект с последующей заменой его на пероральные формы.
Ключевые слова: остеоартроз, нестероидные противовоспалительные средства, хондроитина сульфат
The results of the study aimed to evaluation the efficacy, tolerability and safety of intramuscular administration of chondroitin sulfate (CS) in patients with osteoarthrosis (OA) of the knee are presented. The 2-month prospective study involved 70 patients, 67 (96 %) women and 3 (4 %) men aged 45-70 years with primary OA of knee joints II (79 % ) and III (21 %) radiographic stages by Kellgren-Lawrence, who were in need of administration of nonsteroidal anti-inflammatory drugs (NSAIDs). The drug Chondrogard was administered intramuscularly each alternate day (a total of 30 injections); 66 (94 %) patients have completed the study. The results showed that the therapeutic effect occurred at the 23th day of treatment on average. Thus, Chondrogard has significant symptomatic effect, reducing pain, stiffness, and improving functional performance. The advantages include the rapid onset of drug effect, potential for the withdrawal or reducing the NSAID dose during treatment, and good tolerability. The drug Chondrogard can be recommended to the OA patients as a first-line drug with a more immediate effect, with subsequent replacement by oral forms of drug.
Key words: osteoarthrosis, nonsteroidal anti-inflammatory drugs, chondroitin sulfate
Введение
Остеоартроз (ОА) - заболевание суставов, характеризующееся клеточным стрессом и деградацией экстрацеллюлярного матрикса, возникаютттих при макро- и микроповреждениях, которые активируют ненормальные адаптивные процессы восстановления, включая провоспалительные реакции иммунной системы, костного ремоделирования и образования остеофитов [1]. Основными клиническими проявлениями ОА являются боль различной степени выраженности, как правило механического стартового характера, умеренно выраженная непродолжительная скованность в суставах и нарушение функции. Терапия ОА носит комплексный характер и зависит от выраженности воспалительной реакции, степени функциональной недостаточности, структурных изменений и наличия сопутствующих заболеваний. В клинической практике наиболее часто для купирования симптомов ОА применяют нестероидные противовоспалительные средства (НПВС). Однако их применение может оказывать токсическое действие на органы желудочно-кишечного тракта (ЖКТ), сердечно-сосудистой системы, почек и печени. Российские, Европейские и Американские руководства рекомендуют использовать НПВС короткими курсами в минимальных эффективных дозах [2, 3]. В 2003 г. Европейская антиревматическая лига (EULAR — The European League Against Rheumatism) отдельно выделила группу лекарственных средств, определяемых как препараты замедленного действия для симптоматической терапии ОА (SYSADOA — symptomatic slow acting drugs for osteoarthritis). К настоящему времени накоплен большой научный и клинический опыт, позволивший сделать предварительные выводы и о возможном наличии структурно-модифицирующего эффекта, присущего этим препаратам.
ХС является типичным представителем группы лекарственных средств замедленного действия. Несмотря на то что ХС используется в медицине уже более 30 лет, до настоящего времени не утихают споры о месте и роли этого препарата в терапии пациентов с ОА, что, впрочем, относится ко всей группе лекарственных средств замедленного действия. Отражением этих споров, в частности, являются рекомендации Американской коллегии ревматологов, где авторы условно не рекомендуют использовать ХС и глюкозамин в качестве терапии пациентов с ОА [4]. Тем не менее в большинстве национальных рекомендаций, включая и таких авторитетных организаций, как Международное общество по изучению ОА (OARSI - Osteoarthritis Research Society International) и EULAR, ХС включен в качестве терапевтического средства для лечения пациентов с ОА.
Фармакокинетика и биологическая активность ХС в значительной степени определяются массой молекулы и степенью сульфатирования [10]. В качестве исходного сырья для получения ХС используется хрящевая ткань крупного рогатого скота, свиней, цыплят или рыб [11-14]. Разные источники получения ХС определяют особенности молекулярной структуры ХС, что в свою очередь помимо степени очистки оказывает влияние на эффективность применения того или иного препарата.
Большая часть ХС выпускается в виде форм для перорального применения. При попадании в ЖКТ происходит разрушение большинства молекул ХС, и в системный кровоток, как правило, попадают низкомолекулярные дериваты, обладающие небольшой терапевтической активностью. По некоторым данным, доля нативных молекул в системном кровотоке при пероральном приеме составляет всего 10 %. Максимальная концентрация препарата в крови достигается через 3-4 часа после приема, а в синовиальной жидкости — через 4-5 часов. В целом же биодоступность ХС при пероральном приеме составляет в среднем от 10 до 20 % [15-17].
При внутримышечном введении ХС выявляется в значительных концентрациях в системном кровотоке уже через 30 минут, а максимальная концентрация достигается через час. В синовиальной жидкости препарат выявляется через 15 минут после внутримышечной инъекции, а максимальная концентрация в хрящевой ткани достигается через 48 часов [18]. Внутримышечный способ введения ХС увеличивает биодоступность и долю нативных молекул в системном кровотоке, благодаря чему может повышаться как эффективность проводимой терапии, так и более быстрое развитие симптоматического эффекта.
Целью исследования явилась оценка эффективности, переносимости и безопасности ХС (Хондрогарда) для пациентов с ОА коленных суставов при внутримышечном применении.
Материал и методы
В 2-месячное проспективное когортное исследование были включены 70 человек с диагнозом ОА коленных суставов, среди них были 67 (96 %) женщин и 3 (4 %) мужчины. Диагноз остеоартроза устанавливался на основе классификационных критериев Американской коллегии ревматологов (АКР) 1986 г. [5].
Критерии включения:
В исследование не включали лиц с вторичным гонартрозом, внутрисуставным введением любых препаратов за последние 6 недель до начала исследования, наличием хондрокальциноза, асептического некроза мыщелков бедренных и большеберцовых костей, оперативных вмешательств на коленном суставе, а также с известной повышенной чувствительностью к ХС, тяжелыми сопутствующими заболеваниями, язвой желудка или двенадцатиперстной кишки в течение последнего месяца, кровотечениями в анамнезе, тромбофлебитами, беременностью и периодом лактации, принимавшими препараты с симптоматическими и структурно-модифицирующими свойствами. Разрешалось использование НПВС, которые пациенты принимали на момент включения в исследование. Не допускались внутрисуставные инъекции, в т. ч. глюкокортикоидов и препаратов гиалуроновой кислоты, прием антикоагулянтов, антиагрегантов, фибринолитиков, проведение физиотерапевтических процедур.
В исследование вошли лица в возрасте от 45 до 70 лет, средний возраст составил 61,0 ± 6,4 года, рост - 1,63 ± 0,06 м, масса тела - 81,6 ± 12,9 кг, индекс массы тела (ИМТ) - 31 ± 4,6 кг/м2, медиана длительности заболевания - 9 лет (25-й, 75-й процентили -5 и 12 лет), медиана длительности последнего обострения - 2 месяца (25й, 75-й процентили - 1,4 и 4,0 месяца). Наиболее выраженная симптоматика на момент включения в исследование, как правило, отмечалась в правом коленном суставе (64 %) по сравнению с левым (36 %). При этом большинство (79 %) лиц имели ОА II рентгенологической стадии и 21 % - ОА III стадии.
Характеристика участников исследования представлена в табл. 1.
Таблица 1
Характеристика участников исследования
| Параметры | Мин. | Макс. | Среднее | SD |
| Возраст, годы | 45 | 70 | 61 | 6,4 |
| Рост, м | 1,5 | 1,77 | 1,63 | 0,06 |
| Масса тела, кг | 54 | 110 | 81,6 | 12,9 |
| ИМТ, кг/м2 | 22 | 40 | 31 | 4,6 |
| Длительность болезни | Медиана - 9 лет, 25-й процентиль - 5 лет, 75-й процентиль - 12 лет |
|||
| Длительность обострения | Медиана - 2 месяца, 25-й процентиль - 1,4 месяца, 75-й процентиль - 4 месяца |
|||
Пол: Ж - 67 (96 %), М - 3 (4 %) |
||||
Суставы: правый - 64 %, левый - 36 % |
||||
Рентгенологическая стадия: II - 79 %, III - 21 % |
||||
В качестве показателей эффективности использовали динамику индекса WOMAC (Western Ontario and McMaster University) в целом, а также отдельных параметров: значение боли, скованность и функциональная недо статочность (ФН). Оценивали динамику изменений скорости ходьбы на 15 метров, потребность в НПВС на протяжении исследования и общую оценку эффекта пациентом в конце исследования. Также оценивали частоту и характер нежелательных явлений (НЯ), их связь с исследуемым препаратом.
Всем пациентам через день внутримышечно вводили ХС на протяжении 2 месяцев (№ 30). Первые три инъекции выполнялись в дозе 1 мл (100 мг), последующие - в дозе 2 мл (200 мг). В случае необходимости пациенты продолжали терапию НПВС, при этом применения другого НПВС на протяжении исследования не допускалось.
Статистическая обработка данных проведена с помощью программы SPSS 16.0. Результаты представлены в виде среднего значения и стандартного отклонения или медианы и 25-й и 75-й процентилей. Нормальность распределения оценивали с помощью теста Колмогорова-Смирнова. Оценка изменений проведена с помощью однофакторного дисперсионного анализа с повторными измерениями и парного t-теста.
Результаты исследования
Всего в исследовании приняли участие 70 человек, среди них 67 (96 %) женщин и 3 (4 %) мужчины. Полностью завершили исследование 66 (94 %) человек, 4 (6 %) пациента выбыли: трое - в результате появления НЯ и один — из-за отсутствия эффекта от проводимой терапии.
Терапия ХС в виде внутримышечных инъекций была эффективной для большинства больных. Были выявлены статистически значимые улучшения как отдельных показателей: боль, скованность, ФН, так: и WOMAC в целом. Результаты представлены на рис. 1.
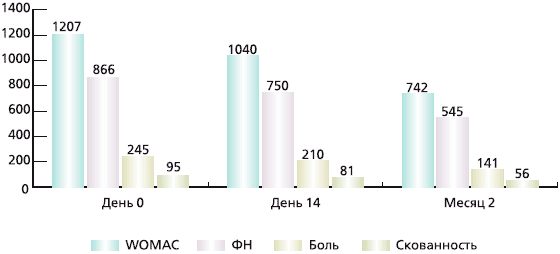
Рис 1. Динамика показателей WOMAC, боли, скованности функциональной недостаточности (указаны средние значения), р < 0,001 для всех показателей
Показатели WOMAC значимо уменьшились уже через две недели, в среднем на 167 (14 %) мм (95 % доверительный интервал [ДИ] — 112—219; р < 0,001), а через 2 месяца — на 465 (39 %) мм (95 % ДИ — 387— 569; р < 0,001).
На фоне лечения препаратом Хондрогард отмечено статистически значимое уменьшение боли по шкале WOMAC через две недели на 14 %, или в абсолютных значениях — на 35 мм (95 % ДИ — 21—49; р < 0,001). При продолжении терапии ко второму месяцу положительная динамика достигла 43 %, что соответствовало снижению боли в среднем на 104 мм (95 % ДИ — 85—124; р < 0,001).
Скованность в оцениваемом коленном суставе через 2 недели статистически значимо уменьшилась на 14 мм (95 % ДИ — 8—22; р < 0,001), 15 %, через два месяца — на 39 мм (95 % ДИ —31—51; р < 0,001), 41 %. Отмечено статистически значимое улучшение функциональных показателей через 2 недели на 13 % и снижение ФН на 116 мм (95 % ДИ —78—154; р < 0,001), ко второму месяцу терапии улучшение достигло 37 %, а показатели ФН снизились на 321 мм (95 % ДИ — 265—393; р < 0,001; табл. 2).
Таблица 2
Динамика показателей WOMAC, боли, скованности ФН в процессе лечения
| Параметры | День 0 | 14-й день | 2-й месяц | р |
| WOMAC | 1207 (350) | 1040 (404), 14 % | 742 (412), 39 % | < 0,001 |
| Боль | 245 (65) | 210 (86), 14 % | 141 (87), 43 % | < 0,001 |
| Скованность | 95 (37) | 81 (38), 15 %, 14 мм | 56 (40), 39 мм, 41% | < 0,001 |
| ФН | 866 (265) | 750(297) | 545 (297), 321, 37 % | < 0,001 |
Через две недели терапии достигнуто незначительное увеличение скорости прохождения дистанции 15 метров, время прохождения дистанции снизилось на 0,75 секунды (95 % ДИ — 0,12— 1,38, р = 0,021), 5 %; через 2 месяца — на 1,88 секунды (95 % ДИ — 1,25—2,51, р < 0,001), 13 %.
Из 63 пациентов, отметивших положительный эффект от проводимой терапии, полностью прекратили прием НПВС 28 (44 %) человек, или 40 % от общего числа участников исследования. Уменьшили дозу в 2 раза или стали принимать НПВС не чаще 1 раза в 3 дня 21 (33 %) участник, или 30 % от общего их числа. Отметили улучшение состояния, но продолжали принимать прежнюю дозу НПВС 14 (22 %), или 20 % от общего числа участников. Два человека прекратили прием НПВС, но отметили усиление симптоматики и в дальнейшем выбыли из исследования.
В среднем на 23 ± 10-й день пациенты отмечали эффект от лечения. Из 70 участников исследования эффективность препарата оценили 68 человек (двое выбыли и не принимали участие в общей оценке). Из оставшихся 68 пациентов полностью закончили исследование 66 и 2 выбыли, но также принимали участие в оценке эффективности. Хороший эффект препарата отметил 41 (59 %) пациент, удовлетворительный — 22 (31 %) и 5 (7 %) человек не заметили какого-либо эффекта (рис. 2).
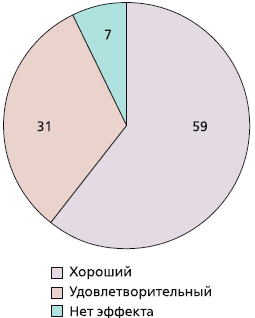
Рис. 2. Общая оценка пациентами эффективности терапии ХС, %
В ходе исследования были выявлены следующие НЯ: небольшие гематомы в месте введения препарата - 8 (11%) пациентов; кожный зуд, папулезную сыпь - 4 (6 %); болезненные уплотнения в месте инъекции - 2 (3 %); чувство жара после инъекции - 1 (1 %); тошноту, диарею - 1 (1%). Серьезные НЯ отсутствовали.
Из-за НЯ выбыли 3 (4 %) человека и 1 - из-за неэффективности лечения. При этом у двоих отмечены папулезная сыпь и кожный зуд, что было расценено исследователями как реакция, связанная с препаратом; у одного пациента - тошнота и диарея, которые купировались после прекращения введения препарата. Эта реакция также была расценена исследователями как связанная с применением препарата.
Обсуждение
ХС относится к группе препаратов замеленного действия для симптоматической терапии ОА, препарат обладает большим спектром биологической активности, оказывая влияние почти на все ключевые моменты патогенеза ОА. Литература располагает массой работ, в которых оценивался симптомагический эффект ХС. В некоторых мета-анализах был выявлен значимый эффект ХС на боль, скованность и ФН. Так, у 372 больных ОА Leeb и соавт. [6] отметили положительный эффект ХС на боль 0,9 (95 % ДИ 0,8—1,0) и функцию суставов 0,74 (95 % ДИ -0,65-0,85). По данным мета-анализа 15 рандомизированных контролируемых исследований (РКИ) McAlindon и соавт. [7] обнаружили достаточно выраженный эффект ХС. Размер общего терапевтического эффекта составил 0,78 (95 % ДИ - 0,6-0,95). Согласно общепринятому подходу, эффект менее 0,2 рассматривается как незначительный, 0,5 - как средний и более 0,8 -как выраженный. Однако при учете только крупномасштабных исследований или исследований, характеризующихся высоким качеством, показатели размера эффекта снижались. Проведя мета-анализ 20 РКИ влияния ХС на боль у 3846 больных ОА коленных и тазобедренных суставов, Reichenbach и соавт. [8] тоже выявили довольно высокие показатели эффективности проведенной терапии - 0,75 (-0,99 до -0,5).
В представленной работе, которая имела дизайн открытого проспективного исследования, авторы выявили статистически значимое улучшение показателей боли, скованности, ФН и общего WOMAC по сравнению с исходными данными уже через две недели, хотя изменения и не достигли уровня клинической значимости (улучшение показателя более чем на 20 %). Однако уже ко второму месяцу терапии все значения индекса WOMAC (боль, скованность, ФН) снизились на 43 %, 41 и 37 % соответственно. Эффект от проводимой терапии отмечен 90 % пациентов, в 3 % случаев присутствовал положительный эффект, однако после отмены НПВС этот эффект исчезал. В РКИ, проведенном в США (n = 1583) [9], авторы в целом не обнаружили клинически значимого влияния ХС и глюкозамина на показатели боли (эффект считался клинически значимым при снижении уровня боли на 20 %) по сравнению с плацебо. Однако комбинированное применение ХС и глюкозамина лицами с умеренными и выраженными болями оказалось более эффективным по сравнению с плацебо (79,2 против 54,3 % соответственно; р = 0,002).
Недостаточная эффективность применения ХС может быть обусловлена различными причинами: особенностью самого препарата, его химической структурой, степенью очистки, способом введения препарата, а также активностью заболевания и степенью деструктивных изменений в суставе.
Следует отметить, что ХС обладает высоким профилем безопасности. Ни в одном из проведенных клинических исследований не было выявлено каких-либо значимых побочных эффектов, в т. ч. и при длительном применении. EULAR рассматривает ХС в качестве одного из самых безопасных лекарственных препаратов терапии ОА. При использовании внутримышечных форм отмечено увеличение числа локальных побочных эффектов по сравнению с пероральными. В нашем исследовании в 8 (11 %) случаях были выявлены небольшие гематомы в месте введения препарата, что указано в инструкции по применению Хондрогарда; кожный зуд; папулезная сыпь — в 4 (6 %); болезненные уплотнения в месте инъекции — в 2 (3 %); чувство жара после инъекции — в 1 (1 %); тошнота, диарея — в 1 (1 %) случае. Серьезные НЯ отсутствовали.
Таким образом, препарат Хондрогард, представляющий собой раствор ХС натрия для внутримышечного применения, обладает достоверным симптоматическим эффектом, уменьшая боль, скованность и улучшая функциональные показатели. Преимущество препарата состоит в быстром наступлении эффекта при внутримышечном применении, возможности отмены или снижения дозы НПВС на фоне лечения и хорошей переносимости. Препарат Хондрогард может быть рекомендован в качестве терапии лицам, страдающим ОА, как первое средство, дающее более быстрый эффект с последующей заменой его на пероральные формы.
ЛИТЕРАТУРА
1. Lane NE, Brandt K, Hawker G и соавт. OARSIFDA initiative: defining the disease state of osteoarthritis. Osteoarthritis Cartilage 2011;19(5):478-82.
2. Клинические рекомендации. Ревматология / Под ред. Е.Л. Насонова. М., 2010. 326 с.
3. Zhang W, Nuki G, Moskowitz RW, et al. OARSI recommendations for the Management of hip and knee osteoarthritis Part III: changes in evidence following systematic cumulative update of research published through January 2009. Osteoarthritis Cartilage 2010;18(4): 476-99.
4. Hochberg MC, Altman RD, April KT, et al. American college of Rheumatology 2012 Recommendations for the Use of Nonpharmacologic and Pharmacologic Therapies in Osteoarthritis of the Hand, Hip and Knee. Arthritis Care & Res 2012;64(4):465-74.
5. Клинические рекомендации. Ревматология / Под ред. Е.Л. Насонова. М.,2010. 329 с.
6. Leeb BF, Schweitzer H, Montag K, et al. A metaanalysis of chondroitin sulfate in the treatment of osteoarthritis. J Rheumatol 2000;27(1): 205-11.
7. McAlindon TE, LaValley MP, Gulin JP, Felson DT. Glucosamine and chondroitin for treatment of osteoarthritis: a systematic quality assessment and meta-analysis. JAMA 2000;283(11):1469-75.
8. Reichenbach S, Sterchi R, Scherer M, et al. Meta-analysis: chondroitin for osteoarthritis of the knee or hip. Ann Intern Med 2007;146(8): 580-90.
9. Clegg DO, Reda DJ, Harris CL, et al. Glucosamine, chondroitin sulfate, and the two in combination for painful knee osteoarthritis. N Engl J Med 2006;354(8):795-808.
10. Volpi N, ed. Chondroitin sulfate: structure, role and pharmacological activity. Amsterdam: Academic Press, 2006.
11. Fuentes EP, Diaz VB. Oligosaccharide mapping of chondroitin sulfate obtained from different animal sources. Acta Farm Bonaerense 1998;17:135-42.
12. Luo XM, et al. Chicken keel cartilage as a source of chondroitin sulfate. Poult Sci 2002;81: 1086-89.
13. Sugahara K, et al. Structural analysis of unsaturated hexasaccharides isolated from shark cartilage chondroitin sulfate D that are substrates for the exolytic action of chondroitin ABC lyase. Eur J Biochem 1996;239:871-80.
14. Lignot B, Lahogue V, Bourseau P. Enzymatic extraction of chondroitin sulfate from skate cartilage and concentration-desalting by ultra filtration. J Biotechnol 2003;103:281-84.
15. Volpi N. Quality of different chondroitin sulfate preparations in relation to their therapeutic activity. J Pharm Pharmacol 2009;61(10): 1271-80.
16. Volpi N. Oral absorption and bioavailability of ichthyic origin chondroitin sulfate in healthy male volunteers. Osteoarthritis Cartilage 2003;11(6):433-41.
17. Volpi N. Oral bioavailability of chondroitin sulfate (Condrosulf) and its constituents in healthy male volunteers. Osteoarthritis Cartilage 2002;10(10):768-77.
18. Ronca F, Palmieri L, Panicucci P, Ronca G. Antiinflammatory activity of chondroitin sulfate. Osteoarthritis Cartilage 1998;6 Suppl A:14-21.
