Противовоспалительная терапия хронической обструктивной болезни легких
СтатьиОпубликовано в журнале:
«Пульмонология», 2009, № 4, с. 85-90
А.В.Безлепко 1, Е.А.Безлепко 2, Н.К.Захарова 3, В.Е.Ефимова 4
1 – ФГУ "Главный военный клинический госпиталь им. Н.Н.Бурденко Минобороны России": 105229, Москва, Госпитальная пл., 3.;
2 – Войсковая часть: 129334, Москва, ул. Искры, 31а;
3 – ФГУ "9-й Лечебно-диагностический центр Минобороны России": 119021, Москва, ул. Большая Пироговская, 15;
4 – ФГУ "12-й Лечебно-диагностический центр Минобороны России": 109337, Москва, ул. Академика Скрябина, 3
Резюме
В 7-летнем открытом сравнительном исследовании в параллельных группах изучена эффективность и безопасность Эреспала (фенспирида) при лечении пациентов с легкой и среднетяжелой хронической обструктивной болезнью легких (ХОБЛ). В основной группе (n = 95) больные получали фенспирид в дозе 160 мг в сутки в сочетании с бронхолитиками. Пациентам, у которых данная терапия была мало эффективной или неэффективной, через 2 года наблюдения фенспирид отменяли и назначали базисную терапию ингаляционными глюкокортикостероидами (флутиказона пропионатом) или комбинированными препаратами (сальметеролом / флутиказона пропионатом, будесонидом / формотеролом). Больные группы сравнения (n = 45) весь период наблюдения получали терапию короткодействующими b2-агонистами или, в последующем, длительнодействующим b2-агонистом формотеролом. При сравнении результатов исследования были выявлены преимущества комбинированной терапии фенспиридом в сочетании с бронхолитиками у больных с легкой стадией ХОБЛ и среднетяжелой (объем форсированного выдоха за 1-ю с (ОФВ1 < 60 %), по сравнению с обычной терапией. Так, за период наблюдения кумулятивный индекс респираторной симптоматики в основной группе снизился с 1,92 до 0,54 балла, в группе сравнения — с 1,96 до 1,49 балла. Падение ОФВ1 у пациентов основной группы за 7 лет составило 252,0 ± 13,6 мл, а в группе сравнения — 336,0 ± 22,4 мл. Количество госпитализаций на 1 больного в основной группе было 0,30 ± 0,12, а в группе сравнения —1,40 + 0,16 (до начала исследования — 1,43 ±0,16 и 1,36 ±0,14 соответственно). Итоговая оценка качества жизни больных основной группы за период лечения увеличилась с —40 до —21, чего не произошло в группе сравнения. Вместе с тем у больных среднетяжелой стадией ХОБЛ с ОФВ1 0,05).
Ключевые слова: хроническая обструктивная болезнь легких, фенспирид, терапия.
Anti-inflammatory therapy in chronic obstructive lung disease
A.V.Bezlepko, E.A.Bezlepko, N.K.Zakharova, V.E.Efimova
Summary
This 7-year open comparative parallelgroup trial investigated efficacy and safety of fenspirid (Eurespal) in patients with mild to moderate chronic obstructive pulmonary disease (COPD). The treatment group patients (n = 95) received fenspirid 160 mg daily in combination with bronchodilators. After 2 years of the treatment, fenspirid was withdrawn and basic therapy with inhaled corticosteroids (fluticasone propionate) or combined drugs (salmeterol / fluticasone propionate or budesonide / formoterol) was administered in patients who gained faint effect or no effect of the treatment. The control group (n = 45) were treated with short-acting в2-agonists or long-acting в2-agonist formoterol during the follow-up period. Combination of fenspirid with bronchodilators was more effective in mild COPD patients when compared to the standard treatment. Over the follow-up period, the cumulative respiratory symptom index decreased from 1.92 to 0.54 in the treatment group and from 1.96 to 1.49 in the control group. Over 7 years, the decline of FEV1 was 252.0 ± 13.6 mL and 336.0 ± 22.4 mL, respectively. At the end of the study, number of hospitalizations per one patient was 0.30 ± 0.12 and 1.40 ± 0.16, respectively (vs 1.43 ± 0.16 and 1.36 ± 0.14, respectively, at the baseline). The total quality of life score improved from –40 to –21 in the treatment group but it was not a case in the control group. Meanwhile, this treatment was insufficient in patients with moderate COPD (FEV1 Key words: COPD, fenspirid, therapy.
Хроническая обструктивная болезнь легких (ХОБЛ) является одним из наиболее распространенных заболеваний органов дыхания. В настоящее время она считается "болезнью века" из-за неуклонного роста заболеваемости, инвалидизации и летальности, а также колоссального ущерба, наносимого обществу. Смертность от ХОБЛ растет быстрее смертности от других причин, за исключением СПИДа, и занимает в России 4—5-е место [1—4].
В основе современной фармакотерапии ХОБЛ лежит ступенчатый подход, при котором препараты назначают в соответствии со степенью тяжести заболевания. При этом используются следующие фармакологические группы: М-холинолитики, симпатомиметики, метилксантины, муколитики, глюкокортикостероиды (ГКС), антибиотики. В качестве базисной терапии рекомендуются бронхорасширяющие препараты [1, 3, 5]. Независимо от степени тяжести, ХОБЛ рассматривается как хроническое воспаление с преимущественным поражением дистального отдела дыхательных путей [1, 3, 4]. Исходя из этого противовоспалительная терапия также должна составлять основу базисного лечения ХОБЛ. Федеральная программа по ХОБЛ [1] и международный документ GOLD (Глобальная инициатива: стратегия ведения больных ХОБЛ) [3] в качестве противовоспалительной терапии рекомендуют систематически применять ингаляционные ГКС (иГКС) только при тяжелой и крайне тяжелой стадиях ХОБЛ. До настоящего времени не решен вопрос о необходимости противовоспалительной терапии у больных с легкой и среднетяжелой ХОБЛ. Результаты исследований, в которых изучалось влияние длительного применения иГКС на стабильное течение тяжелой и крайне тяжелой ХОБЛ, также противоречивы, и некоторые из них не продемонстрировали способность иГКС приостановить неуклонное падение объема форсированного выдоха за 1-ю с (ОФВ1). Поэтому постоянно ведутся поиски новых эффективных противовоспалительных средств и комбинаций препаратов для терапии ХОБЛ [2—5].
В связи с этим привлекает внимание фенспирид (Эреспал) — негормональный препарат, обладающий оригинальным противовоспалительным действием на респираторную систему [6—9]. Многочисленными исследованиями доказана его эффективность и хорошая переносимость [10—13].
Целью настоящего клинического исследования было изучение эффективности и безопасности длительного применения фенспирида в лечении легкой и среднетяжелой стадий ХОБЛ стабильного течения.
Материалы и методы
В 7-летнем открытом рандомизированном исследовании изучалось влияние противовоспалительной терапии на течение ХОБЛ у пациентов с легкой и среднетяжелой стадиями заболевания. Диагноз ХОБЛ был подтвержден данными анамнеза, клинической картины, функциональными и рентгенологическими методами исследования [1, 3]. Критериями включения в исследования были: возраст > 40 лет; кашель, который клинически определяется как хронический продуктивный и длится 3 мес. в течение 2 последовательных лет при отсутствии других его причин [1, 3]; продукция мокроты и / или одышка, не связанные с другими заболеваниями; анамнестические указания на воздействие факторов риска для этой болезни, особенно курения (индекс курения > 10 пачек / лет); показатели спирометрии, подтверждающие наличие хронической бронхиальной обструкции (ОФВ1 > 50 %Д0Лж.; отношение ОФВ1 к форсированной жизненной емкости легких (ФЖЕЛ) В исследование не включались больные с типичными приступами удушья в анамнезе, подтвержденной кожными тестами атопией, эозинофилией крови и мокроты, повышенными значениями иммуноглобулина Е, получавшие терапию ГКС (системными или иГКС) на момент включения в исследование, с тяжелой сопутствующей патологией. Пациенты, у которых в течение 4 нед., предшествовавших скрининговому визиту, имели место любая респираторная инфекция, обострение ХОБЛ или сопутствующего заболевания, включались в исследование по прошествии 3-месячного срока после купирования острого процесса и восстановления нормального самочувствия.
Обязательным было наличие информированного согласия каждого пациента.
Исследование проводилось в 2 этапа. На 1-м, амбулаторном, этапе проводился скрининговый отбор больных. На 2-м этапе осуществлялись окончательное (стационарное) обследование больных, распределение их по группам лечения и динамическое наблюдение.
Дизайн исследования был следующим: в течение первых 2 лет (96 нед.) все пациенты основной группы кроме базисной терапии короткодействующими b2-агонистами (КДБА) в течение 2 лет получали фенспирид в дозе 80 мг (по 1 таблетке утром и вечером до еды). В базисную терапию этих больных не включались системные ГКС, иГКС, фиксированные комбинации иГКС и длительно действующих b2-агонистов (ДДБА). Лечение проводилось амбулаторно в течение 3 мес. В дальнейшем, после 3-месячного перерыва, терапия фенспиридом была постоянной в течение 1,5 лет. Затем больным, у которых данное лечение было малоэффективным или неэффективным, фенспирид отменяли и назначали в виде базисной терапии либо иГКС (флутиказона пропионат), либо иГКС + ДДБА (сальметерол / флутиказона пропионат или будесонид / формотерол). Пациенты группы сравнения весь период наблюдения получали терапию только КДБА или ДДБА (формотерол).
Показаниями для продолжения лечения фенспиридом в основной группе были: ухудшение клинических, лабораторных и функциональных показателей при отсутствии признаков обострения ХОБЛ, изменение соотношения клеточного состава слизистой бронхов и бронхоальвеолярного лаважа (БАЛ) в пользу нейтрофилов.
Контрольные обследования выполнялись в стационаре (3—4 дня) в первые 3 мес. в конце каждого месяца лечения фенспиридом, затем через каждые 3 мес. в течение 1-го года лечения, впоследствии — каждые 4 мес. амбулаторно или в стационаре.
В период каждого стационарного обследования изучались жалобы и осуществлялся общий осмотр больных. Кроме того, выполнялись общеклинические анализы крови и мочи, биохимический анализ крови, определялось содержание иммуноглобулинов классов А, М, G, Е, циркулирующих иммунных комплексов. Сатурацию (8аОг) изучали посредством аппарата Pulse oximeter-305 (Palco Labs, Inc., США). Функцию внешнего дыхания исследовали в соответствии с рекомендациями Европейского респираторного общества [14]. Полученные результаты сопоставлялись с должными величинами. Бронходилатационный тест выполняли с ингаляцией сальбутамола в дозе 400 мкг. [1]. Бронхиальную обструкцию считали обратимой при приросте ОФВ[ > 12 % и > 200 мл [1, 3]. Чтобы выявить влияние противовоспалительной терапии на клеточный состав трахео-бронхиального дерева, выполнялась фибробронхоскопия посредством аппарата Olympus BFP20 (Olympus Corporation, Япония). После забора бронхоальвеолярного смыва (БАС) из той же зоны выполняли браш-биопсию слизистой дистального отдела бронха. Анализировалось процентное соотношение альвеолярных макрофагов, лимфоцитов, нейтрофилов, эозинофилов и др. Клетки бронхиального эпителия в мазке БАС не учитывались в связи с их незначительным количеством. Рентгенографию органов грудной клетки проводили при первичном обследовании больных, в дальнейшем — по показаниям. До начала исследования, а затем каждые 3 мес. изучались показатели качества жизни (КЖ) больных с помощью адаптированной русскоязычной версии Респираторного опросника Госпиталя святого Георгия [15].
Выраженность одышки, кашля, продукции мокроты оценивали по бальной системе модифицированной шкалы симптомов больных ХОБЛ Piggaro (1998) с включением в шкалу оценки диспноэ по Medical Research Council Dyspnea Scale [9].
Весь период исследования пациенты ежедневно вели дневник самоконтроля, в котором оценивали кашель, отделение мокроты, одышку, чувство стеснения в груди, пиковую скорость выдоха (ПСВ), отмечали прием антибиотиков и системных ГКС и госпитализации по поводу обострения ХОБЛ.
Материалы исследования были статистически обработаны с использованием программы Statistica for Windows 7.0 (StatSoft, Inc.). Все данные представлены как mean ± SD (среднее значение + среднее квадратическое отклонение). Достоверность различий показателей внутри одной группы определяли с помощью t-критерия Стьюдента. Различия считались статистически достоверными при р Результаты и обсуждение
На этапе скрининга обследованы 179 больных ХОБЛ. Из-за несоответствия критериям включения выбыли 17 пациентов (9,8 %).
В исследовании участвовали 162 больных ХОБЛ, мужчины в возрасте от 40 до 80 лет (средний возраст — 61,2 ± 18,1 года). Из них 152 человека (93,8 %) курили и 10 (6,2 %) — прекратили курить в течение нескольких лет. Средний индекс курения составил 33,65 ± 12,85 пачки/лет. 109 пациентов (67,3 %) связывали развитие ХОБЛ с частыми простудными заболеваниями, 82 (50,6 %) — с перенесенными острыми пневмониями. Контакт с профессиональными вредностями (переохлаждение, токсические пары и газы, радиация, ионизирующее излучение, запыленность) имели 32 пациента (19,8 %). Средняя длительность заболевания составила 15,75 ± 11,95 года. Обострения развивались в среднем 2 раза в год и требовали медицинского вмешательства.
В начале исследования пациенты методом случайной выборки были распределены в 2 группы — основную и сравнения — в зависимости от базисной терапии и стадии ХОБЛ. Стадия ХОБЛ оценивалась в соответствии с Федеральной программой "Хроническая обструктивная болезнь легких" (1998, 2004) и GOLD (2001, 2003, 2006). При обследовании у 45 пациентов (27,8 %) была диагностирована легкая стадия ХОБЛ, у 117 (72,2 %) — сред нетяжелая.
По разным причинам из исследования выбыли 22 больных (12,0 %), большинство — 21 человек (95,5 %) — в 1-й год исследования. Из них из-за невыполнения назначений, пропусков визитов были исключены 4 пациента (18,2 %), из-за нежелания продолжать исследование — 9 больных (40,9 %). В связи с обострением язвенной болезни желудка и 12-перстной кишки были вынуждены выйти из исследования 4 пациента (18,2 %). По причине других нежелательных явлений проводимой терапии (тахикардия, гипотония и др.) выбыли 4 человека (18,2 %). На 3-м году наблюдения умер от острой коронарной недостаточности 1 больной (4,5 %) со среднетяжелой стадией ХОБЛ.
Полностью 7-летний период исследования прошли 140 больных. Пациенты основной группы — 19 человек (20 %) с легкой стадией ХОБЛ (1-я группа) и 76 человек (80 %) со среднетяжелой стадией ХОБЛ (2-я группа) в течение первых 2 лет принимали фенспирид в сочетании с короткодействующими бронходилататорами (КДБД). Пациенты группы сравнения — 13 человек (28,9 %) с легкой стадией ХОБЛ (3-я группа) и 32 человека (71,1 %) со средне-тяжелой стадией ХОБЛ (4-я группа) в течение этого же периода принимали только КДБД.
Сравнивались показатели пациентов с одной и той же стадией ХОБЛ (1-я группа — с 3-й и 2-я — с 4-й). На момент включения в исследование сформированные группы существенно не различались по выраженности клинических симптомов, потребности в КДБА, лабораторным, функциональным и эндоскопическим данным. Однако больные ХОБЛ среднетяжелой стадии по выраженности кашля, одышки, хрипов в легких, изменениям функциональных показателей и кумулятивному индексу достоверно отличались от пациентов с легкой стадией заболевания (табл. 1).
Таблица 1. Выраженность респираторной симптоматики у больных ХОБЛ в период ремиссии заболевания
| Признаки | Основная группа (n = 95) | Группа сравнения (n = 45) | ||
| 1-я группа (n = 19) | 2-я группа (n = 76) | 3-я группа (n = 13) | 4-я группа (n = 32) | |
| Кашель, баллы | 1,46 ± 0,16* | 2,38 ± 0,31* | 1,49 ± 0,15* | 2,42 ± 0,28* |
| Выделение мокроты, баллы | 1,18 ± 0,21 | 1,97 ± 0,24 | 1,15 ± 0,18 | 1,96 ± 0,23 |
| Гнойность мокроты, баллы | 1,27 ± 0,23 | 1,86 ± 0,17 | 1,23 ± 0,16 | 1,82 ± 0,15 |
| Одышка (шкала MRC), баллы | 0,97 ± 0,13* | 2,48 ± 0,12* | 0,96 ± 0,15* | 2,52 ± 0,10* |
| Одышка (шкала Borg), баллы | 0,92 ± 0,82* | 2,67 ± 0,86* | 0,94 ± 0,78* | 2,68 ± 0,82* |
| Сухие хрипы в легких, баллы | 0,88 ± 0,11 | 1,64 ± 0,14 | 0,84 ± 0,12 | 1,64 ± 0,21 |
| Кумулятивный индекс | 1,11 ± 0,28 | 2,17 ± 0,31* | 1,12 ± 0,29* | 2,19 ± 0,27* |
| SaО2, (%) | 96,22 ± 0,21 | 95,84 ± 0,42 | 96,16 ± 0,11 | 95,92 ± 0,23 |
| ФЖЕЛ,% | 101,20 ± 1,23 | 92,32 ± 1,16 | 99,86 ± 0,68 | 94,18 ± 1,32 |
| ОФВ1,% | 81,20 ± 0,12* | 65,3 ± 13,2* | 81,20 ± 0,14* | 64,8 ± 13,6* |
Примечание: * -р
При эндоскопическом исследовании только у 15 больных (10,7 %) состояние трахео-бронхиального дерева было нормальным, у 89 пациентов (63,6 %) были выявлены признаки диффузного катарального эндобронхита. Секрет в бронхиальном дереве обнаружен у 36 человек (25,7 %): у 29 — слизистого и у 7 — слизисто-гнойного характера (табл. 2).
Таблица 2. Характеристика эндоскопической картины у больных ХОБЛ в период ремиссии заболевания
| Эндоскопические признаки | Стадия ХОБЛ | |
| Легкая (n = 32) | Среднетяжелая (n = 108) | |
| Норма, n (%) | 11(34,4) | 4(3,7) |
| Катаральный эндобронхит, n (%) | 19(59,4) | 70 (64,8) |
| Катарально-слизистый эндобронхит, n (%) | 2(6,2) | 27 (25,0) |
| Слизисто-гнойный эндобронхит, n (%) | - | 7(6,5) |
Сопоставление результатов цитограмм БАЛ и браш-биопсии слизистой бронхов не выявило достоверного различия между материалами исследования (р > 0,05), что свидетельствует о взаимозаменяемости этих методов в изучении клеточного состава трахео-бронхиального дерева. Данные цитологического исследования жидкости БАЛ (ЖБАЛ) и мазков слизистой бронхов свидетельствовали о наличии практически у всех больных признаков воспаления, что проявлялось в значительном преобладании нейтрофилов над макрофагами и лимфоцитами (табл. 3).
Таблица 3. Клеточный состав слизистой бронхов больных ХОБЛ в период ремиссии
| Эндоскопические признаки | Стадия ХОБЛ | |
| Легкая n = 32 |
Среднетяжелая n = 108 |
|
| Макрофаги, % | 26,80 ± 1,28 | 16,40 ± 1,22 |
| Нейтрофилы, % | 58,20 ± 2,32 | 68,60 ± 2,16 |
| Лимфоциты, % | 12,90 ± 0,15 | 5,1 ± 0,9 |
После 1-го мес. лечения у большинства пациентов основной группы, в отличие от группы сравнения, улучшилось самочувствие, что проявлялось уменьшением выраженности кашля, отделяемой мокроты и одышки (рис. 1). Однако во время лечения фенспиридом (1—3-й мес.) клинико-лабораторные и функциональные показатели больных были лучше, по сравнению с периодом, когда этот препарат был отменен (3—6-й мес). После 3-месячного перерыва у всех пациентов основной группы базисная терапия фенспиридом была возобновлена.
Рис. 1. Динамика выраженности клинических показателей основной группы
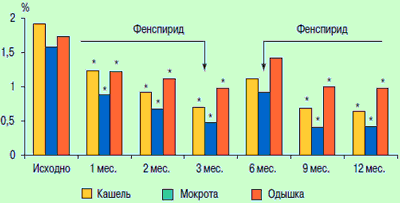
Примечание: здесь и на рис. 2—4: * — р
Положительная динамика клинической картины основной группы коррелировала с данными лабораторных и функциональных показателей и достоверно была более выраженной, чем в группе сравнения (р > 0,05). Существенно изменился и клеточный состав слизистой трахео-бронхиального дерева (рис. 2).
Рис. 2. Показатели клеточного состава слизистой бронхов основной группы
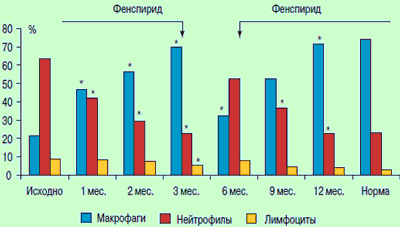
В цитограмме значительно увеличилось количество макрофагов. Соотношение клеточных элементов практически у всех пациентов приблизилось к показателям, соответствующим норме, и только у 9 больных (11,8 %) ХОБЛ среднетяжелой стадии со- хранились умеренные признаки воспаления. Купирование явлений воспаления трахео-бронхиального дерева сопровождалось также нормализацией иммуноглобулинов периферической крови и ЖБАЛ.
Проведенные ранее исследования эффективности и безопасности фенспирида в терапии ХОБЛ продолжались в основном 6 мес, что недостаточно для объективной оценки влияния препарата на такие важные показатели, как обострение ХОБЛ, госпитализации, связанные с заболеванием, показатель ежегодного падения ОФВ[ и КЖ. В настоящем исследовании лечение фенспиридом проводилось в течение 2 лет. За этот период у пациентов основной группы с легкой стадией ХОБЛ все изучаемые показатели были достоверно лучше (р 60 % (подгруппа А, n = 19) продолжили терапию фенспиридом в течение следующих 5 лет; больные с ОФВ1 60 % в последующие 5 лет продолжили терапию КДБД, остальные 19 человек с ОФВ1 В период наблюдения у больных основной группы выраженность кашля, количества отделяемой мокроты, одышки достоверно были меньше, чем в группе сравнения (рис. 3).
Рис. 3. Динамика респираторной симптоматики (по кумулятивному индексу) у больных основной группы
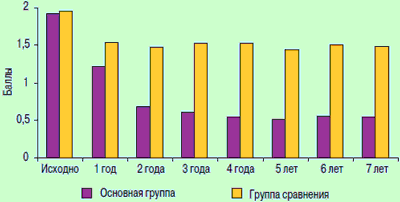
Положительная динамика респираторной симптоматики ХОБЛ у больных основной группы, принимающих фенспирид постоянно в течение 7 лет, коррелировала с рядом показателей, которые оценивались в период наблюдения. Так, пациенты основной группы внепланово использовали КДБД в среднем на 2,6 ингаляции меньше, чем в группе сравнения. Падение ОФВ1 у больных основной группы за 7 лет составило 252,0 ± 13,6 мл, а в группе сравнения данный показатель достоверно был выше и составил 336,0 ± 22,4 мл (р Наиболее достоверным показателем оценки воспаления трахео-бронхиального дерева является изучение его клеточного состава. У больных основной группы на протяжении всего периода наблюдения количество таких маркеров воспаления, как нейтрофилов, было достоверно меньше, чем в группе сравнения (р Одним из эффективных методов оценки состояния здоровья является изучение КЖ — показателя, которые интегрирует множество физических и психологических характеристик пациента, отражающих его способность адаптироваться к проявлению заболевания [17]. Результаты анализа КЖ, представленные на рис. 4, позволяют сделать вывод, что применение фенспирида позволяет уменьшить выраженность симптомов ХОБЛ и неблагоприятных психологических последствий данной патологии, а также повысить физическую активность больных. В группе сравнения такие результаты получены не были.
Рис. 4. Показатели качества жизни больных основной группы
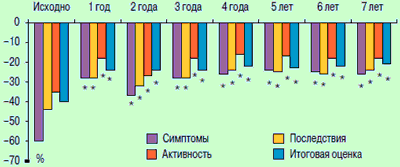
Безопасность
В ходе лечения фенспиридом отклонения лабораторных показателях, отражающих функцию печени, почек и других органов, а также электрокардиографические изменения, выявлены не были. Нежелательные явления, связанные с приемом фенспирида, зарегистрированы у 9 больных (9,1 %). Из них у 4 пациентов (4 %) рецидивировала язвенная болезнь 12-перстной кишки, у 2 (2 %) — возникла гипотония, а у 2 (2 %) — тахикардия. Эти больные были исключены из исследования на начальном его этапе. У 1 (1 %) пациента отмечалась сонливость, которая прошла после адаптации к препарату.
Заключение
Таким образом, даже в период стабильного течения заболевания у пациентов с ХОБЛ имеются признаки воспаления трахео-бронхиального дерева, которые подтверждаются данными цитологического исследования. Наличие персистирующего воспаления, вероятнее всего, лежит в основе прогрессирующего течения ХОБЛ. В связи с этим противовоспалительная терапия должна начинаться уже при легкой стадии заболевания и составлять основу лечения.
Длительное применение фенспирида в сочетании с бронхолитическими препаратами позволяет контролировать воспаление в трахео-бронхиальном дереве у больных легкой и среднетяжелой ХОБЛ (OФВ1 > 60 %), уменьшить клинические проявления и улучшить КЖ пациентов.
ЛИТЕРАТУРА
1. Чучалин А.Г. (ред.). Хроническая обструктивная болезнь легких. Федеральная программа. М.; 2004. 1—61.
2. Чучалин А.Г. (ред.). Хроническая обструктивная болезнь легких: Серия монографий Российского респираторного общества. М.: Изд-во "Атмосфера"; 2008.
3. Global Initiative for Chronic Obstructive Lung Diseases (GOLD). Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease. Updated 2007. www.goldcopd.com
4. Шмелев Е.И. Хроническая обструктивная болезнь легких. В кн. Чучалин А.Г (ред.). Пульмонология: Нац. руководство. М.: ГЭОЕАР-Медиа; 2009: 303-360.
5. Лещенко И. В. Медикаментозная терапия стабильного течения хронической обструктивной болезни легких. Пульмонология 2008; 3: 73—82.
6. Carre Ph., Pinelli Е., Forgue M.F. et al. In vitro effects of fenspiride on the production of free oxygen radicals, prostaglandins and leucotrienes by guinea-pig alveolar macrophages. Eur. Respir. Rev. 1991; 1, 2: 79—85.
7. Pipy В., Pinelli E., Forgue M.F. et al. Fenspiride inhibits arachidonic acid metabolite production and cytosolic Ca2 + increase by inflammatory macrophages. Eur. Respir. J. 1992; 5: 237.
8. Pinelli E., Frisach M.F, Crambes O., Pipy B. Fenspiride inhibits the production of eicosanoids after stimulation of airways epithelial cells by histamine. Eur. Respir. J. 1994; 7 (suppl. 18): 186.
9. Pipy В., Quartulli F., Pinelli E. etal. Histamine HI receptor mediated calcium increase and eicosanoid production in Wl 26VA4 human lung epithelial cell line: effect of fenspiride". Eur. Respir. J. 1995; 8 (suppl. 19): 43.
10. Чучалин А.Г., Шмелев Е.И., Овчаренко СИ. и др. Эффективность фенспирида (Эреспала) у больных хронической обструктивной болезнью легких. Материалы фармацевтической группы Сервье. М.; 2005.
11. Akoun G, ArnaudF., Blanchon F. et al. Effects du fenspiride (Pneumorel 80) sur la fonction respiratorie et la gazometrie de patients presentatn une bronchopathie chronique obstructive stable. Eur. Respir. Rev. 1991; 1 (suppl. 2): 51—65.
12. Pirozynski M., Skucha W., Smolenski M. Lhe efficacy of fenspiride on the number of exacerbation and the time of first exacerbation in patients with chronic bronchitis. Pol. Merk. Lek. 2005. 19(110): 139-143.
13. Tardif C., Ozenne G., Patron P. et al. Effect of fenspiride on exercise performance in chronic obstructive pulmonary disease patients. Eur. Respir. J. 1993; 6 (suppl. 17): 426.
14. Стандартизация тестов исследования легочной функции. Пульмонология 1993; прил.: 1—92.
15. Jones P. W. Quirk of health status for chronic air flow limitation — the St. Georgeys Respiratory Questionnaire. Am. Rev. Respir. Dis. 1992; 145 (6): 1321-1327.
16. Bestall J.C., Paul E.A., Garrod R. et al. Usefulness of the Medical Research Council (MRC) dyspnea scale as measure of disability in patients with chronic obstructive pulmonary disease. Lhorax 1999; 54: 581—586.
17. Чучалин А.Г. (ред.). Качество жизни у больных бронхиальной астмой и хронической обструктивной болезнью легких. М.: Изд-во "Атмосфера"; 2004.
Информация об авторах
Безлепко Александр Викторович - к. м н., доцент, начальник пульмонологического отделения Главного военного клинического госпиталя им. Н.Н.Бурденко Минобороны РФ;
Безлепко Евгений Александрович - врач-терапевт, начальник медицинской службы, начальник медицинского пункта Войсковой части Минобороны РФ;
Захарова Наталья Константиновна - к. м. н., зав. пульмонологическим кабинетом ФГУ "9-й Лечебно-диагностический центр Минобороны России"; тел: (499) 244-55-30;
Ефимова Валентина Евгеньевна - зав. пульмонологическим кабинетом ФГУ "12-й Лечебно-диагностический центр Минобороны России".
Поступила 15.06.09
