Двойное-слепое сравнение агомелатина и венлафаксина XR по влиянию на половую функцию, антидепрессивной эффективности и переносимости
СтатьиA Double-Blind Comparison of Sexual Functionong, Antidepressant Efficacy, and Tolerability Between Agomelatine and Venlafaxine XR
Sidney H. Kennedy, MD, FRCPC,* Sakina Rizvi, HBSc,** Kari Fulton, BSc,*** Jill Rasmussen, MD****
*Department of Psychiatry, University of Toronto;
**University Health Network, Toronto;
***Pharmaceutical Sciences, University of Toronto, Toronto, Ontario, Canada;
****Psi-Napse,
Surrey, United Kingdom. J Clin Psychopharmacol 2008;28:329-333
Резюме: Нарушения половой функции относятся к проявлениям не леченного большого депрессивного расстройства и часто обнаруживают более высокую распространенность у пациентов, получающих терапию антидепрессантами, оказывая негативное влияние на комплаентность. В данном двойном-слепом, мультицентровом исследовании проводилась сравнительная оценка эффектов агомелатина (агонист MT1 и MT2 рецепторов и антагонист 5HT2C рецепторов) и венлафаксина XR на половую функцию по Шкале половых эффектов у пациентов с депрессией. 276 пациентов мужского и женского пола получали терапию агомелатином (50мг) или венлафаксином XR (титрация до целевой дозы 150 мг/сут) в течение 12 недель. Пациенты с исходно сохранной половой активностью (n = 193) и те из них, кто достиг ремиссии (n = 111), a priori включались в анализ изменений половой функции. Связанные с терапией половые дисфункции достоверно реже встречались у пациентов, получавших агомелатин, тогда как терапия венлафаксином XR была связана с достоверно более выраженными нарушениями по категориям влечения и оргазма Шкалы половых эффектов. Оба препарата обеспечивали одинаково высокие уровни ремиссии (агомелатин 73%; венлафаксин XR 66.9%), но в группе пациенты группы агомелатина реже преждевременно исключались из исследования из-за нежелательных явлений (агомелатин, 2.2% против венлафаксин XR 8.6%). Агомелатин является эффективным антидепрессантом более благоприятным профилем половых побочных эффектов в сравнении с венлафаксином XR, однако в данном исследовании сравнения с плацебо не предусматривалось.
Агомелатин является новейшим мелатонинергическим (MT и MT2 агонист) антидепрессантом со свойствами антагониста серотонина (5-HT)2C,[1-3] - тогда как венлафаксин XR представляет собой прототипический антидепрессант из класса ингибиторов обратного захвата серотонина и норадреналина. В соответствии с данными исследований венлафаксин обеспечивает более высокие уровни ремиссии в терапии большого депрессивного расстройства (БДР) в сравнении с селективными ингибиторами обратного захвата серотонина (СИОЗС),[4] но также связан с выраженными побочными эффектами, включая связанные с терапией половые дисфункции.[5-7] Поскольку выброс 5-HT и стимуляция 5-HT2 рецепторов вызывает нарушения функции полового возбуждения и оргазма[8], а применение антидепрессантов, действующих как блокаторы постсинаптических 5-HT2 рецепторов, таких как миртазапин[9] и нефазодон[10], сопряжено с меньшей частотой половых дисфункций[11], можно предположить, что агомелатин должен обладать благоприятным профилем половых побочных эффектов.
Нарушения половой функции (преимущественно влечение или либидо) выявляются более чем у половины не леченных пациентов с БДР[12-15]. Применение антидепрессантов, особенно СИОЗС, связано с дополнительными половыми дисфункциями, включая нарушения возбуждения и оргазма[5,13,16], которые часто приводят к снижению комплаентности к фармакотерапии.[6] Учитывая эти данные клиницистам следует оценивать каждую категорию половой функции до на чала и в ходе терапии антидепрессантами, по возможности используя стандартные рейтинговые шкалы. Шкала половых эффектов (Sex FX) обладает подтвержденной валидностью и уже использовалась в предыдущих исследованиях для сравнения половых побочных эффектов при терапии разными антидепрессантами. [1,17] Это короткий инструмент, разработанный для регистрации изменений частоты влечения, возбуждения и оргазма, который предусматривает возможность расчета суммарного балла шкалы и балла общего удовлетворения. При необходимости пункты шкалы Sex FX имеют половую специфичность; чем выше балл, тем лучше половая функция.
Данное исследование планировалось с целью сравнения половых побочных эффектов агомелатина и венлафаксина XR с помощью шкалы Sex FX у мужчин и женщин, страдающих большим депрессивным расстройством в соответствии с критериями Диагностического и Статистического руководства по психическим расстройствам 4-й редакции с ревизией текста (APA, 2000). Главным результирующим показателем было изменение половой функции, в качестве дополнительных показателей предусматривались оценки антидепрессивного эффекта и переносимости.
МАТЕРИАЛЫ И МЕТОДЫ
Выборка пациентов
В исследование было включено 320 амбулаторных пациентов в возрасте от 18 до 60 лет, из них 277 пациентов было рандомизировано для терапии агомелатином (n = 137) или венлафаксином XR (n = 140). Основными причинами исключения из рандомизации были аномальные лабораторные показатели или неприемлемая для исследования сопутствующая фармакотерапия. 276 из 277 рандомизированных пациентов были включены в полную выборку анализа (Full Analysis Set; FAS); 1 пациент из группы венлафаксина XR выбыл до начала 2-й недели исследования.
Для назначения рандомизированной терапии требовалось минимум 20 баллов по Шкале депрессии Монтгомери-Асберг[18] (MADRS) и отсутствие терапии антидепрессантами в течение минимум 7 дней (3 недель в случае флуоксетина или неселективных ингибиторов моноаминоксидазы). Для участия в исследовании также требовалось, чтобы пациенты вели активную половую жизнь (половые контакты и/или самостимуляция) в течение последних 2-х недель. К критериям исключения относились другие психические расстройства по Оси I, в том числе сопутствующие тревожные расстройства, злоупотребление или зависимость от психоактивных веществ, биполярное расстройство, БДР с психотическими или кататоническими симптомами, послеродовая депрессия, а также беременность, лактация, неадекватная контрацепция, актуальные суицидальные мысли или суицидальные попытки за последние 6 месяцев, неэффективность предыдущей терапии. Исключались пациенты с неврологическими и нестабильными соматическими заболеваниями. Протокол исследования был одобрен этическими комитетами всех центров. Исследование проводилось на базе 43 центров в Канаде, Франции и США. У всех пациентов получено письменное информированное согласие.
Дизайн исследования
В исследовании использовался двойной-макетный дизайн. Пациенты в группе агомелатина получали 2 капсулы плацебо утром и 2 капсулы агомелатина 25 мг вечером. Пациенты в группе венлафаксина получали 2 капсулы плацебо в течение всего исследования и 2 капсулы венлафаксина 37.5 мг capsules утром в течение первых 2-х недель, затем по 2 капсулы 75 мг утром в течение последующих 10 недель исследования. Измерения результирующих показателей проводились до начала терапии, затем через 2, 6, 10 и 12 недель лечения.
Измерения
Изменения половой функции оценивались с помощью 13-пунктовой шкалы Sex FX, которая заполнялась клиницистом. Первые 11 пунктов шкалы образуют 3 категории половых функций - влечение (пункты 1-4), возбуждение (пункты 5-8) и оргазм (пункты 9-11); все эти пункты оцениваются по 5-балльной системе (от 0 до 4 баллов). Сумма баллов по пунктам с 1 по 11 образует суммарный балл шкалы Sex FX. Баллы по категориям влечение и возбуждение также суммируются для общей оценки состояния, предшествующего оргазму. Пункты 12 и 13 оцениваются от 0 до 10 баллов; сумма баллов по этим пунктам обеспечивает оценку общего удовлетворения.
Тяжесть депрессии за весь период терапии оценивалась по шкале MADRS, Шкале общего клинического впечатления-Тяжесть (CGI-S) и шкале CGI-Улучшение. Надежность оценок разный рейтеров по всем клиническим шкалам обеспечивалась до начала исследования. Спонтанно сообщаемые пациентами нежелательные явления регистрировались для оценки безопасности и переносимости.
Статистические анализы
В целях статистических анализов в данном исследовании предусматривались 2 заранее определенные выборки пациентов. Пациенты в ремиссии с охранной половой активностью (SA-R, n = 111: агомелатин, n = 60; венлафаксин, n = 51) - пациенты с половой активностью на старте исследования, достигшие редукции стартового суммарного балла MADRS минимум на 50% на 10-й неделе терапии в сочетании с редукцией суммарного балла MADRS до 12 или меньше на финальном визите исследования. Полная выборка сексуально активных пациентов (SA-FS, n = 193: агомелатин, n = 103; венлафаксин, n = 90) включала всех пациентов с активной половой жизнью на момент начала исследования.
Главным результирующим показателем был процент пациентов в выборке SA-R с ухудшением стартовых баллов по категориям шкалы Sex FX минимум на 1 балл за период между начальным измерением и финальной оценкой по шкале Sex FX. В ходе анализа проводилось сравнение групп по процентным долям пациентов с ухудшением, отсутствием изменений и улучшением стартовых баллов с помощью теста хи-квадрат. Аналогичные анализы проводились в выборке SA-FS.
Различия между агомелатином и венлафаксином XR по эффективности редукции тяжести депрессии оценивались в выборке FAS на основании последних измерений после стартовых оценок с использованием 95% доверительного интервала (CI). Процентные доли респондеров (пациенты с редукцией стартового суммарного балла MADRS минимум на 50%) и пациентов в ремиссии (редукция суммарного балла MADRS до <12) рассчитывались по финальным оценкам. Все статистические анализы проводились в общей выборке терапии (intent-to-treat) методом замещения недостающего значения предыдущим значением.
РЕЗУЛЬТАТЫ
Демографические и клинические характеристики
Группы не различались по стартовым показателям. Средний возраст в выборке (72% женщины) FAS составил 40.9 лет (SD, 10.2 лет). Терапевтические группы не различались по стартовым баллам MADRS (агомелатин = 27.9 [SD, 4.1], венлафаксин XR = 27.9 [SD, 4.5]) и CGI-S (агомелатин = 4.4; венлафаксин XR = 4.5), а также по числу предыдущих аффективных эпизодов (агомелатин = 2.3, венлафаксин XR = 2.4) и длительности текущего эпизода депрессии в месяцах (агомелатин = 3.0 [SD, 1.4], венлафаксин XR = 2.9 [SD, 1.3]).
Связанные с терапией половые дисфункции
В выборке SA-R (n = 111) выявлены достоверные различия между группами: процент пациентов с половыми дисфункциями по суммарным баллам шкалы Sex FX составил 7.3% в группе агомелатина против 15.7% в группе венлафаксина XR. Эти различия были преимущественно обусловлены 5-кратным превышением доли пациентов мужского пола с нарушениями влечения в группе венлафаксина XR, которая составила 19.4% против 3.6% в группе агомелатина (P = 0.007) и таким же повышением частоты нарушений функции оргазма у женщин (агомелатин = 4.3% против венлафаксин XR = 21.2%; P<0.0001).
Кроме того в выборке SA-R установлены достоверные различия по показателям преоргазма и оргазма. Процент пациентов без дисфункции на стадии преоргазма был значительно выше в группе агомелатина в сравнении с венлафаксином XR на уровне статистически достоверных различий между терапевтическими группами (21.2% [SD, 8.6%]; 95% CI, 4.3-38.1; P = 0.015 на момент финальной оценки). Сходным образом доля пациентов с сохранной функцией (отсутствие дисфункции) оргазма при финальной также была достоверно выше в группе агомелатина в сравнении с группой венлафаксина XR (27.1% [SD, 8.7%]; 95% CI, 10.0-44.1; P=0.002).
Суммарные баллы по всей шкале Sex FX и отдельным категориям шкалы Sex FX в выборке SA-R отдельно для мужчин и женщин представлены в Таблице 1. У женщин обнаружены достоверные различия между группами по категории оргазма (агомелатин = 8.2 [SD, 1.5] - 8.5 [SD, 2.3]; венлафаксин XR = 7.8 [SD, 1.4] - 6.6 [SD, 3.5]; P<0.01) в пользу агомелатина. У мужчин также установлено более благоприятное изменение суммарного балла шкалы Sex FX при терапии агомелатином, однако эти различия не были статистически достоверными в связи с малым количеством мужчин в выборке SA-R.
ТАБЛИЦА 1. Баллы шкалы Sex FX у пациентов выборки SA-R.
| Агомелатин (n=46) | Венлафаксин (n=33) | ||||
| Исходно | Неделя 12 | Исходно | Неделя 12 | ||
| A. SA-R, пациенты женского пола | |||||
| Влечение | 4.7 (3.3) | 7.0 (3.4) | 5.0 (3.6) | 7.0 (4.7) | 0.908 |
| Возбуждение | 9.3 (1.5) | 10.0 (2.2) | 9.4 (1.3) | 9.7 (3.4) | 0.543 |
| Оргазм | 8.2 (1.5) | 8.5 (2.3) | 7.8 (1.4) | 6.6 (3.5) | 0.009 |
| Суммарный балл | 22.2 (5.2) | 25.4 (6.3) | 22.2 (4.5) | 23.2 (10.4) | 0.237 |
| Общее удовлетворение | 8.5 (4.7) | 11.5 (5.0) | 9.8 (4.8) | 11.9 (5.2) | 0.804 |
| Агомелатин (n=14) | Венлафаксин (n=18) | ||||
| Исходно | Неделя 12 | Исходно | Неделя 12 | ||
| B. SA-R, пациенты мужского пола | |||||
| Влечение | 6.6 (2.9) | 9.9 (3.4) | 9.7 (4.8) | 10.1 (4.2) | 0.245 |
| Возбуждение | 9.9 (1.6) | 10.6 (2.8) | 11.1 (2.5) | 11.6 (3.1) | 0.995 |
| Оргазм | 8.9 (0.9) | 8.9 (2.8) | 9.7 (1.4) | 8.3 (3.3) | 0.117 |
| Суммарный балл | 25.4 (4.6) | 29.3 (7.2) | 30.4 (7.9) | 29.9 (8.9) | 0.176 |
| Общее удовлетворение | 9.9 (2.9) | 12.7 (2.6) | 9.5 (4.1) | 12.3 (4.8) | 0.875 |
В более крупной выборке SA-FS (n = 193) установлены достоверные различия между группами по процентным долям пациентов с нарушениями влечения (агомелатин = 6%; венлафаксин XR = 16.4%; P < 0.0001), оргазма (агомелатин = 9.1%; венлафаксин XR = 18.5%; P = 0.001), а также по суммарным баллам шкалы Sex FX (агомелатин = 8.2%; венлафаксин XR = 15.2%; P < 0.0001). Различия по этим показателям оставались статистически достоверными и по результатам отдельных анализов у пациентов мужского и женского пола.
Также выявлены достоверные различия между группами по показателю общего удовлетворения. В выборке SA-R снижение общего удовлетворения зафиксировано у 2.5% пациентов группы агомелатина против 11.8% пациентов группы венлафаксина XR (P = 0.006); в выборке SA-FS тот же показатель составил 4.9% в группе агомелатина и 12.8% в группе венлафаксина XR (P = 0.005). Эти различия были преимущественно обусловлены различиями у женщин (SA-R: агомелатин = 2.2%, венлафаксин XR = 15.2%; P = 0.002; SA-FS: агомелатин = 4.1%, венлафаксин XR = 15.3%; P = 0.002).
Исход депрессии
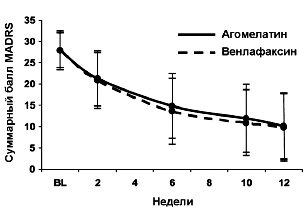
В обеих терапевтических группах зафиксирована достоверная редукция стартовых суммарных баллов MADRS на момент финальной оценки: агомелатин - с 27.9 (SD, 4.1) до 10.1 (SD, 7.8); венлафаксин - с 27.9 (SD, 4.6) до 9.8 (SD, 7.9), при отсутствии достоверных различий между группами (Рисунок 1). Расчетная стандартная ошибка различий между группами составила -0.030 (SE, 0.94) при 95% CI от -2.16 до 1.55. Статистически достоверных различий между группами в динамике стартовых баллов CGI-S или CGI-Улучшение на финальных визитах также не выявлено.
В терапевтических группах установлены одинаковые доли респондеров (агомелатин = 82.5%, венлафаксин XR = 79.9%; E = -2.63% [SE, 4.70]; 95% CI, от -11.84 до 6.59) и пациентов, достигших ремиссии (агомелатин = 73%, венлафаксин XR = 66.9%; E = -6.09 [SE, 5.51]; 95% CI, от -16.88 до 4.71), на момент финальной оценки.
РИСУНОК 1. FAS: Суммарные баллы MADRS (среднее [SD]): сравнение эффектов агомелатина 50 мг (n=137) и венлафаксин XR 150 мг (n=139); метод замещения недостающего значения предыдущим.
Безопасность и переносимость
В группе венлафаксина было примерно в 2 раза больше пациентов со связанными с терапией нежелательными явлениями (38.1%) в сравнении с группой агомелатина (20.4%). Наиболее частыми нежелательными явлениями в группах агомелатина и венлафаксина были тошнота, головная боль и инфекции верхних дыхательных путей (11.7.%/17.3%, 10.2%/7.9%, 7.3%/6.5%, соответственно). Доля пациентов, преждевременно выбывших из исследования в связи со связанными с терапией нежелательными явлениями, составила 2.2% в группе агомелатина (без предпочтительных дисфункций какого либо органа/системы) и 8.6% в группе венлафаксина (преимущественно побочные эффекты со стороны гастроинтестинальной и центральной нервной системы).
ОБСУЖДЕНИЕ
Выполнено первое исследование агомелатина, главной целью которого была оценка половой функции. Главным результирующим показателем исследования было изменение половой функции во время терапии антидепрессантами, что обосновано высокой частотой половых дисфункций и значимым влиянием этого побочного эффекта на приверженность пациентов к терапии и преждевременную отмену препаратов[6]. Дополнительной целью исследования была оценка клинической эффективности и переносимости агомелатина в сравнении с венлафаксином XR.
Связанные с терапией половые дисфункции у пациентов с исходно сохранной половой активностью достоверно реже развивались в случае терапии агомелатином в сравнении с венлафаксином XR. Частота нарушений по 2 из 3 категорий шкалы Sex FX (влечение, оргазм) и неблагоприятных изменений суммарного балла Sex FX была достоверно выше в группе венлафаксина, что установлено как в выборке SA-FS, так и в выборке SA-R. Метод отдельного анализа данных пациентов с сохранной половой активностью, достигших ремиссии, позволил дифференцировать побочные эффекты антидепрессантов в сфере половой функции от половых дисфункций, связанных с депрессией. Различия в показателях общего удовлетворения между терапевтическими группами определялись достоверно более высокой частотой половых дисфункций у женщин в группе венлафаксина.
Столь благоприятный профиль половых побочных эффектов в группе агомелатина можно объяснить механизмом действия этого антидепрессанта, который является агонистом мелатонинергических MT1 и MT2 рецепторов и антагонистом 5-HT2C рецепторов. Получены данные о том, что мелатонинергический агонизм[19] и 5-HT2C антагонизм[20-21] благоприятно влияют на сексуальное поведение. Более того, на клиническом уровне прототипический 5-HT2 антагонист ципрогептадин давно рекомендуется в качестве антидота для коррекции вызванных терапией СИОЗС половых дисфункций[22-23]. Кроме того, нефазодон[24] и миртазапин[25], которые являются антагонистами 5-HT2A и 5-HT2C рецепторов, не оказывают столь выраженного влияния на половую функцию, которое свойственно СИОЗС.
Эффективность агомелатина и венлафаксина XR была эквивалентной по всем предусмотренным показателям антидепрессивного эффекта, включая равные доли респондеров и пациентов в ремиссии в обеих группах. Особенно следует отметить показатели ремиссии (агомелатин = 73%, венлафаксин = 66.9%), по которым венлафаксин, как правило, превосходил СИОЗС в предыдущих исследованиях. 4 Возможно, что столь высокие показатели ремиссии связаны, в том числе, с назначением более высоких доз (150 мг в группе венлафаксина XR и 50 мг в группе агомелатина) и увеличенной продолжительностью терапии (12 недель). Тем не менее, в отсутствие плацебо контроля не представляется возможным подтвердить превосходство каждого из антидепрессантов над плацебо эффектом.
В ряде предыдущих исследований получены данные, соотносящиеся с результатами нашего исследования. В двойном-слепом сравнительном исследовании бупропиона XL и венлафаксина XR, выполненном Thase с соавторами[7], использовался Вопросник по изменениям половой функции[26] для оценки сексуально активных пациентов с депрессией в ходе терапии. В этой работе установлено достоверное превосходство бупропиона XL по всем показателям половой функции через 2 недели у мужчин и через 5 недель у женщин.
В отдельном исследовании с применением шкалы Sex FX для сравнения изменений в половой функции при 8-недельной терапии пароксетином и бупропионом XL установлено достоверное превосходство бупропиона XL у мужчин по всем категориям шкалы и показателю общего удовлетворения, однако у женщин подобные различия не были статистически достоверными[17]. Дополнительные доказательства благоприятного профиля побочных эффектов агомелатина со стороны половой функции получены у здоровых добровольцев, участвовавших в 8-недельном рандомизированном плацебо-контролируемом сравнительном исследовании влияния агомелатина и пароксетина на половую функцию[27].
Несмотря на отчетливые половые дисфункции в этом исследовании следует отметить, что, как и в других исследованиях антидепрессантов, в которых нежелательные явления выявлялись с помощью не направленных вопросов, в данном исследовании не зарегистрировано ни одного нежелательного явления, связанного с терапией. Вероятно половые дисфункции остаются не распознанными не только в стандартных клинических исследованиях, но и в клинической практике, если не прилагаются целенаправленные усилия для их выявления.
Надежность данных нашего исследования подтверждается использованием стандартизованного вопросника для оценки половой функции, сопоставимостью терапевтических групп по стартовым показателям половой функции и отбором пациентов в ремиссии с сохранной половой активностью для главного анализа. Однако следует отметить и ряд ограничений проведенного исследования. Поскольку группы плацебо не предусматривалось, мы не можем подтвердить абсолютную эффективность ни одного из тестированных антидепрессантов; однако, уровни терапевтического эффекта (респондеры) и ремиссии были значительно выше в сравнении с аналогичными показателями для плацебо в других исследованиях. Несмотря на относительно большой объем выборки на момент рандомизации ограничение анализа данными пациентов в ремиссии с сохранной половой активностью привело к уменьшению размера выборки, что могло снизить вероятность достоверных различий по разным показателям. В целом результаты данного исследования подтверждают гипотезу о том, что агомелатин обладает благоприятным профилем половых побочных эффектов при терапии пациентов с БДР и сопоставим по эффективности с венлафаксином XR.
ВЫРАЖЕНИЕ БЛАГОДАРНОСТИ
Авторы выражают благодарность всем исследователям в Канаде, Франции и Великобритании, которые включали пациентов в данное исследование, а также персонально Del Rasmussen за помощь в статистической обработке результатов.
РАЗГЛАШЕНИЕ ИНФОРМАЦИИ ОБ АВТОРАХ
Д-р Kennedy получает финансовую исследовательскую поддержку от Astra-Zeneca, Eli Lilly, GlaxoSmithKline, Janssen Ortho, Lundbeck и Merck Frosst. В настоящее время он выполняет функции консультанта для ANS, Biovail, Boehringer Ingelheim, Eli Lilly, GlaxoSmithKline, Institut de Recherches Internationales Servier, Janssen-Ortho, Lundbeck, Organon, Pfizer и Wyeth. Dr Rasmussen является консультантом Institut de Recherches Internationales Servier.
Список использованной литературы
