Резюме по клиническим испытаниям силденафил таблетки 25 мг, 50 мг и 100 мг
СтатьиРезюме по биофармацевтическим исследованиям и по применяемым аналитическим методам
Исходная информация и обзор
В ходе фармацевтической разработки данного препарата, растворимость изучалась с целью лучшей характеристики действующего вещества и для создания адекватных предпосылок растворения. На основании этих исследований была установлена среда растворения для контроля качества и производственный процесс был масштабирован до производственных серий. Подобным образом был проведен анализ испытуемого препарата и препарата сравнения, а также было выполнено исследование биоэквивалентности для оценки их сравнительной биодоступности и доказательства их биоэквивалентности.1 Этапы решений в плане исследования были составлены таким образом, чтобы лучше понять развитие проекта.
План разработки был основан на руководящих указаниях по биодоступности и биоэквивалентности пероральных дозировочных форм. Дозировка по 100 мг была выбрана для испытания на основании аналитических и фармакокинетических результатов исходя из безопасности. Фармакокинетика силденафила приблизительно дозо - пропрциональна в диапазоне 1,25-200 мг при пероральном применении. При дозах по 100 мг не предвиделись аналитические проблемы, а проблемы переносимости были признаны приемлемыми.
Форма выпука была определена в виде таблеток, покрытых оболочкой. Для достижения заданной цели было проведено рандомизимрованное, открытое, перекрестное исследование в двух фазах с однократными дозами силденафила для сравнения испытуемого состава (Grupo Tecnimende) с препаратом сравнения, натощак.
Сводка результатов отдельных исследований
Фаза фармацевтической разработки этого исследования дала релевантную физикохимическую характеристикудействующего вещества в аспекте растворимости и растворения. В данном документе подчеркнуты релевантные и критические черты отдельгых исследований.
Исследования растворения: биосерии
Таблица 1:
Биосерии, включенные в исследование
| Препарат | № серии | Дозировка | Торговое название | Страна приобретения препарата | Держатель регистрационного удостоверения | Производитель | Срок Годн. |
| Испытуемый | 60663 | 100 мг | Н.п. | Н.п. | Н.п. | West Pharma | 09/2008 |
| Сравнения | 4202505Р | 100 мг | Виагра | Португалия | Pfizer Limited, UK | Pfizer PGM, France | 12/2009 |
Таблица 2:
Условия испытания на растворение при определении профиля растворения
| Среда | 01 Н HCl | Буфер ( рН 4,5 ) | Буфер ( рН 6,8 ) с 0,5 % ДДС-Na |
| Прибор | Прибор 2 ( лопастный ) | Прибор 2 ( лопастный ) | Прибор 2 ( лопастный ) |
| Объём | 900 мл | 900 мл | 900 мл |
| Скорость вращения ( об./мин ) | 75 об./мин | 75 об./мин | 75 об./мин |
| Время отбора проб | 2,5; 5; 7,5; 10; 15 и 30 минут | 2,5; 5; 7,5; 10; 15 и 30 минут | 2,5; 5; 7,5; 10; 15 и 30 минут |
| Температура ( 0С ) | 37,0 ± 0,5 | 37,0 ± 0,5 | 37,0 ± 0,5 |
В соответствии с Европейским руководством, в тех случаях, когда за 15 минут количество перешедшего в раствор действующего вещества было больше чем 85 %, можно было утверждать о подобии без любой другой математической обработки данных, и в других случаях подобие можно было сравнивать спосособом модель-независимой аппроксимации, применяя расчётную Формулу 1
Расчётная формула 1: Расчёт модель незавимого подобия 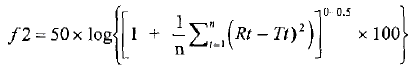
Таблица 3:
Среднее количество ( для 12 единиц ) перешедшего в раствор силденафила ( 100 мг ) в среде растворения: 0,1 Н HCL
| Время ( мин ) | 4202505P (Эталонная Биосерия ) | 60663 ( тест - биосерия) |
| 2,5 | 62,8 | 74,1 |
| 5 | 92,8 | 85,0 |
| 7,5 | 95,3 | 89,5 |
| 10 | 96,3 | 92,6 |
| 15 | 96,7 | 93,9 |
| 30 | 97,3 | 94,1 |
Таблица 4:
Среднее количество ( для 12 единиц ) перешедшего в раствор силденафила ( 100 мг ) в среде растворения: рН 4,5 ( ЕР буфер )
| Время | 4202505P (Эталонная Биосерия ) | 60663 ( тест - биосерия ) |
| 2,5 | 72,7 | 78,5 |
| 5 | 87,7 | 85,8 |
| 7,5 | 88,3 | 86,7 |
| 10 | 89,3 | 87,4 |
| 15 | 89,6 | 88,0 |
| 30 | 91,0 | 89,3 |
Таблица 5:
Среднее количество ( для 12 единиц ) перешедшего в раствор силденафила ( 100 мг ) в среде растворения: рН 6,8
| Время | 4202505P (Эталонная Биосерия ) | 60663 ( тест - биосерия ) |
| 2,5 | 30,2 | 63,2 |
| 5 | 72,9 | 80,2 |
| 7,5 | 76,6 | 82,0 |
| 10 | 77,3 | 83,1 |
| 15 | 78,6 | 83,8 |
| 30 | 82,5 | 85,6 |
В процессе определения профиля растворения в 0,1 Н HCl и ЕР буфере ( рН 4,5 ) более чем 85 % силденафила перешло в раствор в пределах 15 минут. Дальнейшая математическая обработка данных не требовалась. Касательно результатов, полученных в среде растворения с рН 6,8, не растворилось 85 % силденафила в пределах 15 минут. Следовательно, был рассчитан коэффициент подобия при рН 6,8, который составил 42 %.
В качестве среды контроля качества использовали 0,1 Н НCl, при таких же условиях, как это применялось при определении профиля растворения.
Испытание на растворение: разные дозировки в сравнении с тест-биосерией
Таблица 1:
Биосерии, включенные в исследование
| № серии | Дозировка | Торговое название | Страна приобретения препарата | Держатель регистрационного удостоверения | Производитель | Срок Годн. | |
| Испытание | 60663 (биосерия) | 100 мг | Н.п. | Н.п. | Н.п. | West Pharma | 09/2008 |
| 70131 | 25 мг | Н.п. | Н.п. | Н.п. | West Pharma | --- | |
| 70283 | 50 мг | Н.п. | Н.п. | Н.п. | West Pharma | --- |
Таблица 7:
Условия испытания на растворение при определении профиля растворения
| Среда | 01 Н HCl | Буфер ( рН 4,5 ) | Буфер ( рН 6,8 ) с 0,5 % ДДС-Na |
| Прибор | Прибор 2 ( лопастный ) | Прибор 2 ( лопастный ) | Прибор 2 ( лопастный ) |
| Объём | 900 мл | 900 мл | 900 мл |
| Скорость вращения ( об./мин ) | 75 об./мин | 75 об./мин | 75 об./мин |
| Время отбора проб | 2,5; 5; 7,5; 10; 15 и 30 минут | 2,5; 5; 7,5; 10; 15 и 30 минут | 2,5; 5; 7,5; 10; 15 и 30 минут |
| Температура ( 0С ) | 37,0 ± 0,5 | 37,0 ± 0,5 | 37,0 ± 0,5 |
В соответствии с Европейским руководством, в тех случаях, когда за 15 минут количество перешедшего в раствор действующего вещества было больше чем 85 %, можно было утверждать о подобии без любой другой математической обработки данных, и в других случаях подобие можно было сравнивать спосособом модель-независимой аппроксимации, применяя расчётную Формулу 1
Расчётная формула 2: Расчёт модель незавимого подобия 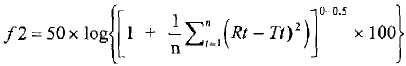
Таблица 8:
Среднее количество ( для 12 единиц ) перешедшего в раствор силденафила ( 100 мг ) в среде растворения: 0,1 Н HCL
| Время | 60663 ( тест - биосерия, 100 мг) | 70131 ( тест - серия, 25 мг) | 70283 (тест серия, 50 мг) |
| 2,5 | 74,1 | 86,7 | 6,7 |
| 5 | 85,0 | 109,0 | 88,3 |
| 7,5 | 89,5 | 104,5 | 103,4 |
| 10 | 92,6 | 104,7 | 108,7 |
| 15 | 93,9 | 104,6 | 109,8 |
| 30 | 94,1 | 104,8 | 109,9 |
Таблица 9:
Среднее количество ( для 12 единиц ) перешедшего в раствор силденафила ( 100 мг ) в среде растворения: рН 4,5 ( ЕР буфер )
| Время | 60663 ( тест - биосерия, 100 мг) | 70131 ( тест - серия, 25 мг) | 70283 ( тест серия, 50 мг) |
| 2,5 | 78,5 | 78,2 | 7,2 |
| 5 | 85,8 | 90,5 | 75,0 |
| 7,5 | 86,7 | 93,2 | 86,5 |
| 10 | 87,4 | 93,9 | 89,3 |
| 15 | 88,0 | 95,6 | 91,1 |
| 30 | 89,3 | 97,6 | 92,8 |
Таблица 10:
Среднее количество ( для 12 единиц ) перешедшего в раствор силденафила ( 100 мг ) в среде растворения: рН 6,8
| Время | 60663 ( тест - биосерия, 100 мг) | 70131 ( тест - серия, 25 мг) | 70283 ( тест серия, 50 мг) |
| 2,5 | 63,2 | 63,3 | 59,5 |
| 5 | 80,2 | 83,0 | 77,0 |
| 7,5 | 82,0 | 85,7 | 81,5 |
| 10 | 83,1 | 86,9 | 82,6 |
| 15 | 83,8 | 88,4 | 84,0 |
| 30 | 85,6 | 92,2 | 86,9 |
Так как больше чем 85 % силденафила перешло в раствор в пределах 15 минут, поэтому профили растворения в 0,1 Н HCl и буфере с рН 4,5 оценивались как подобные без любой дальнейшей математической обработки. Коэффициент подобия был рассчитан в случае растворения в буфере с рН 6,8. Полученные результаты были выше 50 % ( как это видно из таблицы, представленной ниже ).
| f2 | 60663 ( тест - биосерия, 100 мг) | 70131 ( тест - серия, 25 мг ) | 70283 ( тест серия, 50 мг ) |
| 4202505P ( Эталонная биосерия, 100 мг) | 42 | 40 | 45 |
| 60663 ( тест - биосерия, 100 мг) | --- | 69 | 84 |
| 70131 ( тест - серия, 25 мг ) | 69 | --- | 67 |
| 70283 ( тест серия, 50 мг ) | 84 | 67 | --- |
В качестве среды контроля качества использовали 0,1 Н НС1, при таких же условиях, как это применялось при определении профиля растворения.
Испытание на растворение: другие препараты сравнения
Неприменимо.
Пилотные испытания биоэквивалентности
Неприменимо.
Базовое исследование биоэквивалентности
План исследования
Исследование биоэквивалентности предусматривалось провести в условиях натощак, где были получены данные по переносимости и фармацевтические результаты, и затем оценивались взаимодествия с рационом питания - согласно требованиям Европейских директив. Исследование биоэквивалентности проводилось по одноцетровому, рандомизированному, открытому, перекрестному плану в двух периодах с однократными дозами, с целью сравнения скорости и степени всасывания испытуемого силденафила и препарата Виагра -препарата сравнения, содержащего силденафил, в условиях их приема натощак. Субъекты на время клинических процедур были госпитализированы в Anapharm Clinical Research Facility. Клинический надзор выполнили квалифицированные исследователи: Benoit J. Deschamps, M.D. и Denis Audet, M.D. Применяемые дозы по 100 мг давались в виде однократных доз в каждом преиоде исследования с 7 дневными и большими периодами вымывания между дозами.
Протокол клинического исследования (от 11 -го октября 2006 г. ) был безоговорочно утвержден этическим коммитетом 18-го октября 2006 г. Письмо о невозражении от ведомства Канады поступило 23-го октября 2006 г (за номером 109289).
Все клинические процедуры были выполнены в соответсвии с НКП/GCP согласно рекомендациям в Директивах ICH ( ICH Е6 ), местному нормативно-правовому регулированию и принципам, сформулированным в Хельсинкской декларации.
Плазменные концентрации силденафила определяли в каждом случае после отбора проб у каждого субъекта и средние плазменные уровни, были построены средние плазменные уровни за весь период отбора проб и представлены в нетрансформированном и ln-трансформированном виде. Фармакокинетическими параметрами в исследовании были: AUC0-t, AUC0-?, Смакс, Остаточная площадь, Тмакс, Кэл и Т1/2эл. Для получения этих параметров образцы крови отбирались перед приемом, затем после приема за 0,167, 0,333, 0,500, 0,750, 1,00, 1,25, 1,50, 1,75, 2,00, 2,33, 2,67, 3,00, 3,50, 4,00, 6,00, 8,00, 10,0, 12,0, 16,0, и 18,0 часов в каждом периоде.
Биоанализы были выполнены на Anapharm Europe ( Испания ), а статистическая обработка и анализ на Anapharm ( Канада ).
План исследования был адекватным для определения фармакокинетических параметров испытуемого состава и состава сравнения. Период вымывания продолжался не менее 7 дней и был признан достаточным для полной элиминации препарата до начала 2-го периода и чтобы исключить любую накладку эффектов.
Средняя остаточная площадь была менее 20 % во всех лечениях, указывая на то, что отбор проб в течение вплоть до 18 часов был достаточным.
Не была установлена статистически значимая разница между лечениями с помощью ANOVA в ln-трансформированных параметрах AUC0-t, AUC0-?, Смакс и в нетрансформированных параметрах Кэл и Т1/2эл. Не была установлена статистически значимая разница между лечениями с помощью теста Уилкоксона в параметрах Тмакс.
Испытуемый препарат и препарат сравнения
Испытуемый препарат
Действующее вещество: Силденафил; № серии:60663; Срок хранения:28/09/2008; дозы по 100 мг; Торговое название: неприменимо, Владелец лицензии на маркетинг:неприменимо; Производитель: West Pharma, Португалия.
Препарат сравнения
Действующее вещество: Силденафил; № серии: 4202505Р; Срок хранения:12/2009; Дозы: по 100 мг; Тарговое название: Вмагра; Владелец разрешения на маркетинг: Pfizer Ltd, СК; Производитель: Pfizer PGM, Франция.
Изучаемая популяция
Субъекты должны были быть здоровыми мужчинами в возрасте ? 18 ? 55 лет; с индексом массы тела ? 20,0 и < 25 кг/м2. Все субъекты должны были отвечать требованиям включения - исключения, изложенным в протоколе и признанными достаточным для включения субъектов в исследование на основании истории болезни, демографических данным (в том числе: пол, возраст, раса, масса тела(кг), рост ( см ) и ИМТ (кг/м2), измерении жизненно важных функций, 12 канального ЭКГ, физического обследования анализа мочи на наркотики, и анализов лабораторных анализов ( гаматология, биохимия, анализ мочи, СПИД, антитела гептита С, поверхностный антиген гепатита В ). Все 28 субъектов принимали не менее одну дозу исследуемого препарата и, таким образом была составлена популяция по безопаности. Все 26 субъектов, закончивших оба периода лечения были включены в фармакокинетические анализы.
Аналитические методы
Анализ силденафила был выполнен в аналитическом отделе на SFBC Anapharm Europe, S.L.. Аналитические методы были разработаны и валидированы на Anapharm Inc. и были в частности валидированы на SFBC Anapharm Europe, S.L.. Был применен аналитический метод SOP ANE 5103/01 под названием: «Определение силденафила в плазме человека с ЭДТА в диапазоне концентрации 2-500 нг/мл методом ЖХ/МС/МС». Метод включил твердофазную экстракцию на пластинках Oasis MCX. Силденафил и внутренний стандарт измерялся с высокоэффективной жидкостной хроматографией с обратной фазой и тандемной масс-спектрометрией (ЖХ/МС/МС).
Биоанализы выполнялись на SFBC Anapharm Europe, S.L.( Испания ).
Силденафил и исходный раствор внутреннего стандарта были приготовлены 14 ноября 2006 г. Все растворы хранились при номинальной температуре -20Со .
Максимальное время хранения исходных растовров силденафила от даты приготовленя (14 ноября 2006г) до даты приготовления калибровочных стандартов и образцов для контроля качества 29 ноября 2006г) составило 15 дней. Стабильность силденафила в метаноле при номинальной температуре -20Со была определена в 64 дней. Результаты по стабильности представлены в отчете по валидации.
Максимальное время хранения исходных растовров внутреннего стандарта от даты приготовленя 14 ноября 2006г до анализа последнего образца (14 декабр я 2006г) составило 30 дней. Внутренний стандарт стабилен в метаноле при номинальной температуре - 20Со в течение 64 дней. Результаты по стабильности представлены в отчете о валидации.
Фармакокинетические переменные
Анализ ANOVA был выполнен на ln-трансформированных AUC0-t, AUC0-?, Смакс и нетрансформированных параметрах Кэл и T 1/2эл. Непараметрический тест ( критерий знаков Уилкоксона) был выполнен для сравнения Тмакс между лечениями. Отношение средних наименьших квадратов и 90 % геометрические доверительные интервалы были рассчитаны по ln-трансформированных AUC0-t, AUC0-?, Смакс, (см. более подробно в разделе 11.4.1.). Меду и внутрисубъектные СО были также рассчитаны. Биоэквивалентность должна была быть установлена при 90% геометрическом доверительном интервале отношения (Ф/В) средних наименьших квадратов ln-трансформированных AUC0-t, и Смакс, были в пределах принятия 80 %-125 %.
Статистические методы
Демографические парамтеры были суммированы в письменном виде. Исходные характеристики субъектов были представлены для оценки того, сбалансированы ли они после рандомизации, но конкретные статистические тесты не были выполнены.
Фармацевтические параметры были суммированы по ходу лечения. Плазменные концентрации были суммированы по ходу лечения и в моментах отбора проб. Графически были изображены индивидуальные и средние плазменные концентрации по сравнению с профилем времени.
Не был выполнен статистический анализ данных по безопасности. Эти данные оценвались всего лишь в письменном виде.
Результаты
План исследования был адекватным для определения фармакокинетических параметров испытуемого препарата и прпарата сравнения.
Средняя остаточная площадь была меньше 20 % по всем лечениям, указывая на то, что отбор проб в течение 18 часов был достаточным.
В ходе этого исследования не были отмечены тяжелые или значимые неблагоприятные явления. После приема доз было отмечено всего 40 неблагоприятных явлений 16 из 28 субъектов, получивших не менее одной дозы испытуемого препарата (безопасность популяции). Срывы в группах лечения были следующими: 23 неблагоприятных явлений были отмечены 40,7 % (n=11) из 27 субъектов, получивших лечение А и 17 неблагопрятных явлений были отмечены 40,7 % (n=11) из 27 субъектов, получивших лечение В.
Сравнение и анализ результатов исследований
Биовейвер
Сравнение 100 мг таблеток выпуска Grupo Tecnimende и 100 мг таблеток препарата сравнения ( с рынка Португалии ) показало, что оба показывают подобные профили раствоерния в среде растворения 0,1Н HCl и с рН 4,5. При значении рН 6,8 f2 был рассчитан и составил 42 %.
In vitro результаты оказались в соответсвии с результатами in vivo в исследованиях биоэквивалентности за вычетом рН 6,8, где коэффициент подобия составил 42 %. Это не означает, что проблемы по in vivo результатам преобладают над резульаьами in vitro. Кроме того, применяемая среда в контроле качества была 0,1 H HCl, при подобных условиях как представлены при установлении профиля растворения.
В условиях in vivo исследования испытуемый препарат и препарат сравнивания были биоэквивалентны
Было проведено сравнение между дозировками испытуемого препарата. Фармацевтические препараты были произведены тем же производителем и процессом; силденафил проявил линейные свойства в пределах терапевтических доз; качественный состав различных дозировок является одинаковым, также как отношение между количеством действующего вещества и вспомогательных веществ и профили растврения одинаковы при идентичных условиях в случае других дозировок и серии дозировок, использованных в исследовании биоэквивалентности.
Программа исследованиий, проведенная с испытуемым препаратом производства Grupo Tecnimende 100 мг показала, что он является биоэквивалентным с препаратом сравнения 100 мг, приоретенного на рынке Португалии. Эти результаты могут быть распространены на препараты 25 мг и 50 мг дозировки.
Обобщение выводов
На основании вышепредставленных результатов, можно сделать вывод, что испытуемый силденафила цитрат ( Лечение А ) является биоэквивалентным с препаратом сравнения Виагра ( лечение В ) после введения доз по 100 мг в условиях приема натощак. Оба состава были хорошо переносимыми без тяжелых побочных эффектов и не наблюдались релевантные различия в профилях безопасности между препаратами, особенно с учетом числа и качества побочных явлений.
Препарат производства Grupo Tecnimed можно считать по существу подобным препарату сравнения. Данные, полученные in vivo с составом по 100 мг можно распротранить на дозировки по 25 мг и 50 мг.
Испытуемый препарат производства Grupo Tecnimede можно считать существенно подобным препарату сравнения в дозировках по 25, 50 и 100 мг.
Приложение
Таблица 12:
Сводка по исследованиям биодоступности
| № Иссл | Цель исследования | План исследования | Режим дозировки (Доза, дозировка. формы, путь введения) [Product ID] | Субъекты |
| 60522 | Исследование биоэквивалентности | Одноцентровое,открытое, рандомизированное, перекрестное исследование биоэквивалентности с однократными дозами в 2 периодах лечения натощак. Субъекты были госпитализированы на Ana-pharm Clinical Research Facility не менее за 10 часов до приема доз до приблизительно 24 после приема в периоде отбора проб в каждом периоде. Между фазами лечения был предусмотрен 7 дневный период вымы-вания. | Испытуемый препарат Действующее вещество: силденафил; № серии: 60663; Срок хранения: 28/09/2008г; Доза: 100 мг; Торговое название: неприменимо. Владелец лицензии на маркетинг: неприменимо; Производитель: West Pharma, Португалия. Препарат сравнения | 28 мужчин. Средний возраст: ± СО: 33 ± 11; Планировалось включить: 28; Включено: 26; Прекратил: 1; Исключен: 1; Прошли фармакинетический анализ: 26; Прошли онализ безопасности:28; |
Таблица 13:
Сводка исследований растворения in vitro
| № Исследования | Цель исследования | Product ID/№ серии | Лекарственная форма | Место отчета в досье |
| Растворение биосерий | Испытуемый препарат Действующее вещество: силденафил; № серии: 60663; Срок хранения: 28/09/2008г; Доза: 100 мг; Торговое название: неприменимо, Владелец лицензии на маркетинг: неприменимо; Производитель: Weast Pharma, Португалия. Препарат сравнения | Таблетки покрытые оболочкой | Модуль 5 |
Таблица 13:
Сводка исследований растворения in vitro ( продолжение )
| Среда |
Результаты растворения | Место отчета в досье | ||
|
HCl 0,1 Н | Время ( мин ) | 4202505P (Эталонная Биосерия ) | 60663 ( тест - биосерия) |
Модуль 5 |
| 2,5 | 62,8 | 74,1 | ||
| 5 | 92,8 | 85,0 | ||
| 7,5 | 95,3 | 89,5 | ||
| 10 | 96,3 | 92,6 | ||
| 15 | 96,7 | 93,9 | ||
| 30 | 97,3 | 94,1 | ||
|
рН 4,5 | 2,5 | 72,7 | 78,5 | |
| 5 | 87,7 | 85,8 | ||
| 7,5 | 88,3 | 86,7 | ||
| 10 | 89,3 | 87,4 | ||
| 15 | 89,6 | 88,0 | ||
| 30 | 91,0 | 89,3 | ||
|
рН 6,8 | 2,5 | 30,2 | 63,2 |
Модуль 5 |
| 5 | 72,9 | 80,2 | ||
| 7,5 | 76,6 | 82,0 | ||
| 10 | 77,3 | 83,1 | ||
| 15 | 78,6 | 83,8 | ||
| 30 | 82,5 | 85,6 | ||
| № Исследования | Цель исследования | Product ID/№ серии | Лекарственная форма | Место отчета в досье |
| Растворение других дозировок испытцемого препарата | Действующее вещество: силденафил; № серии: 60663; Срок хранения: 28/09/2008г; Доза: 100 мг; Торговое название: неприменимо, Владелец лицензии на маркетинг: неприменимо; Производитель: Weast Pharma, Португалия Действующее вещество: силденафил; № серии: 70131; Срок хранения: 28/09/2008г; Доза: 25 мг; Торговое название: неприменимо, Владелец лицензии на маркетинг: неприменимо; Производитель: Weast Pharma, Португалия Действующее вещество: силденафил; № серии: 70283; Срок хранения: 28/09/2008г; Доза: 50 мг; Торговое название: неприменимо, Владелец лицензии на маркетинг: неприменимо; Производитель: Weast Pharma, Португалия | Таблетки покрытые оболочкой | Модуль 5 |
| Среда | Результаты растворения | Место отчета в досье | |||
HCl 0,1 Н | Время | 60663 ( тест - биосерия, 100 мг) | 70131 ( тест - серия, 25 мг) | 70283 (тест серия,50 мг) | Модуль 5 |
| 2,5 | 74,1 | 86,7 | 6,7 | ||
| 5 | 85,0 | 109,0 | 88,3 | ||
| 7,5 | 89,5 | 104,5 | 103,4 | ||
| 10 | 92,6 | 104,7 | 108,7 | ||
| 15 | 93,9 | 104,6 | 109,8 | ||
| 30 | 94,1 | 104,8 | 109,9 | ||
рН 4,5 | 2,5 | 78,5 | 78,2 | 7,2 | |
| 5 | 85,8 | 90,5 | 75,0 | ||
| 7,5 | 86,7 | 93,2 | 86,5 | ||
| 10 | 87,4 | 93,9 | 89,3 | ||
| 15 | 88,0 | 95,6 | 91,1 | ||
| 30 | 89,3 | 97,6 | 92,8 | ||
| Среда | Результаты растворения | Место отчета в досье | |||
рН 6,8 | Время | 60663 ( тест - биосерия, 100 мг) | 70131 ( тест - серия, 25 мг) | 70283 ( тест серия, 50 мг | Модуль 5 |
| 2,5 | 63,2 | 63,3 | 59,5 | ||
| 5 | 80,2 | 83,0 | 77,0 | ||
| 7,5 | 82,0 | 85,7 | 81,5 | ||
| 10 | 83,1 | 86,9 | 82,6 | ||
| 15 | 83,8 | 88,4 | 84,0 | ||
| 30 | 85,6 | 92,2 | 86,9 | ||
ЛИТЕРАТУРНЫЕ ССЫЛКИ
1. Руководящие указания по биодоступности и биоэквивалентности. CPMP/EWP/QWP/1404/98, EMEA г.Лондон, 26 июля 2007г. ( Note for guidance on Bioavailabilitz and Bioequivalence CPMP/EWP/QWP/1404/98, EMEA. London. 26 July 2007 )
2. Nochols, D.J.; Mulrhead, G.J.; Harness, J.A. Фармакокинетика силденафила цитрата после приема однократных пероральных доз у здоровых мужчин; влияние приема пищи и дозо-пропорциональность ( Pharmacokinetics of sildenafil citrate after single oral doses in healthy male subjects; absolute bioavailability. Food effects and dose proportionality. 2002; J. Clin. Pharmacol, 53, 55-12S.
Комментарии
ПРАКТИКА ПЕДИАТРА
