Опыт применения неомыляемых соединений авокадо и бобов сои (Пиаскледин) в лечении остеоартроза различной локализации
Статьи Опубликовано в журнале:
« РМЖ РЕВМАТОЛОГИЯ » № 6, 2014г. Профессор Н.В. Чичасова1, профессор Л.И. Алексеева2, профессор В.В. Бадокин3, профессор Н.А. Шостак4
1 ГБОУ ВПО «Первый МГМУ имени И.М. Сеченова» Минздрава России
2 ФГБУ «НИИ ревматологии им. В.А. Насоновой» РАМН, Москва
3 ГБОУ ДПО РМАПО Минздрава России
4 ГБОУ ВПО «РНИМУ им. Н.И. Пирогова» Минздрава России
Мышечно-скелетные заболевания чрезвычайно распространены в популяции, поражают все возрастные группы, как правило, уменьшают функциональную способность больных вплоть до инвалидности, что приводит к экономическим нагрузкам и для самого больного, и для общества [1, 2]. Социально-экономический ущерб вследствие мышечно-скелетных заболеваний велик – в основном за счет болей в нижней части спины, остеоартроза (ОА) и ревматоидного артрита [2]. Боль является основным симптомом всех заболеваний суставов [3], при ОА именно боль определяет нетрудоспособность и ухудшение качества жизни [4]. В среднем распространенность клинически манифестного ОА в большинстве стран составляет около 10–12%. С возрастом нарастает частота обращения в связи с болью при ОА крупных суставов (до 25% и более) [5, 6].
Многие годы считалось, что ОА является следствием возрастного «изнашивания» хряща. Однако в настоящее время не вызывает сомнения, что ОА – заболевание со сложным патогенезом (рис. 1), так что изучение его звеньев до сих пор является актуальным. Данная патология рассматривается как гетерогенная группа заболеваний суставов, патоморфологически характеризующихся фокальным разрушением суставного хряща, изменениями в субхондральной кости (включая микропереломы и образование кист) и образованием остеофитов, а также сопутствующим поражением других компонентов сустава (синовиальная оболочка, связки, капсула и периартикулярные мышцы).

Рис. 1. Патофизиологическая диаграмма ОА
Рентгенологически ОА характеризуется сужением суставной щели, остеофитозом, субхондральным склерозом, образованием кист и неровными костными контурами.
Основные звенья патогенеза ОА – дегенеративные процессы в хрящевой ткани, развитие воспаления в синовиальной оболочке и патологические процессы в субхондральной кости. Нормальный метаболизм хрящевой ткани изменяется с превалированием катаболических процессов над анаболическими [7]. При ОА синтез хондроцитами гликозаминогликанов (ГАГ) снижается (табл. 1) [8].
Таблица 1.
Синтетическая активность хондроцитов при различной тяжести ОА и у здоровых людей [8]
| Ткань | Головка бедра | Кондиллус бедра | ||
|---|---|---|---|---|
| Число больных | Синтез ГАГ (М±) | Число больных | Синтез ГАГ (М±) | |
| Без ОА | 185 | 3,63±0,30 | 15 | 6,02±0,41 |
| ОА легкий | 101 | 2,45±0,15 | 12 | 3,76±0,16 |
| ОА умеренный | 74 | 2,01±0,14 | 15 | 2,39±0,14 |
| ОА тяжелый | 66 | 1,31±0,14 | 5 | 1,95±0,1 |
| Весь ОА | 486 | 1,88±0,38 | 60 | 3,73±0,36 |
Снижается синтез коллагена II типа с повышением синтеза коллагена I, III, X типов. Активация хондроцитов приводит не только к ухудшению синтеза полноценных компонентов матрикса хряща, но и к повышенной экспрессии провоспалительных цитокинов (интерлейкина (ИЛ)-1, ИЛ-6, фактора некроза опухоли-α), циклооксигеназы 2-го типа (ЦОГ-2), оксида азота [9].
Важная роль в деградации хряща принадлежит матриксным металлопротеиназам (ММП) [10], основными мишенями которых становятся структурные компоненты экстрацеллюлярного матрикса (протеогликаны и коллаген 2-го типа). Кроме того, коллагенолитические ММП влияют и на функциональную активность клеток субхондральной кости, усугубляя остеокластическую резорбцию [11].
Возможность использовать растительные соединения при ОА представляет большой интерес. Известно, что бромелайн – экстракт ананаса обладает противовоспалительным и анальгетическим действием при ОА [12], вытяжка из куркумы – противовоспалительной активностью [13]. Масло авокадо и сои содержит биологически активные компоненты – неомыляемые липиды (фитостерол, β-ситостерол, кампестерол и стигмастерол) [14]. Фитостерол ингибирует абсорбцию холестерола и препятствует его эндогенному биосинтезу [15]. Также было показано, что фитостерол и частично β-си-тостерол являются противовоспалительными агентами с антиоксидантной и анальгетической активностью [16–18]. Стироловые экстракты из различных растений в экспериментах на животных показали противовоспалительное действие [19, 20].
Неомыляемые соединения авокадо и сои (Пиаскледин) продемонстрировали разнообразное влияние на патологические значимые активные соединения, участвующие в деградации хряща. В культуре хондроцитов, полученных при экспериментально вызванном ОА, было показано их ингибирующее влияние на стромелизин, что приводило к увеличению синтеза аггреканов [21].
In vitro отмечалось уменьшение активности ММП, индуцируемое ИЛ–1, синтеза оксида азота и эйкозаноидов (агентов, участвующих в деградации хряща и формировании воспаления) [22], кроме подавления активности ММП-2 и ММП-3, более высокая концентрация неомы-ляемых соединений авокадо и сои вызывала нарастание эндогенного тканевого ингибитора металлопротеиназ [21]. При тестировании неомыляемых соединений авокадо и сои на суставном хряще было показано, что комбинация этих соединений в отношении 1:2 более эффективна, чем неомыляемые фракции авокадо или сои, используемые по отдельности или в других соотношениях [23]. Такая комбинация вызывала достоверное снижение активности стромелизина, экспрессии ИЛ-6 и ИЛ-8 и активности коллагеназы. В данном исследовании уровень простагландина (Pg) Е2 снижался при любой концентрации соединений, а в исследовании L. Lipi-ello et al. [24] подавление повышенного уровня Pg Е2 после экспозиции клеток с ИЛ-1 на 45–54% происходило при использовании неомыляемых соединений авокадо и сои именно в дозе, используемой в коммерческом препарате, но не меньше, что было подтверждено и в других исследованиях [25, 26]. При использовании культуры макрофагов также было показано уменьшение концентрации Pg Е2 при добавлении фитостерола [27]. Ан-тикатаболическое действие неомыляемых соединений авокадо и сои приводило к стимуляции продукции коллагена и протеогликана – предположительно за счет увеличения синтеза трансформирующего фактора роста β [28], а также ингибитора активатора плазминогена-1 [29], который принимает участие в повреждении хряща как вследствие прямого воздействия (путем деградации протеогликанов), так и опосредованно – через стимуляцию металлопротеиназ.
Хотя стеролы составляют наибольшую фракцию неомыляемых соединений авокадо и сои, другие компоненты этого соединения, включая α- и β-амирин, также могут осуществлять противовоспалительное и, возможно, анаболическое действие [19, 30].
При ОА наиболее часто поражаются «нагрузочные» суставы: коленные, тазобедренные и суставы позвоночника. Поражение мелких суставов кистей, дистальных и проксимальных, реже привлекает внимание исследователей. Однако эта локализация поражения, кроме косметического дефекта, приводит к формированию хронической боли и явной функциональной недостаточности кисти, ограничивая пациента в выполнении простейших бытовых функций.
Известно, что большинство препаратов, используемых в лечении, обладают «симптом-модифицирующим» действием, уменьшая боль. Такими препаратами являются и широко используемые нестероидные противовоспалительные препараты (НПВП), и анальгетики (парацетамол), и так называемые медленно действующие симптоматические средства (symptomatic slow acting drugs for osteoarthritis (SYSADOA)).
Для SYSADOA в ряде рандомизированных контролируемых исследований (РКИ) показана возможность замедлять прогрессирование заболевания (хондропро-тективное действие), т. е. структурно-модифицирующее действие. Однако основная цель лечения ОА (купирование боли) особенно отражена в рекомендациях Американского колледжа ревматологов (АКР), которые предлагают использование фармакологических препаратов только с целью уменьшения боли (табл. 2) [31]. Европейские рекомендации по ведению больных с гонартрозом [6] отмечают симптом-модифицирующий эффект SYSADOA и наличие у препаратов этой группы структурно-модифицирующего действия (табл. 3), а в рекомендациях EULAR по ведению больных с коксартрозом [32] отмечено, что SYSADOA имеют симптоматический эффект и низкую токсичность, но структурно-модифицирующий эффект достоверно не установлен.
Таблица 2.
Рекомендации АКР 2000: фармакологическое лечение ОА
Таблетированные препараты:
|
Внутрисуставное введение:
|
Локальные средства:
|
Возможности Пиаскледина, применяемого для лечения ОА всех основных локализаций, являются предметом обсуждения в данном сообщении. Пиаскледин представляет собой неомыляемые соединения масла авокадо и соевых бобов, получаемые в результате гидролиза, в пропорции 1:2 (Пиаскледин, A1S2, Laboratoi-res Expanscience, Courbevoie, France). Препарат принимается в дозе 300 мг 1 р./сут. Симптом-модифицирую-щий эффект Пиаскледина при ОА коленных и тазобедренных суставов изучен в ряде РКИ [33–36]. В двойном слепом плацебо-контролируемом РКИ [33] оценена потребность в НПВП у 163 больных с умеренными и сильными болями при ОА коленных и тазобедренных суставов, получавших либо 300 мг/сут Пиаскледина, либо плацебо. Потребность в НПВП в течение 3-го мес. лечения была достоверно меньше в группе больных, получавших активный препарат, чем в группе плацебо (43,4 и 69,7% больных соответственно; p Таблица 3.
Рекомендации EULAR 2003 по ведению больных гонартрозом и EULAR 2005 по ведению больных коксартрозом,
основанные на данных доказательности и мнении экспертов
| № | Рекомендации при гонартрозе | Рекомендации при коксартрозе |
|---|---|---|
| 1. | Оптимальное ведение больных с гонартрозом проводится при комбинации нефармакологических и фармакологических методов | Оптимальное ведение больных с гонартрозом проводится при комбинации нефармакологических и фармакологических методов |
| 2. | Лечение ОА коленного сустава проводится с учетом: а) факторов риска гонартроза (ожирение, нежелательные механические факторы, физическая активность); б) общих факторов риска (возраст, коморбидность, сопутствующая терапия); в) выраженности боли и функциональных затруднений; г) симптомов воспаления – например, выпота в полость сустава; д) локализации и выраженности структурных повреждений | Лечение ОА тазобедренного сустава проводится с учетом: а) факторов риск коксартроза (ожирение, нежелательные механические факторы, физическая активность, дисплазия); б) общих факторов риска (возраст, коморбидность, сопутствующая терапия); в) выраженности боли, функциональных затруднений, увечий; г) локализации и выраженности структурных повреждений; д) пожеланий и ожиданий больного |
| 3. | Нефармакологическое лечение ОА коленного сустава включает регулярное обучение больного, упражнения, приспособления (палки, костыли, ортезы), снижение веса | Нефармакологическое лечение ОА коленного сустава включает регулярное обучение больного, упражнения, приспособления (палки, костыли, ортезы) и снижение веса при наличии ожирения |
| 4. | Парацетамол – анальгетик первой линии, предпочтение при длительном приеме оральным анальгетикам | С учетом эффективности и безопасности парацетамола (до 4 г/сут) он используется первым, предпочтение при длительном приеме оральным анальгетикам |
| 5. | Локальные аппликации (НПВП, капсацаин) клинически эффективны и безопасны | НПВП в наименьших эффективных дозах используют при недостаточном эффекте парацетамола. У пациентов с риском ЖКТ-осложнений используют неселективные НПВП в комбинации с эффективными гастропротекторами или селективные ЦОГ-2 ингибиторы |
| 6. | НПВП используют при недостаточном эффекте парацетамола. У пациентов с риском ЖКТ-осложнений используют неселективные НПВП в комбинации с эффективными гастропротекторами или селективные ЦОГ-2 ингибиторы | Опиоидные анальгетики с парацетамолом или без используют у пациентов, которым НПВП, включая ЦОГ-2 ингибиторы, противопоказаны, или они не эффективны и/или плохо переносимы |
| 7. | Опиоидные анальгетики с парацетамолом или без используют у пациентов, которым НПВП, включая ЦОГ-2 ингибиторы, противопоказаны, или они не эффективны и/или плохо переносимы | SYSADOA (глюкозамин сульфат, хондроитин сульфат, неомыляемые соединения авокадо и сои, диацереин, гиалуроновая кислота) имеют симптоматический эффект и низкую токсичность, но выраженность эффекта мала, отбор пациентов недостаточно определен, а структурно-модифицирующее действие и фармакоэкономические преимущества не строго доказаны |
| 8. | SYSADOA (глюкозамин сульфат, хондроитин сульфат, неомыляемые соединения авокадо и сои, диацереин, гиалуроновая кислота) имеют симптоматический эффект и могут модифицировать структуру | Внутрисуставные инъекции стероидных препаратов (проводятся под контролем УЗИ или рентгена) показаны при обострении болей, не купируемых применением анальгетиков или НПВП |
| 9. | Внутрисуставные инъекции длительно действующих глюкокортикоидов показаны при обострении болей в колене, сопровождающихся выпотом | Остеотомия и хирургические процедуры не на суставе могут быть проведены молодым пациентам с симптоматическим коксартрозом, особенно при наличии дисплазии или варисной/вальгусной деформации |
| 10. | Эндопротезирование показано больным с доказанным рентгенологически гонартрозом, рефрактерных к лечению боли и функциональной недостаточности | Эндопротезирование показано больным с доказанным рентгенологически коксартрозом, рефрактерных к лечению боли и функциональной недостаточности |
В более длительном (8 мес.) плацебо-контролируемом РКИ [34] оценивалась динамика количественных показателей, отражающих боль при ОА за 6 мес. терапии у 164 больных с гон- и коксартрозом, а также сохранение эффекта в течение 2-х мес. наблюдения после окончания приема препаратов. Достоверное превосходство Пиаскледина по сравнению с плацебо было показано по следующим параметрам: уменьшение боли (оценка по визуально-аналоговой шкале (ВАШ), мм) с р=0,003; уменьшение функционального индекса Лекена с pОтносительно короткое 3-месячное РКИ [35] преследовало цель сравнения с плацебо 2-х дозировок Пиаскледина – 300 и 600 мг/сут у 260 больных с ОА коленных суставов. Было подтверждена эффективность Пиаскледина, значительно превышающая эффективность плацебо. Отмечено, что более 70% больных за 3 мес. приема Пиаскледина уменьшили суточную потребность в НПВП в 2 раза против 36% больных, получавших плацебо. Эффективность обеих дозировок Пиаскледина оказалась равной.
В отечественном открытом исследовании [36], включившем 92 пациентов с ОА коленных, тазобедренных суставов, симптоматический эффект Пиаскледина (n=46) сравнивался с эффектом НПВП (n=46; суточная доза, эквивалентная 100 мг/с диклофенака) за 6-месячный период. Исходно группы больных были сопоставимы по демографическим данным, выраженности боли (не менее 30 мм по ВАШ), функциональному индексу Лекена (5 баллов и более). В группе больных, получавших НПВП, анальгетический эффект проявлялся раньше, через 1 мес. снижение боли в покое и особенно при движении было более выраженным (достоверно отличаясь для последнего показателя, p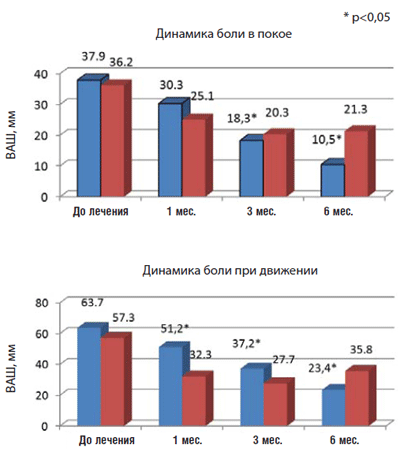

Рис. 2. Динамика боли и индекса Лекена у больных с ОА
коленных и тазобедренных суставов при приеме Пиаскледина и НПВП
Однако после 3-х мес. терапии позитивная динамика боли в группе, принимавшей Пиаскледин, была достоверно более выражена, чем в группе сравнения (pВ большей степени при приеме НПВП уменьшалась интенсивность утренней скованности, хотя и без достоверных отличий от основной группы. По всей вероятности, анальгетический эффект Пиаскледина определяется не только противовоспалительным действием, но и его многогранным влиянием на цитокин-опосредованные патологические эффекты при ОА. Структурно-модифицирующий эффект Пиаскледина был оценен в 2-х многоцентровых плацебо-контролируемых РКИ [37, 38]. Исследование, проведенное M. Lequesne et al. в 2002 г. , включило 163 пациента с одно- или двухсторонним коксартрозом. Стадия по Kell-gren и Lawrence к началу исследования была I–II. Обязательным критерием включения в исследование было регистрируемое рентгенологически сужение щели тазобедренного сустава, все больные отмечали постоянную боль в пораженных суставах продолжительностью не менее 6 мес., индекс Лекена был 4 балла и более. Ран-домизированно пациенты были разделены на 2 группы: 85 больных весь срок исследования получали 300 мг/сут Пиаскледина, а 78 больных получали плацебо. По демографическим и клиническим параметрам группы были сопоставимы. В целом в обеих группах отмечалась сходная динамика изменения суставной щели, но среди больных, имевших ширину суставной щели в начале исследования менее 2 мм, прием Пиаскледина уменьшил отрицательную динамику по сравнению с плацебо практически в 2 раза: при приеме Пиаскледина уменьшение ширины щели в год составило 0,24 мм, и на фоне плацебо – 0,47 мм (pВторое исследование E. Maheu et al., опубликованное в 2013 г., было проведено в течение 3-х лет, включило 399 больных с коксартрозом при наличии клинической симптоматики (постоянная или рецидивирующая боль в течение последнего года и ощущаемая не менее половины времени за последние 3 мес., альгофункциональный индекс Лекена для тазобедренного сустава – от 3 до 10 баллов). В этом исследовании оценка изменения суставной щели в тазобедренном суставе была первичной конечной точкой и проводилась независимым оценщиком (рентгенограммы были «заслеплены») в соответствии с последними рекомендациями по стандартным позициям и методике рентгенологического обследования тазобедренных суставов [39–41]. Включались пациенты с передне-латеральным или передне-медиальным поражением, величина щели должна была варьировать от 1 до 4 мм.
Учитывая, что уже после начала исследования международный консенсуc [42–44] не рекомендовал использовать изменение суставной щели в качестве первичной конечной точки в связи с трудностью трактовки такого изменения (не равномерность и не симметричность изменений), то дополнительно в группах больных, получавших Пиаскледин или плацебо, оценивалось число больных с рентгенологическим прогрессированием. Прогрессирование деструкции регистрировалось, если уменьшение суставной щели было ≥0,5 мм за 3 года. Среди больных, закончивших исследование (по 170 пациентов в каждой группе), уменьшение суставной щели за 3 года составило -0,67 мм в группе плацебо и -0,64 мм в группе больных, получавших активный препарат (разница 0,034 мм; 95%CI -0,156 до 0,225), различия не достоверны (р=0,72) (табл. 4).
Таблица 4.
Результаты анализа изменения суставной щели на рентгенограммах таза или тазобедренных суставов с использованием мануальной радиохондрометрии и числа прогрессирующих за 3 года больных
| Параметр | Плацебо | Пиаскледин | Р | OR/Diff | 95% CI |
|---|---|---|---|---|---|
| Изменение суставной щели (мм) (средняя (SD)) | -0,672 (0,066) | -0,638 (0,070) | 0,723 | 0,034 (0,096) | -0,156 до 0,224 |
| Прогрессирующие больные (%) | 50,3 | 40,4 | 0,040 | 1,63 | 1,023 до 2,543 |
При этом, как видно из данных таблицы 4, достоверно меньше было больных с рентгенологическим прогрессированием сужения суставной щели при лечении Пиаскледином (40,4%), чем в группе плацебо (50,3%) (р=0,040). Интересны данные о возможности Пиаскледина влиять на боль при спондилоартрозе у 30 больных в течение 6 мес. [45]. Для группы больных, получавших Пиаскледин (основные группы), рандомизированно подбиралась равная по численности и основным показателям группа сравнения, получавшая НПВП (нимесулид 200 мг/сут). Оценивались исходно и через 1, 3, 6 мес. уровень болей по ВАШ в покое и при движении в суставах и спине, тест Шобера, функциональный индекс Освестри. Регистрировалась суточная потребность в НПВП. Критериями включения были: уровень боли в спине >40 мм по ВАШ, индекс Лекена >5 баллов.
На фоне применения терапии Пиаскледином у больных с болями в спине (n=15) наблюдалось уменьшение выраженности болевого синдрома, в т. ч. по мере увеличения длительности приема исследуемого препарата (рис. 3). К 3 мес. лечения уменьшение выраженности боли в спине было статистически значимо (р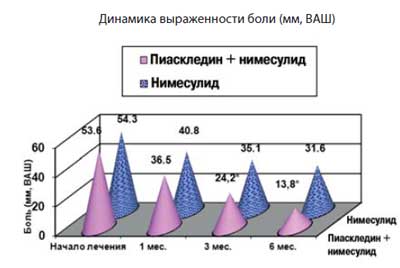
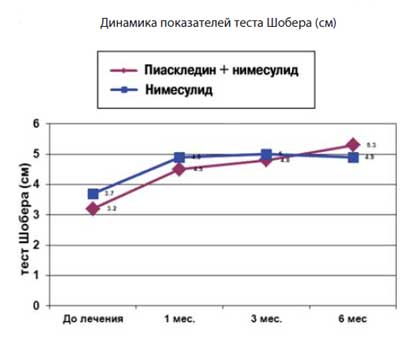

Рис. 3. Пиаскледин в лечении боли в нижней части спины:
динамика боли и функционального состояния
Отмечается значимое улучшение функциональной активности позвоночника к 1-му мес. лечения в обеих группах пациентов, однако в группе комбинированной терапии с применением Пиаскледина сохраняется тенденция к нарастанию функциональной активности по мере увеличения длительности терапии (рис. 3). Показатели, отражающие функциональное состояние пациентов при боли в спине, имеют сходную динамику с показателями интенсивности болевого синдрома в спине по ВАШ.
Повышение двигательной активности больных, отраженное в снижении индекса Освестри, со статистически значимым преобладанием отмечалось в основной группе больных к 3-му мес. лечения (рВ контрольной группе положительная динамика данного показателя имела статистически значимые отличия только к 6-му мес. терапии (рК 3-му мес. лечения интенсивность боли в основной группе уменьшилась в 2,4 раза, а в контрольной – в 1,5 раза. При подсчете числа болезненных узелков в ходе проводимого лечения также отмечалась значительная положительная динамика, при этом в основной группе больных уменьшение числа болезненных суставов было статистически значимым уже в 1-й мес. лечения (рПоскольку оценка влияния Пиаскледина на выраженность симптомов ОА с локализацией в мелких суставах кистей специально не проводилась, было запланировано исследование по оценке эффективности и безопасности Пиаскледина в сравнении с терапией ибупрофеном (ИП) у пациентов с ОА суставов кистей [29]. В исследование были включены 40 амбулаторных пациентов обоего пола ( женщин – 37, мужчин – 3; средний возраст – 65,3±6,9 года) с ОА суставов кистей, удовлетворяющих критериям Althman et al. (1995) с болью в суставах кистей более 40 мм по ВАШ. Все пациенты регулярно принимали НПВП в течение не менее 30 дней за последние 3 мес. 20 больных (основная группа) принимали Пиаскледин 300 мг/сут и ИП 1200 мг/сут, остальные 20 пациентов (группа сравнения) – ИП 1200 мг/сут. Длительность наблюдения составила 4 мес. Далее у части больных терапия Пиаскледином была продолжена в течение еще 8 мес. (всего 12 мес.) для оценки эффективности и безопасности длительного лечения, а также влияния препарата на рентгенологические изменения при ОА суставов кистей.
Оценка эффективности лечения проводилась по следующим критериям:
1) функциональный индекс AUSCAN (боль, скованность, состояние функции суставов);
2) модифицированный функциональный индекс Дрейзера (FIHOA);
3) оценка эффекта от проводимой терапии врачом (лучше, хуже, без изменений);
4) оценка эффекта от проводимой терапии пациентом (лучше, хуже, без изменений);
5) суточная потребность в пероральных НПВП и/или анальгетиках.
Эти параметры анализировались до начала лечения (визит 1) и каждый месяц в последующем. Нежелательные явления и оценка эффективности от проводимой терапии регистрировались на каждом визите.
Достоверные показатели уменьшения боли были зарегистрированы у всех больных через 2 мес. терапии и сохранялись до конца лечебного периода (табл. 5). В конце лечебного периода, т. е. через 4 мес. терапии, улучшение было отмечено у всех больных, получавших Пиаскледин + ИП, по сравнению с 65% в группе, принимавшей только ИП. В конце продленной фазы исследования (через 1 год) 100% больных оценили свое состояние как улучшение. Показатели боли на фоне приема Пиаскледина + ИП были гораздо ниже, чем при приеме только ИП (97,6±63,9 мм против 131,5±89,4 мм соответственно) (рис. 4), но статистически значимых различий выявлено не было, возможно, из-за малочисленности групп. Достоверные показатели уменьшения боли сохранялись у всех больных через 12 мес. терапии.
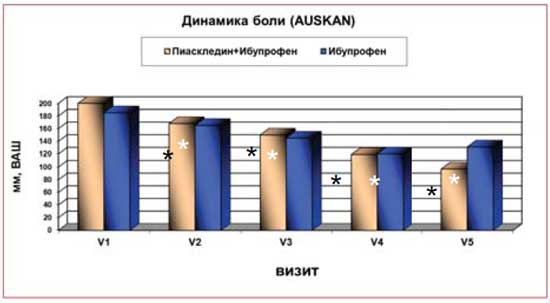
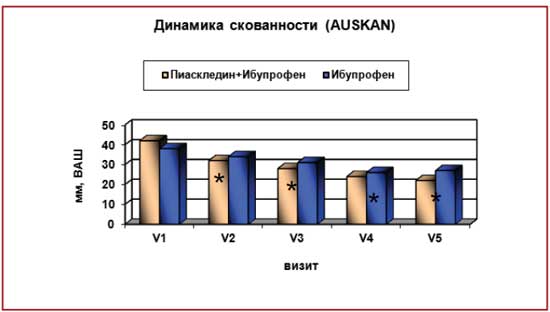
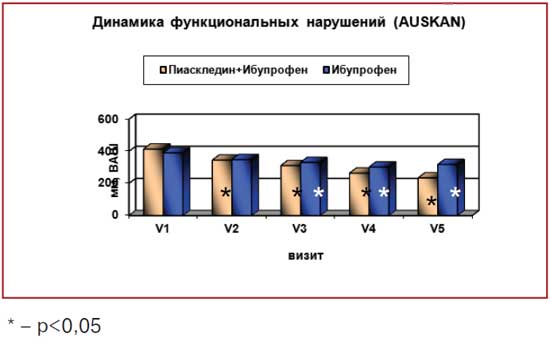
Рис. 4. Пиаскледин в лечении узелкового ОА:
первое полугодие применения Пиаскледина + НПВП или только НПВП
При оценке скованности в мелких суставах достоверные различия с исходным показателем были отмечены при всех визитах только в основной группе. Учитывая, что боль часто сочетается с утренней скованностью и является признаком вторичного синовита, данные результаты подтверждают, что Пиаскледин обладает хорошей противовоспалительной активностью. Анализ состояния функции суставов показал достоверное улучшение показателей в 1-й группе уже через 2 мес. терапии, в то время как во 2-й группе улучшение было отмечено только на 3-м мес. лечения. В конце наблюдения достоверное улучшение функционального состояния суставов отмечено в основной группе (235,5±116,8 мм против 318,3±131,0 мм в группе сравнения; р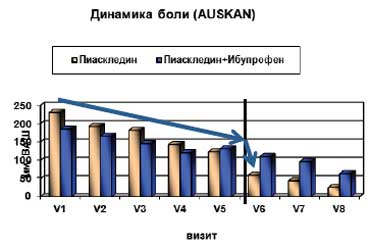

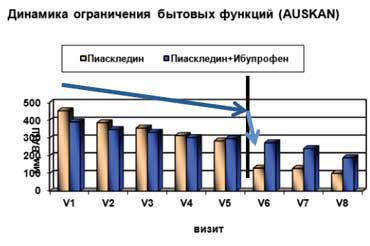
Рис. 5. Пиаскледин в лечении узелкового ОА:
год применения Пиаскледина + НПВП или только НПВП
Таким образом, Пиаскледин продемонстрировал симптом-модифицирующий эффект при лечении ОА любой локализации. Структурно-модифицирующий эффект препарата нуждается в дальнейших исследованиях, которые проводились бы в соответствии с современными требованиями, в первую очередь в отношении методики проведения рентгенологического исследования.
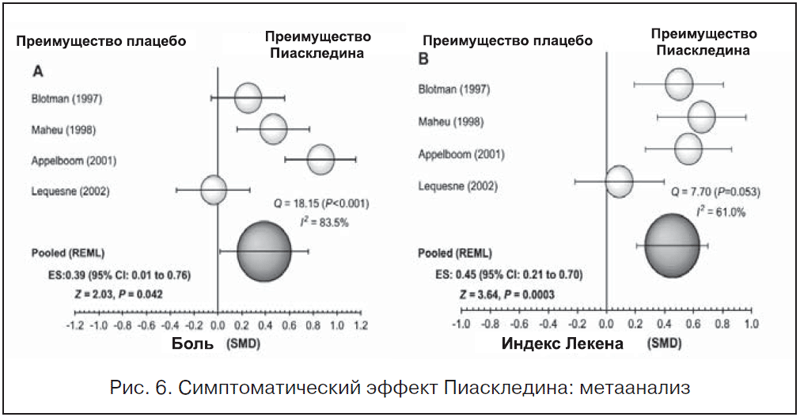
В 2008 г. был проведен метаанализ РКИ Пиаскледина [46]. Из 20 РКИ для анализа были отобраны 4 РКИ [33–35, 37], в которых приняли участие 664 пациента с ОА тазобедренных (41,4%) и коленных суставов (58,6%), из которых 336 больных получали Пиаскледин по 300 мг/сут. и 328 – плацебо в течение 6 мес. Пиаскледин превосходил плацебо по влиянию на боль (среднее уменьшение боли по ВАШ составило 10,7% при гонартрозе и 11,3% при коксартрозе; р=0,04) и на функциональный индекс Лекена (р=0,0003) (рис. 6). В 3-х исследованиях отмечался достоверно больший, чем при применении плацебо, положительный эффект Пиаскледина, только в исследовании M. Lequesne et al. [37] симптоматический эффект Пиаск-ледина не отличался от эффекта плацебо. Напомним, что основным критерием отбора больных в это исследование было значимое уменьшение ширины суставной щели тазобедренного сустава. А поскольку при ОА хорошо известна диссоциация между клиническими и рентгенологическими проявлениями ОА, возможно, группа больных не имела выраженных симптомов ОА. В отечественных исследованиях Пиаскледин продемонстрировал отчетливое и достоверное преимущество перед активными препаратами из группы НПВП в подавлении боли и улучшении функции больных. Отмечено, что сроки лечения должны составлять не менее 6 мес. [29, 36].
Высокая безопасность Пиаскледина отмечена во всех клинических исследованиях, в которых не было зарегистрировано каких-либо значимых побочных эффектов или случаев передозировки препарата при его длительном приеме. Немаловажным аспектом безопасности является отсутствие значимых лекарственных взаимодействий Пиаскледина с известными препаратами. Особенно это важно для пожилых больных ОА, принимающих довольно широкий набор препаратов для лечения сопутствующих заболеваний.
Таким образом, Пиаскледин продемонстрировал достоверный симптоматический эффект при ОА крупных и мелких суставов (включая суставы позвоночника), развивающийся в первые месяцы применения и нарастающий при продолжении лечения до 6–12 мес. Структурно-модифицирующий эффект оценивался только при коксартрозе и показал, что препарат предпочтительнее использовать на ранних рентгенологических стадиях ОА, когда можно добиться замедления прогрессирования, а при длительном использовании Пиаскледина (3 года) прогрессирующее сужение суставной щели отмечается у достоверно меньшего числа больных по сравнению с таковым при приеме плацебо.
Хорошая переносимость и возможность сочетания Пиаскледина с любыми лекарственными средствами позволяют использовать его у больных любого возраста, независимо от наличия коморбидных состояний. Препарат удобен для приема – 1 капсула в день, что, несомненно, увеличивает комплаентность в его применении больными. Литература 1. Woolf A.D., Akesson K. Understanding the burden of musculoskeletal conditions. The burden is huge and not reflected in national health priorities // BMJ. 2001. Vol. 322. Р. 1079–1080.
2. Woolf A.D. Healthcare services for those with musculoskeletal conditions: a rheumatology service. Recommendations of the European Union of Medical Specialists Section of Rheumatology/European Board of Rheumatology 2006 // Ann Rheum Dis. 2007. Vol. 67. Р. 293–301.
3. Kazis L.E., Menan R.F., Anderson J.J. Pain in the rheumatic diseases. Investigation of a key health status component // Arthritis Rheum. 1983. Vol. 26. Р. 1017–1022.
4. Van Baar M.E., Dekker J., Lemmens J.A. et al. Pain and disability in patients with osteoarthritis of hip or knee: the relationship with articular, kinesiological, and psychological characteristics // J Rheumatol. 1998. Vol. 25. Р. 125–133.
5. Peat G., McCarney R., Croft P. Knee pain and osteoarthritis in older adults: a review of community burden and current use of primary health care // Ann Rheum Dis. 2001. Vol. 60. Р. 91–97.
6. Jordan K.M., Arden N.K., Doherty M. et.al. EULAR Recommendations 2003: an evidence based approach to the management of knee osteoarthritis: report of a Task Force of the Standing Committee for Internal Clinical Studies Including Therapeutic Trials (ESCI-SIT) // Ann Rheum Dis. 2003. Vol. 62. Р. 1145–1155.
7. Pelletier J.P., Martel-Pelletier J., Howell D.S., Etiopathogenesis of osteoarthritis In: Koopman WJ., Ed Arthritis and Allied Conditions. A Textbook of Rheumatology 13th edn. Baltimore: Williams & Wilkins 1969/1984/1997.
8. Reginster Ed.J.-E., Pelletier J.-P., Henrotin Y. Osteoarthritis. Clinical and Experimental aspects. Springer, 1999.
9. Насонов Е.Л., Алексеева Л.И. Хондроитин сульфат (Структум) при лечении остеоартроза: патогенетическое обоснование и клиническая эффективность // Тер. архив. 2001. № 11. С. 87–89.
10. Murphy G., Lee M.H. What are the roles of metalloproteinases in cartilage and bone damage? // Ann. Rheum. Dis. 2005. Vol. 64. Р. 44–47.
11. Andersen T.L., del Carmen Ovejero M., Kirkegaard T. et al. A scrutinu of matrix metalloproteinases in osteoclasts: evidence for heterogeneity and for the presence of MMPs synthesized by over cells // Bone. 2004. Vol. 35. Р. 1107–1119.
12. Brien S., Lewith G., Walker A., Hicks S.M., Middleton D. Bromelain as a treatment for osteoarthritis: a review of clinical studies // Evid Based Complement Alternat Med. 2004. Vol. 1. Р. 251–257.
13. Tohda C., Nakayama N., Hatanaka F., Komatsu K. Comparison of anti-inflammatory activities of six Curcuma rhizomes: a possible curcuminoid-independent pathway mediated by Curcuma phaeocaulis extract // Evid Based Complement Alternat Med. 2006. Vol. 3. Р. 255–260.
14. Zorn J. New aspects in rheumatism therapy: experiences with a sitosterin preparation in chronic polyarthritis // Med Welt. 1981. Vol. 32. Р. 135–138.
15. Ling W.H., Jones P.J. Dietary phytosterols: a review of metabolism, benefits and side effects // Life Sci. 1995. Vol. 57. Р. 195–206.
16. Bouic P.J. The role of phitosterols and phitosterolins in immune modulation: a review of the past 10 years // Curr Opin Clin Nutr Metab Care. 2001. Vol. 4. Р. 471–475.
17. De Jong A., Plat J., Mensink R.P. Metabolic effects of plant sterols and stanols (review) // J Nutr Biochem. 2003. Vol. 14. Р. 362–369.
18. Gupta M.B., Nath R., Srivastava N., Shanker K., Kishor K., Bhargava K.P. Anti-inflammatory and antipyretic activities of beta sito-sterol // Planta Med. 1980. Vol. 39. Р. 157–163.
19. Deepak M., Handa S.S. Anti-inflammatory activity and chemical composition of extracts of verbena officinalis // Phytother Res. 2000. Vol. 14. Р. 463–465.
20. Soeken K.L. CAM therapies for arthritis-related pain: the evidence from systemic reviews // Clin J Pain. 2004. Vol. 20. Р. 13–18.
21. Kut-Lasserre C., Miller C.C., Ejei A.L.. et al. Effect of avocado and soybean unsaponifiables on gelatinase A (MMP-2), stromelisin 1 (MMP-3) and tissue inhibitors of matrix metalloproteinase (TIMP-1 and TIMP-2) secretion by human fibroblasts in culture // J Pe-riodontol. 2001. Vol. 72. Р. 1685–1694.
22. Henrotin Y.E., Sanchez C., Deberg M.A., Piccardi N., Guillou G.B., Msika P. et al. Avocado/soybean unsaponifiables increase ag-grecan synthesis and reduce catabolic and proinflammatory mediator production by human osteoarthritis chondrocytes // J Rhematol. 2003. Vol. 30. Р. 1825–1834.
23. Henrotin Y.E., Labasse A.H., Jaspar J.M., De Groote D.D., Zheng S.X., Guillou G.B. et al. Effects of three avocado/soybean unsa-ponifiable mixtures on metalloproteinases, cytokines and PG E2 production by human articular chondrocytes // Clin Rheumatol. 1998.
24. Lippiello L., Nardo J.V., Harlan R. and Chiou T. Metabolic effects of avocado/soy unsaponifiab-les on articular chondrocytes // Alternat Med. 2008. Vol. 5. Р. 191–197.
25. Mauviel A., Daireaux M., Hartmann D.J., Galera P., Loyau G., Pujol J.P. Effects of unsaponifiab-les extracts of avocado/soybeans (PIAS) on the production of collagen by cultures of synoviocytes, articular chondrocytes and skin fibroblasts // Rev Rhum Mal Osteoartic .1989. Vol. 56. Р. 207–211.
26. Werman M.U., Mokady S., Nimni M.E., Neeman I. The effect of various avocado oils on skin collagen metabolism // Connect Tissue Res. 1991. Vol. 26. Р. 1–10.
27. Awad A.B., Toczek J., Fink C.S. Phytosterols decrease prostaglandin release in cultured P388D1/MAB macrophages // Prostaglandons Leukot Essent Fatty Acidis. 2004. Vol. 70. Р. 511–520.
28. Boumediene K., Felisaz N., Bogdanowiez P., Galera P., Guillou G.B., Pujol J.P. Avocado/soya unsaponifiables enhance the expression of transforming growth factor beta 1 and beta 2 in cultured articular chondrocytes // Arthritis Rheum. 1999. Vol. 42. Р. 148–156.
29. Алексеева Л.И., Чичасова Н.В., Кашеварова Н.Г. и др. Применение пиаскледина при ос-теоартрозе суставов кистей // Фарматека. 2010. № 10. С. 48–55.
30. Little C.V., Parsons T. Herbal therapy for treating osteoarthritis // Cochrane Database Syst Rev. 2001. Vol. 1. CD002947.
31. Recommendations for the medical management of osteoarthritis of the hip and knee: 2000 update. American College of Rheumatology / Subcommittee on Osteoarthritis Guidelines // Arthritis Rheum. 2000. Vol. 43. Р. 1905–1915.
32. Zhang W., Doherty M., Arden N. et al. EULAR evidence based recommendations for the management of hip osteoarthritis: report of a Task Force of the Standing Committee for Internal Clinical Studies Including Therapeutic Trials (ESCISIT) // Ann Rheum Dis. 2005. Vol. 64. Р. 669–681.
33. Blotman F., Maheu E., Wulwic A. et al. Efficacy and safety of avocado/soybean unsaponifiables in the treatment osteoarthritis of the knee and hip // Rev Rhum (Engl Ed). 1997.Vol. 64.825–34.
34. Maheu E., Mazieres B., Valat J.-P. et al. Symptomatic efficacy of avocado/soybean unsaponifi-ables in the treatment of osteoarthritis of the knee and hip // Arthritis Rheum. 1998. Vol. 41. Р. 81–91.
35. Appelboom T., Schuermans J., Verbruggen G. et al. Symptoms modifying effect of avocado/soybean unsaponifiables (ASU) in knee osteoarthritis. A double blind, prospective, placebo-controlled study // Scand J Rheumatol. 2001. Vol. 30 (4). Р. 242–247.
36. Бадокин В.В. Пиаскледин – хондропротективный препарат с антицитокиновой активностью // Consilium medicum. 2007. Т. 9. № 8. С. 147–152.
37. Lequesne M., Maheu E., Cadet C. et al. Structural effect of avocado/soybean unsopanifiables on joint space loss in osteoarthritis of hip // Arthritis Care Research. 2002. Vol. 47. Р. 50–58.
38. Maheu E., Cadet C., Marty M., et. al. Randomised, controlled trial of avocado-soybean un-saponifiables (Piaskledine) effect on structure modification in hip osteoarthritis: the ERADIAS study // Ann Rheum Dis. 2013. 0:1–9. doi: 10.1136/annrheumdis-2012-202485.
39. Maheu E., Cadet C., Marty M., et. al. Reproductibility and sensitivity to change of various methods to measure joint space width in osteoarthritis of the hip: a double reading of three different ra-diographic views taken with a three-year interval // Arthritis Res Therapy. 2005. 7: R1375–1385.
40. Conrozier T., Lequesne M.G., Tron A.M., et. al. The effect of position on the radiographic joint space in osteoarthritis of the hip // Osteoarthritis Cartilage. 1997. 5: 17–22.
41. Lequesne M. Quantitative measurement of joint space during progression of osteoarthritis: «Chondrometry». In: Kuettner K, Goldberg V, eds. // Osteoarthritis disorders. Rosemont, IL: American Academy of Orthopaedic Surgeons. 1995: 427–444.
42. Altman R.D., Bloch D.A., Dougados M., et. al. Measurement of structural progression in os-teoarthritis in hip: the Barcelona consensus grouuuup. // Osteoarthritis Cartilage. 2004; 12: 515–524.
43. Abadie E., Ethgen D., Avouac B., et. al. Recommendation for the use of new methods to assess the efficacy of disease-modifying drugs in the treatment of osteoarthritis // Osteoarthritis Catilage. 2004. 12: 263–268.
44. Ornetti P., Brandt K., Hellio Le Graverand M.P., et. al. OARSI-OMERACT definition of relevant radiological progression in hip/knee osteoarthritis // Osteoarthritis Cartilage. 2009. 17: 856–63.
45. Шостак Н.А., Правдюк Н.Г. Дегенеративное поражение позвоночника: представления о болезни, подходы к терапии (собственные данные) // Современная ревматология. 2008. № 3. С. 30–36.
46. Zhang W., Moskowitz R.W., Abramson A. et al. OARSI recommendations for the management of hip and knee osteoarthritis, part I: clinical appraisal of existing treatment guidelines and systematic review of current research evidence // Osteoarthritis Cartilage. 2007. Vol. 15. Р. 981–1000.
