Определение дозы Вальдоксана, мелатонинергического агониста и селективного 5-HT-антагониста, в терапии большого депрессивного расстройства: двойное слепое плацебо-контролируемое исследование с ранжированием доз
СтатьиDetermination of the dose of agomelatine, a melatoninergic agonist and selective 5-HT2c antagonist, in the treatment of major depressive disorder: a placebo-controlled dose range study
H. Lôoa, A. Haleb и H. D'haenenc
aService Hospitalo Universitaire de Sante Mentale et de Therapeutique, Hopital Sainte Anne, Paris, France,
bTrust Headquarters, St Martin's Hospital, Canterbury, Kent, UK,
cAcademisch Ziekenhuis VUB, Bruxelles, Belgium International Clinical Psychopharmacology 2002, 17:239-247
Вальдоксан обладает уникальным и принципиально новым фармакологическим профилем. Он действует как мелатонинергический агонист и селективный антагонист 5-HT2с-рецепторов. Фармакологическая активность Вальдоксана подтверждена на нескольких моделях депрессии у животных. Целью данного исследования было определение активной дозы Вальдоксана в терапии большого депрессивного расстройства (критерии DSM-IV). В исследовании использовался стандартный метод двойной слепой терапии для сравнения трех разных доз Вальдоксана (1, 5 и 25 мг однократно в сутки) с плацебо в течение 8 недель терапии. Пароксетин использовался в качестве валидатора. В исследование было включено 711 пациентов со средним стартовым баллом 17-пунктовой Шкалы депрессии Гамильтона (HAM-D), равным 27,4. По результатам основного анализа финальный средний суммарный балл шкалы HAM-D (Полный комплект анализов LOCF) Вальдоксан 25 мг статистически достоверно превосходил плацебо. Этот вывод был дополнительно подтвержден результатами оценок других показателей эффективности (доли респондеров и пациентов в ремиссии, отдельно в подгруппе больных с тяжелой депрессией, Шкала депрессии Монтгомери-Асберг и Шкала общего клинического впечатления - Тяжесть заболевания). В соответствии с баллами Шкалы тревоги Гамильтона Вальдоксан 25 мг эффективно купировал симптомы тревоги, связанные с депрессией. Пароксетин также был эффективен по результатам основного анализа и оценок большинства дополнительных критериев, использовавшихся для валидизации выборки и методологии исследования. Вальдоксан, независимо от дозы, обнаруживал хорошую переносимость с профилем побочных эффектов, сопоставимым с плацебо. В исследовании показано, что Вальдоксан является эффективным средством терапии большого депрессивного расстройства, а его целевая доза составляет 25 мг.
Ключевые слова: Вальдоксан, депрессия, доза, ремиссия.
ВВЕДЕНИЕ
Появление новых антидепрессантов обеспечило значительный прогресс в области терапии депрессии и в определенной степени способствовало уменьшению стигм, связанных с этим расстройством. Однако терапия назначается лишь небольшой части пациентов и более того, далеко не все из этих пациентов получают лечение антидепрессантами (Kessler et al., 1997; Lepine et al, 1997; Lecrubier, 1998).
Терапия трициклическими антидепрессантами часто затрудняется в связи с выраженными побочными эффектами этих препаратов. Значительный прогресс в этом направлении был достигнут благодаря новым препаратам с улучшенной переносимостью (Montgomery и Kasper, 1995). Однако наиболее широко использующийся в настоящее время класс антидепрессантов, селективные ингибиторы обратного захвата серотонина (СИОЗС), вызывают целый ряд побочных эффектов, которые приводят к нарушению комплаентности к терапии, в связи с чем остаются нерешенными важные проблемы терапии депрессии, требующие дальнейшей разработки новых антидепрессантов (Dunner, 2000).
Новые антидепрессанты получат преимущество, если будут обладать хорошей переносимостью с меньшим уровнем таких побочных эффектов, как половые дисфункции, тошнота, синдром отмены, прибавка в весе и сонливость в дневное время, типичные для различных препаратов класса СИОЗС (Rosenbaum et al, 1998; Dunbar et al, 1991; Montejo et al, 2001). Ожидаемое в связи с улучшением профилей переносимости повышение уровня комплаентности будет играть важную роль для оптимизации терапии депрессии в будущем. Более того, требования к любому новому антидепрессанту включают необходимость благоприятного профиля безопасности, желательно с меньшим риском лекарственных взаимодействий, а также минимальным либо нулевым потенциалом кардиотоксичности при отсутствии признаков антихолинергической и адренергической активности и низкой вероятностью инверсии аффективной фазы с развитием мании.
Однако превосходство над доступными сегодня препаратами по эффективности также остается одной из наиболее важных целей новых антидепрессантов, хотя реализация этой цели, несомненно, является очень трудной задачей. Превосходство в этом аспекте терапии депрессии предусматривает более быстрое начало действия и более высокий терапевтический эффект, как в общей популяции пациентов с депрессией, так и в отдельных подгруппах больных. В любом случае для доказательства таких преимуществ потребуются специально разработанные исследования. Ожидается, что антидепрессанты с более быстрым эффектом позволят значительно облегчить страдания пациентов с депрессией и снизить затраты на лечение благодаря сокращению сроков пребывания больных в стационаре или возможности избежать госпитализации. Также предполагается, что антидепрессанты с более быстрым эффектом будут способствовать улучшению комплаентности пациентов в связи с ощущением незамедлительного улучшения состояния. Повышение эффективности в качестве важного атрибута нового антидепрессанта с улучшенным профилем переносимости может быть доказано более успешными результатами лечения в проблематичных для лечения подгруппах пациентов, включая госпитальных больных с тяжелыми депрессиями. В последнее время публикуется все больше данных, касающихся различий в эффективности современных антидепрессантов. Например, считается, что СИОЗС в целом менее эффективны в терапии тяжелой депрессии. Такая точка зрения подкрепляется результатами серии исследований, в которых СИОЗС достоверно уступали по эффективности в терапии тяжелой депрессии у больных психиатрических стационаров антидепрессантам двойного действия - кломипрамину (DUAG 1986, 1990), венлафаксину (Clerc et al, 1994) и милнаципрану (Clerc et al, 2001).
Вальдоксан является новым перспективным антидепрессантом, эффективность которого подтверждена на нескольких валидизированных моделях депрессии у животных, включая обученную беспомощность (Seligman и Beagly, 1975), тест отчаяния (Porsolt et al, 1977), хронический легкий стресс (Papp et al, 1996) и ольфакторную бульбэктомию (Kelly et al, 1997).
Вальдоксан обладает уникальным фармакологическим профилем, так как является агонистом человеческих клонированных мелатонинергических MT1 и МТ2-рецепторов (1,29 x 10-10М и 2,13 x 10-10М соответственно) (Conway et al, 2000), а также антагонистом человеческих клонированных 5-НТ2С-рецепторов (IC50 = 2,7 x 10-7 М).
В предварительном исследовании (Lôo et al, 2002) в результате сравнения двух доз Вальдоксана (5 мг и 100 мг) у 28 пациентов с большой депрессией по критериям DSM-III-R (American Psychiatric Association, 1987) показано, что применение Вальдоксана в течение 4 недель сопровождается статистически достоверным улучшением показателей Шкалы депрессии Монтгомери-Асберг (MADRS) (Montgomery и Asberg, 1979) и Шкалы депрессии Гамильтона (HAM-D) (Hamilton, 1967) в сочетании с хорошей переносимостью. В соответствии с данными этого исследования доза 5 мг как минимум сопоставима по эффективности, но несколько превосходит по переносимости дозу 100 мг. Однако эффективность антидепрессанта может быть подтверждена только двойными слепыми плацебо-контролируемыми исследованиями. В исследовании, результаты которого приводятся в данной публикации, использовался стандартный метод сравнительной оценки трех разных доз Вальдоксана с плацебо и активным препаратом сравнения пароксетином (CPMP, 1998). Пароксетин, эффективность которого в терапии большого депрессивного эпизода подтверждена специальными исследованиями (Dunbar et al., 1991), использовался для валидизации методологии и чувствительности данного исследования.
МЕТОДЫ
Исследование проводилось как двойное слепое, рандомизированное, мультицентровое, мультинациональное, плацебо-контролируемое с фиксированными дозами Вальдоксана и пароксетина длительностью терапии 8 недель.
Включались пациенты, соответствовавшие диагностическим критериям большого депрессивного расстройства или биполярного расстройства II типа (депрессия) DSM-IV (American Psychiatric Association, 1994), без сезонного характера обострений, с единичным или повторным эпизодом. Для участия в исследовании требовалось, чтобы стартовый суммарный балл 17-пунктовой шкалы HAM-D был не менее 22. Возраст пациентов варьировал от 18 до 65 лет включительно.
Для исключения больных с быстрым плацебо-эффектом предусматривался вводный 1-недельный период приема плацебо; пациенты с редукцией стартового суммарного балла шкалы HAM-D по завершении 1-недельного плацебо-периода на 20% и более не включались в основное исследование. До начала исследования все пациенты подписали информированное согласие, а протокол исследования был одобрен в соответствующих национальных и местных этических комитетах. Исследование проводилось в соответствии с требованиями Качественной клинической практики (Good Clinical Practice), установленными Комиссией европейского сообщества (CPMP, 1991).
В ходе исследования сопутствующая терапия психотропными препаратами запрещалась, за исключением бензодиазепинов в ограниченных дозах. Применения высокопотенциальных бензодиазепинов, таких как альпразолам и триазолам, не допускалось. Также не разрешалось применения препаратов, которые могли бы повлиять на результаты оценок в исследовании вследствие их действия на настроение пациента или циркадианные ритмы; к таким препаратам относились ß-блокаторы, центральные α-блокаторы, нестероидные противовоспалительные средства и экзогенный мелатонин. Пациентам, принимавшим ранее психотропные средства, назначался период отмывки длительностью 1-4 недели в зависимости от периода полувыведения препаратов.
Препарат исследования назначался перорально, по одной капсуле два раза в сутки: одна капсула утром, другая - вечером. После вводного 1-недельного плацебо-периода пациентам методом рандомизации в рамках двойного слепого метода лечения назначалась одна из фиксированных доз Вальдоксана (1, 5 или 25 мг в вечерних капсулах), пароксетин 20 мг (в утренних капсулах) или плацебо.
Оценки и статистический анализ
Измерения по шкалам HAM-D и CGI проводились на стартовом визите, затем на неделях 1, 2, 4, 6 и 8. Измерения по шкалам MADRS и HAM-A проводились на стартовом визите, затем на 4 и 8 неделе.
Главным показателем эффективности был окончательный суммарный балл 17-пунктовой шкалы HAM-D - последнее значение после стартового измерения в рамках Полного набора анализов (FAS), также обозначаемого как общая выборка терапии (ITT; intention-to-treat) (Sokal и Rohlf, 1981). В FAS включались все пациенты, получившие минимум одну капсулу после рандомизации, прошедшие стартовые измерения и минимум одно измерение после стартового визита. Уровни эффекта (респондеры) и интервалы времени до первого проявления эффекта также определялись по шкале HAM-D (пациенты с редукцией стартового суммарного балла HAM-D на >50%). Дополнительно проводился анализ в подгруппе пациентов с тяжелой депрессией (стартовый балл HAM-D > 25). Для анализа долей пациентов в ремиссии использовался критерий снижения финального суммарного балла HAM-D до < 7. В качестве дополнительных показателей эффективности использовались финальные баллы шкалы MADRS, Шкалы тревоги Гамильтона (HAM-A, Hamilton, 1959) и Шкалы общего клинического впечатления - Тяжесть заболевания (CGI) (Guy, 1976) в выборке FAS. Сравнения каждой дозы Вальдоксана с плацебо проводились с применением одностороннего вариационного анализа по группирующему фактору для количественных показателей и с помощью теста хи-квадрат для количественных показателей, либо логарифмического теста для показателей интервалов времени до первого проявления эффекта. Для учета множества терапевтических групп в случае статистически достоверного эффекта терапии анализы каждой дозы активного препарата в сравнении с плацебо проводились методом t-теста Даннетта (Dunnett's t-test), теста хи-квадрат с коррекцией Бонферрони и логарифмического теста с коррекцией Бонферрони. Для анализа различий между пароксетином и плацебо (оценка чувствительности) использовался двусторонний тест Стьюдента, тест хи-квадрат или логарифмический тест. Для проведения анализов использовался уровень достоверности (риска) 0,05.
Перед назначением и по завершении терапии проводилась регистрация показателей безопасности, включая данные физикального обследования, стандартные лабораторные анализы и электрокардиографию. Нежелательные эффекты, сообщаемые пациентами, и сопутствующая терапия регистрировались на каждом визите исследования.
Для статистического анализа использовался пакет компьютерного программного обеспечения SAS версии 6.09 (SAS Institute Inc., Cary, NC, USA).
РЕЗУЛЬТАТЫ
Демографические показатели
Всего в исследование было включено 711 пациентов: 238 мужчин (33,5%) и 473 женщины (66,5%), средний возраст 42,3 лет, в 102 центрах, расположенных в Бельгии, Франции и Великобритании. Терапевтические группы не имели статистически достоверных различий по демографическим и клиническим показателям: 67,1% пациентов соответствовали критериям DSM-IV для рекуррентного большого депрессивного расстройства, 33,5% пациентов страдали тяжелым депрессивным эпизодом. Средняя продолжительность текущего эпизода на момент включения составила 4,8 месяцев, среднее число перенесенных депрессивных эпизодов - 2,7±2,7. На момент включения 19% больных находились в стационаре.
Средний стартовый балл HAM-D равнялся 27,4; MADRS - 31,5, без статистически достоверных различий между группами (табл. 1).
Таблица 1. Выборка исследования: диагноз, тяжесть депрессии и тревоги на момент включения
| Вальдоксан (1 мг/сут) n = 141 |
Вальдоксан (5 мг/сут) n=147 |
Вальдоксан (25 мг/сут) n=137 |
Плацебо n=139 |
Пароксетин (20 мг/сут) n = 147 |
|
| Диагноз, n (%) | |||||
| Большое депрессивное расстройство | 140 (99,3) | 145 (98,6) | 133 (97,1) | 135 (97,1) | 145 (98,6) |
| Биполярное расстройство II типа | 1 (0,7) | 2 (1,4) | 4 (2,9) | 4 (2,9) | 2 (1,4) |
| Суммарный балл HAM-D, среднее ± SD | 27,9±3,0 | 27,3±2,6 | 27,4±2,7 | 27,4±3,1 | 27,3±3,4 |
| Суммарный балл MADRS, среднее ± SD | 31,5±5,0 | 31,6±3,7 | 30,9±4,5 | 31,8±4,8 | 31,7±4,5 |
| Суммарный балл HAM-A, среднее ± SD | 27,1±5,8 | 27,2±5,8 | 25,8±6,0 | 27,0±6,4 | 26,0±6,4 |
| CGI-Severity, среднее ± SD | 4,8±0,7 | 4,9±0,7 | 4,7±0,7 | 5,0±0,7 | 4,9±0,7 |
Преждевременное исключение из исследования
Всего 26% пациентов были преждевременно исключены из исследования, из них 10% - по причине неудовлетворительной эффективности терапии. Максимальная частота преждевременного исключения из-за неудовлетворительной эффективности терапии отмечалась в группе плацебо (13,7%), минимальная - в группе Вальдоксана 25 мг (6,6%). Средняя частота преждевременных исключений из исследования по причине нежелательных явлений составила 6,5% с групповыми вариациями от 4,3% для Вальдоксана 1 мг до 8,0% для Вальдоксана 25 мг, тогда как в группе плацебо этот показатель равнялся 6,5% (табл. 2).
Средняя длительность терапии в исследовании составила 49±15 дней, без статистически достоверных различий между терапевтическими группами. Также не обнаружено достоверных различий между группами по уровням комплаентности к терапии, которые рассчитывались для каждого пациента за 8 недель терапии.
Таблица 2. Преждевременная отмена терапии
| Вальдоксан (1 мг/сут) n = 141 |
Вальдоксан (5 мг/сут) n=147 |
Вальдоксан (25 мг/сут) n=137 |
Плацебо n=139 |
Пароксетин (20 мг/сут) n = 147 |
|
| Всего, n (%) | 27 (19,1) | 45 (30,6) | 32 (23,4) | 35 (25,2) | 34 (23,1) |
| Нежелательное явление, n (%) | 6 (4,3) | 10 (6,8) | 11 (8,0) | 9 (6,5) | 10 (6,8) |
| Недостаточная эффективность, n (%) | 11 (7,8) | 17 (11,6) | 9 (6,6) | 19 (13,7) | 11 (7,5) |
| Не медицинская причина, n (%) | 8 (5,7) | 12 (8,2) | 6 (4,4) | 4 (2,9) | 7 (4,8) |
| Серьезное отклонение от протокола, n (%) | 2 (1,4) | 6 (4,1) | 6 (4,4) | 3 (2,2) | 6 (4,1) |
| Утрата контакта в катамнезе, n (%) | 2 (1,4) | 1 (0,7) | 1 (0,7) | - | - |
ЭФФЕКТИВНОСТЬ
Основной анализ
В результате анализа LOCF в выборке FAS установлены достоверные различия в средних финальных баллах HAM-D при сравнении с каждой из трех доз Вальдоксана с плацебо (P = 0,037). В дополнительных анализах только Вальдоксан 25 мг обнаруживал явное превосходство над плацебо по эффективности (P<0,05; тест Даннетта), тогда как Вальдоксан в дозах 1 и 5 мг не отличался от плацебо (табл. 3). Средний суммарный балл HAM-D был достоверно ниже в группе пароксетина в сравнении с плацебо (P = 0,030). В анализах с поправками на потенциальные эффекты стран были получены данные, сопоставимые с результатами основного анализа, который проводился без внесения подобных поправок.
Респондеры
В результате применения теста хи-квадрат по завершении терапии установлены статистически достоверные различия между Вальдоксаном во всех дозах в сумме и плацебо по долям респондеров - пациентов с редукцией стартовых суммарных баллов HAM-D на > 50% (P = 0,016). В результате парных сравнений с коррекцией Бонферрони показано, что доли респондеров в группах Вальдоксана l мг (62,5%; Р = 0,021) и 25 мг (61,5%; P = 0,036) были достоверно больше, чем в группе плацебо (46,3%). В то же время ни Вальдоксан 5 мг (51,4%), ни пароксетин (56,3%) не обнаруживали достоверного превосходства над плацебо по этому показателю.
По данным анализа кривых выживания для показателя времени до первого проявления эффекта установлены достоверные отличия в пользу Вальдоксана 25 мг в сравнении с плацебо (P = 0,008). Менее значимые различия выявлены в группах Вальдоксана 1 мг и пароксетина (P<0,05) (рис. 1).
Пациенты в ремиссии
По результатам анализа (FAS LOCF) доли больных в ремиссии (балл HAM-D < 7) были достоверно больше в группах Вальдоксана 25 мг (30,4%; P<0,01) и пароксетина (25,7%; P<0,05) в сравнении с плацебо (15,4%). В других группах достоверного увеличения долей пациентов с ремиссией в сравнении с плацебо не выявлено (табл. 3).
Таблица 3. Критерии исследования: финальные оценки (LOCF) в выборке FAS
| Вальдоксан (1 мг/сут) n = 136 |
Вальдоксан (5 мг/сут) n=146 |
Вальдоксан (25 мг/сут) n=135 |
Плацебо n=136 |
Пароксетин (20 мг/сут) n = 144 |
|
| Суммарный балл HAM-D, среднее ± SD | 13,17±8,18 | 14,70±8,54 | 12,77±8,23* | 15,34±8,87 | 13,09±8,37t |
| Респондеры, n (%) | 85±62,5* | 75±51,4 | 83±61,5* | 63±46,3 | 81±56,3 |
| Ремиссия, n (%) | 29±21,3 | 26±17,8 | 41±30,4* | 21±15,4 | 37±25,7t |
| CGI-тяжесть, среднее ± SD | 2,85±1,45 | 3,07±1,48 | 2,84±1,39 | 3,26±1,53 | 2,75±1,46t |
| n=130a | n = 127a | n = 125a | n = 125a | A7 = 135a | |
| Суммарный балл MADRS, среднее ± SD | 15,25±10,72 | 15,74±10,20 | 13,62±9,25* | 17,26±11,05 | 13,99±9,77t |
| Суммарный балл HAM-A, среднее ± SD | 13,95±9,51 | 14,24±9,30 | 12,58±8,61 | 16,02±9,98 | 12,61±8,77t |
*P < 0,05 (парные сравнения с плацебо с применением теста Даннетта или хи-квадрат с коррекцией Бонферрони). *P
Скорость наступления эффекта
В соответствии с результатами анализа динамики суммарных баллов шкалы HAM-D (выборка FAS, анализ LOCF) Вальдоксан 25 мг достоверно превосходил плацебо по всем показателям эффективности, начиная со 2-й недели терапии и далее, тогда как достоверное превосходство пароксетина над плацебо отмечалось не ранее 4-й недели лечения (рис. 2).
Дополнительные критерии
Сопоставимые результаты получены в ходе дополнительных анализов.
В выборке FAS установлены достоверные различия в средних баллах MADRS при сравнении пациентов на терапии Вальдоксаном 25 мг и пароксетином с больными, принимавшими плацебо (P<0,05). Низкие дозы Вальдоксана не обнаруживали достоверных отличий от плацебо.
Также выявлены достоверные различия в средних финальных баллах шкалы HAM-A (FAS LOCF) при сравнении Вальдоксана 25 мг (P<0,05) и пароксетина (P = 0,004) с плацебо (табл. 3). Вальдоксан 1 мг и Вальдоксан 5 мг не были достоверно эффективнее плацебо.
В результате общего сравнительного анализа показателей CGI-Тяжесть заболевания установлены различия между группами Вальдоксана и плацебо на уровне статистической тенденции (P= 0,054). Данные анализа 95% доверительных интервалов свидетельствуют о достоверном превосходстве Вальдоксана 25 мг над плацебо (0-0,84), тогда как меньшие дозы Вальдоксана не отличались от плацебо. Пароксетин также обнаруживал достоверное преимущество в сравнении с плацебо (P = 0,005).
Независимый анализ был выполнен в подгруппе пациентов с тяжелой депрессией (586 больных с баллом HAM-D > 25 при включении). В этой подгруппе установлено статистически достоверное преимущество Вальдоксана 25 мг в сравнении с плацебо по показателям редукции баллов HAM-D (P<0,05). В свою очередь, пароксетин не обнаруживал достоверного превосходства над плацебо в той же подгруппе пациентов (P = 0,09) (табл. 4).
Безопасность и переносимость
За весь период терапии 402 из 711 (56,5%) пациентов сообщали о минимум одном новом нежелательном явлении (которого не было на момент включения) или утяжелении предшествовавшего включению нежелательного явления. Доли пациентов с минимум одним нежелательным явлением были несколько меньше в группах Вальдоксана 25 мг (51,1%) и плацебо (54,7%) в сравнении с пароксетином (66,0%). Большинство из зарегистрированных нежелательных явлений были легкой или умеренной степени тяжести (85%).
Вальдоксан 25 мг не обнаруживал статистически достоверных отличий от плацебо ни по одному из выявленных нежелательных явлений (табл. 5).
В группе пароксетина регистрировалось достоверно больше (P = 0,001) гастроинтестинальных нежелательных явлений (n = 41; 32,0%), чем в группе плацебо (n = 21; 15,1%). Наиболее выраженные отличия зафиксированы в показателях тошноты: 17% (n = 25) пациентов в группе пароксетина против 4,3% (n = 6) в группе плацебо (P = 0,001). В группе Вальдоксана 25 мг тошнота встречалась несколько реже (n = 4; 2,9 %) в сравнении с плацебо. Клинически значимых изменений в витальных показателях, весе, параметрах электрокардиограммы и лабораторных анализах по завершении терапии не обнаружено.
Рис. 1. Анализ респондеров (анализ выживаемости для показателей интервалов времени до первого проявления эффекта
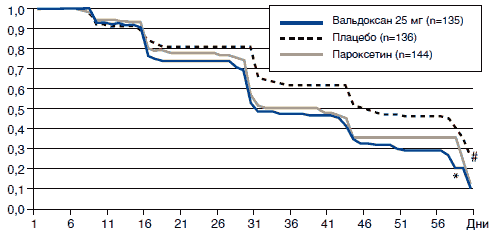
* Р = 0,008 (сравнение с плацебо: логарифмический тест с коррекцией Бонферрони)
# Р = 0,038 (сравнение с плацебо: логарифмический тест)
Рис. 2. Средний суммарный балл шкалы HAM-D (выборка FAS, анализ LOCF). Двусторонний вариационный анализ повторных измерений по одному фактору
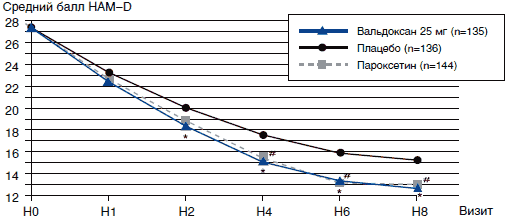
Двусторонний вариационный анализ повторных измерений по одному фактору.
* Отличие Вапьдоксана от плацебо (Р < 0,05)
# Отличие пароксетина от плацебо (Р < 0,05)
В ходе исследования зафиксировано два случая самоубийства, один - в группе пароксетина через 11 дней терапии, еще один - в группе Вальдоксана 25 мг через 10 дней терапии (в обоих случаях исследователи не выявили связи между смертью и терапией исследования). Других случаев смерти не отмечалось. Дополнительно зарегистрировано 7 суицидальных попыток: 1 - в группе Вальдоксана 1 мг, 3 - в группе Вальдоксана 5 мг, 1 - в группе Вальдоксана 25 мг, 2 - в группе пароксетина и ни одной в группе плацебо.
В одной из указанных 7 суицидальных попыток зафиксирована передозировка Вальдоксана. Пациент принял 18 капсул по 5 мг в сочетании с неизвестным количеством алкоголя. Пациент оставался в сознании, обнаруживал лишь небольшое учащение пульса (95 ударов в минуту) с полным восстановлением состояния здоровья.
Отмечалось два случая инверсии аффективной фазы с развитием маниакального эпизода - один в группе Вальдоксана 5 мг через 46 дней терапии у пациента с установленным ранее диагнозом биполярного расстройства II типа, еще один - в группе пароксетина через 7 дней после завершения исследования у пациента с признаками биполярного расстройства в анамнезе.
Таблица 4. HAM-D: среднее финальное значение в подгруппе пациентов с тяжелой депрессией (балл HAM-D > 25 при включении)
| Вальдоксан (25 мг/сут), n=120 |
Плацебо n=114 |
Пароксетин (20 мг/сут), n=110 |
|
| Финальный суммарный балл HAM-D, среднее ± SD | 13,14±8,40* | 16,10±9,10 | 14,10±8,40 |
Таблица 5. Основные связанные с терапией нежелательные явления (% пациентов в выборке безопасности§) (нежелательные явления, зарегистрированные минимум у 3,5% пациентов в любой терапевтической группе)
| Вальдоксан (1 мг/сут) n=141 |
Вальдоксан (5 мг/сут) n=147 |
Вальдоксан (25 мг/сут) n=137 |
Плацебо n=139 |
Пароксетин (20 мг/сут) n=147 |
|
| Всего | 58,2 | 52,4 | 51,1 | 54,7 | 66,0 |
| Головная боль | 9,2 | 9,5 | 6,6 | 8,6 | 8,2 |
| Тревога | 5,7 | 0,7 | 3,6 | 3,6 | 2,7 |
| Абдоминальная боль | 0,7 | 2,7 | 3,6 | 3,6 | 3,4 |
| Диарея | 1,4 | 1,4 | 3,6 | 2,9 | 4,1 |
| Тошнота | 6,4 | 7,5 | 2,9 | 4,3 | 17,0* |
| Сонливость | 4,3 | 2,7 | 2,9 | 5,0 | 7,5 |
| Депрессия | 7,1 | 2,7 | 2,9 | 2,7 | 4,3 |
| Инсомния | 2,8 | 2,0 | 2,9 | 2,9 | 4,8 |
| Ринит | 4,3 | 1,4 | 2,2 | 1,4 | 0,7 |
| Сухость во рту | 3,5 | 2,7 | 0,7 | 1,4 | 3,4 |
| Инфекции верхних дыхательных путей | 4,3 | 1,4 | - | 1,4 | 0,7 |
ОБСУЖДЕНИЕ
В исследовании с участием 711 пациентов получены убедительные доказательства эффективности Вальдоксана в терапии большой депрессии. Вальдоксан был достоверно эффективен только в дозе 25 мг в сутки (P<0,05), а в более низких суточных дозах 1 и 5 мг не обнаруживал значимых отличий от плацебо. Таким образом, на основании оценки Вальдоксана в суточных дозах от 1 до 25 мг можно заключить, что достоверно эффективной является доза 25 мг в сутки. Весьма вероятно, что Вальдоксан может быть эффективным и в более высоких дозах, однако это могут подтвердить только специальные исследования.
Пароксетин в дозе 20 мг использовался в данном исследовании в качестве валидатора. Пароксетин был эффективен по главному и большинству дополнительных показателей, что подтверждает валидность методологии и выборки проведенного исследования.
Сообщается, что во многих плацебо-контролируемых исследованиях эффективности терапии депрессии не удалось подтвердить, что антидепрессант, используемый в качестве валидатора, достоверно превосходит по эффективности плацебо в выборке исследования (Montgomery, 1999). Такие неудачи, постигающие от 50 до 60% всех исследований, являются серьезной проблемой клинического развития антидепрессантов. Рассматривается несколько причин, которые могут объяснить эти факты. Одна из них - включение пациентов с недостаточно тяжелыми расстройствами, что затрудняет доказательство статистически достоверного терапевтического эффекта антидепрессанта в сравнении с плацебо. Настоящее исследование планировалось с учетом этого фактора, в связи с чем были включены пациенты с достаточно тяжелыми депрессивными расстройствами, что подтверждается средним суммарным баллом шкалы HAM-D при включении, который был равен 27,4±3,0. Результаты анализа эффективности в подгруппе пациентов с тяжелыми депрессиями (балл HAM-D > 25) убедительно подтверждают эффективность Вальдоксана 25 мг в терапии тяжелой депрессии в отличие от пароксетина, который не обнаруживал превосходства над плацебо в этой подгруппе пациентов. Эти данные сопоставимы с результатами оценки различных антидепрессантов (DUAG, 1986, 1990; Clerc et al, 1994; Montgomery, 1999). Анализ долей респондеров (пациенты с редукцией стартового суммарного балла HAM-D на > 50%) является стандартным методом оценки эффективности антидепрессантов. В настоящем исследовании доля респондеров в группе Вальдоксана 25 мг (61,5%) была статистически достоверно больше, чем в группе плацебо (46,3%), тогда как пароксетин (56,3%) не обнаруживал достоверного превосходства над плацебо по этому показателю. Однако при использовании указанного критерия популяция респондеров может оказаться крайне неоднородной. Несмотря на определенное улучшение в ходе терапии, у части из этих пациентов могут сохраняться проявления расстройства, тогда как другие больные могут достигать ремиссии. В настоящем исследовании анализ долей респондеров дополнялся анализом пропорций пациентов, достигших ремиссии, с использованием достаточно строгого критерия ремиссии - балл HAM-D менее 7. Ремиссия является наиболее важной целью купирующей терапии депрессии, так как соотносится с состоянием общего благополучия и уровнем симптомов, свойственным для общей популяции лиц, не страдающих депрессией. Вальдоксан 25 мг (30,4%; P<0,01) и пароксетин (25,7%; Р<0,05) достоверно превосходили плацебо по долям пациентов, достигших ремиссии. Достоверные отличия от плацебо по долям пациентов в ремиссии редко выявляются в исследованиях антидепрессантов, поэтому установление такого превосходства, причем с достаточно высоким уровнем ремиссии - 30%, позволяет предполагать, что выбор Вальдоксана позволит достичь основной цели терапии депрессии - достижения ремиссии.
Настоящее исследование не было разработано специально для оценки скорости наступления терапевтического эффекта. Тем не менее установлены достоверные различия между Вальдоксаном 25 мг и плацебо по степени редукции стартового суммарного балла HAM-D на 2-й неделе терапии, тогда как эффект пароксетина достигал уровня статистически достоверного отличия от плацебо лишь на 4-й неделе лечения. Результаты анализа выживания с учетом количества респондеров и времени до наступления эффекта подтверждают эффективность Вальдоксана 25 мг; пароксетин также оказался эффективным, но с меньшим уровнем статистической достоверности. Эти данные позволяют предположить более быстрое начало действия Вальдоксана. Однако требуются дополнительные специальные исследования для количественного подтверждения этого преимущества Вальдоксана в сравнении с СИОЗС.
В настоящем исследовании средний стартовый балл HAM-D составил 27,4, что является достаточно высоким показателем и свидетельствует о значительном количестве пациентов с тяжелой депрессией. В связи с этим была возможность провести отдельный анализ эффективности Вальдоксана в подгруппе пациентов с тяжелой депрессией. В целях этого анализа для квалификации тяжелой депрессии использовался балл HAM-D > 25 - стандартный и широко используемый критерий для выявления популяции больных с тяжелой депрессией (Tignol et al, 1992; Kasper, 1997; Guelfi et al, 2001).
В подгруппе пациентов с тяжелой депрессией Вальдоксан 25 мг достоверно превосходил плацебо по степени редукции основного показателя, суммарного балла HAM-D, тогда как пароксетин не обнаруживал достоверных отличий от плацебо. Эти результаты согласуются с данными ряда публикаций, в которых высказываются сомнения в эффективности СИОЗС при тяжелых депрессиях (Clerc et al, 1994; DUAG, 1986, 1990). Вальдоксан, напротив, обнаруживал отчетливый терапевтический эффект у больных с тяжелой депрессией.
Оба антидепрессанта, Вальдоксан 25 мг и пароксетин, превосходили плацебо по степени редукции тревожной симптоматики, сопутствующей депрессии (шкала HAM-A). Эти данные позволяют предполагать, что Вальдоксан, как и пароксетин, обладает выраженным эффектом в отношении тревожных симптомов при депрессии. В свое время сходные данные, полученные в ранних исследованиях пароксетина в терапии депрессии, послужили основанием для предположения о возможной эффективности пароксетина при тревожных расстройствах, которое было полностью подтверждено последующими исследованиями пароксетина при разных тревожных расстройствах (генерализованное тревожное расстройство, социальное тревожное расстройство, паническое расстройство) (Ballenger et al, 1998; Bakker et al, 1999; Baldwin, 2000; Pollack et al, 2001). Аналогичным образом значимый противотревожный эффект Вальдоксана 25 мг, верифицированный показателями шкалы HAM-A, служит достаточным основанием для специальных исследований Вальдоксана в терапии тревожных расстройств.
Результаты настоящего исследования свидетельствуют, что Вальдоксан переносится лучше, чем пароксетин. В группе Вальдоксана частота нежелательных явлений, по сообщениям пациентов, была ниже, чем в группе плацебо (51,1% в сравнении с 54,7%). Ни одно из зарегистрированных нежелательных явлений не встречалось в группе Вальдоксана 25 мг достоверно чаще, чем в группе плацебо. Вальдоксан 25 мг был полностью сопоставим с плацебо по показателям частоты наиболее типичных нежелательных явлений (головная боль, абдоминальная боль и диарея). В свою очередь, гастроинтестинальные расстройства, характерные для антидепрессантов класса СИОЗС, достоверно чаще развивались при терапии пароксетином в сравнении с плацебо. По частоте преждевременной отмены терапии из-за нежелательных явлений Вальдоксан 25 мг (8,0%) был близок к плацебо (6,5%), что еще раз подтверждает хорошую переносимость Вальдоксана в максимальной из тестировавшихся в этом исследовании доз.
В целом по результатам данного исследования эффективность Вальдоксана 25 мг была того же уровня, что и эффективность пароксетина. Однако большие доли респондеров с достоверным терапевтическим эффектом в группе Вальдоксана 25 мг в сравнении с пароксетином, в совокупности с более высокой пропорцией больных в ремиссии и достоверным превосходством над плацебо у больных с тяжелыми депрессиями при отсутствии такого эффекта в группе пароксетина свидетельствуют о превосходстве Вальдоксана 25 мг над пароксетином. Сопоставимые небольшие, но потенциально важные различия выявлены при сравнении СИОЗС с трициклическими антидепрессантами и новыми антидепрессантами двойного действия, причем данные множества мета-анализов также свидетельствуют о потенциальном превосходстве антидепрессантов двойного действия над СИОЗС (Anderson и Tomenson, 1994; Lopez-Ibor et al, 1996; Montgomery, 1999).
В заключение следует отметить следующее. В результате проведенного плацебо-контролируемого исследования убедительно показано, что из трех доз, подвергавшихся тестированию, доза Вальдоксана 25 мг (агомелатин) является эффективной в терапии большой депрессии и определяется как целевая терапевтическая доза препарата. Вальдоксан 25 мг эффективен в терапии тяжелой депрессии и купировании тревожных симптомов, связанных с депрессией. Также получены определенные свидетельства быстрого развития антидепрессивного эффекта с достоверным превосходством над плацебо уже на 2-й неделе терапии, которые, однако, требуют дальнейшего подтверждения в дополнительных исследованиях. Вальдоксан очень хорошо переносился пациентами и обнаруживал сопоставимый с плацебо профиль нежелательных явлений. Более благоприятный профиль нежелательных явлений нового антидепрессанта в сочетании с отчетливой эффективностью в терапии большой депрессии и более быстрым началом действия позволяет предполагать, что Вальдоксан будет ценным дополнением арсенала средств терапии большого депрессивного расстройства. Необходимы дальнейшие исследования для подтверждения результатов настоящего исследования и оценки эффективности Вальдоксана при более длительной терапии. Полученные в настоящем исследовании данные представляют особый интерес в связи с тем, что Вальдоксан обладает принципиально иным механизмом действия в сравнении с другими антидепрессантами и, соответственно, открывает новый подход к терапии депрессии.
Список использованной литературы
