Анемия при болезни Крона
СтатьиОпубликовано в журнале:
«КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ И ТЕРАПИЯ»; № 22(1); 2013; стр. 1-6.
В.Г.Авдеев,1 С.В.Моисеев1,2
Кафедра внутренних болезней факультета фундаментальной медицины МГУ им. М.В.Ломоносова
Кафедра терапии и профболезней Первого МГМУ им. И.М.Сеченова
Обсуждаются методы лечения анемии при болезни Крона. Для коррекции железодефицита у таких пациентов предпочтительно применение внутривенных препаратов железа, которые по эффективности и переносимости имеют преимущества перед пероральными железосодержащими средствами.
Ключевые слова. Болезнь Крона, анемия, железодефицит, внутривенные препараты железа, карбоксимальтозат железа.
ANEMIA IN PATIENTS WITH CROHN'S DISEASE
V.G.Avdeev, S.V.Moiseev
The authors discuss etiology, mechanisms and treatment of anemia in patients with inflammatory bowel diseases (Crohn's disease and ulcerative colitis). Because of extensive gastrointestinal adverse effects, and data showing that the use of oral iron in inflammatory bowel diseases may be associated with disease exacerbation, current guidelines suggest that iron supplementation in IBD should be administered intravenously.
Key words. Inflammatory boew disease, anemia, iron deficiency, intravenous iron, ferric carboxymaltose.
Анемия — это самое распространенное внекишечное проявление болезни Крона. Частота ее у больных воспалительными заболеваниями кишечника (ВЗК) варьируется от 16% у амбулаторных пациентов до 68% у госпитализированных больных [1]. По данным систематизированного обзора 19 исследований [2] в 70-80-х гг. прошлого века анемия встречалась примерно у 2/3 больных болезнью Крона, однако в последующем ее частота ее снизилась, вероятно, за счет улучшения результатов лечения основного заболевания и более частого применения препаратов железа. В самом крупном исследовании, опубликованном в 2005 году, частота анемии у 7200 пациентов с ВЗК составила 13% [3], однако в других недавно завершенных исследованиях она была существенно выше и достигала 29-60% [2]. Вариабельность этого показателя может отражать различия критериев диагностики анемии и особенности выборок пациентов. В отличие от других внекишечных проявлений болезни Крона исследователи не уделяют должного внимания изучению анемии, хотя она сопровождается различными симптомами, в том числе одышкой, утомляемостью, головной болью, тахикардией, головокружением, которые ухудшают трудоспособность пациентов и их качество жизни и могут быть причиной госпитализаций.
Механизмы развития анемии при болезни Крона
Основная причина анемии у больных болезнью Крона — дефицит железа, который может быть следствием скрытой кровопотери, нарушения всасывания и/или низкого потребления железа [4]. На втором месте среди причин снижения уровня гемоглобина находится анемия хронических заболеваний. Значительно реже встречаются другие формы анемии (В12- и фолиеводефицитная, гемолитическая, анемия, вызванная некоторыми лекарственными средствами, такими как месалазин, сульфасалазин и пуриновые аналоги).
В норме запасы железа в организме человека (в основном в эритроцитах) составляют 3,5 г. В среднем ежедневно теряется 1-2 мг железа за счет десквамации эпителиальных клеток и кровопотери при менструации. Соответственно, у женщин потери железа выше и чаще развивается железодефицитная анемия. Запасы железа восполняются за счет его всасывания в тонкой кишке. С пищей железо поступает в виде гема (мясные продукты) и других белков и органических кислот (овощи). Всасывание железа, не входящего в состав гема, происходит в 4 этапа [4]. На первом этапе в кислом содержимом желудка из пищевых продуктов высвобождаются ионы Fe3+, которые превращаются в ионы Fe2+ под действием соляной кислоты или дуоденального цитохрома В на апикальной мембране (соответственно, изменения слизистой оболочки двенадцатиперстной кишки приводят к ухудшению всасывания железа). Затем ионы Fe2+ поступают в клетки слизистой оболочки с помощью дивалентного катионного транспортера, экспрессия которого увеличивается при дефиците железа. На третьем этапе внутри клетки часть железа связывается с ферритином и образует депо, в то время как другая часть поступает в кровь через ферропортин 1 на базолатеральной оболочке. При этом ионы Fe2+ окисляются до Fe3+ под действием гефестина, а также других оксидаз, таких как церулоплазмин. В плазме ионы Fe3+ связываются с основным транспортным белком — трансферрином. Всасывание железа, входящего в состав гема, недостаточно изучено. Предполагается, что оно происходит с помощью специального транспортера. Внутри клетки железо высвобождается из порфирина под действием гемоксигеназы, а дальнейшие этапы его всасывания соответствуют описанным выше.
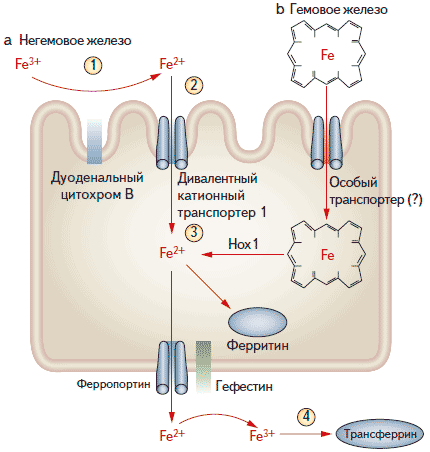
Рис. 1. Этапы связывания железа в кишечнике (объяснения см. в тексте)
Важную роль в регуляции обмена железа играет гепсидин — гормон, который образуется в печени, взаимодействует с ферропортином (белком, осуществляющим транспорт железа через мембрану) и подавляет всасывание железа в кишечнике и его освобождение из депо и макрофагов [5]. Экспрессия гепсидина увеличивается при инфекциях и воспалительных состояниях под действием провоспалительных цитокинов, прежде всего интерлейкина-6 [6]. Увеличение уровня гепсидина при воспалении, в том числе болезни Крона, — это один из основных механизмов развития анемии хронических заболеваний. Экспрессия гепсидина регулируется различными факторами, в частности костным морфогенетическим протеином 6 (BMP6) [7]. Поступление железа в энтероциты вызывает активацию экспрессии BMP6, которые поступает в печень и взаимодействует с рецепторами. Транслокация образующегося комплекса в ядро сопровождается активацией промотера гена HAMP и увеличением синтеза гепсидина.
Диагностика железодефицитной анемии
В соответствии с рекомендациями ВОЗ анемию диагностируют при снижении уровня гемоглобина <12 г/дл у женщин и <13 г/дл у мужчин. При дефиците железа обычно развивается микроцитарная гипохромная анемия, которая характеризуются следующими признаками:
Нормальный средний объем эритроцитов не исключает дефицит железа, так как в 40% случаев железодефицитная анемия является нормоцитарной. С другой стороны, микроцитарная анемия может быть обусловлена не только дефицитом железа, но и другими причинами (например, анемией хронических заболеваний или сидеробластной анемией) [3]. В связи с этим важную роль в диагностике железодефицитной анемии играет определение показателей обмена железа. Критериями диагностики железодефицита у пациентов с воспалительными заболеваниями кишечника считают снижение сывороточного уровня ферритина <30 мкг/л и степени насыщения трансферрина <16% [8]. Уровень ферритина увеличивается при воспалении, поэтому у пациентов с высокой активностью болезни Крона недостаточность железа диагностируют при снижении содержания белка <100 мкг/л. Повышенный уровень ферритина в сочетании с низкой концентрацией гемоглобина характерен для анемии хронических заболеваний [9]. Для повышения точности диагностики железодефицитной анемии при воспалении предлагают также определять содержание гемоглобина в эритроцитах (СНr) и процент гипохромных эритроцитов [10,11].
Лечение анемии при болезни Крона
Цели лечения железодефицитной анемии у больных болезнью Крона — увеличение уровня гемоглобина до нормальных значений или по крайней мере на 2 г/дл в течение 4 недель и восстановление запасов железа (увеличение уровня ферритина и степени насыщения трансферрин) [4]. Выбор метода лечения зависит от тяжести анемии, клинических симптомов, этиологии, динамики снижения уровня гемоглобина, сопутствующих заболеваний [8]. Препараты железа можно вводить внутрь, внутримышечно или внутривенно. Внутримышечное введение препаратов железа сегодня не рекомендуется [4,12], учитывая болезненность инъекций, возможность изменения цвета кожи и отсутствие каких-либо преимуществ этого пути применения перед пероральным или внутривенным по эффективности или безопасности.
При отсутствии абсолютных показаний к внутривенному введению препараты железа могут быть назначены внутрь. Пероральные препараты разделяют на две группы: ионные солевые препараты железа, преимущественно двухвалентного, и неионные препараты на основе гидроксидполимальтозного комплекса трехвалентного железа. В двенадцатиперстной кишке в сутки всасывается не более 10-20 мг железа, поэтому назначение больших доз железа внутрь, вероятно, не имеет смысла [13]. В некоторых исследованиях, например, у пациентов старческого возраста, была показана сопоставимая эффективность солей железа в дозах 15 и 50150 мг/сут, при этом частота нежелательных эффектов была выше при назначении более высоких доз [14]. В связи с этим при лечении железодефицитной анемии у больных болезнью Крона рекомендуется пероральный прием препаратов железа в невысоких дозах (например, 50-100 мг) [4].
Хотя пероральное применение железосодержащих препаратов достаточно эффективно, дешево и удобно, оно имеет существенные недостатки:
Таблица 1
Внутривенные препараты железа
| Декстран | Глюконат | Сахарат | Карбоксимальтозат | |
| Молекулярная масса, кДа | 73 | 37,5 | 43 | 150 |
| Стабильность комплекса | Высокая | Низкая | Средняя | Высокая |
| Необходимость тестовой дозы | Да | Нет | Да (в Европе) | Нет |
| Максимальная однократная доза | 200 мг | 62,5 мг | 500 мг | 1000 мг |
| Длительность введения дозы | 4-6 ч | 5-10 мин | 3,5 ч | 15 мин |
| Дозозависимые реакции | Гипотония, отеки | Гипотония, отеки | Гипотония, отеки | Нет |
| Риск тяжелых нежелательных эффектов | Средний | Низкий | Очень низкий | Нет данных |
Внутривенное введение железосодержащих препаратов позволяет быстро восстановить дефицит железа, гарантирует полную приверженность и лучше переносится, чем пероральный их прием. Абсолютными показаниями к внутривенному введению препаратов железа считают следующие [8]:
При выборе пути введения железосодержащих препаратов следует учитывать и предпочтения пациента.
Перед началом внутривенного лечения необходимо рассчитать оптимальную кумулятивную дозу препарата, которую не следует превышать. Ее вычисляют по формуле Ганзони:
Кумулятивный дефицит железа (мг) = масса тела [кг] X (целевой Hb* — фактический Hb) [г/дл] X 2,4 + содержание депонированного железа [мг], где целевой уровень гемоглобина (Hb) у человека с массой тела более 35 кг = 15 г/дл (9,3 ммоль/л), депо железа = 500 мг. Для перевода уровня гемоглобина в ммоль/л в г/дл показатель следует умножить на 1,61145.
Для внутривенного введения применяют сферические железоуглеводные коллоиды (карбоксимальтозат, сахарат, глюконат и декстран) [19]. Углеводная оболочка обеспечивает стабильность комплекса, замедляет высвобождение железа и поддерживает образующиеся формы в коллоидной суспензии. Эффективность и безопасность внутривенных препаратов железа зависят от их молекулярной массы, стабильности и состава. Комплексы с низкой молекулярной массой, такие как глюконат железа, менее стабильны и быстрее высвобождают в плазму железо, которое в свободном виде может катализировать образование реактивных форм кислорода, вызывающих перекисное окисление липидов и повреждение тканей. Значительная часть дозы подобных препаратов выводится через почки в первые 4 часа после приема препарата и не используется для эритропоэза. Препараты декстрана железа обладают высокими молекулярной массой и стабильностью, однако их недостатком является повышенный риск аллергических реакций. Карбоксимальтозат железа (Феринжект) сочетает в себе положительные свойства высокомолекулярных комплексов железа с декстраном или сахарозой, но редко вызывает реакции гиперчувствительности, характерные для препаратов, содержащих декстран. Кроме того, в отличие от сахарата и глюконата, карбоксимальтозат железа можно вводить в более высокой дозе [20]. При применении карбокси-мальтозата железа 1000 мг железа можно ввести внутривенно капельно в течение 15 минут, в то время как максимальная доза железа в виде сахарата составляет 500 мг и вводится в течение 3,5 ч, а длительность инфузии декстрана железа достигает 6 ч. Причем в двух последних случаях перед началом инфузии необходимо ввести тестовую дозу препарата. Введение большой дозы железа позволяет сократить необходимое число инфузий и затраты на лечение. Помимо удобства применения важными свойствами карбокси-мальтозата железа являются низкая токсичность и отсутствие оксидативно-го стресса, которые определяются медленным и физиологичным высвобождением железа из стабильного комплекса с углеводом, по структуре сходного с ферритином. Феринжект вводят внутривенно в виде болюса (максимальная доза 4 мл, или 200 мг железа, не более трех раз в неделю) или капельно (максимальная доза 20 мл, или 1000 мг железа, не чаще одного раза в неделю).
В многоцентровом, рандомизированном, контролируемом исследовании эффективность карбоксимальтозата железы изучали у 200 пациентов с железодефицитной анемией на фоне воспалительных заболеваний кишечника [21]. Примерно 30% из них страдали болезнью Крона. Препарат вводили в дозе 1000 мг железа один раз в неделю. Пациенты группы сравнения получали железа сульфат внутрь в дозе 100 мг два раза в день. Через 12 недель средняя концентрация гемоглобина была сходной в двух группах, однако пациенты быстрее отвечали на внутривенное введение препарата железа. Так, уже через 2 недели доля больных, у которых уровень гемоглобина увеличился по крайней мере на 2 г/дл, в основной группе была достоверно выше, чем в группе сравнения (p=0,0051). Сходные результаты были получены через 4 недели (p=0,0346). Кроме того, внутривенное введение препарата железа позволяло значительно быстрее восполнить запасы железа. Уже через 2 недели средний сывороточный уровень ферритина в основной группе увеличился с 5,0 до 323,5 мкг/л. Хотя в дальнейшем он снизился, при лечении сульфатом железа было отмечено только умеренное увеличение уровня ферритина с 6,5 до 28,5 мкг/л через 12 недель. В группе карбоксимальтозата железа доля пациентов, у которых уровень ферритина увеличился до целевого значения (100-800 мкг/л), при всех визитах была выше, чем группе сравнения. Общая частота нежелательных явлений была сопоставимой в двух группах, однако из-за нежелательных реакций лечение карбоксимальтозатом железа прекращали реже, чем пероральным препаратом (1,5% и 7,9%, соответственно). Кроме того, в основной группе была ниже частота желудочно-кишечных расстройств (5,8% и 14,2%), хотя из исследования были исключены пациенты с известной непереносимостью пероральных препаратов железа. Таким образом, внутривенное введение карбоксимальтозата железа у больных с воспалительными заболеваниями кишечника, в том числе болезнью Крона, осложнившимися железодефицитной анемией вызывало более быстрое увеличение уровня гемоглобина и восполнение запасов железа, а также имело преимущества перед пероральным препаратом по переносимости.
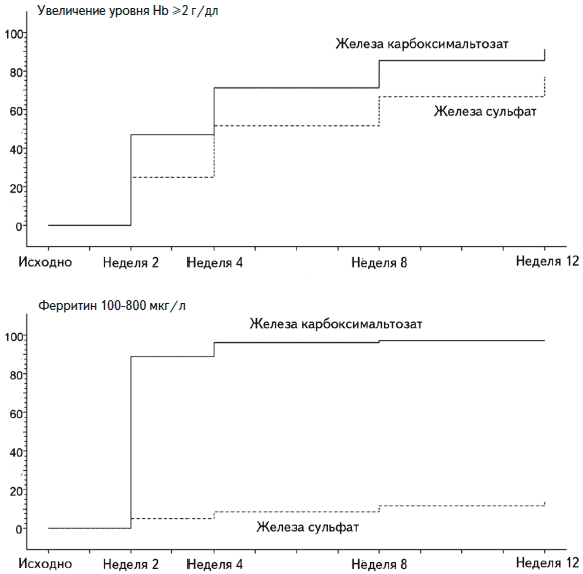
Рис. 2. Процент ответивших на лечение (метод Каплана-Мейера) железа карбоксимальтозатом или сульфатом (вверху - увеличение Hb по крайней мере на 2 г/дл, внизу - уровень ферритина 100-800 мкг/л)
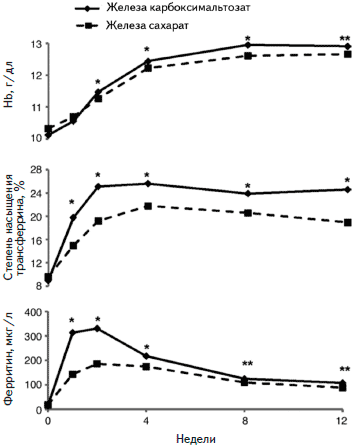
Рис. 3. Динамика уровня гемоглобина, степени насыщения трансферрина и содержания ферритина при лечении железа карбоксимальтозатом или сахаратом
В исследовании FERGI были сопоставлены эффективность и безопасность железа карбоксимальтозата в фиксированной дозе и железа сахарата в индивидуально рассчитанной дозе у 485 больных ВЗК, осложнившейся железодефицитной анемией (уровень ферритина <100 мкг/л, уровень гемоглобина 7-12 г/дл у женщин и 7-13 г/дл у мужчин) [22]. У 160 из них была диагностирована болезнь Крона. Железа карбоксимальтозат вводили в дозе 1000 или 500 мг (максимум 3 инфузии), а железа сахарат — в дозе 200 мг (до 11 инфузией). Дозу карбоксимальтозата железа подбирали с учетом массы тела и тяжести анемии. У пациентов с массой тела <70 кг и ≥70 кг общая доза железа при введении железа карбоксимальтозата составляла, соответственно, 1000 и 1500 мг при уровне гемоглобина ≥10 г/дл и 1500 и 2000 мг при уровне гемоглобина <10 г/дл. Первичным критерием эффективности было увеличение уровня гемоглобина по крайней мере на 2 г/дл. Железа карбоксимальтозат по эффективности превосходил железа сахарат. Частота увеличения уровня гемоглобина ≥2 г/дл в двух группах составила 65,8% и 53,6%, соответственно (р=0,004), а нормализации концентрации гемоглобина - 72,8% и 61,8% (р=0,015). Более высокая эффективность железа карбоксимальтозата была подтверждена и при анализе вторичных конечных точек. Так, частота нормализации степени насыщения трансферрина в двух группах составила 52,7% и 36,4%, соответственно (p<0,001), уровня ферритина (≥100 мкг/л) — 42,5% и 27,3% (p=0,001), нормализации уровней гемоглобина и ферритина — 31,1% и 16,7% (p<0,001). При лечении обоими препаратами было отмечено достоверное улучшение показателей качества жизни, которое оценивали с помощью SF-36 и специального вопросника, предназначенного для больных ВЗК. Переносимость двух препаратов была хорошей. Несмотря на более высокую стоимость железа карбоксимальтозата общие затраты на его применение оказались ниже, чем в группе сравнения, за счет уменьшения числа инфузий. Таким образом, исследование показало, что применение железа карбоксимальтозата для лечения железодефицитной анемии у больных более эффективно, чем введение железа сахарата, и позволяет сократить число инфузий и общие затраты.
После завершения исследования FERGI 204 больных были включены в рандомизированное контролируемое исследование и продолжили лечение карбоксимальтозатом железа или плацебо в течение еще 8 месяцев [23]. Целью исследования было изучить эффективность препарата железа в профилактике рецидивов железодефицитной анемии, которая нередко развивается вновь после завершения терапии. Исследуемый препарат вводили каждый второй месяц, если уровень ферритина снижался менее 100 мкг/л. Развитие анемии наблюдали у 26,7% и 39,4% пациентов основной группы и группы плацебо, соответственно. Лечение карбоксимальтозатом железа сопровождалось также значительным увеличением времени до рецидива анемии (р=0,049). В основной группе уровень ферритина увеличился в среднем на 30,3 мкг/л, а степень насыщения трансферрина — на 0,6%, в то как в группе плацебо эти показатели снизились на 36,1 мкг/л и 4,0%, соответственно. Частота нежелательных явлений, в том числе серьезных, была сходной в двух группах. Тем не менее, частота рецидивов анемии в основной группе была достаточно высокой, что обосновывает необходимость оптимизации лечения железосодержащими препаратами.
Неэффективность или недостаточная эффективность железосодержащих препаратов может объясняться тем, что причиной снижения уровня гемоглобина является анемия хронических заболеваний или реже другие причины. Предполагать анемию хронических заболеваний следует также в тех случаях, когда уровень ферритина превышает 100 мкг/л. Если лечение препаратами железа в адекватной дозе не приводит к увеличению уровня гемоглобина по крайней мере на 2 г/дл или его нормализации в течение 4 недель, то у больных с его концентрацией ниже 10 г/дл возможно применение препаратов, стимулирующих эритропоэз [8]. При стимуляции эритропоэза под действием эритропоэтина скорость мобилизации железа из депо становится недостаточной для обеспечения возросших потребностей костного мозга. Пролиферирующим эритробластам необходимо все большее количество железа, что приводит к истощению лабильного пула железа и снижению сывороточного уровня ферритина. В связи с этим лечение эритропоэтином сочетают с внутривенным введением препаратов железа. Эффективность стимуляторов эритропоэза у больных болезнью Крона изучалась в небольших исследованиях. C.Gasche и соавт. [24] в двойном слепом рандомизированном исследовании у 40 больных с болезнью Крона и концентрацией гемоглобина <10,5 г/дл в течение 16 недель применяли железа сахарат с эритропоэтином или плацебо. Частота ответа на лечение в основной и контрольной группе составила 95% и 75%, соответственно (разница не достигла статистической значимости). Тем не менее, лечение эритропоэтином привело к более выраженному увеличению уровня гемоглобина по сравнению с плацебо (р=0,004). У всех пациентов, не ответивших на лечение, назначение эритропоэтина или титрование его дозы позволило достичь увеличения уровня гемоглобина. Полученные данные свидетельствуют о том, что у большинства больных болезнью Крона, осложнившейся анемией, эффективна монотерапия препаратами железа, однако при отсутствии требуемого ответа назначение эритропоэтина приводит к увеличению концентрации гемоглобина. Эту точку зрения подтверждают результаты других исследований. Например, I.Koutroubakis и соавт. [25] у 20 больных ВЗК и рефрактерной анемией наблюдали достоверное увеличение средней концентрации гемоглобина с 9,48 до 12,71 г/дл (p<0,0001) в течение 4 недель в результате еженедельного введения дарбэпоэтина-α в сочетании с железа сахаратом. Частота ответа на лечение составила 75%.
Заключение
Болезнь Крона часто осложняются анемией, которая в большинстве случаев связана с дефицитом железа. Препаратами выбора в лечении железодефицитной анемии у больных болезнью Крона считают внутривенные препараты железа, которые обладают высокой эффективностью, позволяют быстро восполнить запасы железа и переносятся лучше, чем пероральные железосодержащие средства. Для внутривенного введения применяют сферические железоуглеводные коллоиды (карбоксимальтозат, сахарат, глюконат и декстран). Углеводная оболочка обеспечивает стабильность комплекса, замедляет высвобождение железа и поддерживает образующиеся формы в коллоидной суспензии. Преимуществом карбоксимальтозата железа перед другими внутривенными препаратами железа является возможность однократного введения большой дозы железы (1000 мг за 15 минут), что позволяет восстановить показатели обмена железа за 2-3 инфузии. При неэффективности железосодержащих препаратов у больных тяжелой анемией возможно назначение стимуляторов эритропоэтина, хотя опыт их применения при болезни Крона ограничен.
ЛИТЕРАТУРА
1. Gisbert J., Gomollon F. Common misconceptions in the diagnosis and management of anemia in inflammatory bowel disease. Am. J. Gastroenterol., 2008, 103, 1299-1307.
2. Kullnigg S., Gasche C. Systemic review: managing anaemia in Crohn’s disease. Aliment. Pharmacol. Ther., 2006, 24, 1507-1523.
3. Ershler W., Chen K., Reyes E., Dubois R. Economic burden of patients with anemia in selected diseases. Value Health, 2005, 8, 629-638.
4. Stein J., Hartmann F., Dignas A. Diagnosis and management of iron deficiency anemia in patients with IBD. Nat. Rev. Gastroenterol. Hepatol., 2010, 7 (11), 599-610.
5. Collins, J., Wessling-Resnick M., Knutson M. Hepcidin regulation of iron transport. J. Nutr., 2008, 138, 2284-2288.
6. Wrighting D., Andrews N. Interleukin-6 induces hepcidin expression through STAT3. Blood, 2006, 108, 3204-3209.
7. Knutson M. Iron-sensing proteins that regulate hepcidin and enteric iron absorption. Annu. Rev. Nutr., 2010, 30, 149-171.
8. Gasche C., Berstad A., Befrits R. et al. Guidelines on the diagnosis and management of iron deficiency and anemia in inflammatory bowel diseases. Inflamm. Bowel Dis., 2007, 13 (12), 1545-1553.
9. Козловская Л.В., Рамеев В.В., Саркисова И.А. Патогенез и клиническое значение анемии хронических заболеваний. Анемия, 2005, 4, 4-10.
10. Thomas C., Thomas L. Biochemical markers and hematologic indices in the diagnosis of functional iron deficiency. Clin. Chem., 2002, 48, 1066-1076.
11. Mast A., Blinder M., Dietzen D. Reticulocyte hemoglobin content. Am. J. Hematol., 2008, 83, 307-310.
12. Auerbach M., Ballard H., Glaspy J. et al. Clinical update: intravenous iron for anaemia. Lancet, 2007, 369, 1502-1504.
13. Zhu A., Kaneshiro M., Kaunitz J. Evaluation and treatment of iron deficiency anemia: a gastroenterological perspective. Dig. Dis. Sci., 2010, 55, 548-559.
14. Rimon E. et al. Are we giving too much iron? Low-dose iron therapy is effective in octogenarians. Am. J. Med., 2005, 118, 1142-1147.
15. Ganzoni A. Intravenous iron-dextran: therapeutic and experimental possibilities [German]. Schweiz. Med. Wochenschr., 1970, 100, 301-303.
16. Semrin G., Fishman D., Bousvaros A. et al. Impaired intestinal iron absorption in Crohn’s disease correlates with disease activity and markers of inflammation. Inflamm. Bowel Dis., 2006, 12, 1101-1106.
17. Aghdassi E., Carrier J., Cullen J. et al. Effect of iron supplementation on oxidative stress and intestinal inflammation in rats with acute colitis. Dig. Dis. Sci., 2001, 46, 1088-1094.
18. Erichsen K., Ulvik R., Nysaeter G. et al. Oral ferrous fumarate or intravenous iron sucrose for patients with inflammatory bowel disease. Scand. J. Gastroenterol., 2005, 40 (9), 1058-1065.
19. Моисеев С.В. Железа карбоксимальтозат (Феринжект) - новый внутривенный препарат для лечения. Клин. фармакол. тер., 2012, 21 (2), 48-53.
20. Geisser Р. The pharmacology and safety profile of ferric carboxymaltose (Ferinject®): structure/reactivity relationships of iron preparations. Port. J. Nephrol. Hypert., 2009, 23 (1), 11-16.
21. Kulnigg S., Stoinov S., Simanenkov V. et al. A novel intravenous iron formulation for treatment of anemia in inflammatory bowel disease: the ferric carboxymaltose (FERINJECT®) randomized controlled trial. Am. J. Gastroenterol., 2007, 103 (5), 1182-1192.
22. Evstatiev R., Marteau P., Iqbal T. et al.; FERGI Study Group. FERGIcor, a randomized controlled trial on ferric carboxymaltose for iron deficiency anemia in inflammatory bowel disease. Gastroenterology, 2011, 141 (3), 846-853.
23. Evstatiev R., Alexeeva O., Bokemeyer B. et al.; FERGI Study Group. Ferric carboxymaltose prevents recurrence of anemia in patients with inflammatory bowel disease. Clin. Gastroenterol. Hepatol., 2012, Oct 16. pii: S1542-3565( 12)01212-8. [Epub ahead of print].
24. Gasche C, Dejaco C, Waldhoer T, Tillinger W, Reinisch W, Fueger GF, Gangl A., Lochs H. Intravenous iron and erythropoietin for anemia associated with Crohn disease. A randomized, controlled trial. Ann. Intern. Med., 1997, 126 (10), 782-787.
25. Koutroubakis I., Karmiris K., Makreas S. et al. Effectiveness of darbepoetin-alfa in combination with intravenous iron sucrose in patients with inflammatory bowel disease and refractory anaemia: a pilot study. Eur. J. Gastroenterol. Hepatol., 2006, 18 (4), 421-425.
