Применение препарата «Пантовигар» для лечения диффузного телогенного выпадения волос у женщин
СтатьиОпубликовано в журнале:
«Вестник Эстетической Медицины», 2008, том 7, №2 с. 1-8
Т. В. Цимбаленко, дерматолог-трихолог Центра эстетики и здоровья «Валентина»
В. П. Ткачев, трихолог, руководитель курса трихологии РУДН
О. С. Панова, профессор кафедры эстетической медицины ФПК МР РУДН, президент ОЭМ, генеральный директор МЦКК «Эклан» РАН
В рандомизированном исследовании с оценкой результатов слепым методом исследовалась эффективность препарата «Пантовигар» («Мерц Фарма») при диффузном выпадении волос у практически здоровых женщин. Критерием включения являлось исходное превышение нормального количества волос в стадии телогена более чем на 15%. Действие препарата оценивалось по интенсивности выпадения, плотности и диаметру волос, в том числе диспластичных. Полученные данные свидетельствуют о высокой результативности лечения диффузной телогенной алопеции «Пантовигаром».
Диффузное телогенное выпадение волос является наиболее часто встречающейся формой выпадения волос у женщин [16,13, 22, 26, 27, 28, 31]. Оно может протекать как в острой, так и в хронической форме.
Острая телогенная алопеция длится менее 6 месяцев, а затем спонтанно проходит; хроническая продолжается более 6 месяцев, иногда в течение нескольких лет. Постановка диагноза острого телогенного выпадения обычно не вызывает затруднений: внезапное начало и связь с перенесенной лихорадкой, приемом лекарств, психоэмоциональным стрессом облегчают диагностику [13, 21]. Эта форма диффузного телогенного выпадения волос имеет благоприятный прогноз и зачастую не требует лечения в связи с краткосрочностью вызвавшего ее фактора.
Больные с хронической формой телогенной алопеции отмечают длительное сильное выпадение волос с волнообразным течением процесса. В таких случаях обязательно исключение соматической патологии: гиперандрогении, гипо- и гипертиреоза, дефицитных состояний [9, 11, 18, 25, 27]. Однако четкой причины алопеции этой формы приблизительно в 30% случаев обнаружить не удается [27]. Сопровождающие ее невротические расстройства очень часто служат фактором, усугубляющим течение заболевания, или даже основной причиной хронизации [11, 15, 29]. Дифференциальная диагностика данной формы выпадения волос осложняется тем, что и андрогенная алопеция на начальной стадии также отличается равномерным характером поредения и невысоким процентом истонченных волос (происходит своего рода имитация диффузного выпадения волос).
В патогенезе диффузной алопеции и структурных повреждений волос огромную роль играют процессы метаболизма, проходящие на уровне волосяных фолликулов: от уровня обмена веществ напрямую зависит сопротивляемость волоса внешним неблагоприятным воздействиям, а также его рост. Для полноценного развития волос волосяной фолликул должен получать необходимые питательные вещества: аминокислоты, минералы, белки, витамины. Поэтому при лечении пациентов с диффузным выпадением волос наибольший эффект достигается именно стимуляцией метаболизма в волосяных фолликулах.
Спектр препаратов, обладающих стимулирующим воздействием на корни волос, достаточно узок. Применение средств на основе миноксидила у женщин при отсутствии явных признаков андрогенного выпадения волос ограничено, так как длительный, а зачастую постоянный прием препаратов, сопровождающийся нежелательными побочными эффектами, не оправдан при многих формах диффузного телогенного выпадения волос. Имеющиеся на рынке лекарственные средства не всегда удовлетворяют запросы современных потребителей, да и требования к состоянию волос возросли. Поэтому производство эффективных и безопасных препаратов, обладающих стимулирующим воздействием на рост волос, становятся все более актуальным.
ИССЛЕДОВАНИЕ ПРЕПАРАТА ДЛЯ ЛЕЧЕНИЯ ДИФФУЗНОЙ ТЕЛОГЕННОЙ АЛОПЕЦИИ У ЖЕНЩИН «ПАНТОВИГАР»
В Медицинском центре косметологической коррекции «Эклан» было проведено рандомизированное открытое исследование препарата «Пантовигар» («Мерц Фарма»).
Цель исследования — изучение действенности терапии препаратом «Пантовигар» при диффузном телогенном выпадении волос у практически здоровых женщин.
Оценка эффективности проводилась слепым методом.
Критерии включения. В группу добровольцев для участия в испытаниях включались женщины в возрасте от 18 до 45 лет при наличии жалоб на выпадение волос. Пациентки, имеющие клинические признаки андрогенной алопеции (поредение волос 1-2 степени по Людвигу), также участвовали в исследовании. При соответствии пациентки критериям включения и подписании ею информированного согласия она входила в состав испытуемых.
Критерии исключения. В группу испытуемых не включались женщины, имеющие:
- симптоматическое выпадение волос на фоне железодефицита, гипо- и гипертиреоза,
- гиперандрогению (поликистоз яичников, адреногенитальный синдром, опухоли яичников),
- системные аутоиммунные заболевания,
- поредение волос 3-й степени по Людвигу,
- очаговую и рубцовую формы алопеций; а также
- принимающие препараты, приводящие к потере волос,
- получающие заместительную гормонотерапию или принимающие оральные контрацептивы в течение 6 месяцев до начала исследования,
- беременные и кормящие.
Подготовительный период исследования
Диагноз диффузной телогенной алопеции ставился на основании превышения нормального количества волос в стадии телогена более чем на 15% в лобнотеменной и затылочной зонах по фототрихограмме при исключении других причин выпадения.
В процессе сбора анамнеза определялось, когда началось выпадение волос, его тип и продолжительность, наличие или отсутствие поредения волос. Также уточнялись следующие факторы: перенесенные заболевания, операции, прием гормональных препаратов, характер диеты. Проводилось лабораторное исследование уровня ферритина (более 20 мг/л) и TSH (0,27-4,2 mU/I). Было сформировано две группы: рабочая (группа исследования) — 20 человек и контрольная — 20 человек. Женщины в обеих группах были сопоставимы по возрасту и состоянию волос.
Возраст пациенток:
1 группа — от 18 до 45 лет (средний возраст — 31 год),
2 группа — от 20 до 44 лет (средний возраст — 34 года).
Исходное состояние волос:
- отсутствие поредения волос — у 29 женщин (14 — в 1 группе, 15 — во 2-й);
- разрежение волос 1-й степени по Людвигу — у 7 женщин (3 — в 1-й группе, 4 — во 2-й);
- разрежение волос 2-й степени по Людвигу — у 2 женщин (1 — в 1-й группе, 1 — во 2-й).
Методы исследования и техническое обеспечение
Препарат «Пантовигар» принимался пациентками в рабочей группе по 1 капсуле 3 раза в день во время еды в течение 4 месяцев.
В контрольной группе препарат не принимался.
В обеих группах трехкратно (до лечения, через 3 месяца и через 4 месяца после начала приема препарата) проводились следующие исследования:
- обзорные фотографии волосистой части головы,
- определение плотности волос (количества волос на 1 см2) в стандартных точках теменной и затылочной зон,
- определение среднего диаметра волос в стандартных точках теменной и затылочной зон,
- подсчет количества волос, подобных пушковым (менее 30 мкм), в теменной и затылочной зонах (в %),
- фототрихограммы с контрастированием в стандартных точках с подсчетом количества телогенных и анагенных волос (в %).
Для исследования выбривался участок волос площадью 8х8 мм в стандартной точке в андрогензависимой (теменной) зоне и аналогичный по размеру участок в стандартной точке в андрогеннезависимой (затылочной) зоне.
Спустя 48 часов выбритые участки окрашивались краской для бровей и ресниц (Londa, Германия). Краска фиксировалась в течение 10 минут, после чего остатки смывались этиловым спиртом. Исследование проводилось при помощи видеокамеры Dolphin (Корея) c линзой, соединенной с ПК, с увеличением х50.
Результаты исследования обрабатывались специализированной компьютерной программой Trichoscience v. 1.3. Проводился подсчет общего количества волос на выбритом участке, а также волос в фазе роста и фазе выпадения. Волосы в фазе анагена отрастали за 48 часов в среднем на 0,75 мм, волосы в фазе телогена за данный временной интервал не отрастали.
В исследуемых зонах также подсчитывалось количество истонченных волос диаметром менее 30 мкм (подобных пушковым).
Диаметр волос в теменной и затылочной зонах определялся при помощи компьютерной программы Trichoscience, при увеличении линзы х200.
Результаты лечения
Из 40 испытуемых завершили исследование 38 человек. У одной пациентки при приеме «Пантовигара» развилась аллергическая реакция по типу аллергического дерматита, в связи с чем прием препарата был прекращен. Данное побочное действие можно связать с индивидуальной непереносимостью пациенткой витаминов группы В, о чем она не сообщила до начала приема препарата. Еще одна пациентка самостоятельно прекратила прием «Пантовигара» в связи с наступлением беременности, поэтому была исключена из исследования.
Подсчет количества волос в стадии телогена* проводился до начала исследования, через 3 месяца и через 4 месяца приема препарата «Пантовигар» (табл. 1). Процент волос в стадии телогена в теменной зоне до начала лечения был сопоставим в 1-й и 2-й группе: 21% и 22 % соответственно.
*Резулътаты всех подсчетов количества волос представлены в процентном выражении.
Таблица 1. Динамика изменения количества волос (в %) в стадии телогена.
| Средние значения % волос в стадии телогена | Группа исследования (n=18) |
Группа контроля (n=20) |
| До начала лечения N±S | 21 (±6,5) | 22 (±3,2) |
| Через 3 месяца лечения N±S | 18 (±6,7) ** | 21 (±4,8)** |
| Через 4 месяца лечения N±S | 14 (±6,9) * | 23 (±5,2)** |
Примечание: n — количество испытуемых; * p0,054.
Через 3 месяца приема препарата в обеих группах у пациенток отмечалось некоторое уменьшение количества выпадающих волос: в 1-й группе — 18% телогенных волос, во 2-й — 21%.
Через 4 месяца приема препарата количество телогенных волос у добровольцев, принимавших «Пантовигар», составило 14% . В группе контроля процент волос в стадии телогена был сопоставим с исходным (23%).
| Фототрихограмма 1. |
 |
| До начала лечения.
Анагенных волос всего 79%, телогенных — всего 21%. |
 |
| Через 4 месяца после начала лечения.
Анагенных волос всего 93%, телогенных — всего 7%. |
| Фототрихограмма 2. |
 |
| До начала лечения.
Анагенных волос всего 75%, телогенных — всего 25%. |
 |
| Через 4 месяца после начала лечения.
Анагенных волос всего 87%, телогенных — всего 13%. |
| Фототрихограмма 3. |
 |
| До начала лечения.
Анагенных волос всего 78%, телогенных — всего 22%. |
 |
| Через 4 месяца после начала лечения.
Анагенных волос всего 85%, телогенных — всего 15%. |
Данные об изменении диаметра волос в теменной зоне и количества диспластичных волос у пациенток обеих групп отражает таблица 2. У женщин, принимавших «Пантовигар», до начала приема препарата средний диаметр волос в теменной зоне составлял 55 мкм, количество диспластичных волос (с диаметром менее 30 мкм) — 24%. В группе контроля средний диаметр волос и количество диспластичных волос у испытуемых были сопоставимы по значениям, 53 мкм и 22% соответственно.
Таблица 2. Изменения диаметра волос в теменной зоне.
| Изменения диаметра волос в теменной зоне (мкм) | Группа исследования (n=18) |
Группа контроля (n=20) |
| Средний диаметр волос в теменной зоне до начала исследования N±S (мкм) | 55 (±7,9) | 53 (±5,7) |
| Средний диаметр волос после 4 месяцев исследования N±S (мкм) | 62 (±6,1) ** | 51 (±5,3)* |
| % диспластичных волос до начала исследования N ±S | 24 (±7,6) | 22 (±6,8) |
| % диспластичных волос после 4 месяцев исследования N ±S | 15 (±4,5) *** | 23 (±6,1)* |
Примечание: n — количество испытуемых; * p>0,05; ** p
Через 4 месяца после начала приема «Пантовигара» в рабочей группе у пациенток наблюдалось статистически значимое утолщение волос — до 62 мкм (р0,05).
Подсчет плотности волос в теменной и затылочной зонах в обеих группах не показал статистически значимых изменений (табл. 3).
Таблица 3. Изменение плотности волос в теменной и затылочной зонах.
|
Средняя плотность волос |
Группа исследования (n=18) | Группа контроля (n=20) | ||
| До начала |
Через 4 месяца | До начала |
Через 4 месяца | |
| Плотность волос в теменной зоне (на 1 см2) N±S | 296 (±67,6) |
285* (±77,6) |
285 (±49) |
287* (±46) |
| Плотность волос в затылочной зоне (на 1 см2) N ±S | 272 (±61,4) |
281* (±74,3) |
256 (±50) |
252* (±55,1) |
Примечание: n — количество испытуемых; * (р>0.05)
Субъективная оценка состояния волос. После курса лечения препаратом «Пантовигар» пациентки отмечали:
- снижение выпадения волос — в 10 случаях (56%),
- улучшение внешнего вида — в 16 случаях (89%),
- увеличение скорости роста — в 13 случаях (72%),
- снижение сальности кожи волосистой части головы — в 8 случаях (44%),
- общее улучшение состояния кожных покровов вне волосистой части головы (снижение сальности кожи лица, груди и уменьшение количества папулопустулезных элементов) — в 2 случаях (11%) (табл. 4).
Таблица 4. Субъективная оценка пациентками состояния волос и кожи головы через 4 месяца.
| Субъективные характеристики состояния волос | Группа исследования (n=18) | Группа контроля (n=20) |
| Снижение выпадения | 10 (56%) | 4 (20%) |
| Улучшение внешнего вида | 16 (89%) | 3 (15%) |
| Увеличение скорости роста | 13 (72%) | 4 (20%) |
| Снижение сальности | 8 (44%) | 0 (0%) |
| Улучшение состояния кожи | 2 (11%) | 0 (0%) |
Примечание: n — количество испытуемых.
В целом препарат переносился хорошо. У 2 пациенток отмечались временные диспепсические явления, самопроизвольно прекратившиеся.
ЗАКЛЮЧЕНИЕ
Витамины группы В (в том числе пантотеновая и парааминобензойная кислоты), а также L-цистеин традиционно включаются в препараты для лечения и профилактики выпадения волос. К настоящему времени выполнено большое количество актуальных исследований как по отдельным витаминам группы В, так и по группе в целом [14, 11].
В основе лечения диффузного телогенного выпадения волос «Пантовигаром» лежит воздействие на клетки матрикса волосяного фолликула аминокислот и витаминов группы В, в оптимальном сочетании входящих в состав данного препарата. Суточная дозировка препарата «Пантовигар» содержала:
- тиамин — 180 мг,
- экстракт медицинских дрожжей — 300 мг,
- D-пантотенат кальция — 180 мг,
- L-цистеин — 60 мг,
- ПАБК — 60 мг.
Тиамин, как и другие витамины группы В (в том числе пантотеновая кислота), — это прежде всего кофермент важнейших ферментов, обеспечивающих функционирование клетки, особенно митохондрий. Митохондрии — главные внутриклеточные органеллы, производящие молекулы АТФ: витамин B1 в результате процессов фосфорилирования превращается в кокарбоксилазу — фермент, который и участвует в обеспечении энергетического ресурса клетки.
Парааминобензойная кислота, входящая в состав фолиевой кислоты и ее производных, оказывает влияние на пигментацию волос.
Экстракт медицинских дрожжей включен в состав препарата как природный комплекс витаминов группы В, аминокислот, минералов и белков.
L-цистеин — природная серосодержащая аминокислота, структурная основа кератина, находится в большом количестве в стержне волоса — 15,9%. Является мощным антиоксидантом. Известны патологии стержня волос и виды алопеций, связанные с дефицитом L-цистеина (трихотиодистрофия, ВИЧ-ассоциированная алопеция). Диета с полноценным содержанием аминокислот с серой (цистеин, метионин) приводит к улучшению качества волос, а также повышает их воспроизводство [25, 31, 32]. В экспериментах на животных с применением метода авторадиографии было установлено, что аминокислоты, подобные L-цистеину, оказывают положительное влияние на пролиферацию и рост волос.
Благодаря применению препарата «Пантовигар» клетки матрикса волосяного фолликула, обладающие сильной митотической активностью и высоким метаболизмом, обеспечиваются необходимыми для их жизнедеятельности аминокислотами и большими дозами витаминов группы В.
Известно, что и методы, наиболее активно стимулирующие рост волос (лечение миноксидилом, лазеролечение), направлены прежде всего на активизацию митотической и пролиферативной активности волосяного фолликула.
С целью изучения влияния «Пантовигара» на качество и рост волос проводились многочисленные до- и постклинические испытания, результаты которых показывали увеличение доли анагенных волос после завершения курса лечения, нормализацию числа ежедневно теряемых волос, значительное улучшение показателей при подсчете анагенных волос, при этом отмечалось отсутствие улучшения по данным подсчета общего числа волос, их плотности и общей толщины [6, 8, 17, 19, 20]. По мнению исследователей, это было связано с тем, что «Пантовигар» селективно влияет на телогенное облысение, возникающее вследствие феномена синхронизации циклов роста волос, и эффект препарата связан, вероятно, с индукцией именно фазы анагена.
В предлагаемом исследовании, проведенном Медицинским центром косметологической коррекции «Эклан», было установлено, что в результате применения препарата «Пантовигар» для лечения диффузной телогенной алопеции наряду с увеличением количества анагенных волос происходит увеличение среднего диаметра волоса в фазе телогена, в том числе за счет утолщения волос, подобных пушковым.
После 4 месяцев применения «Пантовигара» у пациенток, входивших в 1-ю группу, отмечалось статистически значимое (pЗначимое улучшение состояния волос, заметное на обзорных фотографиях проблемных зон волосистой части головы, отмечалось в группе наблюдаемых, принимавших препарат, а не в группе контроля (фото 1-2). Объяснением полученных данных может служить влияние препарата на повышение количества терминальных волос в стадии анагена, что свидетельствует о его способности оказывать хорошее стимулирующее воздействие на рост волоса.
Фото 1. До начала и через 4 месяца после начала лечения.
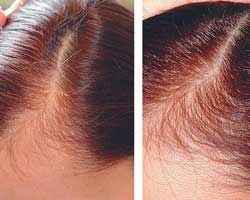
Фото 2. До начала и через 4 месяца после начала лечения.
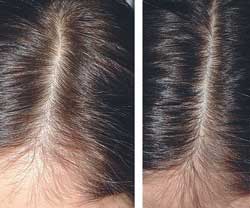
Препарат «Пантовигар», выпускаемый компанией «Мерц Фарма», может быть рекомендован для лечения диффузного телогенного выпадения волос у женщин, а также в составе комплексной терапии для лечения андрогенной алопеции у женщин.
ЛИТЕРАТУРА
1. Скальная М.Г., Дубовой Р.М., Скальный А.В. Химические элементы-микронутриенты как резерв восстановления здоровья жителей России. - Оренбург, - 2004. - 239 с.
2. Спиричев В.Б. Витамины, витаминоподобные и минеральные вещества. - М, 2004.
3. Спиричев В.Б., Шатнюк Л.Н., Позднянский В.М. Обогащение пищевых продуктов витаминами и минераль-ными веществами. Новосибирск, 2004. - 547 с.
4. Тищенко Л.Д. Витамины в дерматологии. - М., 1987.
5. Ahrens J. Systemische Behandlung des diffusen Haarausfalls. Therapiewoche Schweiz, 1994. - 10: 551-554.
6. Bergner T. Diffuse effluvium, damage to hair structure, and disturbances of nail growth treated successfully, Results of a multicenter study, Dt Derm. - 1999. - 47: 881-884.
7. Budde J., TronnierH., Rahlfs V.W., Frei-Kleiner S. Systemic therapy of diffuse effluvium and hair structure damage. Hautarzt. - 1993. - 44: 380-384.
8. Budde J., Tronnier H., Rahlfs V.W., Frei-Kleiner S. Systemische Therapie von diffusem Effluvium und Haarstrukturschdden. Hautarzt 1. -1993.- 44: 380-384.
9. GarcHa-Hern6ndez M.J., Camacho F.M. Chronic telogen effluvium: incidence, clinical and biochemical features, and treatment. Arch. Dermatol.- 1999. - 135:1123-1124.
10. Gehring W, Gloor M. Das Phototrichogramm als Verfahren zur Beurteilung haarwachstumsfurdernder Prdparate am Beispiel einer Kombination von Hirsefruchtextrakt, L-Cystin und Calciumpantothenat. Zeitschrift fbr Hautkrankheiten 2000; 75: 419-423.
11. Girman C.J., Hartmaier S., Roberts J., Bergfeld W., Waldstreicher J. Patient-perceived importance of negative effects of androgenetic alopecia in women. J Womens Health Gend Based Med. 1999 Oct. - 8(8): 1091-5.
12. GoetteD.U., Odum R.B. Alopecia in crash dieters. JAMA. - 1976. - 235: 2622-2623.
13. Guy W.B., Edmundson W.F. Diffuse cyclic hair loss in women. Arch Dermatol. - 1960. - 81: 205-27.
14. Headington J.T. Telogen effluvium. Arch Dermatol. - 1993. - 129: 356-363.
15. Holzegel K. Zur Behandlung das Effluviums. Ergebnisse einer Feldstudie mit Pantogar. Swiss Med. - 1985. - 7/5b: 29-33.
16. Ina M. Hadshiew, Kerstin Foitzik, Petra C. Arck and RalfPaus. Burden of Hair Loss: Stress and the Underestimated Psychosocial Impact of Telogen Effluvium and Androgenetic Alopecia. Journal of Investigative Dermatology. - 2004. - 123, 455-457.
17. Kligman A.M. Pathologic dynamics of human hair loss. Telogen effluvium. Arch Dermatol. - 1961. - 83:175-198.
18. Lengg N., Heidecker B., Seifert B., Tneb R. The value of dietary supplements: results of a double-blind placebo controlled study with oral combination of cystine, yeast and pantothenic acid. Future medicine, Therapy. - 2007. - № 4.
19. Odom R.B., James W.D., Berger T.G. Nutritional diseases. In: Andrew’s diseases of the skin. 9th edition. Philadelphia: W.B. Saunders. 2000. - 606-615.
20. Petri H., Perchalla P., Tronnier H. Die Wirksamkeit einer medikamentu,sen Therapie bei Haarstrukturschdden und dif- fusen Effluvien - vergleichende Doppelblindstudie. Schweiz Rundsch Med Prax . - 1990. - 79: 1457-1462.
21. Pfitzer H. Methodische Untersuchungen bber die Wirkung einer medikamentu,sen Behandlung auf die Haarqualitdt. Dissertation Tbbingen. - 1971.
22. Pillans P.I., Woods D.J. Drug induced alopecia. Int J Dermatol. - 1995. - 34:149-158.
23. Rand S. Chronic telogen effluvium: potential complication for clinical trials in female androgenetic alopecia? [Letter] J Am Acad Dermatol. - 1997. - 37:1021.
24. Randall V.A., Ebling F.J.G. Seasonal changes in human hair growth. Br J Dermatol. - 1991. - 124:146-151.
25. Randall V. Randall V.A. The biology of androgenetic alopecia. In: FM Camacho, VA Randall, VH Price (eds.) Hair and its Disoders.-London, Martin Dunitz, 2000. - 123-136.
26. Rebora A. Telogen effluvium. Dermatology. - 1997. - 195: 209-212.
27. SperlingL.C., Mezebish D.S. Hair disease. Med Clin North Am. - 1998.
28. SulzbergerM.B., Witten V.H., Kopf A.W. Diffuse alopecia in women. Its unexplained apparent increase in incidence. Arch Dermatol. - 1960. - 81: 556-560.
29. Trueb R.M. Das idiopathische chronische Telogeneffluvium der Frau. Hautarzt. - 2000. - 51: 899-905.
30. Whiting D.A. Chronic telogen effluvium: increased scalp hair shedding in middle-aged women. J Am Acad Dermatol. - 1996. - 35: 899-906.
31. Wilma F. Bergfeld, Fabiane Mulinari-Brenner, Shedding. How to manage a common cause of hair loss. Cleveland Clinic J.of Medicine. - V. 68. - № 3. - March, 2001. - P. 256-261.9.
