Постинфарктная ишемическая митральная регургитация у пациентов пожилого и старческого возраста
СтатьиЖелнов В. В., Андреева Н. В., Щеглова Ю. М., Комарова И. С.
ГБОУ ВПО «Первый МГМУ имени И. М. Сеченова» МЗ РФ, 119991, Москва, ул. Трубецкая, д. 8, стр. 2 Ключевые слова: инфаркт миокарда, митральная регургитация, пожилой возраст, старческий возраст
Keywords: myocardial infarction, mitral regurgitation, elderly age, senile age
Ссылка на эту статью: Желнов В. В., Андреева Н. В., Щеглова Ю. М. и др. Постинфарктная ишемическая митральная регургитация у пациентов пожилого и старческого возраста. Журнал Сердечная Недостаточность. 2014;82 (1):9–13.
Резюме
Актуальность. Ишемическая митральная регургитация (ИМР) играет существенную роль в развитии СН и определяет прогноз заболевания у пациентов с ИМ. В настоящее время не выяснено взаимное влияние ИМР, систолической и диастолической функций ЛЖ на развитие СН, особенно у пациентов с острым ИМ пожилого и старческого возраста. В проведенном нами исследовании оценивалось влияние ИМР на клиническое течение острого ИМ у пациентов разных возрастных групп. Материалы и методы. Обследовано 124 пациента с острым Q-ИМ. Пациенты были разделены на 2 группы в соответствии с возрастом. Средний возраст пациентов до 60 лет (средняя возрастная группа) составил 45,4±6,8 лет, после 60 лет (старшая возрастная группа) – 71,3±6,1 лет. В процессе стандартного ЭхоКГ исследования пациентов количественные показатели ИМР определяли двумя допплер–ЭхоКГ методами исследования: цветовое допплеровское картирование площади проксимальной изоскоростной поверхности сходящегося потока регургитации (PISA-метод) и метод количественной допплер–ЭхоКГ (Q-DE-метод). Результаты. У пациентов средней возрастной группы с острым ИМ с зубцом Q на ЭКГ, ФВ 47,9±6,60 % и фракцией митральной регургитации 20,14±7,9 % острая СН (ОСН) (Killip II–III) развивалась в 37,5 % случаев. Тогда как у пациентов старшей возрастной группы острый ИМ с зубцом Q, ФВ 47,7±6,5 % и фракцией митральной регургитации 20,3±6,4 % ОСН (Killip II–III) была отмечена в 73,5 % случаев (р=0,0001). У пациентов старшей возрастной группы в бoльшем проценте случаев (80 %), чем у пациентов средней возрастной группы (51,8 %), наблюдалось изменение трансмитрального кровотока по типу «нарушения релаксации» ЛЖ (р=0,006). Заключение. В остром периоде ИМ у пациентов пожилого и старческого возраста (старшая возрастная группа) появление нетяжелой митральной регургитации на фоне характерного для этой возрастной группы нарушения релаксации ЛЖ в 2 раза чаще приводит к развитию клинически значимой ОСН (Killip II–III), чем у пациентов молодого и среднего возраста (средняя возрастная группа).
Summary
Background. Ischemic mitral regurgitation (IMR) plays an important role in development of HF and determines the prognosis in patients with myocardial infarction (MI). At present time, the mutual effect of IMR and LV systolic and diastolic function on development of HF is not known, especially in elderly and senile patients with acute MI. Our study evaluated the effect of IMR on the clinical course of acute MI in patients of different age groups. Materials and methods. 124 patients with acute Q-MI were evaluated. Patients were divided into two groups by age. Mean age of patients younger than 60 (mid-age group) was 45.4±6.8 years; mean age of patients older than 60 (older age group) was 71.3±6.1 years. Quantitative IMR variables were measured by the study standard EchoCG using two Doppler EchoCG methods: color Doppler mapping of the proximal isovelocity surface area (PISA) of regurgitation flow convergence and the method of quantitative Doppler-EchoCG (Q-DE method). Results. Acute HF (AHF) (Killip II–III) developed in 37.5 % of mid-age group patients with acute Q-MI, EF 47.9±6.60 % and mitral regurgitation fraction 20.14±7.9 %. In patients of the older age group with acute Q-MI, EF 47.7±6.5 % and mitral regurgitation fraction 20.3±6.4 %, AHF (Killip II–III) was observed in 73.5 % of cases (р=0.0001). Changes in the transmitral flow of the «impaired LV relaxation» type were observed in a greater proportion of older age group (80 %) than in the mid-age group (51.8 %) (р=0.006). Conclusion. In the acute period of MI, mild mitral regurgitation associated with typical age-related disturbance of LV relaxation results in clinically significant AHF (Killip II–III) in elderly and senile (older age group) patients twice as frequently as in younger patients (mid-age group).
Результаты исследований последних лет показали, что у большинства пациентов с Q-ИМ течение заболевания осложняется ишемической митральной регургитацией (ИМР), играющей существенную, а иногда и основную роль в развитии СН [1–3]. ИМР развивается в результате деформации структур митрального клапана (МК) у пациентов с ИМ [4, 5].
Проблема ИМР находится в настоящее время в стадии накопления знаний и опыта, направленного на понимание тонких патофизиологических механизмов ее развития, совершенствования методов диагностики и оптимизации лечения. На основании проведенных исследований было показано, что при тяжелой ИМР у пациентов с ИМ практически всегда развивается СН [1, 2, 6], но до настоящего времени не выяснена взаимосвязь между ИМР, систолической и диастолической функцией ЛЖ и комплексная роль этих показателей в развитии СН, особенно у пациентов с ИМ пожилого и старческого возраста. В последние десятилетия наблюдается увеличение продолжительности жизни. Так, по данным ООН, к 2050 году 22 % населения земли (более 2 млрд.) будет пенсионерами – пациентами пожилого и старческого возраста с повышенным риском развития ИМ.
Исследования, направленные на изучение клинического значения ИМР у пациентов ИМ пожилого и старческого возраста, имеет важное не только медицинское, но и экономическое значение.
Цель исследования – изучить количественные показатели ИМР у пациентов с ИМ пожилого и старческого возраста.
Материалы и методы
Обследованы 124 пациента (93 мужчины и 31 женщина), госпитализированных в блок кардиореанимации отделения неотложной кардиологии с диагнозом острого ИМ в первые 24 часа от начала заболевания. В соответствии с классификацией ВОЗ (1963 г.) возраст до 44 лет считается молодым, 45–59 – средним, 60–74 года – пожилым, 75–89 – старческим, а 90 лет и старше – периодом долгожительства. В статистических целях часто бывает необходимо подразделять население на возрастные группы. В основном в используемых ВОЗ исследованиях статистическим пределом является возраст 60 лет и старше [7]. Нами выделено две группы пациентов для сравнительной оценки влияния ИМР на течение заболевания в разных возрастных группах (табл. 1). Пациенты до 60 лет были включены в среднюю возрастную группу. Средний возраст пациентов до 60 лет составил 45,4±6,8 лет. Пациенты после 60 лет составили старшую возрастную группу (средний возраст 71,3±6,1 лет).
Таблица 1. Клиническая характеристика больных ИМ
| Показатели | Возрастные группы | р | ||
| Средняя 30–59 лет (n=56) | Старшая ≥60 лет (n=68) | |||
| Предшествующая стенокардия | 13 (23,2 %) | 22 (32,3 %) | 0,18 | |
| Гипертоническая болезнь | 32 (57,1 %) | 49 (72,1 %) | 0,07 | |
| Сахарный диабет 2 типа | 5 (8,6 %) | 11 (16,2 %) | 0,28 | |
| Фибрилляция предсердий* | 5 (8,9 %) | 9 (13,2 %) | 0,32 | |
| АВ-блокада II–III ст.* | 3 (5,3 %) | 3 (4,4 %) | 0,98 | |
| Желудочковые нарушения ритма* | 11 (19 %) | 13 (19 %) | 0,63 | |
| Локализация ИМ | передний | 26 (46,4 %) | 39 (57,3 %) | 0,47 |
| задний | 32 (53,6 %) | 29 (42,7 %) | 0,47 | |
Диагноз острого ИМ основывался на критериях, рекомендуемых группой экспертов ВОЗ (1970 г.), и на универсальном определении ИМ, подготовленном объединенной рабочей группой Европейского кардиологического общества, Американской коллегии кардиологов, Американской ассоциации сердца и Всемирной федерации сердца (2007). Выраженность СН в остром периоде ИМ оценивали по классификации Killip.
Пациенты включались в исследование на основании следующих критериев: наличие острого ИМ с Q-зубцом, ХСН, ИМР, интактных створок МК, хорд и папиллярных мышц. Критерии невключения в исследование: врожденная или приобретенная патология МК, увеличенный размер левого предсердия, перенесенный ранее ИМ, аортальная регургитация, неудовлетворительная ЭхоКГ визуализация. Критериями исключения из исследования были: нарушение ритма сердца во время ЭхоКГ исследования, возникновение повторных ишемических событий за время наблюдения.
Всем больным на 2-е сутки заболевания проводилось допплер–ЭхоКГ исследование наряду с общеклиническим, лабораторным (общий анализ крови, КФК и МВ-фракция, тропонин I), рентгенологическим и динамическим ЭКГ исследованиями.
В процессе стандартного ЭхоКГ исследования пациентов, в соответствии с рекомендациями Американской ассоциации ЭхоКГ, были рассчитаны следующие показатели, характеризующие функциональное состояние ЛЖ: конечный систолический объем (КСО), конечный диастолический объем (КДО), ударный объем (УО) и ФВ ЛЖ. Для уточнения локализации зон нарушения локальной сократимости миокарда ЛЖ использовалась схема деления миокарда на сегменты и диаграмма типа «мишень» (Otto СМ., Pearlman A. S., 1995). Важное прогностическое значение имеет расчет так называемого индекса локальной сократимости (ИЛС), который представляет собой сумму балльной оценки сократимости каждого сегмента (ΣS), деленную на общее число исследованных сегментов ЛЖ (n):
| ИЛС = | ΣS |
| n |
Трансмитральный диастолический кровоток оценивался в соответствии с рекомендациями Nishimura R. A. с соавт. (1997 г.).
Показатели ИМР определяли двумя количественными допплер–ЭхоКГ методами исследования: цветовое допплеровское картирование площади проксимальной изоскоростной поверхности сходящегося потока регургитации (PISA-метод) и метод количественной допплерЭхоКГ (Q-DE-метод) [8]. После определения максимальной скорости (Vmax) и интеграла линейной скорости регургитации (RTVI) измерялся радиус (R) сходящегося потока и проводился расчет всех количественных показателей ИМР по приведенным формулам: PISA = 2πR²;
Q = PISA × VR;
SRO = Q / Vmax;
RV = SRO × RTVI;
RF = RV / (RV+SVAo),
где PISA – площадь проксимальной изоскоростной поверхности; Q – объемная скорость регургитационного потока; SRO – площадь регургитационного отверстия; RV – регургитационный объем; RF – регургитационная фракция; SVAo – ударный объем аортального систолического потока; VR – скорость цветовой шкалы.
Методом количественной допплер–ЭхоКГ определяли объем трансмитрального диастолического потока (SVmv) и ударный объем систолического потока (SVAo), как произведение интеграла линейной скорости (VTI) и площади митрального или аортального клапана (S). Разница между этими объемами составляет объем регургитации (RV). Далее рассчитывали площадь регургитационного отверстия (SRO) и фракцию регургитации (RF): SVmv = Smv × VTI;
SVAo = SAo × VTI;
RV = SVmv–SVAo;
SRO = RV / RTVI;
RF = RV / SVmv
Статистическую обработку полученных данных проводили с применением статистических программ Statistica 6.0 и Excel 2003. При обработке данных использовались общепринятые методы параметрической и непараметрической статистики.
Результаты и обсуждение
Для оценки клинического значения ИМР у пациентов разных возрастных групп были исследованы количественные показатели ИМР (табл. 2). Полученные данные свидетельствуют об отсутствии существенного различия индивидуальных показателей ИМР (площадь регургитационного отверстия, регургитационный объем и фракция регургитации) у пациентов в средней и старшей возрастных группах.
Таблица 2. Показатели ИМР у пациентов с ОИМ
| Показатели | Возрастные группы | p | |
| Средняя | Старшая | ||
| SRO (см кв.) | 0,15±0,07 | 0,14±0,05 | >0,05 |
| RV (мл) | 15,39±7,6 | 15,09±7,9 | >0,05 |
| RF (%) | 20,14±7,9 | 20,30±6,4 | >0,05 |
В процессе исследования оценены показатели систолической функции ЛЖ у пациентов с ИМ и ИМР в различных возрастных группах (табл. 3).
Таблица 3. Систолическая функция ЛЖ у пациентов с ИМ и ИМР
| Показатели | Возрастные группы | p | |
| Средняя | Старшая | ||
| КДО (мл) | 126,9±31,8 | 124,8±34,1 | 0,65 |
| КСО (мл) | 63,5±25,9 | 60,1±25,3 | 0,27 |
| УО (мл) | 65,3±16,9 | 63,0±20,1 | 0,46 |
| ФВ (%) | 47,9±6,6 | 47,7±6,5 | 0,83 |
| ИЛС ЛЖ | 1,86±0,56 | 1,85±0,52 | 0,79 |
Все представленные показатели (КДО и КСО, УО, ФВ и ИЛС ЛЖ) не имели статистически значимых различий между группами.
Учитывая наличие у всех пациентов митральной регургитации, не позволяющей достоверно оценить диастолическую функцию ЛЖ [9], мы использовали стандартные термины для характеристики изменений трансмитрального кровотока (ТМК). При анализе ТМК отмечено, что у пациентов старшей возрастной группы изменения ТМК по типу «нарушенной релаксации» наблюдалось достоверно чаще, чем в средней группе (р=0,006) (табл. 4). Другие типы нарушения ТМК у пациентов обеих групп статистически значимо не отличались.
Таблица 4. Трансмитральный диастолический кровоток у пациентов с ИМ и ИМР
| Характеристика ТМК | Возрастные группы | p | |
| Средняя | Старшая | ||
| Нормальный тип диастолической функции | 12 (21,4%) | 4 (5,8%) | 0,014 |
| Нарушение релаксации | 29 (51,8 %) | 53 (80 %) | 0,006 |
| Псевдонормализация кровотока | 13 (23,2 %) | 10 (14,7 %) | 0,25 |
| Рестриктивный тип | 2 (3,6 %) | 1 (1,5 %) | 0,84 |
При оценке клинического значения ИМР у пациентов с острым ИМ тяжелая ЛЖ недостаточность (Killip II–III) у пациентов старше 60 лет выявлялась чаще, чем у пациентов до 60 лет (в 73,5 и 37,5 % случаев соответственно, р<0,001) (табл. 5).
Таблица 5. Острая СН у пациентов с ОИМ и ИМР
| Класс ОСН | Возрастные группы | p | |
| Средняя | Старшая | ||
| Killip I | 35 (62,5 %) | 18 (26,5 %) | 0,0003 |
| Killip II | 18 (32,1 %) | 42 (61,7 %) | 0,0011 |
| Killip III | 3 (5,4 %) | 8 (11,8 %) | 0,55 |
| Killip IV | 0 | 0 | |
Полученные данные свидетельствуют об отсутствии существенного различия индивидуальных показателей ИМР у пациентов в возрастной группе до 60 лет и у более старших пациентов.
Результаты проведенного исследования показали, что у пациентов с ИМ старшей и средней возрастных групп развилась нетяжелая митральная регургитация в острой стадии ИМ, вследствие деформации структур МК. Площадь регургитационного отверстия у пациентов старшей и средней возрастных групп была соответственно 0,14±0,05 и 0,15±0,07 см², регургитационный объем 15,09±7,9 и 15,39±7,6 мл, а фракция регургитации 20,30±10,4 и 20,14±9,9 %.
В исследуемых группах не наблюдалось также существенных различий величины зоны ишемического поражения миокарда ЛЖ. Так индекс нарушения локальной сократимости миокарда ЛЖ у пациентов старшей возрастной группы составлял 1,85±0,52, а в средней 1,86±0,56 и соответствовал средней степени тяжести нарушения региональной сократимости миокарда ЛЖ. У обследуемых пациентов, несмотря на обширную зону поражения миокарда ЛЖ, общая (глобальная) сократимость его поддерживалась на хорошем уровне (ФВ=47,7 %).
При анализе клинико-гемодинамических показателей отмечено, что у пациентов старшей возрастной группы острая СН (Killip II–III) развивалась в два раза чаще, чем у пациентов средней возрастной группы (73,5 и 37,5 % соответственно, р=0,0001).
Необходимо также обратить внимание, что у пациентов старшей возрастной группы в бoльшем проценте случаев (80 %), чем у пациентов средней возрастной группы (51,8 %) наблюдалось изменение ТМК по типу «нарушения релаксации» ЛЖ (р=0,006).
Известно, что у лиц пожилого возраста диастолическая дисфункция ЛЖ по типу «нарушения релаксации» является отражением естественных возрастных изменений миокарда [10–12] и не вызывает развития диастолической СН.
При нарушенной релаксации ЛЖ более энергичное сокращение левого предсердия (ЛП) по механизму Франка–Старлинга поддерживает общее диастолическое наполнение ЛЖ на нормальном уровне и повышения давления в легочных венах не происходит [13, 14].
Выявленное нами более частое развитие острой СН у пациентов старшей возрастной группы, по-видимому, обусловлено развитием ИМР в сочетании с изменением ТМК по типу «нарушения релаксации» ЛЖ. На рисунке 1 Б видно, что у пациентов с нарушенной релаксацией ЛЖ даже небольшой регургитационный объем (нетяжелая митральная регургитация с ФР=21 %) приводит к повышению давления в ЛП и развитию СН, в то время как у пациентов с нормальным расслаблением ЛЖ (рис. 1А) тот же объем МР не приводил к гемодинамически значимому росту давления в ЛП и развитию острой СН.
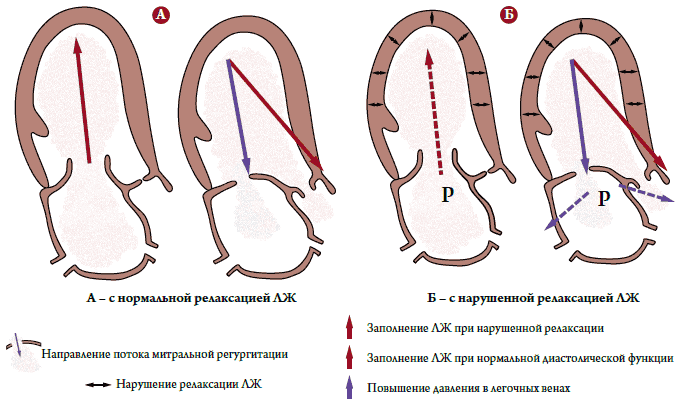
Рисунок 1. Внутрисердечная гемодинамика у пациентов с ИМ и ИМР
Развитие острой СН у пациентов с острым ИМ и ИМР происходит в результате повышения давления в ЛП за счет ИМР (черная стрелка) и дальнейшего нарастания давления и объема крови в малом куге кровообращения (рис. 2). Ретроградное повышение давления в ЛП, легочных венах и капиллярах в результате ИМР (обозначено черными стрелками) увеличивает давление в легочной артерии и приводит к развитию острой СН. В проведенных ранее исследованиях было показано, что ИМР существенно ухудшает прогноз пациентов и приводит к развитию ХСН в отдаленном периоде ИМ [2, 15, 16].
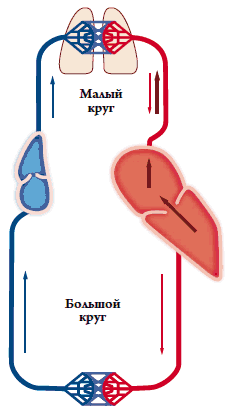
Рисунок 2. Схема кровообращения у пациентов с ОИМ и ИМР (объяснение в тексте)
ИМР является основным патогенетическим механизмом развития острой СН у пациентов с ИМ с удовлетворительной сократительной функцией ЛЖ. Было показано, что у пациентов с ОКС в возрасте 64,08±0,81 лет, с ФВ 54,84±8,27 % и нетяжелой ИМР острая СН развивается в 16,4 % случаев [17], тогда как, в проведенном нами исследовании у пациентов средней возрастной группы с ИМ с зубцом Q на ЭКГ, ФВ 47,9±6,60 % и фракцией митральной регургитации 20,14±7,9 % острая СН развивалась в 37,5 % случаев. А у пациентов старшей возрастной группы с ИМ с зубцом Q на ЭКГ, ФВ 47,7±6,5 % и фракцией митральной регургитации 20,30±6,4 % острая СН развивалась в 73,5 % случаев.
Таким образом, в остром периоде ИМ появление нетяжелой митральной регургитации у пациентов старшей возрастной группы на фоне характерного для этой возрастной группы нарушения релаксации ЛЖ способствует более частому развитию СН, чем у пациентов средней возрастной группы.
Ограничения исследования
Относительно небольшое число пациентов (124 пациента) не позволяет полностью экстраполировать результаты исследования на всю популяцию пациентов с острым ИМ. Используемые нами количественные методы исследования, объективно оценивающие ИМР, не могут быть сопоставимы с качественной и полуколичественной оценкой ИМР, широко используемой в настоящее время в практической и научной работе.
Список литературы
