Витапрост Форте в лечении больных с аденомой предстательной железы
СтатьиА.А. Камалов, Е.А. Ефремов, С.Д. Дорофеев, Я.И. Мельник, Д.А. Охоботов
ФГУ НИИ урологии (дир. - академик РАМН Н.А. Лопаткин) Росздрава, Москва
Введение. По данным международной статистики, аденома предстательной железы (АПЖ) наблюдается в среднем у 80% мужчин в возрасте 60 лет и старше. По данным ООН, численность населения в возрасте старше 60 лет к концу ХХ века возросла более чем в 3 раза. Учитывая тенденцию старения населения планеты, можно предположить возрастание актуальности данной проблемы [1].
АПЖ является одним из наиболее распространенных заболеваний мужчин пожилого возраста и определяется гистологически наличием доброкачественной ткани, расположенной в окружности проксимального сегмента мочеиспускательного канала [2].
J.Isaacs и D.Coffey (1987) [3] на основании аутопсийных исследований заключают, что при профилактическом обследовании мужчин старше 50 лет АПЖ обнаруживается в 10 – 15% случаев, однако клинические проявления болезни наблюдаются далеко не у всех [4]. У 80 – 85% мужчин 60 лет и старше имеет место в той или иной степени увеличение предстательной железы [5].
В.Е. Родоманом с соавт. [6] при обследовании 648 мужчин в возрасте от 50 до 86 лет (средний возраст 66,2 года) АПЖ была диагностирована у 242 (37,34%), среди них лиц от 50 до 59 лет было 11,3% , от 60 до 69 лет – 36,5%, от 70 до 79 лет – 42,8%, 80 лет и старше – 94%[7]. Заболевание проявляется жалобами на прогрессирующее ухудшение качества самостоятельного мочеиспускания: затрудненное мочеиспускание тонкой вялой струей, чувство неполного опорожнения мочевого пузыря, вынужденное ночное мочеиспускание от 1 раза и чаще.
Таким образом, лечение пациентов с АПЖ является важной задачей современной урологии в связи с распространенностью данного заболевания. Медикаментозная терапия АПЖ – одна из наиболее динамично развивающихся областей урологии. Вместе с тем механизмы действия некоторых препаратов изучены недостаточно, отсутствуют четкие показания к применению большинства лекарственных средств. Основные группы лекарственных средств, применяющихся для лечения АПЖ: гормональные препараты (аналоги гонадотропных рилизинг-гормонов, антиандрогены, гестагены, антиэстрогены, ингибиторы ароматазы, антагонисты пролактина), ингибиторы 5-α редуктазы, α-адреноблокаторы, растительные препараты, прочие (полиеновые антибиотики, аминокислотные комплексы и экстракты органов животных).
При лечении АПЖ применяются разнообразные лекарственные препараты растительного и животного происхождения. Один из них – Витапрост®, активным веществом которого является эндогенная субстанция сампрост (экстракт простаты) - комплекс водорастворимых биологически активных пептидов, выделенных из предстательной железы ткани простаты быков и бычков, достигших половой зрелости путем жесткого кислотного гидролиза, глубоко разрушающего клеточные структуры. Особенности выделения этих пептидов нивелируют их молекулярную видоспецифичность, в результате чего полученные препараты лишаются антигенных свойств и ассоциированных с ними побочных эффектов [8].
Экстракт простаты оказывает органотропное действие в отношении предстательной железы. Как все пептидные биорегуляторы, экстракт простаты обладает антиагрегантными и антикоагулянтными свойствами, усиливает синтез антигистаминовых и антисеротониновых антител, улучшает микроциркуляцию в пораженном органе. На этом основана его способность уменьшать отек и активность воспалительных процессов при заболеваниях предстательной железы. Существенным является также наличие у экстракта простаты иммуномодулирующих свойств [8].
В 2001 году в НИИ урологии Минздрава РФ проведено открытое несравнительное исследование по изучению эффективности и безопасности препарата Витапроста® в форме суппозиториев (доза по экстракту простаты - 50 мг) при хроническом простатите (ХП). Исследование продемонстрировало хорошую эффективность препарата при немногочисленных нежелательных явлениях. На основании полученных данных сделаны выводы о том, что Витапрост® может быть применён в комплексной терапии бактериального и абактериального ХП у пациентов всех возрастных групп, в том числе в сочетании с АПЖ [9].
Сегодня компанией «Нижфарм» разработана новая форма препарата - Витапрост® форте суппозитории ректальные 100 мг, что позволяет врачу и пациенту варьировать режим дозирования препарата, осуществляя патогенетическую терапию заболеваний предстательной железы и функционально связанных с ней органов. Витапрост® форте показан при различных заболеваниях и патологических состояниях мужской урогенитальной сферы, в том числе и при АПЖ.
В ФГУ «НИИ Урологии Росздрава» (Москва) в 2006 г. в соответствии с разрешением Федеральной службы по надзору в сфере здравоохранения и социального развития № 133 от 2 мая 2006 г. проведено сравнительное рандомизированное плацебо контролируемое клиническое исследование эффективности и безопасности препарата Витапроста® форте, суппозитории ректальные 100 мг, производства ОАО «Нижфарм» (Россия) у пациентов с АПЖ.
Препарат Витапрост® форте суппозитории ректальные 100 мг представляет собой суппозитории от белого с желтоватым до кремового с сероватым оттенком цвета, торпедообразной формы. Один суппозиторий содержит: в качестве активного вещества: сампроста субстанцию (экстракт простаты) 0,1 г (в пересчёте на водорастворимые пептиды – 0,02 г) и вспомогательные вещества - витепсол в количестве достаточном для получения суппозитория массой 1,25 г.
При планировании исследования были поставлены основная, первичные и вторичная цели.
Основной целью данного исследования явилась оценка эффективности и безопасности лекарственного препарата Витапроста® форте суппозитории ректальные 100 мг в лечении пациентов с АПЖ.
Первичными целями исследования были:
Вторичная цель – оценка переносимости препарата Витапроста® форте на основе анализа зарегистрированных побочных действий и изменений лабораторных показателей (клинического, биохимического анализов крови и клинического анализа мочи).
Материалы и методы. В исследование было включено 120 пациентов, соответствовавших следующим критериям включения:
В исследование не включались пациенты, которые на момент 1-го визита:
Все пациенты, соответствующие критериям включения и включенные в исследование, были рандомизированы на три группы по 40 человек в каждой:
Длительность лечения во всех трех группах составляла 30 дней.
11 пациентов основной группы (Витапрост® форте), 11 пациентов первой контрольной (омник), 21 пациент второй контрольной (плацебо) группы имели сопутствующие заболевания, в том числе: язвенную болезнь желудка и двенадцатиперстной кишки, гипертоническую болезнь I-II стадии, ишемическую болезнь сердца, сахарный диабет 2-го типа и др. 2 (5%) пациента из основной группы и 1 (2,5%) пациент из группы плацебо перенесли инфаркт миокарда, 1 (2,5%) пациент из основной группы – острое нарушение мозгового кровообращения. Кроме этого, некоторые пациенты были подвергнуты в анамнезе оперативным вмешательствам (аппендэктомии, холецистэктомии, герниотомии и др.), а также биопсии простаты.
Исследование включало 5 визитов, в ходе которых проводились сбор анамнеза и физикальный осмотр пациента, регистрация симптоматики АПЖ с использованием шкалы Международной системы суммарной оценки заболеваний простаты (IPSS-Q), пальцевое ректальное исследование и ТРУЗИ с допплерографией сосудов предстательной железы, клинические и биохимические лабораторные исследования крови и мочи, простатспецифический антиген (ПСА), определение объема остаточной мочи, урофлоуметрия.
План обследования
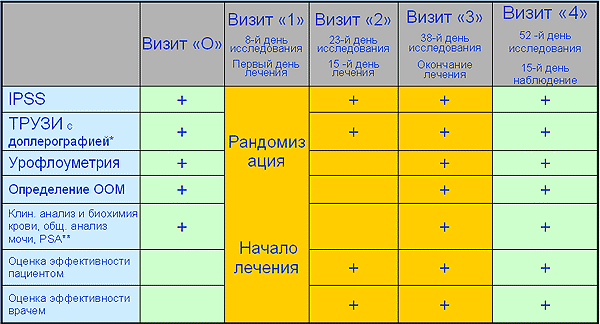
Результаты.
По данным проведенного динамического исследования клинических, а также биохимических анализов крови достоверные параметры для всех рассматриваемых групп колебались в пределах физиологических нормативов либо не имели клинического значения. Общий анализ мочи: сравнение таких параметров, как уровень белка, удельная плотность, содержание бактерий в поле зрения, pH, не выявило достоверных различий во всех группах. При этом колебания значений этих показателей определялись в пределах нормы.
Данные ТРУЗИ простаты являлись одними из критериев эффективности, используемых для оценки терапевтического эффекта терапии и степени выраженности воспалительного процесса в предстательной железе.
В основной группе на фоне приема препарата Витапроста® форте было достигнуто незначительное, но статистически достоверное снижение среднего значения объёма предстательной железы (с 46,05 см3 на 0-м визите до 44,01 см3 на 4-м визите). Среди пациентов, принимавших омник, было выявлено статистически достоверное умеренное увеличение объёма простаты с 44,4 до 45,33 см3 к концу исследования. В группе плацебо также зафиксировано последовательное увеличение объема простаты от 0-го визита к 3-му и 4-му визитам, но статистически недостоверное.
Динамика значений объема простаты по данным ТРУЗИ
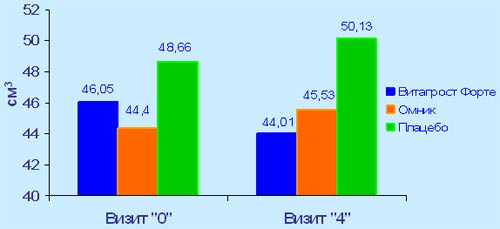
Одними из основных параметров, используемых для оценки терапевтического эффекта применения препарата Витапроста® форте, были показатели урофлоуметрии и величины объёма остаточной мочи, характеризующие степень нарушения мочеиспускания на фоне развития АПЖ и функциональное состояние детрузора (таб. 1).
Таблица 1
Значения основных параметров мочеиспускания у пациентов трёх групп
|
Показатель |
Основная группа |
Омник |
Плацебо |
|||||||
|
Визит |
||||||||||
|
0-й |
3-й |
4-й |
0-й |
3-й |
4-й |
0-й |
3-й |
4-й |
||
|
Qmax (мл/с) |
минимальное и максимальное значения |
8-14 |
9-16 |
8-18 |
8-14 |
8-16 |
7-14 |
8-14 |
7-16 |
8-16 |
|
среднее арифметическое ± стандартное отклонение |
10,48 ±1,8 |
11,48 ±2,05 |
11,7 ±2,29 |
10,13±1,43 |
11,34 ±2,21 |
10,18±1,66 |
10,55±2,11 |
10,23±2,04 |
10,15±2,25 |
|
|
p |
<10-5 |
<10-5 |
<10-5 |
0,83* |
0,04 |
0,003 |
||||
|
Qave (мл/с) |
минимальное и максимальное значения |
3-8 |
3-9 |
3-9 |
2-8 |
2,8-8 |
3-8 |
3-9 |
3-8 |
3-10 |
|
среднее арифметическое ± стандартное отклонение |
5,05 ±1,1 |
5,7 ±1,38 |
5,88 ±1,38 |
4,76 ±1,18 |
5,45 ±1,33 |
4,88 ±1,16 |
5,16 ±1,27 |
5,06 ±1,15 |
5,23 ±1,41 |
|
|
p |
<10-5 |
<10-5 |
<10-5 |
0,002 |
0,47* |
0,18* |
||||
Примечание. Здесь и в табл. 2, 4* - недостоверное значение.
В основной группе (Витапрост® форте) достигнуто увеличение среднего значения Qmax с 10,48 мл/с на 0-м визите до 11,48 мл/с к 3-му и 11,71 мл/с к 4-му визиту. Эти изменения были статистически достоверны. При этом максимальные значения этого параметра среди пациентов, принимавших Витапрост® форте, возросли до 16 и 18 мл/с к 3-му и 4-му визитам соответственно, достигнув нормальных значений. На фоне приема омника также увеличилась Qmax от 0-го визита к 3-му визиту (с 10,13 до 11,34 мл/с), но дальнейшее изменение этого показателя было недостоверно. Среди пациентов, принимавших плацебо, отмечено последовательное уменьшение Qmax от 0-го визита к 3-му и 4-му.
В группе получавшей Витапрост® форте, от 0-го к 4-му визиту происходит достоверное снижение среднего значения объема остаточной мочи, несмотря на прекращение приема препарата на 3-м визите, что может свидетельствовать о терапевтическом последействии препарата Витапроста® форте (терапевтическое действие которого продолжается с прекращением курса лечения) (табл. 2).
Таблица 2
Величины объема остаточной мочи у пациентов трех групп
|
Объём остаточной мочи, мл |
Основная группа |
Омник |
Плацебо |
||||||
|
Визит |
|||||||||
|
0-й |
3-й |
4-й |
0-й |
3-й |
4-й |
0-й |
3-й |
4-й |
|
|
минимальное и максимальное значения |
0-139 |
0-98 |
0-85 |
0-100 |
0-74 |
0-95 |
0-95 |
0-89 |
0-142 |
|
среднее арифметическое ± стандартное отклонение |
51,95 ±31,3 |
30,42 ±25,61 |
28,62 ±24,39 |
49,7±25,11 |
31,35±24,22 |
48,38±25,2 |
45,85±25,19 |
49,53±25,07 |
54,95±29,59 |
|
р |
<10-5 |
<10-5 |
<10-5 |
<10-5 |
0,208* |
0,09* |
|||
* - недостоверное значение
У пациентов, принимавших омник, отмечается достоверное сниженное среднего значения объема остаточной мочи от 0-го к 3-му визиту, а далее от 3-го к 4-му визиту (после отмены препарата) объём остаточной мочи увеличивается. Данное увеличение указывает на симптоматическое действие препарата омника, после прекращения приема которого первоначальные показатели объема остаточной мочи возвращаются к исходным.
В группе плацебо, напротив, объём остаточной мочи увеличивался от визита к визиту, хотя увеличение это и не было статистически достоверно.
Одним из параметров эффективности терапии, используемом при статистическом анализе данных исследования для оценки степени выраженности обструктивной и ирритативной симптоматики АПЖ, являлась сумма баллов по шкале IPSS. Результаты проведенного анкетирования приведены в табл. 3.
Таблица 3
Динамика суммарного балла по шкале IPSS
|
Количество баллов |
Количество пациентов |
||||||||
|
Основная группа |
Омник |
Плацебо |
|||||||
|
Визит |
|||||||||
|
0-й |
3-й |
4-й |
0-й |
3-й |
4-й |
0-й |
3-й |
4-й |
|
|
0 – 7 (незначительная) |
2 (5) |
9 (22,5) |
12 (30) |
4 (10) |
14 (35) |
8 (20) |
3 (7,5) |
3 (7,5) |
3 (7,5) |
|
8 – 19 (умеренная) |
35 (87,5) |
29 (72,5) |
26 (65) |
33 (82,5) |
24 (60) |
30 (75) |
33 (82,5) |
34 (85) |
34 (85) |
|
20 – 35 (выраженная) |
3 (7,5) |
2 (5) |
2 (5) |
3 (7,5) |
2 (5) |
2 (5) |
4 (10) |
3 (7,5) |
3 (7,5) |
