Роль липидов в патогенезе атеросклероза
Статьи П.Х. Джанашия, В.А. Назаренко, С.А. Николенко Содержание »»Роль липидов в патогенезе атеросклероза
Гиперхолестеринемия как фактор риска ИБС
Липидная теория атерогенеза впервые была предложена в 1913 г. отечественным исследователем Н.Н. Аничковым, который совместно с С.С. Халатовым показал, что скармливание кроликам пищи, богатой животными жирами и ХС, приводит к развитию атеросклероза аорты и ее ветвей. В последующем эта теория была подтверждена рядом экспериментальных, эпидемиологических, генетических и клинических исследований. В частности, быстрое развитие атеросклероза было продемонстрировано у кроликов линии Ватанабе с врожденной гиперхолестеринемией (которая является аналогом семейной гиперхолестеринемии человека), получающих обычный растительный рацион. В завершившемся в 1970 г. так называемом Исследовании Семи Стран было показано, что в странах с низким потреблением ХС и насыщенных жиров, таких как Япония и государства Средиземноморья, заболеваемость ИБС и смертность от нее значительно ниже, чем в Финляндии и США, для которых в те годы было характерно высокое потребление насыщенных жиров и ХС. Значение гиперхолестеринемии как независимого фактора риска ИБС было убедительно продемонстрировано во Фремингамском эпидемиологическом наблюдательном исследовании, которое было начато в 1948 г. и продолжается и в наши дни. В него было включено все взрослое население (около 5000 человек) маленького городка Фремингам штата Массачусетс (США). За 30-летний период наблюдения было показано, что лица с уровнем ХС плазмы крови около 6,5 ммоль/л характеризуются вдвое более высокой заболеваемостью ИБС и смертностью от нее по сравнению с теми, у кого уровень ХС не превышал 5,2 ммоль/л.
В 1986 г. в США были опубликованы результаты Исследования по Многофакторной Профилактике (MRFIT), в которое было включено более 350000 мужчин в возрасте от 35 до 57 лет, которых наблюдали в течение 6 лет. Оно показало, что связь между уровнем общего ХС плазмы крови и смертностью от ИБС является весьма жесткой и описывается экспоненциальной кривой (рис. 3). Полученные во Фремингамском исследовании и в MRFIT данные позволили определить границы нормы уровня ХС в плазме крови.
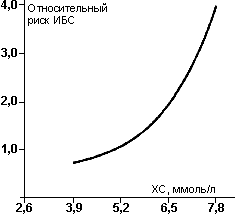
Рис. 3. Связь между уровнем XC плазмы крови и заболеваемостью ИБС.
Липидная теория атерогенеза была подтверждена и рядом клинических исследований, проведенных у больных с достаточно редко встречающимися семейными вариантами гиперхолестеринемии. Так, была выявлена высокая заболеваемость ИБС у больных с гетерозиготным вариантом семейной гиперхолестеринемии, при котором уровень XC плазмы крови примерно в два раза превышает границу нормы (5,2 ммоль/л). И наконец было доказано, что снижение уровня XC с помощью как традиционных (никотиновая кислота, холестирамин), так и новых гиполипидемических препаратов (ловастатин, симвастатин, правастатин) приводит к улучшению прогноза у больных ИБС.
Важное теоретическое и практическое значение имеет вопрос о потенциальном риске, связанном с низким уровнем XC плазмы крови. Согласно данным некоторых эпидемиологических исследований, лица с уровнем общего XC крови менее 160 мг/дл (4,1 ммоль/л) характеризуются более высокими показателями смертности, чем обследуемые с "нормальными" значениями XC. По результатам ранних исследований по вторичной профилактике ИБС терапия клофибратом, гемфиброзилом, холестирамином и никотиновой кислотой приводит к снижению коронарной смертности, но сопровождается увеличением смертности от других причин. В связи с этими обстоятельствами возникли сомнения в безопасности холестеринпонижающей терапии.
Однако дальнейшее изучение этой проблемы показало беспочвенность подобных опасений. Так, у взрослого населения Шанхая в связи с низким потреблением продуктов животного происхождения уровень общего ХС в среднем составляет 162 мг/дл (4,2 ммоль/л) и при этом не наблюдается негативных тенденций в отношении уменьшения продолжительности жизни. Весьма показательны данные, полученные у больных с генетическими аномалиями, характеризующимися низким уровнем ХС крови: абеталипопротеидемией и гипобеталипопротеидемией. Они представляют собой аутосомно-рецессивные заболевания с резким уменьшением или отсутствием апо-В-содержащих классов ЛП (главным образом ЛПНП) и крайне низким уровнем ХС крови (20-45 мг/дл). Абеталипопротеидемия и гипобеталипопротеидемия проявляются периферической нейропатией и синдромом малабсорбции жиров. Однако у подобных больных не выявлено тенденции к увеличению частоты онкологических заболеваний и уменьшению продолжительности жизни.
Повторный детальный анализ результатов тех эпидемиологических исследований, в которых была отмечена связь между низким уровнем ХС и высокими показателями смертности, показал ошибочность первоначальных заключений. Так, в известном исследовании, проведенном в Гонолулу (1981 г.), оказалось, что низкий уровень ХС имел место в основном у больных с тяжелыми сопутствующими заболеваниями (циррозом печени, алкоголизмом) и у перенесших гастрэктомию и колонэктомию по поводу злокачественных новообразований.
Выводы в отношении увеличения некоронарной смертности при терапии фибратами и некоторыми другими гиполипидемическими препаратами в исследованиях 60-70 гг. при повторном анализе полученных данных также не подтвердились. Никаких неблагоприятных тенденций не было отмечено в исследованиях с длительной терапией статинами, проведенных в 80-90 гг. с применением современных методов анализа и интерпретации данных.
Патогенез атеросклероза
Атеросклероз представляет собой сложный, многоэтапный патологический процесс, поражающий внутреннюю оболочку (интиму) артерий крупного и среднего калибра. Интима содержит тонкую прослойку соединительной ткани и отграничена от мышечной оболочки артерии (медии) внутренней эластической мембраной, а от просвета сосуда - монослоем эндотелиальных клеток, образующих сплошную гладкую неадгезивную поверхность. Эндотелий выполняет роль полунепроницаемой мембраны, которая, с одной стороны, является барьером между кровью и сосудистой стенкой, а с другой стороны - обеспечивает необходимый обмен молекулами между ними. На поверхности эндотелия расположены специализированные рецепторы к различным макромолекулам, в частности, к ЛПНП. Эндотелий секретирует ряд вазоактивных субстанций (эндотелин, простациклин, оксид азота), а также факторов свертывающей и противосвертывающей систем, благодаря чему играет ключевую роль в регуляции сосудистого тонуса, кровотока и гемокоагуляции.
В настоящее время наиболее популярна теория, в соответствии с которой атеросклероз рассматривается как реакция на повреждение сосудистой стенки (прежде всего - эндотелия). Под повреждением подразумевается не механическая травма эндотелия, а его дисфункция, которая проявляется повышением проницаемости и адгезивности, а также увеличением секреции прокоагулянтных и сосудосуживающих факторов. Дисфункцию эндотелия могут вызвать инфекционные агенты (в частности, вирусы герпеса), токсические соединения (некоторые компоненты табачного дыма), избыточный уровень гормонов (гиперинсулинемия при сахарном диабете), гемодинамические факторы (артериальная гипертензия). Однако в качестве наиболее важного повреждающего фактора выступает гиперхолестеринемия. Показано, что при гиперхолестеринемии изменяется структура эндотелия: увеличивается содержание ХС и соотношение ХС/фосфолипиды в мембране эндотелиальных клеток, что приводит к нарушению барьерной функции эндотелия и повышению его проницаемости для ЛПНП. В результате возникает избыточная инфильтрация интимы ЛПНП. Следует отметить, что при пассаже через эндотелий ЛПНП подвергаются окислению, и в интиму проникают в основном окисленные формы ЛПНП, которые сами по себе оказывают повреждающее воздействие на структурные элементы как эндотелия, так и интимы.
Следующим этапом атерогенеза является инфильтрация интимы циркулирующими моноцитами, которые трансформируются в макрофаги, осуществляющие захват окисленных ЛПНП с их последующей деструкцией. Вследствие этого в макрофагах накапливаются эфиры ХС и они перерождаются в так называемые пенистые клетки, которые дают начало липидным полоскам - первой морфологической стадии атеросклеротической бляшки. Однако этим роль макрофагов далеко не исчерпывается. Они секретируют биологически активные соединения, включая хемотаксины, митогены и факторы роста, которые стимулируют миграцию из медии в интиму гладкомышечных клеток (ГМК) и фибробластов, их пролиферацию, репликацию и синтез соединительной ткани.
Становится очевидным, что атеросклероз представляет собой процесс, для которого характерны фундаментальные закономерности, свойственные любому воспалению: воздействие повреждающего фактора (окисленных ЛПНП), клеточная инфильтрация, фагоцитоз и формирование соединительной ткани.
Это сходство еще более усилится, если принять во внимание, что в клеточном инфильтрате на любых этапах формирования атеросклеротической бляшки присутствуют Т-лимфоциты, что свидетельствует о роли иммунных, а возможно, и аутоиммунных механизмов. Не исключено, что антигенами, на которые реагируют Т-лимфоциты, являются окисленные ЛПНП.
Миграция из медии в интиму ГМК и фибробластов с их последующей пролиферацией под влиянием стимуляторов (факторов роста), синтезируемых макрофагами, является облигатным этапом атерогенеза. Роль фибробластов очевидна и заключается в синтезе соединительно-тканного матрикса бляшки. Аналогичную роль играют и ГМК. Они способны к синтезу и секреции некоторых форм коллагена, эластических волокон и протеогликанов. Эту функцию выполняют ГМК так называемого синтетического (а не контрактильного) фенотипа, для которых характерны небольшое количество миофиламентов, гипертрофия аппарата Гольджи и эндоплазматического ретикулума. Помимо синтеза соединительной ткани ГМК способны захватывать ЛПНП и, как и макрофаги, трансформироваться в пенистые клетки. Основные этапы атерогенеза представлены на схеме 3.
Схема 3. Патогенез атеросклероза
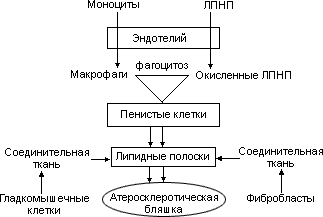
На ранних стадиях атеросклероз представлен так называемыми липидными полосками, которые содержат пенистые клетки, богатые ХС и его эфирами. В последующем вокруг зоны накопления липидов развивается соединительная ткань и происходит формирование фиброзной атеросклеротической бляшки. Этот процесс обычно занимает несколько десятилетий. У лиц пожилого возраста фиброзные атеросклеротические изменения сосудистой стенки рассматриваются как закономерное, хотя и отнюдь не облигатное явление. В тех случаях, когда клинические проявления этого процесса возникают в возрасте до 60 лет, говорят о преждевременном или раннем атеросклерозе.
Согласно принятой в настоящее время концепции, клиническое и прогностическое значение коронарного атеросклероза определяется стадией развития и морфологическими особенностями атеросклеротических бляшек. На относительно ранних этапах формирования они содержат большое количество липидов и имеют тонкую соединительно-тканную капсулу. Это так называемые ранимые, или желтые, бляшки, которые занимают лишь небольшую часть окружности сосуда, то есть являются эксцентрическими. Благодаря своей эластичности и небольшим размерам они обычно не вызывают гемодинамически значимого сужения КА и нередко не выявляются при коронароангиографии. На периферии желтых бляшек расположены Т-лимфоциты, секретирующие гамма-интерферон, который ингибирует синтез коллагена ГМК и тем самым препятствует укреплению фиброзной капсулы бляшки. Тонкая соединительнотканная оболочка желтых бляшек может быть повреждена как в связи с воздействием гемодинамических факторов (перепады давления в сосуде, компрессия и растяжение стенки), так и в результате того, что содержащиеся вблизи оболочки макрофаги и тучные клетки вырабатывают протеиназы (коллагеназу, желатиназу, стромелизин), которые способны разрушить защитный интерстициальный матрикс. Эрозия или разрыв соединительно-тканной капсулы желтых бляшек происходят у края бляшки возле интактного сегмента КА.
Нарушение целостности фиброзной капсулы приводит к контакту содержащихся в бляшке детрита и липидов с тромбоцитами и к немедленному формированию тромба. Выделение тромбоцитами тромбоксана А2 и других вазоактивных субстанций может привести к спазму КА. В результате развивается так называемый острый коронарный синдром - нестабильная стенокардия или мелкоочаговый инфаркт миокарда (при пристеночном тромбозе КА), крупночаговый инфаркт миокарда (при окклюзирующем тромбозе КА). Другим проявлением разрыва атеросклеротической бляшки может быть внезапная смерть (схема 4).
На поздних стадиях развития фиброзные бляшки представляют собой плотные ригидные образования, имеющие прочную сбединительно-тканную капсулу и содержащие относительно мало липидов и много фиброзной ткани. В отличие от ранимых желтых бляшек, сквозь капсулу которых просвечивают липиды, их называют белыми. Такие бляшки обычно расположены концентрически (по всей окружности сосуда), вызывают гемодинамически значимое (на 75% и более) сужение КА и, таким образом, являются морфологическим субстратом синдрома стабильной стенокардии напряжения.
Возможность разрыва плотной фиброзной капсулы белой бляшки не исключена, однако значительно менее вероятна, чем желтой бляшки. Даже у больных, имеющих стенозирующее поражение нескольких КА, риск возникновения осложнений (инфаркта миокарда, нестабильной стенокардии) связан в основном не с эволюцией фиброзных бляшек, а с возможностью разрыва находящейся на более ранней стадии развития желтой бляшки, которая может не выявляться при коронарографическом исследовании и не вызывать нарушений коронарного кровотока.
Схема 4. Осложнения коронарного атеросклероза
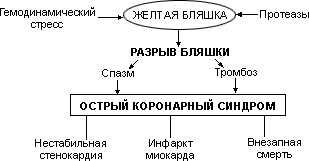
В связи с тем значением, которое в настоящее время придают ранимым (желтым) бляшкам в генезе острого коронарного синдрома, предупреждение их образования рассматривается как основная цель гиполипидемической терапии при первичной и особенно при вторичной профилактике ИБС. В некоторых исследованиях показано, что терапия статинами способна стабилизировать атеросклеротическую бляшку, то есть укрепить ее капсулу и уменьшить вероятность разрыва.
Классификация гиперлипопротеидемий
В зависимости от увеличения в плазме крови содержания ЛП того или иного класса традиционно выделяют 6 основных типов ГЛП в соответствии с классификацией Фредрикксена, принятой ВОЗ (табл. 2).
Таблица 2. Классификация гиперлипопротеидемий (ВОЗ)
| Тип ГЛП | Повышенный уровень ЛП | ХС | ТГ | Атерогенность | Встречаемость |
| I | Хиломикроны | Норма | у/у/у/у | Не доказана | <1% |
| IIa | ЛПНП | у/у | Норма | +++ | 10% |
| IIв | ЛПНП и ЛПОНП | у/у | у/у | +++ | 40% |
| III | ЛППП | у/у | у/у/у | +++ | <1% |
| IV | ЛПОНП | Норма или у | у/у | + | 45% |
| V | ЛПОНП и хиломикроны | у/у | у/у/у/у | + | 5% |
ГЛП того или иного типа представляет собой скорее лабораторный феномен, чем клинический синдром или, тем более, нозологическую единицу. Классификация Фредрикксена не учитывает уровень ЛПВП и не дает возможности разделить ГЛП на первичные и вторичные формы (см. ниже). ГЛП I, III и V типов встречаются крайне редко, причем I и V типов - только в педиатрической практике. Таким образом, у взрослых речь вдет обычно о ГЛП IIа, IIв и IV типов, которые, как правило, легко дифференцируются по уровню ХС и ТГ. Тем не менее, в ряде случаев установить тип ГЛП по уровню липидов не удается и оказывается необходимым применение сложных методов типирования ГЛП. Идентификация типа ГЛП необходима не только для оценки коронарного риска, но и для выбора диетической и медикаментозной гиполипидемической терапии.
Клиническая классификация ГЛП предполагает выделение первичных и вторичных форм; первичные ГЛП в свою очередь подразделяются на моногенные и полигенные (табл. 3).
Таблица 3. Клиническая классификация гиперлипопротеидемий
| Первичные ГЛП | Вторичные ГЛП |
| I. Полигенные ГЛП | Сахарный диабет |
| II. Моногенные ГЛП | Хронический алкоголизм |
| Семейная гиперхолестеринемия | Гипотиреоз |
| Семейная комбинированная гиперлипидемия | Обструктивные заболевания печени |
| Дисбеталипопротеидемия | Нефротический синдром |
| Семейная эндогенная гипертриглицеридемия | Терапия бета-блокаторами, диуретиками |
| Семейная хиломикронемия |
Подавляющее большинство всех ГЛП приходится на так называемую первичную полигенную ГЛП, то есть на банальные случаи гиперхолестеринемии и/или гипертриглицеридемии, сплошь и рядом встречающиеся в повседневной практике. Этот термин подчеркивает, что наследственная предрасположенность определяется не какой-либо локальной генетической аномалией, а совокупностью генов, идентификация которых представляется весьма проблематичной. В происхождении полигенной ГЛП ведущую роль играют такие факторы, как характер питания, малоподвижный образ жизни, избыточная масса тела. Выявление и коррекция полигенной ГЛП являются основными задачами профилактики ИБС.
Первичные моногенные ГЛП представляют собой генетические заболевания, передающиеся по аутосомно-доминантному или рецессивному типу с четким характером наследования в семьях. Обычно ГЛП выявляется не менее чем у половины близких родственников больных. На дoлю первичных моногенных ГЛП приходится около 10-15% всех случаев ГЛП.
Семейная гиперхолестеринемия (СГ) является аутосомно-доминантным заболеванием, вызванным дефектом гена, кодирующего структуру и функцию рецептора к апопротеидам В/Е. У больных с гетерозиготной формой СГ, которая встречается с частотой один случай на 350-500 человек в общей популяции, функционирует половина В/Е рецепторов, в связи с чем уровень ХС оказывается повышенным примерно вдвое (до 9-12 ммоль/л). Гиперхолестеринемия возникает с момента рождения и сохраняется на всю жизнь. В подавляющем большинстве случаев выявляется ГЛП IIа типа (повышение уровня ХС при нормальном содержании ТГ), однако у некоторых больных может быть ГЛП IIв типа (повышение уровня ХС и ТГ). Практически патогномоничным признаком гетерозиготной формы СГ является ксантоматоз, то есть отложение эфиров холестерина в сухожилиях, приводящее к их резко выраженному утолщению. Наиболее доступным для обследования является ахиллово сухожилие. Его ксантоматоз вызывает деформацию стопы и необходимость в ношении ортопедической обуви. Весьма характерен также ксантоматоз сухожилий экстензоров кисти. Может выявляться и липидная дуга роговицы. Основное значение СГ заключается в преждевременном возникновении ИБС, которая у мужчин обычно развивается на 4-5-м десятилетии жизни, а у женщин - на 10 лет позже. Диетическую и медикаментозную терапию СГ следует начинать в раннем детском возрасте и проводить в течение всей жизни.
Гомозиготная форма СГ встречается крайне редко - с частотой один случай на 1 миллион населения. У подобных больных полностью отсутствуют рецепторы к апопротеидам В/Е, в связи с чем уровень ХС может достигать 20-40 ммоль/л. Обычно ИБС развивается не позже 20-летнего возраста; описано и ее возникновение в первые годы жизни. Для пациентов с гомозиготной СГ характерно наличие не только ксантоматоза сухожилий, но и эруптивных ксантом на ягодицах, коленях, локтях, слизистой оболочке полости рта. В связи с тем, что у подобных больных медикаментозная терапия неэффективна, средствами выбора являются плазмаферез или плазмосорбция. Наиболее радикальные результаты могут быть получены при трансплантации печени: В/Е рецепторы гепатоцитов донорской печени быстро нормализуют уровень ХС.
Семейная комбинированная гиперлипидемия (СКГ) встречается примерно у одного из 100 человек. Передается по аутосомно-доминантному типу. Точная природа СКГ неизвестна, предполагают, что в ее основе лежит гиперпродукция апо В-100. Для липидного спектра больных с СКГ характерен полиморфизм: у одних пациентов выявляется IIа тип ГЛП (изолированная гиперхолестеринемия), у других - IIв тип ГЛП (повышение уровня ХС и ТГ), у третьих - ГЛП IV типа (изолированная гипертриглицеридемия). Такой же полиморфизм характерен для родственников больных. Интересно, что тип ГЛП может неоднократно меняться на протяжении жизни больного. Уровень ХС обычно составляет от 6,5 до 8,5 ммоль/л, а содержание ТГ не превышает 4,5 ммоль/л. Чаще всего признаки СКГ возникают у взрослых, но она может проявиться и у детей. Основное значение СКГ заключается в преждевременном развитии ИБС. От семейной гиперхолестеринемии СКГ отличается отсутствием ксантоматоза сухожилий. Медикаментозную терапию МКГ проводят исходя из того типа ГЛП, который имеется на данный момент.
Семейный дефект аполипопротеида В-100 является аутосомно-доминантной генетической аномалией, при которой значительно повышен уровень ЛПНП (IIа тип ГЛП). Дефект вызывается мутацией единственного нуклеотида, приводящей к замещению аргинина на глютамин в апо В-100, в результате чего уменьшается сродство ЛПНП к рецепторам В/Е. Семейный дефект апопротеида В-100 встречается с несколько меньшей частотой, чем семейная гиперхолестеринемия, и отличается от нее отсутствием сухожильных ксантом и более низким уровнем ХС. В сложных диагностических случаях требуется применение методов молекулярного анализа. Для лечения применяют статины, секвестранты желчных кислот и никотиновую кислоту.
Цисбеталипопротеидемия (ГЛП III типа) относится к наиболее редким моногенным формам первичных ГЛП и встречается с частотой 1 случай на 5000 населения. Заболевание передается по аутосомно-рецессивному типу и связано с наличием мутантной формы апо Е (апо Е2). Поскольку этот апопротеин опосредует связывание ремнантных частиц, образующихся при катаболизме ХМ и ЛПОНП с В/Е рецепторами печени с их последующим извлечением из крови, уровень этих частиц значительно возрастает, что проявляется повышением как содержания ХС, так и ТГ в плазме крови. Ремнантные частицы, накапливающиеся в крови при ГЛП III типа, называются бета-ЛПОНП, поскольку они характеризуются более быстрой подвижностью при электрофорезе, чем обычные ЛПОНП. Отсюда и происходит название данной аномалии - дисбеталипопротеидемия. Для формирования ГЛП III типа недостаточно наличия генетического дефекта, необходимы и другие факторы - гипотиреоидизм, сахарный диабет, ожирение, злоупотребление алкоголем. Поэтому заболевание, как правило, развивается у взрослых. Клинические признаки дисбеталипопротеидемии могут включать линейный ксантоматоз складок ладоней и пальцев, а также тубероэруптивные ксантомы. При ГЛП III типа возникает распространенный атеросклеротический процесс с поражением коронарных, сонных, почечных артерий и сосудов конечностей. Диагноз устанавливают с помощью идентификации изоформ апо Е.
Дисбеталипопротеидемия весьма чувствительна к диетической терапии, и резкое ограничение потребления насыщенных жиров наряду со снижением избыточной массы тела нередко устраняет нарушение липидного состава плазмы крови. При медикаментозной терапии предпочтение отдают фибратам и статинам.
Семейная эндогенная гипертриглицеридемия (СЭГ) встречается примерно у одного из 300 человек и характеризуется повышением уровня ЛПОНП (IV тип ГЛП). Уровень ТГ обычно составляет от 200 до 500 мг/дл (2,3-5,7 ммоль/л), содержание ХС нормально или несколько повышено, а уровень ХС ЛПНП понижен. Риск ИБС увеличен в умеренной степени. В редких случаях СЭГ проявляется как ГЛП V типа с содержанием ТГ>1000 мг/дл (11,3 ммоль/л) и гиперхолестеринемией. При этом варианте СЭГ риск ИБС значительно повышен. Кроме того, существует реальная опасность развития острого панкреатита. Проводится терапия, направленная на снижение уровня ТТ (диета с ограничением жира, фибраты).
Семейная хиломикронемия (СХ) встречается крайне редко и характеризуется повышением уровня циркулирующих ХМ, которые сохраняются в плазме крови спустя 12 ч голодания. На наличие ХМ указывает сливкообразный слой над супернатантом. Уровень ТГ может превышать 1000 мг/дл (11,3 ммоль/л), содержание ХС остается нормальным или несколько повышается. СХ возникает вследствие снижения активности липопротеидлипазы в результате ее генетического дефекта или образования мутантных форм апо С-II, который является ее активатором. СХ наследуется по аутосомно-рецессивному типу, возникает у детей и проявляется абдоминальными болями и панкреатитом. Характерно наличие эруптивных ксантом, которые могут занимать большую часть поверхности кожи. Эффективна диетическая терапия, заключающаяся в ограничении потребления жиров до 10% от общей калорийности рациона.
Вторичные ГЛП осложняют течение ряда заболеваний и синдромов, а также могут быть связаны с приемом некоторых лекарственных препаратов. У больных с инсулиннезависимым сахарным диабетом часто выявляется гипертриглицеридемия, обусловленная усилением синтеза ЛПОНП и сочетающаяся со снижением уровня ХС ЛПВП. При злоупотреблении алкоголем также нередко наблюдается гипертриглицеридемия (ГЛП IV типа), которую связывают с образованием дополнительного пула свободных жирных кислот вследствие окисления этанола в печени. Гипотиреоз может быть причиной обратимой ГЛП IIа и IIв типов, а в редких случаях - и решающим фактором возникновения ГЛП III типа (дисбеталипопротеидемии). У больных с механической желтухой вследствие избыточного поступления в кровь лецитина синтезируются аномальные ЛП-Х, что сопровождается повышением уровня ХС и ТГ в плазме крови. Содержание ХС и ТГ также закономерно увеличивается у больных с нефротическим синдромом, при котором наиболее часто встречаются IIа и IIв типы ГЛП. К ГЛП может привести терапия некоторыми лекарственными препаратами. Хорошо известно, что тиазидные диуретики повышают уровень как ХС, так и ТГ, а бета-блокаторы уменьшают концентрацию ХС ЛПВП и увеличивают содержание ТГ.
Основное значение в коррекции вторичных ГЛП принадлежит выявлению и лечению основного заболевания. В частности, показано, что адекватная заместительная гормональная терапия обычно приводит к нормализации уровня липидов у больных с сахарным диабетом и гипотиреозом, аналогичный эффект наблюдается в случае отказа от потребления спиртных напитков при индуцированной алкоголем гипертриглицеридемии. Больным с необратимыми органическими изменениями (хронические заболевания почек, билиарный цирроз печени) необходима гиполипидемическая терапия.
Комментарии
ПРАКТИКА ПЕДИАТРА
