Возможности кардио-метаболической терапии инфекционных миокардитов и кардиомиопатий у детей
СтатьиОпубликовано в журнале:
«Практика педиатра», октябрь 2012, с. 50-55
Т.А. Руженцова, А.В. Горелов, ФБУН ЦНИИ эпидемиологии Роспотребнадзора, Москва
В настоящее время большинством специалистов, занимающихся вопросами некоронарогенной патологии сердца, признается, что частота инфекционных миокардитов очень высока и многие из них остаются недиагностированными [1].
Однако даже легкие и латентно протекающие процессы могут проявиться жизнеугрожающими нарушениями ритма и острой сердечной недостаточностью. По данным российских и зарубежных исследователей, до 2% всех случаев острых респираторных заболеваний, включая грипп, сопровождаются развитием миокардита. Примерно у 10% из всех умерших от инфекционных заболеваний в ходе аутопсий обнаруживают воспалительную инфильтрацию в миокарде [2].
Трудности диагностики связаны с многообразием клинической симптоматики, отсутствием специфичных клинических признаков [3]. Легкие и стертые формы не сопровождаются четкими, типичными для поражений миокарда проявлениями [4, 5]. Отмечаются признаки хронической интоксикации и симптомы левожелудочковой и/или правожелудочковой сердечной недостаточности.
Физические нагрузки и отсутствие своевременно начатой терапии при неустановленном вовремя диагнозе ведут к распространению поражения миокарда, прогрессирующему снижению фракции выброса, а затем – к формированию очагов кардиосклероза. Основной терапией инфекционных миокардитов и кардиомиопатий, без сомнений, можно считать этиотропную, в зависимости от выявленного возбудителя. Однако, против ряда вирусов, на которые приходится наибольшее число миокардитов, в частности против цитомегаловирусной инфекции, вируса Эпштейна – Барр, энтеровирусов, нет препаратов с высокой надежной эффективностью. Противовоспалительные средства назначаются по показаниям. Так, кортикостероиды необходимы при аутоиммунных и аллергических миокардитах. В ситуациях с активной репликацией вирусов эта группа препаратов может приводить к затяжному течению с последующим формированием дилатационной кардиомиопатии, что было доказано в зарубежных исследованиях. НПВС не рекомендуется назначать при легких и среднетяжелых процессах вирусной этиологии, поскольку они задерживают элиминацию вируса. В лечении этих пациентов показаны иммуноглобулины, но в части случаев они не приводят к ликвидации возбудителя и могут стать причиной аллергической реакции. Применение цитостатиков часто влечет за собой подавление различных звеньев иммунной системы и может быть оправдано только при тяжелых формах с выраженным аутоиммунным механизмом. По соответствующим показаниям, безусловно, необходимы коррекция водно-электролитного баланса, дезинтоксикационная терапия, назначение иммуномодуляторов, инотропных, антиаритмических, вазодилатирующих и диуретических препаратов.
Однако из всех вышеперечисленных лекарственных средств нет ни одного достаточно эффективного и безопасного, которое могло бы быть показано любому ребенку с диагнозом «инфекционный миокардит» или «кардиомиопатия».
В условиях инфекционно-воспалительного процесса в миокарде основными задачами терапии, помимо элиминации возбудителя, являются ограничение зоны повреждения и поддержание адекватного функционирования кардиомиоцитов. Любое инфекционное заболевание сопровождается активацией перекисного окисления липидов, что приводит к разрушению мембран, выходу различных веществ из клетки и увеличению зоны повреждения. Естественная антиоксидантная система организма: альфа-токоферол (витамин А), аскорбиновая кислота, бета-каротин (провитамин А) и убихинон (коэнзим Q10) [6–11]. Наибольший интерес из них представляет коэнзим Q10, так как помимо того, что он является сильным антиоксидантом, восстанавливающим не только свою активность, но и активность альфа-токоферола, он обязательный участник аэробного синтеза АТФ в клетках. Также коэнзим Q10 улучшает эндотелиальную функцию. Иммуномодулирующее действие убихинона, выражается в способности активизировать макрофаги в крови [12]. При инфекционных заболеваниях, особенно при тяжелых и среднетяжелых формах, сердечно-сосудистая система работает в условиях повышенного энергопотребления с увеличением образования свободных радикалов, что является теоретической предпосылкой эффективности применения коэнзима Q10.
Недавно появился новый лекарственный препарат, содержащий 30 мг коэнзима Q10 и 4,5 мг витамина Е в 1 мл, – Кудесан. В ряде исследований, проведенных в группах пациентов с вегетососудистой дистонией, нарушениями ритма, иммунодефицитными состояниями, была показана его эффективность [13–17]. Однако эффективность его у детей с поражениями миокарда при инфекционных заболеваниях оценена не была.
Цель настоящего исследования – оценить эффективность Кудесанапри лечении инфекционных миокардитов и кардиомиопатий у детей.
Пациенты и методы.
В исследование было включено 97 детей, госпитализированных в детскую инфекционную больницу № 5 СВАО г. Москвы с различными острыми инфекционными заболеваниями, при которых на различных сроках от начала были выявлены признаки миокардита, миоперикардита или инфекционной кардиомиопатии. Все дети были в возрасте от 1 года до 10 лет, среди них 76 мальчиков и 33 девочки. Больных рандомизировали на 3 группы. В основную вошло 30 пациентов, которым дополнительно к базисной терапии был назначен Кудесанв дозе 1 мг/кг/сут. В группу сравнения («А») включили 30 пациентов, получивших инозин (Рибоксин), в среднем 10 мг/кг/сут. Группа сравнения «В» (37 детей), в которой дополнительная метаболическая терапия не назначалась, была сформирована ретроспективно.
Возрастной состав групп представлен в таблице 1. Все заболевшие были госпитализированы с 1-х по 4-е сутки от момента начала основного заболевания. Преобладали дети со средне-тяжелой формой (таблица 2), преимущественно с сочетанием симптомов острого респираторного заболевания (ОРЗ) и острой кишечной инфекции (ОКИ). Почти у 50% детей была выявлена пневмония, преимущественно односторонняя. ОКИ у большинства пациентов проявлялась в виде гастроэнтерита, значительно реже – в виде гастроэнтероколита. Клинические формы представлены в таблице 3.
Этиологическая структура сравниваемых групп показана в таблице 4.
Таблица 1
Распределение по возрасту в группах детей, включенных в исследование
| Возраст | Основная группа (Дети, получавшие Кудесан), n = 30 (100%) | Группа сравнения «А» (Дети, получавшие инозин), n = 30 (100%) | Группа сравнения «В» (Дети, не получавшие метаболической терапии), n = 37 (100%) |
| От 1 до 3 лет | 19 (63%) | 20 (67%) | 23 (62%) |
| От 3 до 7 лет | 11 (37%) | 8 (27%) | 11 (30%) |
| От 7 до 10 лет | 0 | 2 (6%) | 3 (8%) |
Таблица 2
Распределение по тяжести основного заболевания среди групп детей, включенных в исследование
| Основная группа (Дети, получавшие Кудесан), n = 30 (100%) | Группа сравнения «А» (Дети, получавшие инозин), n = 30 (100%) | Группа сравнения «В» (Дети, не получавшие метаболической терапии), n = 37 (100%) | |
| Легкая форма | 0 | 0 | 3 (8%) |
| Среднетяжелая форма | 27 (90%) | 28 (93%) | 30 (81%) |
| Тяжелая форма | 3 (10%) | 2 (7%) | 4 (11%) |
Таблица 3
Клинические формы основного заболевания в группах пациентов, включенных в исследование
| Клиническая форма | Основная группа (Дети, получавшие Кудесан), n = 30 (100%) | Группа сравнения «А» (Дети, получавшие инозин), n = 30 (100%) | Группа сравнения «В» (Дети, не получавшие метаболической терапии), n = 37 (100%) |
| Ринофарингит | 18 (60%) | 17 (57%) | 11 (30%) |
| Ангина | 1 (3%) | 1 (3%) | 2 (5%) |
| Отит | 1 (3%) | 0 | 0 |
| Бронхит | 3 (10%) | 4 (13%) | 3 (8%) |
| Обструктивный бронхит | 1(3%) | 0 | 0 |
| Пневмония | 14 (47%) | 10 (33%) | 16 (43%) |
| Гастроэнтерит | 17 (57%) | 15 (50%) | 17 (46%) |
| Гастроэнтероколит | 6 (20%) | 6 (20%) | 7 (19%) |
Таблица 4
Этиологическая структура групп пациентов, включенных в исследование
| Этиология заболевания | Основная группа (Дети, получавшие Кудесан), n = 30 (100%) | Группа сравнения «А» (Дети, получавшие инозин), n = 30 (100%) | Группа сравнения «В» (Дети, не получавшие метаболической терапии), n = 37 (100%) |
| Парагрипп | 8 (27%) | 6 (20%) | 11 (30%) |
| Аденовирусная инфекция | 3 (10%) | 4 (13%) | 5 (14%) |
| Респираторно-синцитиальная инфекция | 2 (7%) | 0 | 3 (8%) |
| Сальмонеллез | 3 (10%) | 5 (17%) | 6 (16%) |
| Иерсиниоз | 1 (3%) | 0 | 0 |
| Ротавирусная инфекция | 3 (10%) | 4 (13%) | 5 (14%) |
| Норавирусная инфекция | 1 (3%) | 0 | 1 (3%) |
| Неуточненное ОРЗ (изолированно) | 4 (13%) | 5 (17%) | 7 (19%) |
| Неуточненная ОКИ (изолированно) | 2 (7%) | 3 (10%) | 2 (5%) |
| Неуточненное ОРЗ в сочетании с неуточненной ОКИ | 8 (27%) | 7 (23%) | 5 (14%) |
Детей с ранее диагностированной кардиопатологией в исследование мы не включали.
Диагностика включала ЭКГ в 12 стандартных отведениях и ЭхоКГ, а также определение уровней МВ-КФК, альфа-ГБДГ, АСТ. Спустя 1 месяц после включения в исследование все пациенты приглашались на осмотр и дополнительное обследование. При сохранении симптоматики лечение продолжали еще в течение месяца. По результатам обследования на 56–64-й день терапии по необходимости препарат оставляли на следующий месяц, после чего оценивали итоговую эффективность.
Результаты исследования и обсуждение.
По результатам обследования почти у 50% детей был диагностирован острый инфекционный миокардит, реже – миоперикардит. В остальных случаях нарушения соответствовали инфекционной (вторичной) кардиомиопатии, что представлено в таблице 5.
Таблица 5
Нозологические формы сердечнососудистых осложнений в группах пациентов, включенных в исследование
| Нозологическая форма | Основная группа (Дети, получавшие Кудесан), n = 30 (100%) | Группа сравнения «А» (Дети, получавшие инозин), n = 30 (100%) | Группа сравнения «В» (Дети, не получавшие метаболической терапии), n = 37 (100%) |
| Острый миокардит, легкое течение | 6 (20%) | 7 (23%) | 5 (14%) |
| Острый миокардит, среднетяжелое течение | 8 (27%) | 6 (20%) | 8 (22%) |
| Острый миоперикардит, легкое течение | 1 (3%) | 2 (7%) | 1 (3%) |
| Острый миоперикардит, среднетяжелое течение | 2 (7%) | 0 | 1 (3%) |
| Инфекционная кардиомиопатия | 13 (43%) | 15 (50%) | 22 (59%) |
У всех детей были клинические и ЭКГ изменения в сочетании с повышением активности кардиоспецифичных ферментов. Отклонения по ЭхоКГ наблюдали у 76% больных.
Спустя 2 недели с момента добавления к базисной терапии Кудесана у всех больных мы наблюдали положительную динамику по всем рассматриваемым показателям. У 7 пациентов, не получавших метаболических препаратов, и у 3 детей, принимавших инозин, отмечали отрицательную динамику с повышением МВ-КФК, альфа-ГБДГ и АСТ, изменениям на ЭКГ и по данным ЭхоКГ. Анализ историй болезней показал, что ухудшение, как правило, связано с присоединением сопутствующей инфекции или при тяжелом течении основного заболевания.
Обследование, проведенное в конце 1-го месяца, показало полное выздоровление у 14 человек из основной группы. У 5 больных на фоне приема Кудесана нормализация всех показателей была отмечена через 8 недель и еще у 6 – через 12 недель. У 5 больных изменения сохранялись: у 3 детей – пролапсы митрального и трикуспидального клапанов с регургитацией в сочетании с небольшой гиперферментемией, у 2 из них с нарушениями на ЭКГ. У одного ребенка оставалась гиперферментемия и расширение полости левого желудочка и еще у одного – нарушение де- и реполяризации. Анализ историй болезней этих пациентов привел нас к выводу, что длительное сохранение изменений связано, как правило, с тяжелым течением ОРЗ и ОКИ смешанной этиологии, осложненных миокардитом или миоперикардитом среднетяжелого течения. При сравнении результатов обследования детей, получавших Кудесан, была отмечена ранняя нормализация лабораторных показателей (р = 0,0001) по сравнению с больными, принимавшими инозин или не получавшими метаболических препаратов, что показано на рисунке 1. Восстановление параметров ЭКГ и ЭхоКГ происходило достоверно быстрее в основной группе, чем в группах сравнения (р = 0,0001).
Динамика МВ-КФК, как самого чувствительного из применявшихся лабораторных показателей, представлена на рисунке 2. Средние уровни активности этого ферментов у больных, получавших Кудесан, достоверно ниже, чем при приеме инозина или в отсутствии метаболической терапии, что наиболее ярко проявлялось к концу 2–3-го месяца. Таким образом, при парагриппе, аденовирусной, респираторно-синцитиальной и ротавирусной инфекциях, а также при сальмонеллезе у детей возможно развитие миокардитов, миоперикардитов и инфекционной кардиомиопатии. Необходимым компонентом терапии являются метаболические препараты, поддерживающие энергетические процессы в митохондриях и защищающие мембраны кардиомиоцитов от повреждения свободными радикалами. Проведенное исследование показало, что добавление Кудесана в дозе 1 мг/кг/сут. к необходимой базисной терапии способствует сокращению продолжительности заболевания при инфекционных поражениях миокарда у детей.
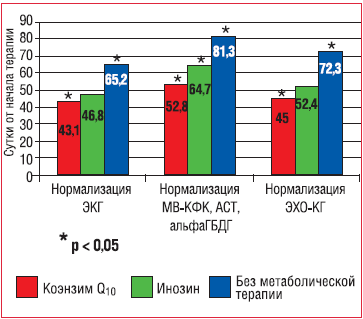
Рисунок 1
Сроки нормализации ЭКГ, уровней МВ-КФК, альфа-ГБДГ, АСТ и ЭХО-КГ в сравниваемых группах детей.
Рисунок 2
Средние уровни активности МВ-КФК у детей в сравниваемых группах.
Список литературы находится в редакции.

