Использование жировых эмульсий ?-3 жирных кислот в интенсивной терапии: взгляд клинициста
СтатьиF. GRIMMINGER, W. SEEGER, К. MAYER
Justus Liebig University Giessen, Germany (Correspondence to: K. Mayer, Department 0' Internal Medicine, Justus. Liebig University Giessen, KlinikstraSe 36, D-35392 Giessen, Germany)
Абстракт
ω-3 липиды использовались в медицине давно, благодаря своей способности снижать активность воспалительных заболеваний. В отделениях интенсивной терапии (ОИТ) у пациентов с острыми воспалительными болезнями, такими как сепсис и острый респираторный дистресс-синдром (ОРДС), часто возникает необходимость в искусственном питании. Патогенетическая основа этих заболеваний - гипервоспалительный ответ с чрезмерной активностью лейкоцитов, последующими нарушениями микроциркуляции и вторичным повреждением органов. Лечение этих пациентов затруднено тем, что гипервоспалительная (синдром системного воспалительного ответа [SIRS]) и гиповоспалительная (компенсаторный противовоспалительный синдром [CARS]) фазы могут чередоваться в течение заболевания. По этой причине широкий ряд противовоспалительных агентов не продемонстрировал эффективности при лечении септических пациентов: являясь эффективными средствами подавления гипервоспаления во время SIRS, они ослабляли антимикробную защиту при CARS. Противовоспалительные цитокины, эффективные в раннюю фазу сепсиса, могут быть вредными, когда назначаются в позднюю фазу. Недавно, в качестве нового подхода, стали доступными ω-3 жировые эмульсии. Назначение ω-3 жирных кислот (ЖК) энтеральным путем для влияния на воспаление при сепсисе не эффективно, т. к. на это потребуются месяцы. Парентеральное введение чистых омега-3 липидов значительно превосходит энтеральное по кинетике и эффективности. При внутривенном использовании ω-3 жировых эмульсий может быть смягчено гипервоспаление и предотвращено последующее развитие противовоспалительной фазы. Так как ω-3 ЖК взаимодействуют с трансмембранными сигнальными молекулами, они, вероятно, способны снижать гиперреактивность в обеих составляющих сепсиса (SIRS и CARS). Благодаря этому свойству ω-3 ЖК способны ингибировать неконтролируемый выброс активных лейкоцитов и перенаправить защитные функции макроорганизма на борьбу с микробами.
Ключевые слова: лейкоциты; сепсис; ОРДС; ω-3 жировые эмульсии; парентеральное питание.
Введение
Концепция фармакологической интервенции с помощью ω-3 липидов
Возможность ω-3 липидов при пероральном / энтеральном назначении изменять активность лейкоцитов, продукцию медиаторов липидной природы и высвобождение цитокинов давно вызывала дискуссии (1, 2). Недавно стали доступны жировые эмульсии на основе рыбьего жира, богатого ω-3 липидами для внутривенного введения, которые имеют еще больший потенциал в фармакологическом воздействии. В этом обзоре описываются биохимические основы введения разных жировых эмульсий на воспалительный ответ и обсуждаются потенциальные возможности использования жировых эмульсий при заболеваниях с гиперактивацией иммунной системы.
Влияние ω-3 липидов на межклеточную передачу информации - медиаторы и цитокины
Медиаторы липидной природы синтезируются по липооксигеназному, циклооксигеназному путям и с помощью цитохрома Р-450 из жирных кислот, таких как арахидоновая (АА), в качестве субстрата. К ним относятся эйкозаноиды (простагландины, тромбоксаны, лейкотриены (LT), липоксины, гидроксидные и эпоксидные производные жирных кислот) и фактор активирующий тромбоциты (PAF). Они действуют как внутриклеточные сигнальные молекулы и могут влиять на секрецию иммунорегуляторных цитокинов. Эйкозаноиды вовлечены как в про- так и в противовоспалительные процессы при сепсисе.
Арахидоновая кислота (АА) относится к семейству ω-6 ЖК и представляет наиболее распространенную полиненасыщенную жирную кислоту в рационе европейского человека. Омега-3 ЖК, в которых последняя двойная связь от метильного конца находится межу третьим и четвертым атомами углерода, представлены эйкозапентаеновой (ЕРА) и докозагексаеновои (DHA) кислотами, входящими в состав мяса тюленей и холодноводных рыб. Они служат альтернативными субстратами для липооксигеназного, циклооксигеназного путей и, возможно, для цитохрома Р-450, что приводит к образованию триеновых простаноидов (вместо диеновых из АА) и 5-го ряда LT (вместо 4-го из АА) (2). Несмотря на тот факт, что большинство воспалительных липидных медиаторов являются производными АА, ЕРА представляет собой более предпочтительный субстрат для липоокигеназного пути, чем АА. При одинаковой доступности обеих жирных кислот в результате их метаболизма образуется больше производных ЕРА за счет уменьшения количества производных АА. Большинство производных ЕРА, включая 5-й ряд цистеинил-лейкотриенов, LTB5 и тромбоксан А3 обладают гораздо меньшим воспалительным и вазомоторным потенциалом, чем производные АА и даже могут иметь антагонистические с ними свойства (5).
Более того, ЕРА и DHA способны модулировать воспаление путем уменьшения синтеза провоспалительных цитокинов: несколько недель приема ω-3 ЖК приводит к уменьшению продукции фактора некроза опухоли а (TNF-а) и интерлейкина 1 (IL-1) мононуклеарными клетками (6, 7). Вдобавок, лейкоциты сами по себе крайне чувствительны к свободным ПНЖК. Обогащение диеты ПНЖК или экспозиция лейкоцитов с ПНЖК in vitro приводила к подавлению продукции IL-2, презентации антигена, пролиферации лимфоцитов и активности натуральных киллеров (2). Таким образом, основной целью назначения ω-3 ЖК больным в критических состояниях является уменьшение метаболизма АА до провоспалительных медиаторов.
Влияние ω-3 липидов на внутриклеточную передачу информации - метаболизм второго мессенджера
Присоединение к рецептору приводит к активации фосфатидил-инозитол-специфичной фосфолипазы С (PI-PLC). Этот фермент расщепляет фосфатидил-инозитол-дифосфат (РIР2) на диацилглицерол (DAG) и инозитол-трифосфат (IР3). От того, какие ЖК входят в состав РIР2, зависит генерация инозитол-фосфатов (IРХ), т. к. накопление ω-3 ПНЖК в фосфатидил-инозитоле (PI) при потреблении рыбьего жира ведет к снижению образования IРХ и DAG с последующим уменьшением лейкоцитарного ответа на воспалительный стимул (8). Далее, жирнокислотный состав DAG влияет на DAG-зависимую активацию протеинкиназы С (РКС). DAG с ω-3 ПНЖК в позиции sn-2 слабее индуцирует РКС, чем если в этой позиции находится АА. После DAG-активации, РКС перемещается на клеточную мембрану и присоединяется к фосфатидилсерину. На реакцию влияет жирнокислотный состав фосфолипидов: фосфатидилсерин с высоким содержанием ω-3 ПНЖК ослабляет связывание и последующую активность РКС (9, 10). В результате этого, принимая во внимание сумму эффектов на систему второго мессенджера, можно ожидать ослабление сопряжения между стимулом и ответом, что влияет на активацию клетки. Следовательно, состояние иммунореактивных лейкоцитов может быть смещено от гиперреактивного в сторону нормальной функции. Таким образом, ω-3 липиды могут применяться при гипервоспалительном состоянии или в качестве профилактики этого состояния у пациентов высокого риска.
Влияние ω-3 липидов на поведение лейкоцитов
Истинное предназначение лейкоцита - это контролируемое высвобождение его деструктивного потенциала во время схватки с инфекционным агентом. На своем пути к очагу инфекции лейкоциты должны покинуть просвет сосуда и мигрировать в направлении бактериальной клетки в воспаленной ткани. Эта основная схема работает при остром и хроническом воспалении. Однако, если лейкоцит гиперреактивен, его оружие может быть неверно направлено против организма хозяина (гипервоспаление) - механизм, который работает при аутоиммунных болезнях и у больных в критическом состоянии. Чрезмерный воспалительный ответ может также сделать острую или хроническую болезнь очень продолжительной. Лейкоциты покидают просвет сосуда через эндотелий. В настоящее время этот процесс представляется многоэтапным. Трансэндотелиальная миграция лейкоцитов начинается с прилипания к стенке сосуда, затем происходит передвижение по эндотелиальным клеткам, плотная адгезия и миграция в субэндотелиальное пространство через межклеточные щели. В этом процессе участвуют молекулы адгезии, к которым относятся селектины и их антагонисты, р, и р2 интегрины и несколько представителей семейства иммуноглобулинов. Провоспалительные цитокины способны усиливать экспрессию молекул адгезии на эндотелиальных клетках. TNF-a и IL-1, образованные в воспаленной ткани, облегчают миграцию и направляют лейкоциты из внутрисосудистого пространства в очаг воспаления. Уменьшая TNF-зависимую активацию молекул адгезии, ω-3 ПНЖК снижают экстравазацию лейкоцитов.
Кроме того, ω-3 ПНЖК, доставленные внутривенной инфузией или освобожденные из липидов эндотелиальной мембраны влияют на поведение лейкоцитов при воспалении, воздействуя на синтез лейкотриенов. В условиях воспаления эндотелиальные клетки освобождают АА для того, чтобы присоединенные к ним нейтрофилы продуцировали LTA4. В свою очередь LTA4 используется самим нейтрофилом для синтеза LTB4 - мощного хемоаттрактанта, или смежной эндотелиальной клеткой для синтеза LТС4 - сильного поскапиллярного вазоконстриктора. Оба эти медиатора липидной природы способствуют экстравазации лейкоцитов. ЕРА, как описано выше, является более выгодным, по сравнению с АА субстратом для продукции лейкотриенов, и уменьшает АА-зависимый синтез лейкотриенов. Более того, лейкотриены - производные ЕРА, - ингибируют хемоаттрактантную активность и стимулирующий потенциал лейкотриенов - производных АА. Описанные эффекты объединяются в системный противовоспалительный эффект со снижением миграции и смягчением активации лейкоцитов.
Различный противовоспалительный потенциал энтерального и парентерального путей введения ω-3 липидов
Несмотря на то что основной опыт по применению ω-3 ПНЖК был получен при их энтеральном назначении, этот путь имеет отрицательные стороны. Терапевтический эффект наступает медленно и, следовательно, такой путь приема неприменим при острых заболеваниях. При использовании капсул с рыбьим жиром биодоступность молекул ω-3 ПНЖК ограничена, т. к. они попадают в системный кровоток после прохождения кишечного барьера, организации в везикулы в виде триглицеридов и попадания в печень, в результате чего теряются свободные ω-3 ПНЖК из-за процесса ремоделирования липидов. При этом доступность свободных жирных кислот для участия в процессе воспаления как в лейкоцитах, так и в эндотелиальных клетках ограничена. В отличие от этого, при внутривенной инфузии жировой эмульсии путь ремоделирования липидов в печени и кишечнике шунтируется, большое количество синтетических липидов активирует эндотелиальные липопротеинлипазы и вызывает перемещение этих ферментов из связанного с клеткой состояния в сосудистое русло. В результате резкого повышения концентрации свободных ЖК в плазме становится возможным их свободное потребление клетками, рост концентрации ЖК в клетках и свободные ЖК - предшественники медиаторов липидной природы (например, ЕРА или АА) становятся доступными в избытке (11). Внутривенная инфузия жировых эмульсий (Омегавен) обладает более выгодной фармакокинетикой и возможностью ввести большее количество ЖК, чем при энтеральном их потреблении (12, 13).
Терапия внутривенными ω-3 ЖК в отделении интенсивной терапии
Несмотря на тот факт, что в отделении интенсивной терапии ОИТ преимущество отдается энтеральному питанию как более физиологичному, некоторые пациенты нуждаются в парентеральном питании, т. к. их состояние не позволяет вводить питательные вещества в кишечник. Это также относится к пациентам после больших операций на желудочно-кишечном тракте и больным с обострениями воспалительных заболеваний толстой кишки, таких как болезнь Крона и неспецифический язвенный колит. Кроме того, в парентеральном питании могут нуждаться пациенты с тяжелым сепсисом или острым респираторным дистресс-синдромом (ОРДС), если у них не может быть обеспечен пассаж по кишечнику по причинам ишемии или применения медикаментов, приводящих к параличу гладкой мускулатуры. Ишемическое повреждение может быть вызвано шоком и сопутствовать синдрому недостаточности спланхнических органов. В этих случаях парентеральное питание является обязательным, а жировые эмульсии - это фундаментальная составляющая современных схем внутривенного питания благодаря своей калорической ценности и предотвращения жировых изменений в печени, которые имеют место при использовании углеводородов, как единственного источника энергии. Внутривенное введение эмульсий рыбьего жира предназначено не для парентерального питания, а для фармакологических эффектов чистых омега-3 ЖК. Поэтому эмульсии очищенного рыбьего жира могут применяться независимо от вида питания (парентеральное, энтеральное, естественное).
Гипервоспаление как терапевтическая мишень в отделении интенсивной терапии
Сепсис, тяжелый сепсис и септический шок продолжают оставаться причинами высокой летальности (от 30 до 60%). Современные достижения в интенсивной терапии не смогли повлиять на эти цифры (14-17). Таким образом, сепсис продолжает оставаться главной причиной смерти больных в ОИТ во всем мире.
Здоровый организм защищен от вторжения микробов сложной, хорошо регулируемой и мощной иммунной системой. Однако в определенных условиях, может происходить неконтролируемый выброс большого количества высокоактивных и потенциально аутотоксичных медиаторов, что ведет к неселективной гиперреактивности иммунной защиты (3, 8, 19). Кроме микробной инвазии, синдром системного воспалительного ответа (SIRS) может быть вызван разными видами повреждения тканей организма. Более того, не только микробы сами по себе, но и такие субстанции, как эндотоксин (липополисахарид [LPS]), экзотоксины, суперантигены, тейхоевая кислота, выделяемые бактерией, могут запустить избыточное высвобождение воспалительных медиаторов и вести к гипервоспалительному повреждению организма.
Традиционные средства для иммуносупрессии
Смягчение избыточного воспалительного ответа считается одной из целей в терапии сепсиса. Такая терапия исследовалась на животных и, несмотря на положительные результаты в эксперименте, III фаза клинических испытаний не показала положительного влияния на выживаемость (15). Главным недостатком обычно используемых иммуносупрессивных средств является то, что врач должен определить, находится ли пациент в состоянии гипервоспаления в данный момент. К сожалению, в настоящее время нет рутинного лабораторного теста, позволяющего дифференцировать гипер- и гиповоспалительный статусы. Задолго до появления современных взглядов на противовоспалительную терапию (например, антитела к TNF-a или IL-1) при сепсисе были опробованы высокие дозы стероидов и нестероидные противовоспалительные средства (НПВС) (например, ибупрофен). В больших мультицентровых исследованиях было доказано отсутствие влияния на выживаемость высоких доз стероидов при септическом шоке (20, 21). Более того, использование кортикостероидов в высоких дозах или в течение длительного времени было связано с повышенным риском желудочно-кишечного кровотечения и присоединения оппортунистических инфекций. В отношении НПВС недавнее мультицентровое исследование не продемонстрировало влияния на выживаемость (22). Кроме того, использование НПВС несет риск возникновения желудочно-кишечного кровотечения, почечной недостаточности и бронхоконстрикции. Оба этих терапевтических принципа в настоящее время считаются неприемлемыми в качестве препаратов первой линии при лечении септических пациентов. В заключении необходимо отметить, что теоретическое преимущество традиционных иммуносупрессивных препаратов в гипервоспалительную фазу оборачивается большим недостатком в фазу иммунопаралича.
Модуляция иммунитета с помощью ω-3 ЖК: влияние на поведение воспалительного лейкоцита при монофазных гипервоспалительных болезнях
В отличие от значительной иммунной супрессии, вызываемой кортикостероидами, метотрексатом или циклоспорином, обогащение диеты рыбьим жиром индуцирует умеренную модуляцию иммунной системы при некоторых заболеваниях. При болезни Крона медиаторы липидной природы и цитокины приводят к развитию хронического поражения кишечника (23). Рыбий жир в энтеросолюбильной оболочке применяли в течение 1 года у пациентов высокого риска с болезнью Крона в стадии ремиссии. Это привело к значительному уменьшению количества рецидивов и снижению лабораторных признаков воспаления (24).
В трансплантологии важнейшей проблемой для клинициста остается острое и хроническое отторжение трансплантата. Рутинно используемые иммуносупрессив-ные препараты обладают серьезными побочными эффектами и заставляют искать альтернативные способы терапии этих осложнений, ω-3 ЖК в экспериментах на животных показали обнадеживающие результаты в отношении реперфузионного повреждения и отторжения. Клиническое доказательство эффективности назначения рыбьего жира получено на реципиентах почки (25), которые начинали принимать его одновременно с трансплантацией. У этих пациентов отмечался поразительно высокий уровень гломерулярной фильтрации, по сравнению с пациентами контрольной группы.
Также сообщается о благоприятных эффектах назначения рыбьего жира у больных псориазом, неспецифическим язвенным колитом и ревматоидным артритом.
Использование ω-3 липидов при ОРДС и сепсисе: влияние на гиперреактивность лейкоцитов
Острый респираторный дистресс-синдром (ОРДС) описан как острое воспалительное нарушение, сопровождающееся повышенной проницаемостью альвеоло-капиллярной мембраны, ведущее к физиологическим и рентгенологическим отклонениям не вследствие гипертензии в левом предсердии. Недавние сообщения акцентируют внимание на локальном дисбалансе про- и противовоспалительных медиаторов, а также дисбалансе оксидантного стресса и антиоксидантов, как на причинах повышенной склонности к развитию ОРДС (26, 27). Основными характеристиками этого синдрома являются: острая легочная гипертензия, вызванная тромбоксаном А2, последующий отек легких, вызванный лейкотриенами, цитокинами и другими медиаторами, и угрожающие нарушения вентиляционно-перфузионного соотношения (28).
Протективный эффект ω-3 ЖК хорошо изучен на моделях острого легочного повреждения. Инфузия свободной арахидоновой кислоты (АА) усиливает развитие отека легких и легочной гипертензии на модели легких при сепсисе. В отличие от этого, инфузия свободной эйкозапентаеновой кислоты (ЕРА) уменьшает отек легких и снижает гипертензию в малом круге кровообращения (29-33), что связано с образованием медиаторов липидной природы из ω-3 ЖК. К тому же обогащение диеты ω-3 ЖК уменьшало острое легочное повреждение при сепсисе путем снижения легочной гипертензии, уменьшения формирования отека и миграции нейтрофилов в легкие, снижения продукции липидных медиаторов - производных арахидоновой кислоты (1,34-38).
Как описано при септическом шоке, гипервоспалительная реакция наблюдается в начальной стадии заболевания. Параллельно с воспалительным ответом на повреждение инициируется противовоспалительная реакция, названная «компенсаторным противовоспалительным синдромом» (CARS) (17). Он состоит из активации противовоспалительных цитокинов, нарушения функции нейтрофилов и инактивации моноцитов, что ведет к ослаблению иммунной защиты и повышению восприимчивости к вторичной инфекции (40-43).
ω-3 липиды могут перенаправить иммунную защиту против микроорганизмов
Обе фазы сепсиса - гипервоспалительная (SIRS) и гиповоспалительная (CARS) - ведут к неэффективности защиты организма (Рис. 1 и 2). При SIRS лейкоциты с повышенной реактивностью высвобождают свой разрушающий потенциал еще до того, как достигнут очага инфекции, и повреждают организм с последующим развитием вторичной недостаточности органов. При CARS лейкоциты неспособны бороться с микроорганизмами, т. к. их потенциал уже использован в SIRS или они парализованы действием противовоспалительных медиаторов. Принимая во внимание описанные выше свойства ω-3 липидов, можно предположить, что назначение септическим пациентам жировых эмульсий на основе рыбьего жира может быть эффективно.
Рис. 1. (а) Двухфазное течение иммунных нарушений при сепсисе. После начала заболевания наблюдается взрывной выброс провоспалительных медиаторов, таких как TNF-a и IL-1, что приводит к возникновению гипервоспалительного ответа (SIRS). Далее, с компенсаторным ростом концентрации противовоспалительных медиаторов, развивается иммунопаралич (CARS).

Рис. 1. (b) Из-за недостаточного клиренса микроорганизмов может развиться порочный круг и обострение септического процесса.
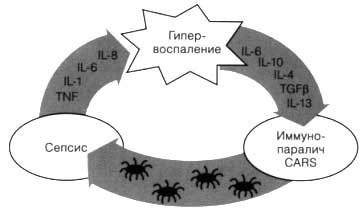
Рис. 2. (а) В двухфазном течении септического процесса гиперактивация лейкоцитов при SIRS приводит к вторичному повреждению органов. Последующий CARS характеризуется нарушением способности лейкоцитов поражать микробы и развитием вторичных инфекций.
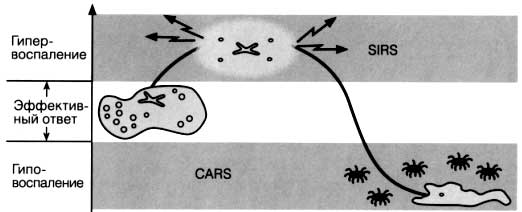
Рис. 2. (b) Инфузия ω-3 липидов смягчает как гипервоспаление, так и выраженный гиповоспалительный ответ путем влияния на меж- и внутриклеточную передачу информации.
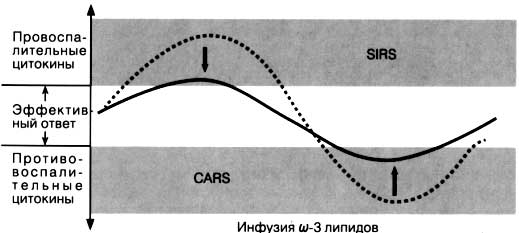
ω-3 жиры способны уменьшать избыточный иммунный ответ при SIRS и перенаправить «заблудившиеся» лейкоциты к очагу инфекции. Ограничивая саморазрушающие процессы в лейкоцитах, ω-3 липиды перенаправляют защиту организма против микроорганизмов и контролируют иммунный ответ. Важное исследование по энтеральному введению, подчеркивающее эту концепцию, было проведено Galban et al. (44), т. к. им удалось продемонстрировать снижение летальности у пациентов с сепсисом. Однако, ввиду того что их энтеральная смесь была обогащена не только ω-3 ЖК, нельзя сделать окончательный вывод об эффективности каждого из компонентов. Кроме того, эффекты перорального / энтерального и парентерального введения ω-З ЖК могут отличаться, т. к. внутривенная инфузия (но не пероральное / энтеральное введение) эмульсии на основе рыбьего жира приводит к массивному повышению концентраций свободных ЕРА и DHA в плазме с выраженным эффектом на высвобождение провоспалительных медиаторов при SIRS.
ω-3 липиды ослабляют повышенную реактивность лейкоцитов и предотвращают CARS /SIRS
Использование внутривенной инфузии чистых ω-3 липидов в ОИТ может влиять на иммунную реактивность организма. Снижение степени гипервоспаления в первой фазе сепсиса приводит к тому, что лейкоциты не истощаются и не растрачивают свой деструктивный потенциал. Благодаря этому во второй фазе повышение концентрации противовоспалительных цитокинов не вызовет столь выраженного паралича лейкоцитов. Более сбалансированная иммунная защита организма будет обеспечена предотвращением «крайностей» в течении сепсиса (периодов гипер- и гиповоспаления).
Заключение
Недавние достижения в медицине показали, что добавление с схемы лечения омега-3 ЖК может влиять на воспалительные и иммунологические процессы при некоторых заболеваниях, ω-3 липиды способны модулировать синтез медиаторов липидной природы, высвобождение цитокинов, регулировать активацию лейкоцитов и эндотелиальных клеток. Энтеральный прием ω-3 липидов воздействует на активность хронических воспалительных болезней, таких как ревматоидный артрит, болезнь Крона, а также эффективен при трансплантации почки. Внутривенное введение ω-3 жировых эмульсий значительно превосходит оральное их потребление по фармакокинетике и конечной концентрации свободных ЖК в плазме и, следовательно, может применяться для терапии острых гипервоспалительных заболеваний в интенсивной терапии. У пациентов с сепсисом, благодаря снижению активности гипервоспалительной фазы, ω-3 ЖК сдерживают развитие последующего иммунопаралича. Они также ограничивают неконтролируемый выброс лейкоцитарных факторов повреждения, вследствие чего их цитотоксическая активность перенаправляется на истинную мишень иммунологической защиты - микроорганизм.
ЛИТЕРАТУРА
1. Murray MJ, Kumar M, Gregory TJ, Banks PL, Tazelaar HD, DeMichele SI. Select dietary fatty acids attenuate cardiopulmonary dysfunction during acute lung injury in pigs. Am J Physiol 1995; 269 (6 Pt 2): H2090-2099
2. Calder PC. Immunoregulatory and anti-inflamrnatory effects of n-3 polyunsaturated fatty acids. Braz J Med Biol Res 1998;31:467-490
3. Heller A, Koch T, Schmeck J, van Ackern K. Lipid mediators in inflammatory disorders. Drugs 1998; 55:487-496
4. Mayer K, Seeger W, Grimrninger F. Clinical use of lipids to control inflammatory disease. Curr Opin Clin Nutr Metab Care 1998; 1: 179-184
5. Kragballe K, Voorhees JJ, Goetzl EJ.Inhibition by leukotriene B5 of leukotriene B4-induced activation of human keratinocytes and neutrophils. J Invest Dermatol 1987; 88: 555-558
6. Endres S, Ghorbani R, Kelley VE, Georgilis K, Lonnemann Ci, van der Meer JWM et al. The effect of dietary supplementation with n-3 polyunsaturated fatty acids on the synthesis of interleukin-l and tumor necrosis factor by mononuclear cells. N Engl J Med 1989; 320: 265-271
7. Caughey GE, Mantzioris E, Gibson RA, Cleland LG; James MJ. The effect on human tumor necrosis factor alpha and interleukin 1 beta production of diets enriched in n-3 fatty acids from vegetable oil or fish oil. Am J Clin Nutr 1996; 63: 116-122
8. Sperling Rl, Benincaso Al, Knoell CT, Larkin JK, Austen KF, Robinson DR. Dietary omega-3 polyunsaturated fatty acids inhibit phosphoinositide formation and chemotaxis in neutrophils. J Clin Invest 1993; 91: 651-660
9. May CL, Southworth AJ, Calder PC. Inhibition of lymphocyte protein kinase С by unsaturated fatty acids. Biochem Biophys Res Commun 1993; 195: 823-828
10. Terano T, Shiina T, Tamura Y. Eicosapentaenoic acid suppressed the proliferation of vascular smooth muscle cells thrOUgh modulation of various steps of growth signals. Lipids 1996; 31: S301-S304
11. Peterson J, Bihain BE, Bengtsson-Olivecrona Ci, Deckelbaum Rl, Carpentier YA, Olivecrona T. Fatty acid control of lipoprotein lipase: A link between energy metabolism and lipid transport. Proc Natl Acad Sci USA 1990; 87: 909-913
12. Rustan AC, Hustvedt BE, Drevon CA. Postprandial decrease in plasma unesterified fatty acids during n-3 fatty acid feeding is not caused by accumulation of fatty acids in adipose tissue. Biochem Biophys Acta 1998; 1390, 245-257
13. Lovegrove JA, Brooks CN, Murphy MC, Gould BJ, Williams CM. Use of manufactured foods enriched with fish oil as a means of increasing long-chain n-3 polyunsaturated fatty acid intake. Br J Nutr 1997; 78: 223-236
14. Friedman Ci, Silva E, Vmcent JL. Has the mortality of septic shock changed with time? CritCare Med 1998; 26: 2078-2086
15. Wheeler AP, Bernard GR. Treating patients with severe sepsis. N Eng! J Med 1999; 340: 207-214
16. Bone RC, Grodzin CI, Balk RA. Sepsis: a new hypothesis tor pathogenesis of the disease process. Chest 1997; 112: 235-243
17. Bone RC. Sepsis SIRS and CARS. Crit Care Med 1996; 24: 1125-1128
18. Dinarello CA. Proinflammatory and anti-inflarnmatory cytokines as mediators in the pathogenesis of septic shock. Chest 1997; 112: 321S-329S
19. Chabot F, Mitchell JA, Guueridge JM, Evans TW. Reactive oxygen species in acute lung injury. Eur Resp J 1998; 11: 745-757
20. Annane D. Replacement therapy with hydrocortisone in catecholamine-dependenset ptic shock. J Endotoxin Res 2001;7:305-309
21. Anel RL, Kumar A. Experimental and emerging therapies fur sepsis and septic shock. Expert Opin Investig Drugs 2001; 10: 1471-1485
22. Bernard GR, Wheeler AP, Russell JA, Schein R, Summer WR, Steinberg KP et al. The effects of ibuprofen on the physiology and survival of patients with sepsis. The Ibuprofen in Sepsis Study Group. N Engl J Med 1997; 336: 912-918
23. Vilaseca J, Salas A, Guamer F, Rodriguez R, Malagelada JR. Participation of thromboxane and other eicosanoid synthesis in the courseo f experimentailn flarumatoryc olitis. Gastroenterology! 990; 98: 269-277
24. Belluzzi A, Brignola C, Campieri M, Pera A, Boschi S, Miglioli M et al. Effect of an enteric-coated fish oil preparation on relapses in Crohn's disease. N Engl J Med 1996; 334: 1557-1560
25. Vand er Heide JJH,B ilo HJG.D onkerj M, Wilmink JM, TegzesAs M. Effect of dietary fish oil on renal function and rejection in cyclosporine-treatedre cipients of renal transplants.N Engl J Med 1993; 329: 769-773
26. Suter PM, Ricou B. Cytokines and lung injury. Update in Intensive Care and Emergency Medicine 1998; 30: 41-53
27. Quinlan GJ, Lamb N, TiHey R, Evans TM, Gutteridge JMC. Plasma hypoxantine levels in ARDS: implications fur morbidity and mortality. Am J Respir Crit Care Med 1997; 155:479-484
28. Connelly KG, RepineJ E. Markers fur predictingt he developmenot f acuter espiratoryd istresss yndromeA. nnu RevM ed 1997; 48: 429-445
29. Grimrninger F, Wahn H, Mayer K, Kiss L, Walmrath D, Bahkdi S, SeegerW . Arachidonic acid increases,h ut eicosapentaenoica cid decreasese xotoxin induced lung vascular leakage- relation to 4-series versus 5-series leukotriene generation. Am J Respir Crit Care Med 1997; 155: 513-519
30. Grimrninger F, Mayer K, Kramer H-J, Stevens J , Walmrath D , Seeger W. Differential vasoconstrictor potencies of free fatty acids in the lung vasculature: 2- versus 3-series prostanoid generation. J Pharmacol Exp Ther 1993; 267: 259-265
31. Grimrninger F, Wahn H, Kramer HJ, Stevens J, Mayer K, Walmrath D, Seeger W. Differential influence of arachidonic vs. eicosapentaenoiacc id on experimentapl ulmonaryh ypertension. A m J Physiol1995; 268 (6 Pt 2): H2252-H2259
32. Grimrninge'r F, Mayer K, Kiss L Wahn H, Walmrath D, Bakhdi S et al. Synthesis of 4- and 5-series leukotrienes in the lung rnicrovasculature challenged with Escherichia coli hemolysin: Critical dependenceo n exogenousfr ее fatty acids upply.A m J Respir Biol Cell Mol 1997; 16: 317-324
33. Grimrninger F, Mayer K, Kiss L, Walmrath D, Seeger W. PAFinduced synthesis of tetraenoic and pentaenoid eukotrienesin a model of pulmonaryr nicrovascularle ukostasis.A m J Physiol Lung Cell Mol Physiol 2000; 278: L268-L275
34. Mancuso P, Whelan J, DeMichele SI, Snider CC, Guszcza JA, Oaycombe К J et al. Effects of eicosapentaenoiacn d y-linolenic acid on lung permeability and alveolar macrophagee Icosanoids ynthesis in endotoxic rats. Crit Care Med 1997; 25: 523-532
35. Mancuso P, Whelan J, DeMichele SI, Snider CC, Guszcza JA, Karlstad MD. Dietary fish oil and fish oil and borage oil suppress intrapulmonary pro-inflarumatory eicosanoid biosynthesis and attenuatep ulmonaryn eutrophil accumulationin endotoxicr ats. Crit Care Med 1997; 25: 1198-206
36. Murray MJ, Svingen BA, Holman RT, Yaksh TL. Effects of a fish oil diet on pig's cardiopulmonary response to bacteremia. J PaTenter Enteral Nutr 1991; 15: 152-158
37. Murray MJ, Svingen BA, Yaksh TL, Holman RT. Effects of endotoxin on pigs prefed omega-3 vs. omega-6 fatty acids-enriched diets. Am J Physiol1993; 265 (6 Pt 1):E920-E927
38. Sane S, Baba M, Kusano C, Shirao K, Andoh T, Kamada T et al. Eicosapentaenoica cid reduces pulmonary edema in endotoxernic rats. J Surg Res 2000; 93: 21-27
39. Gadek JE, DeMichele SI, Karlstad MD, Pacht ER, Donahoe M, Albertson ТЕ et al.and the Enteral Nutrition in ARDS Study Group. Effect of enteral feeding with eicosapentaenoic acid, garumalinolenic acid, and antioxidants in patients with acute respiratory distress syndrome. Crit Care Med 1999; 27: 1409-1420
40. Docke WD, RandowF, Syrbe U, Krausch D.Asadullah K, Reinke P. Monocyte deactivation in septic patients: restoration by IFN-gamrna treatment. Nat Med 1997; 3: 678-681
41. Kox WJ, Bone RC, Krausch D, Docke WD, Kox SN, Wauer H et al. Interferon garnma-lb in the treatment of compensatory antiinflammatory response syndrome. A new approach: proof of principle. Arch Intern Med 1997; 157: 389-393
42. Solomkin, JS, Cotta LA, Brodt JK, Hurst JW, Ogle CK. Neutrophil dysfunction in sepsis, m Degranulation as a mechanism tor nonspecific deactivation. J Surg Res 1984; 36: 407-412
43. Solomkin JS, Jenkins MK, Nelson RD, Chenoweth D , SirnmonsR L. Neutrophil dysfunction in sepsis. II. Evidence for the role of complement activation products in cellular deactivation. Surgery 1981; 90: 319-327
44. Galban C, Montejo JC, Mesejo A, Marco P, Celaya S, Sanchez-Segural M et al. An immune-enhancinegn terald iet reducesm ortality rate and episodeso f bacteremiain septici ntensivec are unit patients. Crit Care Med 2000; 28: 643-648
Комментарии
ПРАКТИКА ПЕДИАТРА
