Что мы знаем об эффективности ризедроната при остеопорозе
Статьи Опубликовано в:«Эффективная фармакотерапия в эндокринологии» »» сентябрь 2010
Н.В. Торопцова
Научно-исследовательский институт ревматологии РАМН, Москва
Остеопороз (ОП) – одно из наиболее распространенных заболеваний среди пожилых людей, для которого характерны снижение минеральной плотности и ухудшение качества кости, следствием чего является повышенная ее хрупкость. Последствия ОП в виде переломов позвонков и трубчатых костей обусловливают значительный подъем заболеваемости, инвалидности и смертности. Риск любого перелома в течение жизни составляет около 40% и эквивалентен риску возникновения сердечно-сосудистых заболеваний (1). Для женщин риск перелома бедра, наиболее грозного осложнения ОП, составляет 1: 6, в то время как риск, например, рака молочной железы – 1: 9 (2).
В соответствии с международной классификацией болезней ОП относится к 13 классу - «Болезни костно-мышечной системы и соединительной ткани». В связи с использованием передовых, в первую очередь, радиологических методов исследования, разработкой и внедрением новых методов профилактики и лечения, а также активной и целеустремленной просветительской деятельностью Международного фонда остеопороза (IOF) и его 186 национальных обществ в 90 странах мира, в том числе и Российской Ассоциации по Остеопорозу (РАОП), социальная и медицинская значимость заболевания значительно возросли. Официальная регистрация заболеваемости ОП началась в РФ с 1999 г., а за прошедшие 10 лет (1999-2008 гг.) общее число зафиксированных случаев ОП среди взрослых жителей России увеличилось почти в 4 раза (с 31 500 чел. в 1999 г. до 115 530 чел. в 2008 г.). Существенное влияние на частоту выявляемости болезни оказало улучшение технической базы для диагностики, а именно, поставка в медицинские учреждения костных денситометров, что позволило измерять минеральную плотность костной ткани (МПК) и ставить диагноз ОП.
ОП развивается постепенно и клинически нередко выявляется уже после переломов, что послужило основанием называть его «скрытой эпидемией». Следует отметить, что частота ОП повышается с возрастом, поэтому наблюдаемое в последние десятилетия увеличение продолжительности жизни в развитых странах и связанный с ним быстрый рост числа пожилых людей, особенно женщин, ведет к нарастанию частоты этого заболевания, делая его одной из важнейших проблем здравоохранения во всем мире.
В 2005 г. эксперты РАОП, специалисты различных областей медицины, разработали клинические рекомендации по диагностике, профилактике и лечению ОП, включая глюкокортикоидный ОП, а в 2009 г. они были переработаны и дополнены (3). Рекомендации ранжированы по единой международной системе уровней доказательности. Несмотря на общие рекомендации, лечение ОП у конкретного больного нередко трудная задача и зависит как от интерпретации врачом состояния больного, так и от готовности пациента к длительной терапии. Оказание медицинской помощи больным ОП проводится на амбулаторном этапе, лечение и наблюдение длительное, в течение нескольких лет, при выявлении вторичных причин возможного развития ОП пациента следует направлять на консультацию к специалисту (ревматологу, эндокринологу и др.).
Лечение ОП включает в себя как нефармакологические способы вмешательства, так и лекарственную терапию.
Медикаментозное лечение ОП представляет непростую задачу, особенно когда в анамнезе уже имеются переломы различной локализации, должно быть длительным, в связи с чем идет постоянный поиск высокоэффективных и недорогих препаратов. В настоящее время спектр лекарственных средств для лечения и профилактики ОП значительно расширился, их применение снижает риск отдельных переломов на 20-70%. Препаратами первого выбора патогенетической терапии являются азотсодержащие бисфосфонаты (БФ), в основе их механизма действия лежит подавление процессов резорбции остеокластами и восстановление процессов метаболизма костной ткани до предменопаузального уровня, что предотвращает микроархитектурные нарушения и потерю костной ткани. Сегодня в нашей стране уже достаточно хорошо известны врачам три препарата этого класса - алендронат, ибандронат и золедроновая кислота. Однако во всем мире, наряду с этими препаратами, широко применяется еще один препарат этого класса, который наряду с алендронатом является «золотым стандартом» лечения ОП - это ризедронат.
Эффективность применения ризедроната у больных ОП была доказана в ходе проведения нескольких рандомизированных клинических двойных слепых плацебо-контролируемых исследований (РКИ). Так, в двух 3-х летних РКИ у 3684 женщин в постменопаузе с установленным остеопорозом и переломами позвонков в анамнезе ризедронат назначался ежедневно в дозах 2,5 мг или 5,0 мг одновременно с 1000 мг кальция и 500 ME витамина D. Уже через год лечения частота новых переломов позвонков снизилась при приеме 5,0 мг на 61-65%, а через 3 года это снижение также оставалось на достаточно высоком уровне - 41-49% по сравнению с контролем (p<0,001). Частота периферических переломов в течение 3-х лет терапии также уменьшилась на 33-39% (4, 5). Прием ризедроната уже в течение первых 6 месяцев привел к достоверному повышению МПК в поясничном отделе позвоночника, а через 3 года лечения прирост минеральной плотности составил +5,9% в позвоночнике, +6,4% - в области большого вертела бедренной кости, +3,1 - в шейке бедра, +2,1% - в дистальном отделе предплечья по сравнению с приростом МПК в контрольной группе (p<0,001).
На биопсийном материале при гистологическом исследовании не было выявлено нарушения процессов минерализации кости, а также повреждения костного мозга при приеме 5,0 мг ризедроната. Основываясь на гистоморфометрическом анализе, было показано, что прием данного препарата снижал костный обмен почти на 50% по сравнению с таковым при приеме плацебо. Прием ризедроната приводил к положительному балансу на уровне единицы ремоделирования, в результате чего отмечалось увеличение толщины кортикального слоя (+20%), в то время как в группе плацебо была отрицательная динамика (-11%) через 3 года лечения (5).
Переносимость препарата была удовлетворительная, при этом следует отметить, что частота нежелательных явлений (НЯ), связанных с поражением верхних отделов желудочно-кишечного тракта (ЖКТ), была схожей во всех трех группах наблюдения. Большинство НЯ были легкой или средней степени тяжести, притом, что у 35% включенных в исследование больных в анамнезе были зафиксированы заболевания ЖКТ (5). Не было отмечено увеличения количества данных НЯ у больных, получавших в качестве сопутствующего лечения нестероидные противовоспалительные препараты и аспиринсодержащие препараты. При гастродуоденальной эндоскопии у больных, получавших в течение 3-х лет ежедневно ризедронат, изменения в пищеводе, желудке и 12-перстной кишке были схожими с таковыми при приеме плацебо (6).
В опубликованном в 2008 г. систематическом обзоре (7) проведена оценка эффективности ризедроната на снижение риска переломов на основе пяти мета-анализов, объединивших в целом десять РКИ, и четырнадцати РКИ, не вошедших ни в один из этих мета-анализов. Объединенный анализ данных мета-анализов показал снижение риска переломов позвонков у женщин в постменопаузе через год лечения 2,5 мг/сут. и 5 мг/сут. ризедроната по сравнению с плацебо на 47% (95% ДИ 23%; 63%) и 62% (95% ДИ 44%; 75%) соответственно. В шести исследованиях, не включенных в мета-анализы, переломы были первичной точкой оценки. Значительное снижение риска переломов позвонков и периферических переломов при лечении ризедронатом по сравнению с плацебо показано в четырех из этих исследований, проведенных на популяции с высоким риском переломов (8-11). В одном РКИ, проведенном на молодых военнослужащих, не выявлено снижение риска стресс-переломов при профилактическом приеме ризедроната по сравнению с плацебо (12).
Кроме того, опубликовано 3 РКИ по сравнению различных доз ризедроната. Риск переломов не различался между группами. Однако переломы в этих исследованиях оценивались как нежелательные явления (вторичная точка оценки), а размер выборок не позволил определить различий между группами. В исследованиях, оценивавших переломы как первичную точку, но не сравнивавших различные дозы ризедроната в рамках одного исследования, показано снижение риска всех переломов, периферических переломов и переломов бедра при приеме 2,5 мг/сут. и снижение риска переломов позвонков на дозах 5,0 мг/сут. и 35 мг/нед. по сравнению с плацебо (7).
Эффективность ризедроната по снижению риска переломов у женщин в постменопаузе с остеопенией (МПК по Т-критерию от -1 до -2,5SD) и без предшествующих деформаций позвонков была показана при проведении ретроспективного анализа 4-х РКИ. Было обнаружено, что прием 5,0 мг ризедроната в течение 3-х лет уменьшал риск любых переломов (позвонков и периферических) на 73% (ОР = 0,27, 95% ДИ 0,090,83, p = 0,023), а при раздельном анализе это снижение составляло для переломов позвонков - 56% (р = 0,249), для периферических переломов - 99% (ОР = 0,09, 95% ДИ 0,01-0,71, p = 0,022) (13).
Изучение последействия ризедроната в течение года после прекращения приема препарата хотя и продемонстрировало снижение МПК в позвоночнике и шейке бедренной кости у пациенток, однако минеральная плотность в этих регионах оставалась достоверно выше этих показателей при включении в исследование и выше, чем в контрольной группе (p Рисунок 1. Влияние ризедроната на риск переломов позвонков: результаты 7-летнего исследования
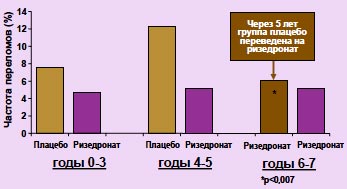
На сегодняшний день имеются данные длительного приема ризедроната (5 и 7 лет) в ходе продления 3-х летнего РКИ. Так, 265 женщин принимали ризедронат (n=135) или плацебо (n=130) в течение 5 лет, при этом конечными точками исследования были не только динамика МПК и маркеров костного обмена, но и переломы (15). Риск переломов позвонков в группе получавшей исследуемый препарат был значимо снижен на 59% (95% ДИ 19-79%, p = 0, 01), в то же время снижение риска периферических переломов составило 41%, однако из-за небольшого количества произошедших переломов этот показатель не достиг уровня статистической достоверности. Через 5 лет на фоне лечения был отмечен дальнейший прирост МПК в позвоночнике, который составил 9,3%, в области шейки бедра - +2,2%, а большого вертела - +5,7%, в то время как в группе плацебо отмечалась потеря костной массы. Ризедронат привел к снижению уровня маркеров костной резорбции уже через 3 месяца лечения, и это снижение было стабильным в течение всего 5-летнего периода лечения. Кроме того, через 6 месяцев терапии было зафиксировано и снижение маркеров костеобразования в группе лечения и составило 18,4% к 5 году наблюдения. Во второй фазе продления (6-7 год) принимали участие всего 164 женщины, а закончили его 136 человек, при этом все пациенты получали ризедронат, включая группу плацебо. В течение этого периода отмечался дальнейший подъем МПК (например, в позвоночнике он составил 11,5%), маркеры костного обмена оставались на предменопаузальном уровне, а частота переломов позвонков не отличалась от таковой в первой фазе продления (6%), что демонстрирует отсутствие снижения эффективности в отношении риска переломов по сравнению с 4-5 годом наблюдения. В тоже время отмечалось достоверное снижение риска переломов позвонков и во второй группе, которая стала принимать ризедронат только через 5 лет наблюдения (p=0,007) (рисунок 1) (16).
Несколько плацебо-контролируемых РКИ посвящено эффективности ризедроната при глюкокортикоидном остеопорозе. В наиболее крупном из них (509 больных) продемонстрировано снижение риска переломов позвонков через 12 мес. на 58% и 70% при приеме 2,5 мг/сут. и 5 мг/сут. соответственно по сравнению с плацебо (17).
В 2008 г. опубликован систематический обзор Кокрановской электронной библиотеки, оценивший эффективность ризедроната 5 мг/сут. по сравнению с плацебо у женщин в постменопаузе. В мета-анализ включено 7 РКИ (14049 женщин). При первичной профилактике не было выявлено влияния ризедроната на риск переломов позвонков и периферических переломов. При вторичной профилактике показано снижение относительного риска переломов позвонков на 39% (ОР = 0,61, 95% ДИ 0,50; 0,76) со снижением абсолютного риска на 5%. Отмечено значимое снижение относительного риска периферических переломов на 20% (ОР = 0,80, 95% ДИ 0,72; 0,90) со снижением абсолютного риска на 2%, а риска перелома бедра - на 26% (ОР = 0,74, 95% ДИ 0,59; 0,94) со снижением абсолютного риска на 1%. При объединении исследований по первичной и вторичной профилактике снижение риска переломов оставалось значимым как для переломов позвонков (ОР = 0,63, 95% ДИ 0,51; 0,77), так и для периферических переломов (ОР = 0,80, 95% ДИ 0,72; 0,90). Ни в одном из проанализированных исследований не было определено значимых различий по нежелательным явлениям между группами. Однако по данным наблюдения возможен риск повреждений верхних отделов ЖКТ и в крайне малом числе случаев -остеонекроза челюсти (18).
И еще одна работа по изучению эффективности ризедроната в отношении периферических переломов, и в частности, переломов бедра, была проведена в ходе наблюдательного исследования в течение первого года лечения в реальной клинической практике. Одновременно изучалась по тем же параметрам и эффективность хорошо известного в нашей стране препарата алендроната (19). Для этого были сформированы 2 когорты женщин 65 лет и старше, одна из них составила 12215 человек, принимавших 35 мг ризедроната 1 раз в неделю, вторая (21615 пациенток) - 70 мг алендроната по той же схеме. Частота периферических переломов была на 18% ниже среди лиц, получавших ризедронат (2,0%), по сравнению с принимавшими алендронат (2,3%), а переломов бедра - ниже на 43% (0,4% и 0,6% соответственно). Авторы не исключают влияние возможных систематических ошибок, которые встречаются при проведении такого рода работ, например, в данном случае изначально когорты различались по ряду входящих характеристик, которые могли в последующем привести к различиям в частоте переломов. Поэтому была проведена дополнительная статистическая обработка полученного материала, исключены из анализа пациентки с факторами риска, которые могли повлиять на частоту переломов. В конечном итоге результаты исследования не претерпели значимых изменений, а выводы этой работы остались прежними.
Таким образом, полученные результаты свидетельствуют об эффективности ризедроната в лечении остеопороза, снижении риска переломов и вполне удовлетворительной переносимости.
Ризедронат необходимо принимать натощак сразу после подъема с постели, таблетку нужно запивать 1 стаканом чистой воды, а после приема следует находиться в вертикальном положении (сидя или стоя), в течение как минимум 30 минут. БФ могут вызывать побочные эффекты, связанные с поражением ЖКТ, а так же головную боль, боли в мышцах и костях, снижение уровня кальция и фосфора в сыворотке крови, в редких случаях - сыпь и эритему. Соблюдение рекомендаций по приему препарата значительно снижает риск возникновения желудочно-кишечных НЯ. Противопоказания к их назначению: гиперчувствительность к препарату, тяжелая почечная недостаточность (клиренс креатинина ниже 30мл/мин.), гипокальциемия, беременность и грудное вскармливание, детский возраст. Следует помнить, что прием препаратов, влияющих на патогенез ОП, в частности БФ, должен проходить на фоне достаточного поступления кальция и витамина D с пищей или в виде лекарственных средств.
Оригинальный ризедронат зарегистрирован в России еще в 2001 г., однако в аптечной сети его нет. В 2010 г. зарегистрирован генерический ризедронат производства фирмы «Зентива» (Чешская Республика), 35 мг 1 раз/нед. Проведенные исследования по сопоставимости действия этих двух препаратов in vitro и in vivo показали их биоэквивалентность в отношении фармакокинетики и биодоступности. Таким образом, сегодня в нашей стране расширена линейка препаратов, с успехом применяющихся во всем мире для лечения ОП.
- Ризедронат необходимо принимать натощак сразу после подъема с постели, таблетку нужно запивать 1 стаканом чистой воды, а после приема следует находиться в вертикальном положении (сидя или стоя), в течение как минимум 30 минут. Результаты разных исследований свидетельствуют об эффективности ризедроната в лечении остеопороза, снижении риска переломов и вполне удовлетворительной переносимости
- Оригинальный ризедронат зарегистрирован в России еще в 2001 г., однако в аптечной сети его нет. В 2010 г. зарегистрирован генерический ризедронат производства фирмы «Зентива» (Чешская Республика), 35 мг 1 раз/нед. Проведенные исследования по сопоставимости действия этих двух препаратов in vitro и in vivo показали их биоэквивалентность в отношении фармакокинетики и биодоступности. Таким образом, сегодня в нашей стране расширена линейка препаратов, с успехом применяющихся во всем мире для лечения ОП.
Список использованной литературы
