Сосудистый паркинсонизм
СтатьиД.м.н. Н.С. Подобедова
Введение
Причины паркинсонизма полиморфны. В настоящее время наиболее изучен патогенез болезни Паркинсона — БП (идиопатического паркинсонизма). Цереброваскулярная болезнь (ЦВБ), лекарственные препараты, травмы и инфекционные заболевания мозга считаются наиболее важными этиологическими факторами вторичного паркинсонизма.
Наше представление о сосудистом паркинсонизме как о заболевании, возникающем в результате ЦВБ, прошло несколько этапов — от признания проблемы к отрицанию и затем вновь к восстановлению проблемы.
Примерно с 1929 г многие исследователи пытались выявить отличительные признаки сосудистого паркинсонизма [2—18]. В 1929 г Critchley привел описание синдрома «атеросклеротического паркинсонизма» у больных старшей возрастной группы, имеющих гипертоническую болезнь. Основными симптомами синдрома были ригидность, маскообразное лицо и ходьба мелкими шагами [1].
Им было выдвинуто предположение о том, что пациенты старшей возрастной группы с атеросклерозом и паркинсонизмом чаще других имеют наибольшее число признаков БП, за исключением «тремора покоя», который обычно отсутствует у этих больных. По данным Critchley, заболевание быстро прогрессирует и в клинической картине синдрома преобладает поражение ног, а не рук. Им впервые было высказано предположение о том, что атеросклеротический паркинсонизм, его ведущие неврологические симптомы возникают в результате множественных поражений базальных ганглиев атеросклеротического генеза.
Schwab и England [2], Parkes и его соавторы [3] отвергли данную теорию, утверждая, что сосудистые изменения являются случайной находкой у больных БП. В результате Critchley пересмотрел свою концепцию о цереброваскулярном заболевании как причине БП и согласился с тем, что описанный им синдром, отличается от БП как по клиническим симптомам, так и по патологоанатомическим данным [4]. Концепция сосудистого паркинсонизма до настоящего времени противоречива и не утратила своей актуальности. Когда мы исследуем больных старшей возрастной группы, всегда возникает вопрос, у данного больного сосудистый паркинсонизм или БП. Ответ на него имеет значение, так как позволяет предположить скорость течения и прогрессирования заболевания и помогает в подборе адекватной медикаментозной терапии, а также определить стратегию вторично обусловленных предупредительных мер и прогноз.
Таким образом, паркинсонизм может быть следствием целого ряда патологических процессов в головном мозге. Если этиология идиопатического паркинсонизма, БП непосредственно связана с дегенеративными изменениями черной субстанции и, как следствие этого, возникающим нарушением баланса нейротрансмиттерных систем мозга, то в вопросах, касающихся диагностики и лечения сосудистого паркинсонизма, до настоящего времени нет четких критериев.
Современные исследования результатов аутопсий пациентов с БП показали, что для заболевания типична дегенерация нейронов латеральной области компактной части черной субстанции и наличие телец Леви [1]. Причина такой избирательности до настоящего времени остается не до конца ясной [2].
Лондонский банк данных результатов исследований мозга в 1999 г опубликовал результаты аутопсий 100 больных, которым при жизни был выставлен диагноз БП. Эти исследования показали совпадение клинического и патоморфологического диагнозов в 76 случаях. В 24 наблюдениях были обнаружены другие патологические изменения, включавшие 3 случая сосудистого поражения мозга [3—1]. Полученные результаты свидетельствуют о трудности проведения клинического дифференциального диагноза между БП и вторичным паркинсонизмом и подтверждают необходимость подробного анализа клинических симптомов, позволяющих более точно разграничить БП и вторичный паркинсонизм.
Эпидемиология
Как свидетельствуют данные UK Parkinson's Disease Society Brain Bank, из каждых 24 случаев БП 3 случая приходится на неправильную диагностику врачами-неврологами БП. В этих 3 случаях по аутопсии диагностировали лакунарное состояние и не обнаруживали специфических изменений в ткани головного мозга, характерные для БП [7]. В Испании было обследовано 5160 больных старшей возрастной группы, имеющих паркинсонизм. В этом исследовании паркинсонизм был идентифицирован как сосудистый у 4,4% от общего числа больных [8]. В аналогичном исследовании популяции в Италии из 68 случаев паркинсонизма у 8 (12%) больных был диагностирован сосудистый паркинсонизм [9]. Соотношение числа случаев паркинсонизма и БП становилось выше в популяционной группе старшего возраста и чаще мужчин. Данные визуальной диагностики и патоморфологические результаты этих исследований подтвердили диагноз сосудистого паркинсонизма и позволили более точно определить его процентное отношение ко всем случаям паркинсонизма. Он равен 3—6% [10].
Таким образом, можно сделать вывод о том, что сосудистый паркинсонизм достаточно редко диагностируется при жизни больного (в приведенных примерах, 5 больным паркинсонизмом при жизни этот диагноз не был поставлен) и чаще является патологоанатомическим диагнозом [11].
Клинико-радиологическое исследование больных, имевших нарушение походки и паркинсонизм, выявило у этих пациентов небольшие глубокие очаги инсультов и поражение белого вещества головного мозга. Было показано, что примерно 1/3 больных, перенесших инсульт, имеют один или больше клинических признаков паркинсонизма спустя 1 год после инсульта [12]. Остается неизвестным ответ на вопрос, имели ли эти больные сосудистый паркинсонизм, или у них появились первые симптомы начинающейся БП.
Следовательно, можно сделать принципиально важный вывод. Выявление у больного паркинсонизмом клинических и (или) нейровизуализационных признаков цереброваскулярной патологии необходимое, но не достаточное условие диагностики сосудистого паркинсонизма. Необходимо установление причинно-следственных связей между сосудистым повреждением мозга и паркинсонизмом. Доказательство сосудистого происхождения паркинсонизма возможно при учете 3 факторов: феноменологических особенностей двигательного дефекта, особенностей течения и данных нейровизуализации.
Факторы риска
Так как в основе сосудистого паркинсонизма лежит сосудистое поражение мозга, логично предположить, что сосудистый паркинсонизм имеет те же факторы риска, что и цереброваскулярное заболевание. Необходимо отметить, что не выявлено четких взаимосвязей между некоторыми сосудистыми поражениями мозга, сосудистым паркинсонизмом и артериосклерозом [13].
Существует мнение, что частота и распространенность сосудистого паркинсонизма увеличиваются с возрастом [9, 10, 14]. Известно, что больные сосудистым паркинсонизмом старше пациентов с БП. В этой возрастной группе сосудистый паркинсонизм чаще возникает у мужчин.
Несколько исследований было предпринято с целью проанализировать частоту развития сосудистого паркинсонизма после инсультов. Было подтверждено, что артериальная гипертония является важным фактором риска для сосудистого паркинсонизма [8], что впервые было высказано Critchley при описании им «артериосклеротического паркинсонизма» [1].
Сахарный диабет так же является коморбидным заболеванием с сосудистым паркинсонизмом. В настоящее время остается не до конца изученной связь последнего с гиперхолестеринемией, курением и семейными случаями ИБС.
Сосудистый паркинсонизм имеет связь с антифосфолипидными антителами и антикардиолипиновыми антителами [15]. Данные литературы противоречивы в отношении связи БП и ЦВБ. Результаты ряда исследований свидетельствуют о низкой или равной распространенности БП и ЦВБ [16]. Некоторые авторы считают, что БП является своеобразным протектором против инсульта, так как происходит снижение уровня дофамина в мозге [17]. Существует предположение, что лечение больных БП с применением дофаминергических препаратов способно повышать риск возникновения эндотелиальной дисфункции и атеросклероза в результате увеличения уровня гомоцистеина [18]. Вместе с тем ряд исследований показал увеличение риска летальности от инсульта у больных БП [19].
Патоанатомия сосудистого паркинсонизма
Практически любое поражение черной субстанции и ее путей теоретически является причиной паркинсонизма. Существует 3 различных патологических состояния, приводящие к типичной клинической манифестации: 1) множественные лакунарные инфаркты, при которых паркинсонизм обычно сочетается с пирамидным дефицитом, псевдобульбарным параличом, когнитивными расстройствами и нарушением походки; 2) субкортикальная атеросклеротическая энцефалопатия (болезнь Binswanger'а), подтвержденная данными КТ/МРТ (наличие перивентрикулярных или субкортикальных поражений белого вещества), клинически проявляющаяся картиной деменции и прогрессирующим нарушением походки; 3) реже можно наблюдать инфаркты (чаще лакунарного типа) в базальных ганглиях, дающие клиническую картину, не отличимую от БП.
В серии аутопсий 700 случаев с клиническим диагнозом паркинсонизма БП была установлена по наличию телец Леви в 80,7% случаев, из них в сочетании с ЦВБ в 19% [20]; в 135 случаях «вторичного паркинсонизма» — в 27 (3,9%). Из этих 135 случаев субкортикальные сосудистые повреждения белого вещества головного мозга составили 32%, лакунарные состояния базальных ганглиев и ствола мозга — 20%; мультинфокальная энцефалопатия — 48%. При мультифокальной энцефалопатии были выявлены выраженные поражения черной субстанции.
МРТ головного мозга больных подтверждает наличие очагов сосудистого генеза в подкорковом белом веществе.
Механизм, посредством которого ишемические очаги в мозге дают начало симптомам паркинсонизма, не выяснены. Сосудистые очаги, локализованные в базальных ганглиях, сами по себе могут считаться этиологическим фактором [4—9, 14—15, 19]. Другим исследователям [17, 19, 20], не удалось выявить столь четкой корреляции между сосудистыми очагами в базальных ганглиях и последующим развитием паркинсонизма.
Между тем доказана роль дофаминергических структур (черной субстанции, ножек мозга, гипоталамуса, таламуса, а также базальных ганглиев пирамидных и экстрапирамидных путей) в развитии насильственного плача и смеха у больных с сосудистыми заболеваниями головного мозга. Наблюдалось существенное снижение клинических проявлений на фоне приема препаратов L-Дофа. Ряд исследований, посвященных изучению ДЭП, показали, что у больных ДЭП II при преимущественном поражении глубоких отделов полушарий и мозгового ствола (лентикулярное ядро, внутренняя капсула, зрительный бугор) наряду с двигательными и чувствительными расстройствами развивается мягкий акинетико-ригидный синдром (33,3%), проявление которого значительно менее выражено, чем у больных паркинсонизмом, что объясняется отсутствием у больных с хронической цереброваскулярной недостаточностью выраженных изменений черной субстанции [28].
Baloh и соавторы [21—22] считают, что такой симптом, как нарушение равновесия, в старшей возрастной группе больных, имеющих очаги поражения в белом веществе головного мозга по данным МРТ, обусловлены ухудшением функции long-loop-рефлексов, проходящих в белом веществе, что, в свою очередь, приводит к нарушению сенсомоторной интеграции.
Таким образом, можно сделать вывод о том, что развитие сосудистого паркинсонизма может идти двумя путями, а именно: 1) возникнуть в результате острого сосудистого поражения одной из структур базальных ганглиев или 2) быть результатом постепенного, более обширного ишемического поражения белого вещества подкорковых структур. Второй тип развития приводит к злокачественному течению паркинсонизма. Более того, ЦВБ может приводить к разным типам паркинсонизма. Эти типы клинически не отличимы от идеопатического паркинсонизма [25], прогрессирующего супрануклеарного паралича, клинически идентичны БП [25, 26], паркинсонизму нижней половины тела [11], а также другим формам нарушения походки паркинсонического типа [27]. Однако проблема заключается в том, что как БП, так и сосудистый паркинсонизм возникают у пациентов старшей возрастной группы. По данным литературы, только в 2—3% случаев результаты аутопсий подтверждают ЦВБ как этиологический фактор паркинсонизма. При отсутствии результатов патоморфологических исследований, мы не можем подтвердить сосудистую причину синдрома и должны предположить возможность сочетанного заболевания, т.е. идеопатический и сосудистый паркинсонизм.
Формирование микроангиопатий артерий головного мозга является не менее важным патогенетическим механизмом развития сосудистого паркинсонизма. Микропатология сосудов головного мозга не бывает изолированной и захватывает все сосуды головного мозга, приводя к двум основным синдромам: болезни Binswange и лакунарному состоянию. При микрозаболеваниях сосудов головного мозга в первую очередь происходят изменения в стенке сосудов, расширяется пространство Virchow-Robin, возникает разряженность периваскулярного паренхиматозного пространства и глиоз ткани. Лакунарные состояния являются следствием окклюзии малых сосудов, что приводит к образованию микрополостей в паренхиме мозга. Они вторичны по отношению к окклюзиям малых пенитрирующих артерий мозга. Лакунарное состояние — это множество микрополостей (лакун) в головном мозге, но их типичной локализацией являются внутренняя капсула, серое вещество базальных ганглиев и белое вещество головного мозга.
При церебральной амилоидной микроангиопатии, или ассоциированной ангиопатии, образуются микроаневризмы и микростенозы сосудов мягкой мозговой оболочки и мелких сосудов головного мозга. Они являются причиной повреждения субкортикального белого вещества. При наследственной цистатин-С-амилоидной ангиопатии у больных моложе 40 лет возникают повторные микрокровоизлияния, которые в дальнейшем могут привести к деменции [29] и паркинсонизму
В связи с обсуждением вопроса формирования сосудистых микроповреждений субкортикального белого вещества крайне интересны данные, показывающие, что образование микроинфарктов в белом субкортикальном веществе и лейкоэнцефалопатия являются следствием редкого аутосомно-доминантного состояния, возникающего в результате изменений в локализации на плече хромосомы 19q12. Эту хромосомную аномалию связывают с церебральными аутосомно-доминантными артериопатиями, проявляющимися в поражении мелких сосудов, снабжающих кровью глубинные отделы белого вещества. Таким образом возникает картина множественных микроскопических инфарктов белого вещества, таламуса, базальных ганглиев и моста.
Причиной сосудистого паркинсонизма (как и сосудистой деменции) могут быть редкие артериопатии. Такие воспалительные (полиартериит nodosa, височный артериит) и невоспалительные (болезнь моя-моя, фибромышечная дисплазия) артериопатии могут явиться причиной множественных инфарктов и привести к сосудистому паркинсонизму и деменции. Гипоперфузия крупных сосудов мозга, обусловленная сердечной патологией, может также привести к поражению зон смежного кровообращения мозга и клинически проявиться сосудистым паркинсонизмом и сосудистой деменцией [30, 31].
Подводя промежуточный итог, можно сделать вывод о том, что в возникновении сосудистого паркинсонизма ключевыми моментами является не столько этиология самого сосудистого заболевания, а сколько локализация сосудистых очагов в структурах базальных ганглиев.
Клинические особенности сосудистого паркинсонизма
Особенности паркинсонического синдрома:
Сопутствующие синдромы:
Сосудистый паркинсонизм может развиваться после одного или нескольких инсультов или транзиторной ишемической атаки, при этом экстрапирамидная симптоматика может развиваться в остром периоде инсульта или спустя несколько месяцев, иногда на фоне регресса пирамидных или мозжечковых нарушений маскирующих паркинсонические симптомы. В последующем симптоматика может стабилизироваться и даже регрессировать. Но чаще сосудистый паркинсонизм развивается постепенно, в рамках дисциркуляторной энцефалопатии. В этом случае для него характерны:
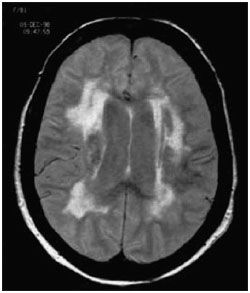
Рис. 1. МРТ головного мозга больного с сосудистым паркинсонизмом
Нейровизуализационные изменения у больных сосудистым паркинсонизмом (рис. 1):
Отсутствие сосудистых изменений при МРТ (но не при КТ, менее чувствительной к патологии белого вещества) исключает диагноз сосудистого паркинсонизма.
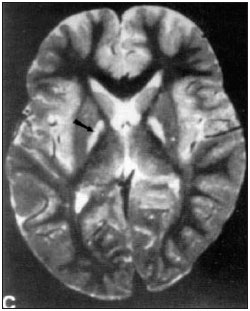
Рис. 2. КТ головного мозга у больного с сосудистым паркинсонизмом
Клинические аспекты сосудистого паркинсонизма
Тремор «покоя» по типу «катания пилюль», характерный для больных БП, как правило, отсутствовал, а тремор не по типу «катания пилюль» был только в 20% случаев возможного сосудистого паркинсонизма [21]. Повышение мышечного тонуса чаще было по смешанному типу (комбинация спастического тонуса и ригидности), но не «зубчатое колесо». Обычно наблюдается сопутствующая паратония или gegenhalten. Распределение гипертонии напоминает о поражении верхних (пирамидных) мотонейронов, вовлекающих антигравитационные мышцы в большей мере, чем экстрапирамидный паттерн, прослеживающийся при БП. У ряда больных часто можно наблюдать сочетание брадикинезии различной степени выраженности с микрографией.
Характерны нарушения походки, они наблюдались во многих сериях исследований [22]. Верхние конечности, как правило, свободны, что подтверждается термином «паркинсонизм нижней половины тела». Поза, как правило, прямая с широко расставленными ногами (в противоположность узкой базе при БП); ассоциативные движения руками утрачиваются. Можно видеть выраженную ретропульсию при отсутствии пропульсии и латеропульсии. Возможны симптомы псевдобульбарного паралича (дизартрия, дисфагия и эмоциональная лабильность). Другие авторы выделяют такие характерные симптомы, как несдержанность, пирамидные знаки и др. [14].
Синдром «чистого паркинсонизма» не отличим от идиопатической БП. О нем крайне редко сообщается в связи с больными, имеющими инфаркты, лакуны или дилатацию васкулярных пространств в области базальных ганглиев [23]. Также описан синдром, аналогичный прогрессирующему супрануклеарному параличу, у больных сосудистым паркинсонизмом. По результатам исследований, проведенных Dubinsky и Jankovic, примерно у 1/3 больных с синдромом, похожим на синдром прогрессирующего супрануклеарного паралича, обследованных ими, возник в результате мультиинфарктного состояния [24]. Проведенное авторами исследование подтвердило положительный эффект лечения препаратами левадопы у многих больных сосудистым паркинсонизмом, имеющих патологию нигростриарной системы [25]. Необходимо помнить, что как сосудистый паркинсонизм, так и БП являются типичными заболеваниями в популяции людей старшей возрастной группы и не является редкостью наличие их сосуществования. Этот так называемый «перекрывающий» (коморбидный) синдром может создать проблему в диагностике и лечении, так как ответ на дофаминергическую терапию может быть не оптимальным.
Результаты МРТ при сосудистом паркинсонизме
Наличие сосудистой патологии мозга по данным МРТ помогает в диагностике сосудистого паркинсонизма, но не устанавливает причину и не выявляет взаимоотношение между ЦВБ и сосудистым паркинсонизмом. В дальнейшем ситуация усложняется и тем, что одинаковые сосудистые повреждения в одних случаях сопровождаются паркинсонизмом, а в других нет. Несмотря на эти ограничения, полезно искать доказательство васкулярного заболевания на МРТ-изображении мозга. МРТ головного мозга в этих случаях может также помочь с исключением других причин возникшего вторичного паркинсонизма у больного, например нормотензивную гидроцефалию и др. МРТ является более чувствительным методом визуальной диагностики, чем КТ при диагностике ишемическом цереброваскулярном заболевании. При сравнительном МРТ-исследовании больных с предположительным диагнозом сосудистого паркинсонизма выявлено значительное превышение субкортикальных сосудистых очагов по сравнению с больными БП или гипертензией [26]. Объем поврежденной ткани мозга, равный 0.6%, наиболее точно определяет точку различия между пациентами с сосудистым паркинсонизмом и пациентами с БП. Существуют различные данные относительно частоты корреляции между сосудистыми повреждениями substantia nigra и БП. Одни предполагают, что случаи сосудистого паркинсонизма среди пациентов с инфарктом базальных ганглиев, с лакунарными инфарктами или с расширением сосудистых пространств были редки. Другие исследования показали, что 38% пациентов с лакунарными инфарктами базальных ганглиев, выявленными на МРТ, также страдали БП [27].
Функциональное изображение
Позитронно-эмиссионная томография (ПЭТ) и single-photon emission-компьтерная томография (SPECT) может быть применена в качестве дополнения к морфологическим данным, полученным при МРТ и КТ с целью диагностики различных паркинсонических синдромов. Использование связи переносчиков дофамина (dopamine transporter — DAT) при функциональных изобразительных технологиях (Спектре) может помочь в дифференциальной диагностике БП (пресинаптическое нарушение) и случаев сосудистого паркинсонизма. Данная техника позволяет определить целостность дофаминергической системы и является основным вспомогательным методом в клинической диагностике легкого, неосложненного паркинсонизма или в случаях, когда нет уверенности в диагнозе паркинсонизма [28]. Изображение DAT изменено при БП, множественной системной атрофии и прогрессирующем супрануклеарном параличе и не выявляет различий между этими заболеваниями. Нормальные результаты сканирования характерны для альтернативных диагнозов, таких как эссенциальный тремор, сосудистый (до возникновения локальных инфарктов в базальных ганглиях), медикаментозный паркинсонизм или психогенный паркинсонизм. SPECT, являющийся специфическим методом изобразительной диагностики, связанный с DAT (FP-CIT, betaCIT, IPT, TRO-DAT), выполняет роль маркера пресинаптической нейрональной дегенерации. При исследовании с использованием данной технологии удалось выявить корреляцию между степенью уменьшения связей стриатума и степенью тяжести БП, но аналогичной корреляции у больных сосудистым паркинсонизмом выявлено не было [29]. Надо отметить, что изображение DAT может не соответствовать норме при сосудистом паркинсонизме в связи с локальным инфарктом в базальных ганглиях. Характеристика «перфорированных» изображений таких повреждений при исследовании методом SPECT приведены в литературе [28].
При проведении ПЭТ больным сосудистой деменцией, имеющим и не имеющих симптомы паркинсонизма, было показано, что локальные ишемические изменения в стриатуме принимают участие в формировании синдрома паркинсонизма у больных сосудистой деменцией [30]. Результаты ПЭТ показали снижение регионального кровотока (rCBF) и регионального уровня метаболизма кислорода (rCMRO) во фронтальной и париетальной коре головного мозга и стриатуме у больных с деменцией и паркинсонизмом по сравнению с группой больных сосудистой деменцией, не имеющих симптомов паркинсонизма. При БП показатели rCBF и rCMRO были значительно ниже в стриатуме, контралатеральном стороне наиболее выраженной клинической картине паркинсонизма. Хотя метод (DAT) является более чувствительным, он не применяется так широко, как SPECT и ПЭТ.
Лечение
Важным направлением терапии сосудистого паркинсонизма является нейропротекция — защита дофаминовых нейронов от факторов, влияющих на их дегенерацию, что способствует замедлению прогрессирования заболевания. В последние годы с помощью методов функциональной нейровизуализации (ПЭТ, SPECT) удалось показать, что на фоне приема агонистов дофаминовых рецепторов численность маркеров дофаминергических окончаний в стриатуме снижается в меньшей степени, чем на фоне приема леводопы, что, возможно, отражает замедление дегенеративного процесса. Предполагаемый нейропротекторный эффект агонистов дофаминовых рецепторов может быть связан с их антиоксидантными свойствами, способностью индуцировать продукцию факторов роста и тормозить апоптоз, активацией пресинаптических ауторецепторов с уменьшением кругооборота дофамина, а также торможением избыточной активности субталамического ядра, которая сопровождается выделением избыточного количества возбуждающих аминокислот, способных оказывать токсическое действие на клетки черной субстанции. Если нейропротекторное действие агонистов будет подтверждено клиническими данными, то станет необходимым назначать их при первых признаках болезни — до развития функционально значимого двигательного дефекта.
Симптоматическое лечение
Поскольку основными нейрохимическими нарушениями при сосудистом паркинсонизме является избыток возбуждающих аминокислот глутамата и аспартата, симптоматическое лечение направлено на коррекцию этих изменений: сохранение количества дофамина, стимуляция дофаминовых рецепторов и подавление избыточной глутаматергической активности.
Препараты леводопы менее эффективны при сосудистом паркинсонизме. Они не лишены недостатков: могут активировать процессы перекисного окисления в нигростриарных нейронах. Леводопа вызывает ряд побочных эффектов (гастроэнтерологические, кардиоваскулярные, психотические, галлюцинаторные нарушения).
Агонисты дофаминовых рецепторов — АДР (пирибедил, прамипексол, бромокриптин) способны непосредственно стимулировать дофаминовые рецепторы в обход дегенерирующих нигростриарных нейронов. Целесообразность назначения АДР подтверждается также тем, что они достаточно (в большей степени, чем амантадины, холинолитики и ингибиторы МАО типа В) купируют тремор, ригидность и гипокинезию. При этом следует обратить внимание, что агонисты существенно уменьшают выраженность тремора — симптома, достаточно резистентного к терапии. АДР хорошо проявили себя в лечении не только двигательных, постуральных расстройств, но и в терапии когнитивных нарушений при сосудистом паркинсонизме.
Проноран (пирибедил) является единственным неэрголиновым АДР, способным блокировать пресинаптические α2-адренорецепторы, выполняющие роль ауторецепторов норадренергических нейронов. Блокируя пресинаптические α2-норадренорецепторы, Проноран облегчает норадренергическую передачу в голубом пятне и увеличивает высвобождение норадреналина в терминалях норадренергических нейронов. Благодаря воздействию на D2/D3-рецепторы, Проноран уменьшает основные двигательные симптомы паркинсонизма — ригидность, тремор и брадикинезию. Благодаря норадренергическому эффекту Проноран устраняет не только малочувствительные к леводопе двигательные симптомы БП (нарушения позы, походки), но также ряд когнитивных и эмоциональных расстройств (нарушения памяти, снижение активности, способности к концентрации, депрессия). Норадренергическая активность Пронорана также способствует предотвращению и лечению вегетативных нарушений, прежде всего ортостатической гипотонии.
Результаты целого ряда зарубежных и отечественных исследований показали, что применение Пронорана на начальных стадиях сосудистого паркинсонизма значительно уменьшает выраженность двигательных нарушений, как при монотерапии, так и в комбинации с амантадином. Следствием уменьшения выраженности двигательной симптоматики стало улучшение качества жизни и социальной адаптации пациентов.
При использовании АДР необходимо иметь в виду возможность развития различных побочных эффектов. Так, при применении бромокриптина, являющегося производным спорыньи, возможны спазм коронарных сосудов (особенно у больных с ИБС), феномен Рейно, ретроперитонеальный и плевропульмональный фиброз. Неэрголиновые препараты (пирибедил, прамипексол) лишены этих побочных действий, кроме того, могут быть без опасения назначены пациентам с ИБС. В последние годы ряд авторов сообщили о развитии приступов внезапного засыпания при приеме различных агонистов дофаминовых рецепторов, чаще нового поколения (прамипексола, ропинирола), которые явились причиной дорожно-транспортных происшествий с весьма серьезными последствиями. Разные АДР в неодинаковой степени вызывают сонливость. Анализ литературных данных показывает, что седативный эффект у прамипексола выше, чем у пирибедила (Пронорана). По данным клинических испытаний, частота появления сонливости при применении Пронорана существенно не превышала таковую при применении плацебо.
Удобство применения препарата прежде всего определяется простотой схемы титрования дозы, что является гарантией хорошей комплаентности больного. Эффективную дозу всех агонистов приходится подбирать путем медленного титрования, чтобы избежать побочных эффектов. Достижение терапевтической дозы (150—250 мг/сут) требует от 3 до 5 недель, при этом схема титрования весьма удобна: каждую неделю суточная доза при необходимости повышается на 1 таблетку. Для предупреждения или коррекции тошноты и рвоты в период подбора дозы может применяться домперидон (мотилиум) в дозе 10—20 мг 3 раза в день. Необходимость в его приеме редко сохраняется более 2 нед.
Когнитивные нарушения при сосудистом паркинсонизме различной выраженности можно выявить у 95% больных БП. В первые годы заболевания у подавляющего большинства больных обычно выявляют легкие или умеренные нарушения в виде замедления психических процессов (брадифрения), снижения внимания, ограничения способности к запоминанию и активному воспроизведению. Данные нарушения преимущественно обусловлены дис-функцией ассоциативных отделов лобной коры, связанной с поражением восходящих дофаминергических, норадренергических и холинергических путей. Исследования последних лет показали, что АДР могут улучшать нейродинамические и регуляторные когнитивные функции и оказывать антидепрессантный эффект. В случае Пронорана важную роль может играть усиление активности норадренергической системы, имеющей значение в поддержании внимания и активности. Положительное влияние агонистов дофаминовых рецепторов на когнитивные функции подкрепляют ноотропные препараты, усиливающие холинергическую передачу.
Целесообразность того или иного сочетания лекарственных средств диктуется прежде всего возрастом пациента и выраженностью различных симптомов.
ЛИТЕРАТУРА
1. John Winikates, MD; Joseph Jankovic, MD. Clinical Correlates of Vascular Parkinsonism. Arch Neurol. 1999; 56: 98—102.
2. Hughes A.J., Daniel S.E., Kilford L., Lees A.J. Accuracy of clinical diagnosis of idiopathic Parkinson's disease: a clinico-pathological study. J Neurol Neurosurg Psychiatry. 1992; 55: 181—184. ABSTRACTCritchley M. Arteriosclerotic parkinsonism. Brain. 1929; 52: 23-83.
3. Critchley M. Arteriosclerotic pseudo-parkinsonism. In: Rose F.C., Capildo R., eds. Research Progress in Parkinson's Disease. London. England: Pitman; 1981: 40-42.
4. Tolosa E.S., Santamaria J. Parkinsonism and basal ganglia infarcts. Neurology. 1984; 34: 1516-1518.
5. Friedman A., Kang U.J., Tatemichi T.K., Burke R.E. A case of parkinsonism following striatal lacunar infarction. J Neurol Neurosurg Psychiatry. 1986; 49: 1087-1088.
6. Mayo J., Aria M., Leno C., Berciano J. Vascular parkinsonism and periarteritis nodosa. Neurology. 1986; 36: 874-875.
7. Quinn N., Parkes D., Janota I., Marsden C.D. Preservation of the substantia nigra and locus coeruleus in a patient receiving levodopa (2 kg) plus decarboxylase inhibitor over a four-year period. Mov Disord. 1986; 1: 65-68.
8. Murrow R.W., Schweiger G.D., Kepes J.J., Koller W.C. Parkinsonism due to a basal ganglia lacunar state: clinicopathological correlation. Neurology. 1990; 40: 897-900.
9. Pullicino P., Lichter D., Benedict R. Micrographia with cognitive dysfunction: «minimal» sequelae of a putaminal infarct. Mov Disord. 1994; 9: 371-373.
10. Parkes J.D., Marsden C.D., Rees J.E. et al. Parkinson's disease, cerebral arteriosclerosis, and senile dementia. Q J Med. 1974; 43: 49-61.
11. FitzGerald P.M., Jankovic J. Lower body parkinsonism: evidence for a vascular etiology. Mov Disord. 1989; 4: 249-260.
12. Chang C.M., Yu Y.L., Ng H.K. et al. Vascular pseudoparkinsonism. Acta Neurol Scand. 1992; 86: 588-592.
13. Agnoli A., Baldassarre M., Stucchi R., Ruggieri S. Can cerebrovascular disease be responsible for extrapyramidal disorders and the question of arteriosclerotic parkinsonism. In: Meyer J.S., Lechner H., Reivich M., Ott E.D., eds. Cerebrovascular Disease 6: Proceedings of the World Federation of Neurology 13th International Salzburg Conference, September 25-27, 1986. Belle Mead, NJ: Excerpta Medica-Princeton; 1987: 113-117.
14. Reider-Groswasser I., Bornstein N.M., Korczyn A.D. Parkinsonism in patients with lacunar infarcts of the basal ganglia. Eur Neurol. 1995; 35: 46-49.
15. Ikeda K., Kotabe T, Kanbashi S., Kinoshita M. Parkinsonism in lacunar infarcts of the basal ganglia. Eur Neurol. 1996; 36: 248-249.
16. de la Fuente Fernandez R., Lopez J.M., Rey del Corral P., de la Iglesia Martinez F. Peduncular hallucinosis and right hemiparkinsonism caused by left mesencephalic infarction. J Neurol Neurosurg Psychiatry. 1994; 57: 870.
17. Straussberg R., Shahar E., Gat R., Brand N. Delayed parkinsonism associated with hypotension in a child undergoing open-heart surgery. Dev Med Child Neurol. 1993; 35: 1011-1014.
18. Hageman A.T.M., Horstink M.W.I.M. Parkinsonism due to a subdural hematoma. Mov Disord. 1994; 9: 107-108.
19. Zijlmans J.C.M., Thijssen H.O.M., Vogels O.J.M. et al. MRI in patients suspected of vascular parkinsonism. Neurology. 1995;45:2183-218 Hupperts R.M.M., Lodder J., Heuts-van Raak E.P.M., Kessels F. Infarcts in the anterior choroidal artery territory: anatomical distribution, clinical syndromes, presumed pathogenesis and early outcome. Brain. 1994; 117: 825-834.
20. Bhatia K.P., Marsden C.D. The behavioural and motor consequences of focal lesions of the basal ganglia in man. Brain. 1994; 117: 859-876.
21. Baloh R.W., Yue Q., Socotch T.M., Jacobson K.M. White matter lesions and disequilibrium in older people, I: case-control comparison. Arch Neurol. 1995; 52: 970-974. ABSTRACT
22. Baloh R.W., Vinters H.V. White matter lesions and disequilibrium in older people, II: clinicopathological correlation. Arch Neurol. 1995; 52: 975-98.
23. Thompson P.D., Marsden C.D. Gait disorder of subcortical arteriosclerotic encephalopathy: Binswanger's disease. Mov Disord. 1987; 2: 1-8.
24. Bonuccelli U., Antonio P.D., Del Dotto P. et al. The elusive vascular parkinsonsim. Neurology. 1995; 45 (suppl 4): A3394.
25. Marks M.H., Sage J.I., Walters A.S. et al. Binswanger's disease presenting as levodopa-responsive parkinsonism: clinicopathological study of three cases. Mov Disord. 1995; 10: 450-454.
26. Winikates J.P., Jankovic J. Vascular progressive supranuclear palsy. J Neural Transm Suppl. 1994 Ghika J, Bogousslavsky J. Presymptomatic hypertension is a major feature in the diagnosis of progressive supranuclear palsy. Arch Neurol. 199; 43: 189-201.
27. van Zagten M., Lodder J., Kessels F. Gait disorder and parkinsonian signs in patients with stroke related to small deep infarcts and white matter lesions. Mov Disord. 1998; 13: 89-95.
28. Article Last Updated: Aug 27, 2007 Kannayiram Alagiakrishnan, MD, MBBS, Associate Professor, Department of Medicine, Division of Geriatric Medicine, University of Alberta.
29. Schmidtke K., Hull M. Cerebral small vessel disease: how does it progress? J Neurol Sci. Mar 15 2005; 229-230: 13-20. [Medline].
30. Jellinger K.A. The enigma of vascular cognitive disorder and vascular dementia. Acta Neuropathol (Berl). Apr 2007; 113 (4): 349-88. [Medline].
