Место растительных природных препаратов при лечении депрессии: эффективность и безопасность
СтатьиОпубликовано в журнале:
«Consilium Medicum» 2008, Том 10, № 2, с. 63-67
Г.Р.Табеева,
Ю.Э.Азимова
ММА им. И.М.Сеченова
Экстракт зверобоя является растительным «антидепрессантом». Эффект препаратов на основе экстракта зверобоя обусловлен сложным биохимическим составом и сочетанием нескольких механизмов действия: ингибированием моноаминоксидазы, ингибированием обратного захвата серотонина и норадреналина. Эффективность лекарственных средств на основе экстракта зверобоя в лечении депрессии легкой и умеренной степени тяжести доказана результатами многочисленных клинических испытаний, а также метаанализом более 20 исследований, в которых принимали участие более 1500 человек. Хороший клинический эффект и безопасность приема позволяют широко применять препараты на основе экстракта зверобоя, в особенности в тех случаях, когда прием синтетических антидепрессантов противопоказан.
Растительные препараты традиционно широко применяются при лечении эмоционально-аффективных нарушений. Природные психотропные лекарственные средства как правило содержат экстракты валерианы, пустырника, пиона, ландыша, мелиссы, мяты перечной, хмеля, ромашки, боярышника, бузины. Эти препараты обладают анксиолитическим и седативным действием, поэтому прежде всего эффективны при тревожных расстройствах и нарушениях сна [35]. У пациентов, страдающих депрессией, такие растительные средства могут использоваться как вспомогательные – с целью уменьшения тревоги и коррекции инсомнии. Для специфического лечения расстройств настроения врачами в течение не одного столетия используются препараты зверобоя (Hypericum perforatum). Свое латинское название растение получило от "hyper", что значит «чрезмерно», и "eikon" – видение. Таким образом, еще в древние времена было известно о психотропном действии этого лекарственного растения. О целебных свойствах Hypericum perforatum при ранах, ожогах, отравлениях, а также невралгиях и умопомешательствах упоминали еще античные врачеватели Гален и Гиппократ, а в дальнейшем и средневековый врач Пара-цельс, однако для лечения «меланхолии» зверобой был впервые применен английским астрологом и травником Николсом Кульпепером в 1652 г. [12, 18]. В наши дни препараты на основе экстракта зверобоя наиболее часто выписывают для лечения депрессии в Европе [23]. В США же за 2002 г. препараты на основе Hypericum perforatum принимали 12% населения [41].
Механизм терапевтического действия растительных препаратов с антидепрессивным эффектом
Экстракт зверобоя имеет сложный биохимический состав. Ранее считалось, что антидепрессивный эффект экстракта зверобоя связан с входящими в его состав нафтодиантронами гиперицином и псевдогиперицином [18], а механизм действия препаратов на основе Hypericum perforatum обусловлен ингибированием моноаминоксидазы (МАО) гиперицином [39]. Однако экспериментальные данные показали, что гиперицин ингибирует МАО в концентрациях, значительно превышающих таковые в экстракте зверобоя [6]. В последнее время появляются сообщения и об антидепрессивном действии гиперфорина, относящегося к классу флованоидов [28]. Было показано, что гиперфорин в дозах, содержащихся в экстракте зверобоя, ингибирует обратный захват серотонина, норадреналина и дофамина [29], а также повышает уровень кортизола [10]. Ряд исследователей [8, 14] полагают, что экстракт Hypericum perforatum стимулирует образование серотонина в нейронах головного мозга. По данным M.Wonnemann и соавт, гиперфорин также влияет на ГАМКергические и глутаматергические системы мозга [43]. Более того, экспериментально подтверждено, что гиперфорин в малых дозах стимулирует выброс ацетилхолина, а в больших - ингибирует его обратный захват [7]. Этот эффект отмечен и в клинической практике: в отличие от синтетических антидепрессантов препараты зверобоя не ухудшают когнитивные функции (быстрота реакции, кратковременная память, тест Струпа), а также не влияют на координацию [37]. Таким образом, эффект препаратов на основе экстракта зверобоя обусловлен сложным биохимическим составом и сочетанием нескольких механизмов действия.
Клиническая эффективность растительных антидепрессантов
Эффективность лекарственных средств на основе Hypericum perforatum в лечении депрессии легкой и умеренной степени тяжести доказана результатами многочисленных клинических испытаний, а также метаанализом данных более чем 20 исследований, в которых участвовали более 1500 человек [4, 18]. Остановимся на результатах наиболее крупных исследований. В двойном слепом рандомизированном плацебо-контролируемом исследовании Y.Lecrubier и соавт. [23] участвовали 375 пациентов с диагнозом «большой депрессивный эпизод». Показателями эффективности были доля больных со снижением выраженности депрессии по шкале Гамильтона на 50% и больше, а также достигших ремиссии (6 баллов и менее по шкале Гамильтона). После 6 нед лечения в группе пациентов, получавших экстракт зверобоя, были отмечены достоверно более высокий ответ на лечение и доля достижения ремиссии. Вместе с тем, препарат на основе экстракта зверобоя не отличался от плацебо по наличию побочных эффектов [23].
В рандомизированном двойном слепом плацебо-контролируемом мультицентровом исследовании S.Kasper и соавт. участвовали 332 пациента во время большого депрессивного эпизода умеренной или средней степени тяжести [20]. Основным показателем эффективности был суммарный балл по шкале Гамильтона до и после лечения, дополнительными показателями являлись число респондеров (больных со снижением уровня депрессии по шкале Гамильтона более чем на 50%), процент ремиссии, уровень депрессии по шкалам Бэка и Монт-гомери–Асберга, а также оценка пациента по шкале общего впечатления проведенного лечения. Пациенты принимали экстракт зверобоя, содержащий гиперицин в дозах 600 мг/сут (1-я группа) и 1200 мг/сут (2-я группа) или плацебо (3-я группа) в течение 6 нед. После курса лечения уровень депрессии в группах снизился на 11,6±6,4, 10,8±7,3 и 6,0±8,1 баллов по шкале Гамильтона соответственно [20] (рисунок).
Динамика уровня депрессии по шкале Гамильтона у пациентов, получавших экстракт зверобоя, содержащий гиперицин в дозах 600 (1) и 1200 мг/сут (2), а также плацебо (3).
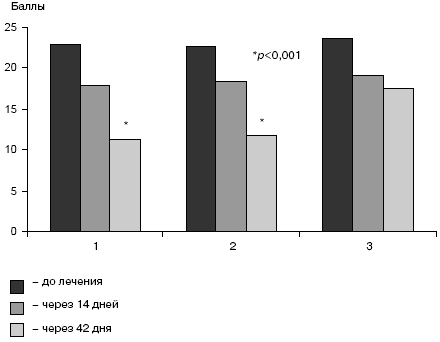
В группах, получавших активный препарат, также достоверно большим по сравнению с плацебо была доля респондеров (69,8% у пациентов, получавших 600 мг/сут экстракта зверобоя, 61,3% – у пациентов, принимавших 1200 мг/сут экстракта зверобоя, и 31,1% – в группе плацебо). Доля ремиссий составила 32,8% в 1-й группе, 40,3% – во 2-й и 14,8% – в группе плацебо. Уровень депрессии по шкалам Бэка и Монтгомери–Асберг также достоверно снижался в группах, получавших активный препарат. Большинство пациентов, принимавших препарат на основе экстракта зверобоя в данном исследовании, оценивали результаты лечения как «хорошие» и «очень хорошие» [20].
Пациенты-респондеры (161 человек), участвовавшие в предыдущем исследовании S.Kasper и соавт., продолжили принимать активный препарат или плацебо в течение последующих 4 мес. При более длительном курсе лечения (4 месяца) антидепрессивный эффект препарата на основе Hypericum perforatum сохранялся, тогда как при приеме плацебо симптомы депрессии возвращались [21]. Анализ данных 4337 пациентов с депрессией показал, что прием препаратов на основе экстракта зверобоя достоверно улучшает качество жизни таких больных [34].
В ряде исследований сравнивали эффективность препаратов на основе Hypericum perforatum и синтетических антидепрессантов. В клиническом исследовании A.Szegedi и соавт. (251 человек), в котором принимали участие пациенты с большими депрессивными эпизодами умеренной и тяжелой степени, экстракт зверобоя в дозе 900 мг/сут по эффективности был сопоставим с пароксетином в дозе 20 мг/сут [40]. При исследовании 388 пациентов с умеренной депрессией препараты на основе экстракта зверобоя (900 мг/сут) показали эффективность, сопоставимую с таковой 20 мг циталопрама [13]. Что же касается флуоксетина, то в одном из исследований препарат зверобоя был сопоставим с ним по эффективности [5], а по данным других авторов лекарственные средства на основе зверобоя оказались менее эффективными, чем флуоксетин, но имели лучший профиль безопасности [27]. В то же время в третьем исследовании было показано, что препараты Hypericum perforatum обладают лучшим эффектом в отношении вегетативных симптомов депрессии по сравнению с флуоксетином [31].
Лекарственные средства на основе зверобоя также оказались сопоставимыми по эффективности с трициклическими антидепрессантами. Так, в исследовании H.Woelk у 157 пациентов, принимавших гиперицин в течение 6 нед, уровень депрессии по шкале Гамильтона снизился с 22,4 баллов до 12,0 баллов, и у 167 больных, получавших имипрамин, с 22,1 до 12,75 баллов [42].
Одним из преимуществ препаратов экстракта зверобоя является быстрое нарастание эффекта. Клинический опыт показывает, что первые признаки эффективности лекарственных средств на основе Hypericum perforatum наблюдаются к началу 2-й недели: улучшается настроение, нормализуется сон, появляется чувство активности, исчезают депрессивные идеи. В дальнейшем улучшение неуклонно продолжается [3].
Эффективность препаратов на основе экстракта зверобоя была доказана и при малой депрессии [33]. К сожалению, несмотря на хороший профиль безопасности, препараты на основе Hypericum perforatum не показали значительной эффективности по сравнению с плацебо при лечении дистимии и тяжелых депрессивных эпизодов [17, 26, 36].
Преимущества использования растительных антидепрессантов у отдельных категорий больных
Главным достоинством препаратов Hypericum perforatum является сочетание эффективности и высокой безопасности препарата. Это делает лекарственные средства на основе экстракта зверобоя препаратами выбора при лечении легких и умеренных депрессивных расстройств в следующих клинических случаях. Прежде всего это касается пожилых пациентов с сопутствующими соматическими и неврологическими заболеваниями и принимающих по этому поводу разные медикаментозные средства. Сопутствующая депрессия оказывает негативное влияние не только на течение основных неврологических заболеваний, таких как инсульт, болезни Альцгеймера и Паркинсона, эпилепсия, рассеянный склероз, но и на проявления соматической патологии (ишемическая болезнь сердца -ИБС, сахарный диабет, ожирение, онкологические заболевания). Негативное влияние депрессии отражается в худшем прогнозе основного заболевания и увеличении смертности пациентов с депрессивными расстройствами по сравнению со страдающими теми же заболеваниями, но без депрессии. Например, у пациентов с ИБС в сочетании с депрессией риск сердечного приступа выше в 2-3 раза, чем у больных с ИБС без депрессии [1]. Соматические заболевания, в первую очередь, болезни сердечнососудистой системы, вызывают значительные ограничения приема синтетических антидепрессантов, особенно трициклических. Назначение растительных препаратов такой категории больным позволит не только уменьшить симптомы депрессии, но и избежать лекарственного взаимодействия и ухудшения течения основного заболевания. Эта идея нашла отражение в ряде клинических исследований. Так, по данным H.Lett и соавт., препараты на основе экстракта зверобоя высоко эффективны и безопасны у пожилых пациентов с депрессией и ИБС [25], а в исследовании M.Siepmann показано, что в отличие от амитриптилина, препараты на основе Hypericum perforatum не влияют на функцию сердечно-сосудистой системы [37]. Поскольку у пожилых пациентов с депрессией легкой или умеренной степени тяжести эффективность препаратов на основе экстракта зверобоя сопоставима с таковой синтетических антидепрессантов [11], то подобный метод альтернативного лечения всегда должен учитываться лечащими врачами.
Значительным преимуществом растительных препаратов является возможность их использования у беременных и кормящих женщин. Следует помнить, что 10% беременных женщин испытывают симптомы деперессии [12]. Послеродовая депрессия в последнее время из медицинской проблемы перерастает в социальную. Депрессию переживают от 10 до 50% рожениц, что негативно сказывается не только на здоровье матери, но и на становлении лактации и состоянии ребенка [22]. Беременность и лактация являются также и основным ограничением в использовании синтетических антидепрессанов. Организация по предоставлению информации о тератогенности препаратов (OTIS) не располагает достаточными данными, чтобы с уверенностью заявить: препараты на основе экстракта зверобоя не представляют опасности для плода [12]. Таким образом, при беременности такие препараты можно рекомендовать лишь в случаях, когда польза от лекарственного средства значительно превышает его потенциальный риск. При лактации использование препаратов на основе зверобоя относительно безопасно. На фоне приема препаратов зверобоя уровень лактации не снижается, концентрация лекарственного препарата в молоке низкая, препараты не вызывают задержки физического и психического развития ребенка [24]. Тем не менее, у грудных детей могут наблюдаться побочные эффекты – колики (2%), вялость и повышенная сонливость (3%), которые не требуют дополнительного врачебного вмешательства [24]. Женщинам, принимающим препараты на основе экстракта зверобоя, следует с особой осторожностью назначать препараты других групп, в особенности антиконвульсанты, антигистаминные средства, оральные контрацептивы, а также омепразол [12, 18].
Существует мнение, что синтетические антидепрессанты не должны быть препаратами первой линии при лечении детей и подростков, особенно при мягких или умеренных депрессивных расстройствах [19]. В отличие от взрослых у детей и подростков депрессия характеризуется более стертым началом, в клинической картине преобладает раздражительность, часто сочетающаяся с другими расстройствами – тревогой, нарушением поведения, гиперкинезами и трудностями в обучении [16]. Синтетические психотропные препараты у детей могут вызвать излишнюю седацию, снижение когнитивных функций и патологическое угнетение физической и эмоциональной активности [2]. В детской и подростковой практике препараты на основе экстракта зверобоя успешно используются не только при депрессивных расстройствах, но и при неврозах, неврастении, бессоннице [2]. Исследование эффективности и безопасности препаратов зверобоя проводили среди подростков (средний возраст 14,8 года) с большим депрессивным эпизодом [38]. Клиническое улучшение наступало у 82% пациентов, при этом переносимость препарата была очень хорошая.
Депрессия широко распространена в популяции (5-12% среди мужчин, 12-20% среди женщин) [1]. В том числе депрессией могут страдать пациенты, деятельность которых связана с управлением механизмами или автомобилем. В этом случае прием синтетических антидепрессантов может привнести существенные ограничения в образ жизни таких больных. Так как препараты зверобоя не ухудшают когнитивные функции (быстрота реакции, кратковременная память, тест Струпа), а также не влияют на координацию [37], то они с особой осторожностью могут применяться и пациентами данной группы.
Симптомы депрессии являются нередкой жалобой у пациентов, обращающихся к врачам самых разных специальностей. Так, врачами общей практики депрессия легкой и умеренной степени тяжести отмечается у 10,5% пациентов [9], гинекологами - у 20% пациенток [32]. Еще одним важным преимуществом растительных препаратов является возможность использовать их не только неврологами и психиатрами, но и врачами других специальностей, имеющими меньший опыт работы с психотропными препаратами. Препараты на основе экстракта зверобоя могут назначать врач общей практики, терапевты, хирурги, гинекологи при депрессивных расстройствах легкой и умеренной степени тяжести в тех случаях, когда консультация психиатра невозможна.
Безопасность растительных антидепрессантов
Обсуждая безопасность препаратов на основе экстракта Hypericum perforatum, необходимо остановится на побочных эффектах препарата, частота возникновения которых по разным данным составляет 1-39% [15, 21]. Побочные эффекты делятся на дерматологические, неврологические, психиатрические, кардиоваскулярные, гастроэнтерологические и урогенитальные. Фотосенситизация, как один из наиболее частых дерматологических побочных эффектов, отмечена учеными еще в начале XX в. у животных, потребляющих зверобой. Данные о фотосенситизации вследствие приема препаратов экстракта зверобоя противоречивы, тем не менее, пациентам, принимающим эти лекарственные препараты, не рекомендуется находиться на открытом солнце или посещать солярий [15]. Среди неврологических побочных эффектов необходимо отметить головную боль, которая при приеме препаратов Hypericum perforatum возникает достоверно чаще, чем при приеме плацебо [17]. Имеются отдельные сообщения о парестезиях в ответ на прием препаратов зверобоя [15].
Препараты на основе экстракта зверобоя следует применять с осторожностью пациентам с биполярными расстройствами, так как они могут спровоцировать развитие тревоги и мании [18]. Также не следует принимать их в сочетании с синтетическими антидепрессантами из-за возможного риск развития серотонинергического синдрома.
В литературе имеются сообщения о подъеме артериального давления и развития тахикардии у пациентов, принимавших препараты зверобоя, однако в крупных контролируемых исследованиях такого побочного эффекта обнаружено не было [15]. Гастроэнтерологические побочные эффекты, к которым относятся сухость во рту, диспепсия, снижение аппетита, тошнота, диарея являются наиболее частыми (19–22%) [18, 21]. Урогенитальные побочные эффекты (частое мочиспускание, аноргазмия) при приеме препаратов на основе экстракта Hypericum perforatum встречаются чаще, чем при приеме плацебо, но реже, чем при приеме синтетических антидепрессантов [15]. Все описанные побочные эффекты носят транзиторный характер и дополнительного лечения не требуют.
Таким образом, среди растительных препаратов с психотропным действием лекарственные средства на основе экстракта зверобоя имеют специфический антидепрессивный эффект. Препараты Hypericum perforatum имеют ряд отличительных особенностей и преимуществ:
- при мягкой и умеренной депрессии их эффективность сопоставима с таковой трициклических антидепрессантов и селективных ингибиторов обратного захвата се-ротонина;
- в отличие от синтетических антидепрессантов сложный биохимический состав и множественные механизмы действия препарата обусловливают быстрое (в течение 2 нед) наступление стойкого эффекта;
- безопасность, позволяющая использовать препарат за рамками психиатрической и неврологической практики, а также назначать его определенным категориям пациентов, которым противопоказан прием синтетических антидепрессантов;
- положительная оценка эффективности и переносимости терапии самими пациентами, а также улучшение качества их жизни.
Одним из лекарственных препаратов, в состав которого входит экстракт зверобоя, является Деприм (в каждой таблетке – 60 мг стандартизированного сухого экстракта зверобоя). Препарат показан при депрессии легкой и средней степени тяжести, сопровождающейся тревогой, при климактерическом синдроме, повышенной чувствительности к изменению метеоусловий. Антидепрессивное действие препарата проявляется через 10–14 дней после начала приема, клиническое улучшение наступает у 80% пациентов [3]. Эффективность и безопасность позволяют Деприму быть в арсенале врача любой специальности.
ЛИТЕРАТУРА
1. Каннер А.М. Депрессия при неврологических заболеваниях. Литера. 2007.
2. Студенкин В.М., Балканская С.В., Шелковский В.И. Беспокойные дети и применение препаратов растительного происхождения. Леч. врач. 2007; 8: 89–92.
3. Точилов В.А. Опыт лечения депрессии депри-мом. Журн. неврол. и психиат. 2000; 5: 63–4.
4. Ушкалова А.В. Эффективность и безопасность Hypericum perforatum при психических расстройствах. Врач. 2007; 9.
5. Bjerkenstedt L, Edman GV, Alken RG et al. Hyper-icum extract LI 160 and fluoxetine in mild to moderate depression: a randomized, placebo-controlled multi-center study in outpatients. Eur Arch Psychiatry Clin Neurosci 2005; 255: 40–7.
6. Bladt S, Wagner H. Inhibition of MAO by fractions and constituents of Hypericum extract. J Geriatr Psychiatry Neurol 1994; 7: S57–9.
7. Buchholzer M-L, Dvorak C, Chatterjee SS et al. Dual modulation of striatal acetylcholine release by hyperforin, a constituent of St. John's wort. JPET 2002; 301: 714–9.
8. Fornal CA, Metzler CW, Mirescu C et al. Effects of standardized extracts of St. John's wort on the single-unit activity of serotonergic dorsal raphe neurons in awake cats: comparisons with fluoxetine and ser-traline. Neuropsychopharmacology 2001; 25: 858–70.
9. Fortes S, Villano LA, Lopes CS. Nosological profile and prevalence of common mental disorders of patients seen at the Family Health Program (FHP) units. Rev Bras Psiquiatr 2007; 67: 538–44.
10. Franklin M, Cowen PJ. Researching the antide-pressant actions of Hypericum perforatum (St. John's wort) in animals and man. Pharmacopsychiatry 2001; 34: S29–37.
11. Frazer CJ, Christensen H, Griffiths KM. Effectiveness of treatments for depression in older people. MJA 2005; 182: 627–32.
12. Dugoua J-J, Mills E, Perri D et al. Safety and efficacy of St. John's wort (hypericum) during pregnancy and lactation. Can J Clin Pharmacol2006; 13: 268–76.
13. Gastpar M, Singer A, Zeller K. Comparative efficacy and safety of a once-daily dosage of hypericum extract STW3-VI and citalopram in patients with moderate depression: a double-blind, randomised, multicentre, placebo-controlled study. Pharma-copsychiatry 2006; 39: 66–75.
14. Gobbi M, Valle FD, Ciapparelli C et al. Hypericum perforatum L. extract does not inhibit 5-HT transporter in rat brain cortex. Naunyn Schmiedebergs Arch Pharmacol 1999; 360: 262–9.
15. Hammerness P, Basch E, Ulbright C et al. St. John's wort: a systematic review of adverse effects and drug interactions for the consultation psychiatrist. Psycho-somatics 2003; 44: 271–82.
16. Hazell P. Depression in children and adolescents. Am Fam Physician 2003; 67: 577–9.
17. Hypericum Depression Trial Study Group. Effect of Hypericum perforatum (St John's wort) in major depressive disorder. A randomized controlled trial. JAMA 2002; 287: 1807–14.
18. Hypericum perforatum. Monograph. Altern Med Rev 2004; 9: 318–25.
19. Jorm AF, Allen NB, O'Donnell CP et al. Effectiveness of complementary and self-help treatments for depression in children and adolescents. Med J Aust 2006; 185: 368–72.
20. Kasper S, Anghelescu I-G, Szegedi A et al. Superior efficacy of St John's wort extract WS® 5570 compared to placebo in patients with major depression: a randomized, double-blind, placebo-controlled, multi-center trial. BMC Med 2006; 4: 14–27.
21. Kasper S, Anghelescu IG, Szegedi A et al. Placebo controlled continuation treatment with Hypericum extract WS 5570 after recovery from a mild or moderate depressive episode. Wien Med Wochenschr 2007; 157: 362–6.
22. Kendall-Tackett K. A new paradigm for depression in new mothers: the central role of inflammation and how breastfeeding and anti-inflammatory treatments protect maternal mental health. International Breastfeeding Journal 2007; 2: 6–20.
23. Lecrubier Y, Clerc G, Didi R et al. Efficacy of St. John's wort extract WS 5570 in major depression: a double-blind, placebo-controlled trial. Am J Psychiatry 2002; 159: 1361–6.
24. Lee A, Minhas R, Matsuda N et al. The safety of St. John's wort (Hypericum perforatum) during breastfeeding. J Clin Psychiatry 2003; 64: 966–8.
25. Lett HS, Davidson J, Blumenthal JA. Nonpharma-cologic treatments for depression in patients with coronary heart disease. Psychosomatic Med 2005; 67: S58–62.
26. Linde K, Berner M, Egger M et al. St John's wort for depression. Meta-analysis of randomised controlled trials. Brit J Psych 2005; 186: 99–107.
27. Moreno RA, Teng CT, de Almeida KM et al. Hyper-icum perforatum versus fluoxetine in the treatment of mild to moderate depression: a randomized double-blind trial in a Brazilian sample. Rev Bras Psiquiatr 2005; 28: 29–32.
28. Muller WE, Singer A, Wonnemann M. Hyperforin – antidepressant activity by a novel mechanism of action. Pharmacopsychiatry 2001; 34: 98–102.
29. Muller WE, Singer A, Wonnemann M et al. Hyper-forin represents the neurotransmitter reuptake inhibiting constituent of Hypericum extract. Phar-macopsychiatr 1998; 31: S16–21.
30. Muller T, Mannel M, Murck H et al. Treatment of somatoform disorders with St. John's wort: a randomized, double-blind and placebo-controlled trial. Psychosomatic Med 2004; 66: 538–47.
31. Murck H, Fava M, Alpert J et al. Hypericum extract in patients with MDD and reversed vegetative signs: re-analysis from data of a double-blind, randomized trial of hypericum extract, fluoxetine, and placebo. Int J Neuropsychopharmacol 2005; 8: 215–21.
32. Poleshuck EL, Giles DE, Tu X. Pain and depressive symptoms among financially disadvantaged women's health patients. J Womens Health (Larchmt). 2006; 15: 182–93.
33. Randlov C, Mehlsen J, Thomsen CF et al. The efficacy of St. John's Wort in patients with minor depressive symptoms or dysthymia–a double-blind placebo-controlled study. Phytomedicine 2006; 13: 215–21.
34. Rudolf GA, Zeller K. Highly dosed St. John's wort extract improves quality of life. MMW Fortschr Med 2004; 146 (Suppl. 2): 77–80.
35. Saeed SA, Blooch RM, Antonacci DJ. Herbal and dietary supplements for treatment of anxiety disorders. Am Family Physician 2007; 76: 549–56.
36. Shelton RC, Keller MB, Gelenberg A et al. Effectiveness of St John's wort in major depression. A randomized controlled trial. JAMA 2001; 285: 1978–86.
37. Siepmann M, Krause S, Joraschky P et al. The effects of St John's wort extract on heart rate variability, cognitive function and quantitative EEG: a comparison with amitriptyline and placebo in healthy men. Br J Clin Pharmacol 2002; 54: 277–82.
38. Simeon J, Nixon MK, Milin R et al. Open-label pilot study of St. John's wort in adolescent depression. J Child Adolesc Psychopharmacol 2005; 15: 293–301.
39. Suzuki O, Katsumata Y, Oya M et al. Inhibition of monoamine oxidase by hypericin. Planta Med 1984; 50: 272–4.
40. Szegedi A, Kohnn R, Dienel R et al. Acute treatment of moderate to severe depression with hyper-icum extract WS 5570 (St John's wort): a randomised controlled double blind non-inferiority trial versus paroxetine. BMJ 2005; 330: 503–8.
41. Williams JW, Holsinger J, Holsinger T. St John's for depression, worts and all. BMJ 2005; 330: 350–1.
42. Woelk H. Comparison of St John's wort and imipramine for treating depression: randomised controlled trial. BMJ 2000; 321: 536–9.
43. Wonnemann M, Singer A, Muller WE. Inhibition of synaptosomal uptake of 3H-L-glutamate and 3H-GABA by hyperforin, a major constituent of St John's wort: the role of amiloride sensitive sodium conductive pathways. Neuropsychopharmacology 2000; 23: 188–97.
