Физиологические основы моторно-эвакуаторной функции пищеварительного тракта
Статьи Опубликовано в:"Российском журнале гастроэнтерологии, гепатологии, колопроктологии, 2007, N 5, с. 4-10 В.Т. Ивашкин1, А.С. Трухманов1, И.В. Маев2
(1Московская медицинская академия им. И.М. Сеченова,
2Московский государственный медико-стоматологический университет) Основные виды нарушений двигательной функции пищеварительного тракта включают в себя: синдром функциональной (неязвенной) диспепсии, гастроэзофагеальную рефлюксную болезнь, различные виды гастропареза (диабетический, идиопатический, постоперационный), синдром раздраженного кишечника, различные виды запоров, синдром хронической кишечной псевдообструкции, постоперационную кишечную непроходимость и др. Двигательная активность желудка проявляется рецептивным расслаблением, адаптивным расслаблением и перистальтическими волнами.
Синхронизированная деятельность желудка и двенадцатиперстной кишки называется антродуоденальной координацией. Согласованная, координированная деятельность парасимпатического и симпатического звеньев нервной регуляции создает условия для нормальной перистальтики. В парасимпатической системе контроль осуществляется через блуждающий нерв, который берет начало в продолговатом мозге. К основным классам рецепторов, участвующим в регуляции моторно-эвакуаторной функции желудочно-кишечного тракта (ЖКТ), относятся холинергические, адренергические, допаминергические, серотониновые, мотилиновые и холецистокининовые. Важнейшим мессенджером в регуляции двигательной функции ЖКТ является допамин, который секретируется в отдельных участках стенки желудка, действует на специальные допаминовые рецепторы, расположенные здесь же, и оказывает ингибирующее, угнетающее влияние на моторику. Торможение двигательной активности стенки приводит к появлению гипомоторной дискинезии, которая в целом встречается чаще.
Прокинетики – фармакологические препараты, которые на разных уровнях и с помощью разных механизмов меняют пропульсивную активность ЖКТ и ускоряют транзит субстрата (пищевого болюса) по нему. Бетанекол, аналог ацетилхолина, оказывает влияние путем прямого взаимодействия с мускариновыми рецепторами клетки. Метоклопрамид и цисаприд обладают прямым стимулирующим влиянием на освобождение ацетилхолина. Следующим механизмом действия является антагонизм к допаминовым (D2) рецепторам клетки. К таким препаратам принадлежат метоклопрамид, L-сульпирид, домперидон и новый прокинетик итоприд, который, обладая двойным механизмом действия, также ингибирует ацетилхолинэстеразу.
Ключевые слова: моторная функция пищеварительного тракта, домперидон, итоприд.
Physiological bases for motor and evacuatory function of the gut
V.T. Ivashkin, A.S. Trukhmanov, I.V. Mayev Main forms of disorders of motor function of gut include: syndrome of functional dyspepsia, gastroesophageal reflux disease, various forms of gastroparesis (diabetic, idiopathic, postsurgical), irritable bowel syndrome, various forms of constipation, syndrome of chronic intestinal pseudo-obstruction, postsurgical ileus, etc. Motor activity of the stomach shows receptive relaxation, adaptive relaxation and peristaltic waves.
The synchronized activity of the stomach and duodenum is called antroduodenal coordination. Compounded, co-ordinated activity of parasympathetic and sympathetic nervous compartments provides conditions for normal peristalsis. In parasympathetic system the control is carried out through vagus nerve which originates from medulla oblongata. Main classes of receptors involved in regulation of motor and evacuatory function of gastro-intestinal tract (GIT), include cholinergic, adrenergic, dopaminergic, serotoninergic, motilin and cholecystokinin receptors. The key messenger in regulation of motor function of the gut is dopamine which is secreted in certain areas of the gastric wall, reacts to specific dopamine receptors, that are located there as well, and give inhibiting, oppressing effect on motility. Inhibition of the stomach motor activity most often results in hypokinetic dyskinesia.
Prokinetics are pharmacological agents which modify GIT propulsive activity at different levels and through different mechanisms accelerate transit of substrate (alimentary bolus). Betanechol, acetylcholine analogue, acts by direct interaction with muscarinic receptors of a cell. metoclopramide and cisapride have direct stimulating effect on acetylcholine release. Another mechanism of action involves antagonism to dopamine (D2) cell receptors. These drugs includes metoclopramide, L-sulpiride, domperidone and new prokinetic itopride which, having the double mechanism of action, also inhibits acetylcholinesterase.
Key words: motor function of the gut, domperidone, itopride.
Внимание, уделяемое в современной гастроэнтерологии проблеме нарушений двигательной функции пищеварительного тракта, значительно возросло. Основная симптоматика гастроэнтерологических заболеваний (изжога, отрыжка, срыгивания, тошнота, рвота, потеря аппетита, чувство раннего насыщения, тяжесть в эпигастрии, вздутие живота, запоры, диарея) возникает вследствие нарушений моторики. Эти нарушения могут быть вторичными – на фоне органических заболеваний или первичными – функциональными. Функциональные нарушения составляют большинство случаев обращения больных к врачу, особенно в амбулаторных условиях.
Ниже будут рассмотрены некоторые вопросы физиологии двигательной функции отделов пищеварительного тракта, а именно пищевода, желудка и толстой кишки, в связи с основными видами нарушений этой функции и соответственно их клиническими проявлениями и методами диагностики.
Вне акта глотания пищевод представляет собой тонически напряженную мышечную трубку, не имеющую просвета. Проглатывание пищи представляет собой активную строго координированную деятельность сфинктеров и стенки пищевода. Достаточно сказать, что в акте глотания принимают участие более 20 мышц, синхронизированных между собой и деятельностью дыхательной системы.
Поступление пищевого комка в просвет пищевода происходит при расслаблении верхнего пищеводного сфинктера. Задержка этого расслабления всего на 250 миллисекунд приводит к тяжелейшим случаям аспирационных пневмоний. После поступления пищи в пищевод инициируется первичная перистальтическая волна. Она движется по пищеводу со скоростью 2–4 см в секунду и проходит весь пищевод за 8–12 с. Причем сокращению стенки предшествует ее расслабление. Тонкий механизм данного процесса заключается в том, что холинергическая стимуляция на некоторое время тормозит собственную активность мускулатуры пищевода, поддерживающую его тонус. Затем после прекращения этой стимуляции возникает так называемая «реакция на выключение» и стенка интенсивно сокращается.
Через полсекунды после глотка начинается расслабление нижнего пищеводного сфинктера, которое длится от 7 до 12 с. За это время пища проходит в желудок. Если в пищеводе остается какое-то количество пищи возникает вторичная перистальтическая волна, которая эти остатки удаляет.
Нижний пищеводный сфинктер плотно закрывается каждый раз после прохождения пищи, препятствуя рефлюксу желудочного содержимого в пищевод. В дальнейшем он может время от времени расслабляться для удаления из желудка избытка воздуха. В том случае когда количество этих эпизодов транзиторного расслабления превышает нормальное, развивается недостаточность сфинктера и появляются изжога, отрыжка, срыгивания.
Двигательная активность желудка начинается с момента прохождения комка пищи через нижний пищеводный сфинктер. Поступление пищевого комка в желудок сопровождается рецептивным расслаблением дна и проксимальной части тела желудка. Рецептивное расслабление возникает при проглатывании любого количества пищи. В дальнейшем в зависимости от объема съедаемой пищи и выпиваемой жидкости начинается адаптивное расслабление дна и тела желудка. Назначение адаптивного расслабления – сохранить примерно постоянное давление в просвете органа независимо от объема пищи. В дистальной части тела и антральном отделе появляются интенсивные перистальтические волны, которые перемешивают содержимое и приводят к его измельчению. Подобные интенсивные сокращения возникают каждые 20 с. После прохождения по антруму перистальтические сокращения появляются в двенадцатиперстной кишке.
Волны перистальтики в двенадцатиперстной кишке, слабые вначале, усиливаются при поступлении желудочного содержимого через пилорический сфинктер. Поступление происходит порциями, содержащими очень маленькие кусочки пищи. При этом именно эти порции активируют перистальтику двенадцатиперстной кишки. В ней поступающий химус смешивается с желчью, соком поджелудочной железы благодаря перистальтическим сокращениям. Эти перистальтические волны возникают координированно с деятельностью антропилорической зоны. Такая синхронизированная деятельность называется антродуоденальной координацией.
Нарушение каждого из компонентов двигательной активности желудка может приводить к появлению соответствующей клинической симптоматики. Так, нарушение рецептивного и адаптивного расслабления желудка вызывает чувство раннего насыщения, в ряде случаев тошноту и рвоту. Вследствие нарушения антродуоденальной координации появляются тяжесть в эпигастрии, вздутие живота, иногда изжога, отрыжка, срыгивания.
Двигательная активность толстой кишки изучена несколько хуже, чем моторика пищевода и желудка. Можно выделить пять видов сокращений стенки толстой кишки, которые возникают в разных отделах. Это сегментарные непропульсивные сокращения, пропульсивные неперистальтические и ретропульсивные сокращения, пропульсивные перистальтические и тонические сокращения. Транзит содержимого по толстой кишке осуществляется в основном благодаря двум разновидностям сокращений стенки и ее тонусу. Первая разновидность – быстрые непропульсивные сокращения в отдельных сегментах, которые уплотняют содержимое, создают условия для всасывания и, по сути, отвечают за формирование нормальных каловых масс. Вторая разновидность – высокоамплитудные перистальтические сокращения, которые перемещают содержимое по кишке. Каловые массы длительное время находятся в одном сегменте кишки, и лишь два раза в сутки возникают указанные перистальтические пропульсивные сокращения и происходит перемещение содержимого.
Моторика толстой кишки стимулируется холинергическим влиянием, которое, в свою очередь, модулируется миоэлектрической активностью. Нарушение каждого из пяти видов сокращений стенки толстой кишки может приводить к появлению как запоров, так и поносов.
Процесс продвижения пищи по ЖКТ зависит от сбалансированного физиологического контроля. Данный контроль осуществляется регулирующей системой, включающей в качестве составных частей нервную и гормональную регуляцию.
Мышечная оболочка стенки пищеварительного тракта состоит из наружного продольного и внутреннего циркулярного мышечных слоев. Между ними располагается межмышечное нервное сплетение. Снаружи органа к межмышечному нервному сплетению подходит экстрамуральная иннервация. Она представлена парасимпатической и симпатической частями. Согласованная, координированная деятельность парасимпатического и симпатического звеньев нервной регуляции создает условия для нормальной перистальтики. В парасимпатической системе контроль осуществляется через блуждающий нерв, который берет начало в продолговатом мозге. Волокна парасимпатической нервной системы приходят к ганглиям межмышечного нервного сплетения. Этот вид регуляции является центральным и имеет место, например, при акте глотания. В данном случае инициируются так называемая первичная перистальтика пищевода, а затем открытие нижнего пищеводного сфинктера, рецептивное и адаптивное расслабление желудка.
Известно, что на электрофизиологическом уровне сокращение гладкомышечной клетки характеризуется деполяризацией мембраны и возникновением спайкового потенциала. В это время в клетку устремляются ионы кальция, и она сокращается.
В адренергической системе контроль осуществляется через симпатические волокна, берущие начало в центрах спинного мозга. При этом симпатическая система уменьшает давление в нижнем пищеводном сфинктере, а также угнетает перистальтические движения тела желудка и его антрального отдела.
Важнейшим мессенджером в регуляции двигательной функции ЖКТ является допамин, который секретируется в отдельных участках стенки желудка, действует на специальные допаминовые рецепторы, расположенные здесь же, и оказывает ингибирующее, угнетающее действие на моторику.
В то же время двигательная активность может определяться самостоятельным функционированием межмышечного нервного сплетения, даже без участия вагусной регуляции. Не останавливаясь подробно на деятельности автономной нервной регуляции, следует указать на важный факт участия в торможении двигательной активности стенки пищеварительного тракта нейротрансмиттера – оксида азота. Учет данного обстоятельства имеет значение при рассмотрении вопроса о терапии моторных нарушений у пациентов, постоянно принимающих препараты – доноры оксида азота, прежде всего пролонгированные нитраты, а также антагонисты кальция группы нифедипина.
Координированное действие стимулирующих и ингибирующих факторов обеспечивает нормальную перистальтику пищевода, желудка и двенадцатиперстной кишки. Когда ингибирующие факторы начинают преобладать над стимулирующими вследствие любой причины, перистальтическая деятельность желудка и двенадцатиперстной кишки ослабевает вплоть до появления некоординированных сокращений и нарушения антродуоденальной координации. Пилорический сфинктер при этом перестает функционировать как своего рода дозатор порций пищи, поступающих в двенадцатиперстную кишку. Двигательная функция антрума, которая обеспечивает перемешивание и продвижение пищи, ослабевает, замедляя опорожнение желудка от содержимого. Давление в нижнем пищеводном сфинктере может уменьшаться, приводя к возникновению недостаточности кардии.
В результате этих двигательных нарушений развиваются соответствующие симптомы. Основные виды нарушений двигательной функции пищеварительного тракта включают в себя: синдром функциональной (неязвенной) диспепсии, гастроэзофагеальную рефлюксную болезнь, различные виды гастропареза (диабетический, идиопатический, постоперационный), синдром раздраженной кишки, различные виды запоров, синдром хронической кишечной псевдообструкции, постоперационную кишечную непроходимость и др.
Нарушения моторики пищевода, желудка и кишки могут быть разделены на нарушение двигательной функции стенки органа и его сфинктеров (схема 1).
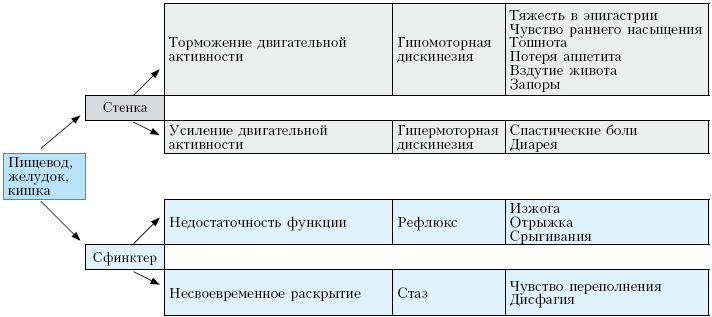
Схема 1. Нарушения двигательной функции стенки и сфинктеров пищевода, желудка и кишки
Торможение двигательной активности стенки приводит к гипомоторной дискинезии, которая в целом встречается чаще. Гипомоторная дискинезия обусловливает появление большинства симптомов: тяжесть в эпигастрии, чувство раннего насыщения, тошнота, потеря аппетита, вздутие живота, запоры. Усиление двигательной активности стенки органа вызывает развитие гипермоторной дискинезии, характеризующейся спастическими болями или, например, диареей.
Нарушение деятельности сфинктеров приводит либо к появлению ретроградного движения содержимого пищеварительного тракта, либо к замедлению антеградного. Из-за недостаточности нижнего пищеводного сфинктера возникает гастроэзофагеальный рефлюкс, появляются изжога, отрыжка, срыгивания. Замедление или несвоевременное раскрытие сфинктеров может приводить к появлению дисфагии, тяжести в эпигастрии.
Выявление того или иного вида нарушений двигательной функции пищеварительного тракта весьма актуально. До сих пор дифференциальная диагностика между гипо- и гипермоторными видами дискинезии проводится недостаточно полно, что ведет к неоправданно частому назначению спазмолитиков. Поэтому необходимо рассмотреть вопросы инструментальной диагностики моторных нарушений.
Рентгенологический метод позволяет визуализировать структуру стенки ЖКТ. В руках опытного рентгенолога этот метод выявляет стеноз или дилатацию любого участка пищеварительной трубки. По сей день в диагностике многих видов нарушений двигательной функции ЖКТ рентгенологический метод является основным.
Проведение рентгенологического исследования дает возможность обнаруживать желудочно-пищеводный рефлюкс (рис. 1, 2), дуоденостаз (рис. 3), а также нарушение опорожнения желудка и, таким образом, диагностировать, например, синдром функциональной диспепсии.
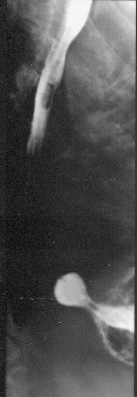 | Рис. 1. Рентгенологическая картина грыжи пищеводного отверстия диафрагмы |
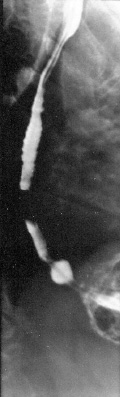 | Рис. 2. Рентгенологическая картина желудочно-пищеводного рефлюкса на фоне грыжи пищеводного отверстия диафрагмы |
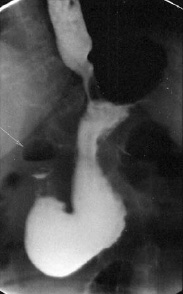 | Рис. 3. Рентгенологическая картина дуоденостаза |
Эндоскопическое исследование необходимо для обнаружения органической патологии, которая может лежать в основе нарушений моторики. Кроме того, при его проведении хорошо визуализируются проявления дуоденогастрального рефлюкса (рис. 4). 
Рис. 4. Эндоскопическая картина дуоденогастрального рефлюкса
Метод внутриполостной манометрии позволяет изучить показатели движения стенки пищеварительного трубки и деятельности сфинктеров. Можно определить амплитуду, продолжительность сокращения стенки органа, производные от этих показателей, понять, является сокращение перистальтическим, спастическим или редуцированным. В сфинктере можно измерить его длину, давление в просвете, степень падения давления при расслаблении.
С помощью сцинтиграфического исследования получают количественные данные относительно опорожнения желудка в физиологических условиях. При сцинтиграфии тонкой кишки оценивают суммарные показатели пассажа по ней и его нарушения. Эффективно применение метода для изучения моторики толстой кишки. Удается диагностировать синдром раздраженной кишки, выделить формы запоров (структурные, аноректальные, медленный транзит).
В ходе ультразвукового исследования имеется возможность определять двигательную функцию желчного пузыря, пищевода, желудка, двенадцатиперстной кишки. Изучать, в частности, движения желудка, наличие дуоденогастрального рефлюкса (рис. 5), антродуоденальную координацию. Важно то, что можно установить, как соотносятся движения стенки желудка и скорость его опорожнения.
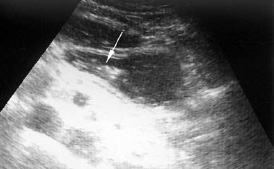 Рис. 5. Ультразвуковая картина рефлюкса дуоденального содержимого в антральный отдел желудка (указано стрелкой) |
Комбинация и применение по точным показаниям различных методов исследования моторики дает реальную возможность поставить точный диагноз и провести эффективное лечение. В последние годы достигнуты существенные успехи в понимании сложной регуляции двигательной функции пищеварительного тракта и, как следствие, увеличились возможности коррекции ее нарушений прокинетическими средствами.
Прокинетики – фармакологические препараты, которые на разных уровнях и с помощью разных механизмов меняют пропульсивную активность ЖКТ и ускоряют транзит субстрата (пищевого болюса) по нему. Тот или иной прокинетический препарат может иметь несколько точек приложения. Во-первых, действовать на тетродотоксинчувствительные места связывания, т. е. блокировать ионный перенос. Во-вторых, стимулировать образование молекул ацетилхолина в нервной терминали и тем самым увеличивать выброс ацетилхолина в синаптическое пространство. Препарат другого класса может ингибировать активность холинэстеразы и в результате увеличивать количество молекул ацетилхолина в синаптическом пространстве нервной терминали. Таким образом, возможны множественные модификации в зоне синаптического контакта, которые усиливают или ослабляют моторный ответ либо нервно-мышечное сопряжение, необходимое для последующего двигательного акта.
В зависимости от взаимодействия с тем или иным рецептором препараты могут оказывать возбуждающее или ингибирующее влияние. В конечном итоге то, что мы получаем в клинической практике в виде исчезновения болевого либо купирования диарейного синдрома или в виде нормализации стула у пациента с предшествующим запором выглядит как некая суммация фаз возбуждения и ингибирования.
Ниже представлены основные классы рецепторов, которые участвуют в регуляции моторно-эвакуаторной функции ЖКТ. Независимо от характера рецепторов, их множественности они имеют три основных опосредующих механизма (схема 2). Первый механизм – это ионные каналы. Взаимодействие прокинетика с тем или иным рецептором обеспечивает поток по этим каналам ионов, в частности ионов натрия и/или кальция, в гладкомышечные образования и повышение их активности. Второй механизм трансформации – клеточная аденилатциклаза. Взаимодействие агониста с соответствующими рецепторами, стимулирующими активность аденилатциклазы, приводит к накоплению в клетке цАМФ и в итоге к целому каскаду процессов фосфорилирования различных белков. В частности, так действуют β-адренергические, δ-опиоидные и мускариновые рецепторы. Третий опосредующий механизм – мембранная фосфолипаза С. Взаимодействие с этим рецептором ведет к накоплению в клетке инозитолтрифосфата (ИТФ). Этим путем действуют холецистокининовые рецепторы. Независимо от механизмов трансформации конечным звеном регуляции является изменение концентрации кальция в цитоплазме гладкомышечной клетки. Под влиянием этих трансформирующих механизмов повышается концентрация кальция и соответственно увеличивается сократительная активность гладких мышц, или, наоборот, концентрация кальция уменьшается и сократительная активность в известной степени редуцируется. 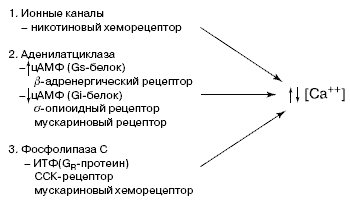
Схема 2. Рецептор-сопряженные системы амплификации сигнала
Основными классами рецепторов, участвующими в регуляции моторно-эвакуаторной функции ЖКТ, являются холинергические, адренергические, допаминергические, серотониновые, мотилиновые и холецистокининовые.
Таким образом, прокинетики осуществляют взаимодействие с теми или иными регуляторными блоками несколькими путями на уровне ганглиев или на уровне нервной терминали. При взаимодействии с клеточной мембраной они могут прямо влиять на рецепторы или на белки, которые, в свою очередь, оказывают воздействие на эти рецепторы. В конечном счете все заканчивается изменением уровня в клетке вторичных мессенджеров – цАМФ, Са, ИТФ. И именно это приводит к итоговому ответу.
Говоря о механизмах действия прокинетиков, необходимо остановиться на понятиях «down regulation» и «up regulation». Эти часто встречающиеся термины обозначают механизм регуляции количества рецепторов на мембране эффекторной, в частности гладкомышечной, клетки в зависимости от количества медиатора. В физиологическихусловиях обычное количество медиатора встречает соответствующее или необходимое количество молекул рецептора. При повышении количества медиатора число рецепторов уменьшается («down regulation»), а при снижении – увеличивается («up regulation»).
В современной клинике используются известные прокинетические препараты с различными механизмами действия (табл. 1). Бетанекол, аналог ацетилхолина, оказывает влияние путем прямого взаимодействия с мускариновыми рецепторами клетки. Аналогичный механизм действия у метоклопрамида. Антагонизмом допаминовым (D2) рецепторам клетки характеризуются метоклопрамид, L-сульпирид, домперидон и новый прокинетик итоприд, который, обладая двойным механизмом действия, также ингибирует ацетилхолинэстеразу. Метоклопрамид и цисаприд оказывают прямое стимулирующее влияние на освобождение ацетилхолина. Ингибирующими ацетилхолинэстеразу свойствами отличается и пиридостигмин.
Таблица 1
Применение в клинике стимуляторов моторной активности желудочно-кишечного тракта
| Механизм действия | Соединение |
|---|---|
| Прямое воздействие с мускариновыми рецепторами | Бетанекол Метоклопрамид |
| Антагонизм с допаминовыми (D2) рецепторами | Метоклопрамид L-сульпирид Домперидон Итоприд |
| Стимуляция высвобождения ацетилхолина | Метоклопрамид Цисаприд |
| Угнетение ацетилхолинэстеразы | Пиридостигмин Итоприд |
Разные прокинетики обеспечивают лигандрецепторное взаимодействие с разными рецепторами. Метоклопрамид обладает антагонизмом к D2-допаминовым рецепторам и агонизмом к 5НТ3-рецепторам, домперидон и итоприд – антагонизмом к D2-допаминовым рецепторам, цисаприд – антагонизмом к 5-НТ3-рецепторам и агонизмом к 5-НТ4-рецепторам, эритромицин – агонизмом к мотилиновым рецепторам, а локсиглумид – антагонизмом к холецистокининовым рецепторам.
Сравнивая профили активности различных прокинетиков (на животных моделях) следует отметить, что антиэметический эффект демонстрируют метоклопрамид, домперидон и итоприд, а активность в дистальной части кишки – цисаприд, эритромицин и итоприд (табл. 2). Активность в проксимальной части кишки присуща всем препаратам. Метоклопрамид проникает через гематоэнцефалический барьер, с чем связано развитие некоторых побочных явлений. При применении итоприда, эритромицина и домперидона неблагоприятное влияние наблюдается редко.
Таблица 2
Прокинетики: сравнительная оценка профилей активности
| Соединение | Переход через гематоэнцефалический барьер | Антиэметический эффект | Активность в проксимальной части кишки | Активность в дистальной части кишки | Неблагоприятные эффекты |
|---|---|---|---|---|---|
| Метоклопрамид | + | + | + | 0 | Много |
| Домперидон | 0 | + | + | 0 | Некоторые |
| Цисаприд | 0 | 0 | + | + | Серьезные |
| Эритромицин | 0 | 0 | + | + | Мало |
| Итоприд | 0 | + | + | +? | Мало |
Приведенные выше данные свидетельствуют о важной роли нарушений двигательной функции пищеварительного тракта в развитии многих распространенных гастроэнтерологических заболеваний, в первую очередь гастроэзофагеальной рефлюксной болезни, неязвенной диспепсии, синдрома раздраженного кишечника. Их целенаправленная диагностика предполагает использование современных методов исследования двигательной функции пищевода, желудка, кишечника.
Применение прокинетических препаратов нового поколения позволяет значительно улучшить результаты лечения таких больных.
Авторы выражают признательность проф. З.А. Лемешко, А.И. Саваровскому, М.Ю. Конькову за предоставленные иллюстрации.
Список литературы
