Тактика ведения больного метастатическим колоректальным раком с изолированными метастазами в печень
СтатьиОпубликовано в журнале:
современная онкология | репринт | 2009
А.А. Трякин
Отделение клинической фармакологии и химиотерапии РОНЦ им. Н.Н.Блохина РАМН, Москва
Вступление
Рак толстой кишки (РТК), включая рак прямой кишки, занимает 3-е место в структуре заболеваемости в России. Так, в 2005 г. в России было диагностировано 53 000 новых случаев РТК, в половине из которых потребовалась химиотерапия по поводу диссеминации заболевания. На протяжении последних двух десятков лет наблюдается значительный прорыв в терапии распространенного РТК. Он, прежде всего, связан с появлением новых лекарственных препаратов (иринотекана, оксалиплатина, бевацизумаба, цетуксимаба), а также с повышением частоты выполнения резекций печени и легких при их метастатическом поражении. Результатом этого явилось драматическое увеличение медианы продолжительности жизни больных с 6 мес до 24 мес.
Несмотря на большое число проведенных исследований, исчерпывающий ответ на ряд вопросов до сих пор не получен. Какой режим химиотерапии первой линии выбрать? Какова оптимальная продолжительность терапии? Есть ли необходимость поддерживающей терапии бевацизумабом и/или химиотерапией после достижения эффекта? Какова оптимальная тактика при операбельных метастазах в печень?
Клинический случай
Мужчина, 39 лет, на фоне полного здоровья 3 июля 2006 г. был экстренно госпитализирован в общехирургический стационар с клинической картиной острой кишечной непроходимости. При лапаротомии выявлена стенозирующая опухоль сигмовидной кишки без признаков диссеминации заболевания. Произведена резекция сигмовидной кишки с формированием колостомы. В послеоперационном периоде были выполнены рентгенография органов грудной клетки и ультразвуковое исследование (УЗИ) органов брюшной полости, не выявившие отдаленных метастазов. Патоморфологическое заключение: умеренно дифференцированная аденокарцинома, pT4N0M0 (исследовано 4 регионарных лимфатических узла). Пациенту было рекомендовано наблюдение.
Через 6 нед после операции пациент самостоятельно обратился в клинику РОНЦ им. Н.Н.Блохина РАМН. На момент обращения в клинику он полностью восстановился после операции, жалоб не предъявлял. Была выполнена компьютерная томография (КТ) органов грудной клетки, брюшной полости и малого таза, при которой были выявлены два метастаза в S6 печени диаметром 2,6 см и 1,3 см соответственно (рис. 1). Анализы крови - без патологии, значения опухолевых маркеров РЭА и СА-19.9 соответствуют норме. Произведена аспирационная биопсия большего очага в печени, подтвердившая метастаз аденокарциномы кишечного типа. Таким образом, у пациента имелись два резектабельных метастаза в правой доле печени. Было решено провести 6 курсов предоперационной химиотерапии по программе FOLFOX в сочетании с бевацизумабом, с последующим выполнением резекции правой доли печени и аналогичной адъювантной химиотерапией.
Рис. 1. КТ до начала лечения (август 2006 г.): два метастаза в S6 правой доли печени.
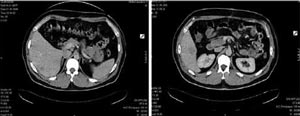
В августе-сентябре 2006 г. проведены 3 курса химиотерапии режимом FOLFOX-6 в сочетании с бевацизумабом 5 мг/кг каждые 2 нед без токсичности. Выполненная контрольная КТ показала полное исчезновение определявшихся ранее метастазов (рис. 2). Учитывая эффект терапии было решено провести еще 1 курс химиотерапии FOLFOX без бевацизумаба и далее выполнить резекцию области ранее определявшихся метастазов. Однако пациент неожиданно отказался от хирургического лечения. В данной ситуации была продолжена лекарственная терапия.
Рис. 2. КТ после 3 курсов FOLFOX в сочетании с бевацизумабом (октябрь 2006 г.): полная регрессия метастазов в печени.
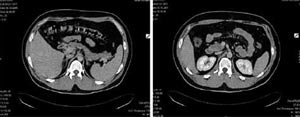
Суммарно проведено 9 курсов химиотерапии FOLFOX в сочетании с бевацизумабом. Лечение хорошо переносилось, явления токсичности не превышали I степень: холодовые реакции, тошнота, общая слабость. Не наблюдались и такие специфические для бевацизумаба токсические явления, как протеинурия и артериальная гипертензия.
Комплексное обследование после 9 курсов терапии подтвердило полный эффект. Было принято решение о продолжении монотерапии бевацизумабом, однако по финансовым причинам лечение не было продолжено: компания, оплачивавшая лечение пациента в рамках добровольного медицинского страхования, не могла продолжать дорогостоящую терапию. Учитывая желание пациента избавиться от колостомы, через 2 мес после завершения химиотерапии (март 2007 г.) была выполнена операция по восстановлению непрерывности кишечной трубки. Обследование, включавшее интраоперационное УЗИ печени, не выявило признаков заболевания. Пациент оставался под наблюдением в клинике РОНЦ им. Н.Н.Блохина РАМН.
По состоянию на последнее наблюдение (март 2009 г.) - 26 мес после завершения лекарственной терапии - у больного сохраняется полный эффект. По данным КТ, на месте ранее существовавшего большего метастаза в S6 печени стал определяться кальцинат (рис. 3). Другой неожиданной находкой стало обнаружение в просветах ветвей правой легочной артерии тромботических масс - рентгенологический признак тромбоэмболии легочной артерии (ТЭЛА). При этом на протяжении нескольких предшествовавших месяцев у пациента отсутствовала всякая специфическая для ТЭЛА симптоматика. При изучении свертывающей системы крови, включая уровень D-димера, все значения были в пределах нормы. Пациенту назначен эноксипарин (Клексан) 40 мг ежедневно на протяжении 6 мес.
Рис. 3. КТ через 26 мес после завершения терапии FOLFOX в сочетании с бевацизумабом (март 2009 г.): сохраняющаяся полная регрессия метастазов в печени. Появление кальцината на месте одного из них.
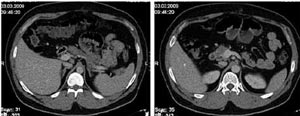
Обсуждение
Данное клиническое наблюдение не является, к сожалению, типичным как по исходной распространенности опухолевого процесса, так и по достигнутому эффекту. Изолированное метастатическое поражение печени при РТК имеет место у 50% пациентов с IV стадией заболевания, при этом лишь 20-30% из них исходно радикально резектабельны. Выполнение радикальной (R0) резекции позволяет увеличить 5-летнюю выживаемость до 30-40% по сравнению с <5% при одной лекарственной терапии.
Оптимальная последовательность химиотерапии и хирургии при операбельных метастазах в печень
Данный пациент исходно имел два небольших резектабельных метастаза в печень, локализующиеся в S6 печени. В таких ситуациях врач всегда встает перед дилеммой: начать лечение с операции, либо отложить ее, проведя предоперационную химиотерапию? В двух рандомизированных исследованиях с только резекцией печени сравнивалась послеоперационная химиотерапия (6 курсов режимом Мейо) [1] или периоперационная химиотерапия (по 6 курсов FOLFOX до и после операции) [2].
Преимущество в длительной безрецидивной выживаемости от добавления химиотерапии в обоих исследованиях оказалось сходным, и в абсолютных значениях составило +7 и +9% соответственно. Несмотря на отсутствие прямого сравнения этих подходов, все более популярным становится проведение периоперационной химиотерапии. Последняя позволяет тестировать in vivo чувствительность опухоли к химиотерапии, а также выявить рефрактерных к терапии больных, кому операция не показана.
Выбор режима предоперационной химиотерапии
Больным с изолированным метастатическим поражением печени необходимо назначение максимально эффективной химиотерапии, позволяющей достичь наибольшего объективного ответа. Эффективность режимов, включающих фторпиримидины с иринотеканом или оксалиплатином (FOLFIRI или FOLFOX), составляет около 30-50% [3, 4], что позволяет выполнить резекцию печени у 10-20% больных с изначально нерезектабельными метастазами в печень [5, 6].
Повысить частоту объективных ответов можно, применяя одновременно все три химиотерапевтических препарата. Благодаря этому эффективность тройной комбинации достигает 66-69%, а частота выполненных резекций печени - 26-36% [7, 8]. Повышенная токсичность таких режимов затрудняет их широкое применение.
Другим подходом является добавление к стандартной комбинации таргетного препарата -цетуксимаба или бевацизумаба. У пациентов с отсутствием мутации гена K-RAS цетуксимаб позволил существенно повысить частоту объективных ответов с ~ 40% (FOLFOX или FOLFIRI) до 60% [3, 4].
Крайне оптимистичными выглядят сообщения об эффективности бевацизумаба в режимах неоадъювантной химиотерапии; 80% объективных ответов и 10% полных патоморфологических регрессий [9].
У данного пациента мы начали химиотерапию по программе FOLFOX с бевацизумабом, опираясь на позитивные результаты исследований, показавших достоверное увеличение частоты объективных эффектов и безрецидивной выживаемости от добавления бевацизумаба к терапии фторпиримидинами или IFL.
Что делать при полной клинической регрессии метастазов в печень?
Прогресс в лекарственной терапии РТК привел к тому, что полные регрессии метастазов перестали быть казуистической редкостью. Они все чаще становятся причиной "головной боли" хирургов, затрудняя выполнение резекции печени при отсутствии там макроскопической опухоли. Поэтому в таких ситуациях нередко уже со стороны хирургов звучат сомнения в необходимости удаления уже несуществующего метастаза из печени.
Имеющиеся данные ясно свидетельствуют о низкой частоте совпадения полных клинических и патоморфологических эффектов, составляющей лишь 17% [10]. Таким образом, даже в случае полного исчезновения части или всех метастазов в печени необходимо стремиться к удалению места их прежней локализации.
Данному пациенту было предложено хирургическое вмешательство на печени, однако он отказался от его выполнения. Была продолжена химиотерапия.
Какова оптимальная продолжительность химиотерапии первой линии при РТК?
Если бы химиотерапия не обладала побочными эффектами, вряд ли вопрос - "А когда мы ее, наконец, закончим?" - поднимался бы так часто пациентами. В настоящее время нет точных данных, как долго она должна проводиться. Если задачей терапии является попытка излечения больного, то максимально активная терапия должна проводиться до достижения максимального эффекта или выраженной токсичности. При проведении паллиативной терапии большее значение приобретает качество жизни. В ряде случаев интермиттирующая химиотерапия позволяет отсрочить наступление кумулятивной дозолимитирующей токсичности по сравнению с непрерывным лечением. Так, возможно использование запланированных двухмесячных перерывов в терапии после двухмесячных блоков режимом FOLFIRI [11].
В то же время при терапии режимом FOLFOX полное прекращение лечения после 6 курсов и возобновление его лишь при прогрессировании достоверно ухудшает продолжительность жизни больных по сравнению с непрерывным лечением до прогрессирования или непереносимости [12]. Поэтому обычно первую линию терапии с оксалиплатином (FOLFOX или XELOX) строят следующим образом: в течение нескольких месяцев проводится лечение с оксалиплатином. При развитии полинейропатии II степени его введение прекращают, продолжая монотерапию фторпиримидинами до прогрессирования или значимой токсичности.
В нашем случае мы завершили терапию на 9 курсах FOLFOX, учитывая, что последние 6 курсов были проведены после достижения полной ремиссии, а также появившуюся (хоть и невыраженную) токсичность.
Какова роль поддерживающей терапии бевацизумабом?
Неопределенной остается и роль поддерживающей терапии бевацизумабом после завершения химиотерапии. Нужна ли она? Должна ли это быть монотерапия бевацизумабом или его комбинация с фторпиримидинами? Имеющиеся данные позволяют утверждать, что эффект бевацизумаба поддерживается лишь при его применении. В исследовании NO 16 966 больные рандомизировались в группы только химиотерапии (XELOX или FOLFOX) или химиотерапии с добавлением бевацизумаба. Абсолютный выигрыш в выживаемости до прогрессирования в экспериментальном режиме составил лишь 1,4 мес (с 8,0 до 9,4 мес). Однако большая часть пациентов в нарушении условий протокола досрочно закончила терапию не по причине прогрессирования заболевания. Проведенный промежуточный анализ показал, что пациенты из группы бевацизумаба, продолжавшие терапию, имеют более длительное время до прогрессирования (10,4 мес), чем пациенты, получавшие только химиотерапию (7,9 мес) [13]. Будущие проспективные исследования должны точнее выяснить роль поддерживающей терапии бевацизумабом.
Мы рекомендовали пациенту продолжить монотерапию бевацизумабом, однако, столкнувшись с реалиями действительности, вынуждены были оставить больного под наблюдением.
Заключение
Течение заболевания в данном клиническом случае поставило перед врачами ряд вопросов. Правильные ответы на некоторые из них трудно дать даже ретроспективно. Роль хирургии в лечении метастазов РТК в печень сложно переоценить. Пациенты данной потенциально курабельной группы должны получать максимально эффективную лекарственную терапию, включающую и биологические препараты. Имеющиеся данные свидетельствуют о необходимости длительного проведения лекарственного лечения, включая и поддерживающую терапию бевацизумабом.
Литература
1. Portier G, Elias D, Bouche O et al. Multicenter randomized trial of adjuvant fluorouracil and folinic acid compared with surgery alone after resection of colorectal liver metastases: FFCD ACHBTH AURC 9002 trial J Clin Oncol 2006; 24:4976-82.
2. Nordlinger B, Sorbye H, Collette L et al. Final results of the EORTC Intergroup randomized phase III study 40983 [EPOC] evaluating the benefit of peri-operative FOLFOX4 chemotherapy for patients with potentially resectable colorectal cancer liver metastases.J Clin Oncol2007; 25 (18 suppl.): 2s.
3. Bokemeyer C, Bondarenko I, Hartmann JT et al. KRAS status and efficacy offirst-line treatment of patients with metastatic colorectal cancer (mCRC) with FOLFOX with or without cetuximab: The OPUS experience. J Clin Oncol 2008; 26 (suppl): abstr 4000.
4. Van Cutsem E, Lang I, Dhaens G et al. KRAS status and efficacy in the first-line treatment of patients with metastatic colorectal cancer (mCRC) treated with FOLFIRI with or without cetuximab: The CRYSTAL experience.]Clin Oncol2008; 26 (suppl.): abstr 2.
5. Bismuth H, Adam R, L?vi F et al. Resection of non-resectable liver metastases from colorectal cancer after neoadjuvant chemotherapy. Ann Surg 1996; 224: 509-20.
6. Adam R, Delvart V, Pascal G et al. Rescue surgery for unresectable colorectal liver metastases down-staged by chemotherapy: A model to predict long-term survival. Ann Surg2004; 240: 644-57.
7. Falcone A, Ricci S, Brunetti I et al. Phase III Trial of Infusional Fluorouracil, Leucovorin, Oxaliplatin, and Irinotecan (FOLFOXXIRI) Compared With Infusional Fluorouracil, Leucovorin, and Irinotecan (FOLFIRI) As First-Line Treatment for Metastatic Colorectal Cancer: The Gruppo Oncologico Nord Ovest. J. Clin Oncol2007; 25 (13): 1670-6.
8. Abad A, Anton A, Massuti B et al. Resectability of liver metastases (LM) in patients with advanced colorectal cancer (ACRC) after treatment with the combination of oxaliplatin (OXA), irinotecan (IRI) and 5FU. Final results of a phase II study. J Clin Oncol 2005 ASCO Annual Meeting Proceedings2005; 23 (16S): abstr. 3618.
9. Bouganim N, Kavan P, Eid M et al. Perioperative chemotherapy with bevacizumab (BV) for liver metastases (LM) in colorectal cancer (CRC): McGill University pilot study. J Clin Oncol 2009; 27 (suppl): abstr e1 5027.
10. Benoist S, Brouquet A, Penna C et al. Complete response of colorectal liver metastases after chemotherapy: Does it mean cure? J Clin Oncol 2006; 24: 3939-4511. Labianca R, Floriani I, Cortesi E et al. Italian Group for the Study of Digestive Tract Can. Alternating versus continuous "FOLFIRI" in advanced colorectal cancer (ACC): A randomized "GISCAD" trial J Clin Oncol 2006; 24 (18 suppl): 3505.
12. Maindrault-GoebelF, Lledo G, Chibaudel B et al. Final results of OPTIMOX2, a large randomized phase II study of maintenance therapy or chemotherapy-free intervals (CFI) after FOLFOX in patients with metastatic colorectal cancer (mCRC): A GERCOR study. J Clin Oncol2007; 25 (18 suppl): 4013.
13. SaltzL, Clarke S, Diaz-Rubio E et al. Bevacizumab (Bev) in combination with XELOX or FOLFOX4: Updated efficacy results from XELOX-1/NO16966, a randomized phase III trial in first-line metastatic colorectal cancer.Journal of Clinical Oncology, 2007 ASCO Annual Meeting Proceedings Part I. 2007; 25 (18S; Suppl): 4028.
