Применение метапрота в лечении хронической гипоксии плода при гестозе
Статьи Клиническая фармакология метапрота, нового противоастенического препарата с психоактивирующими свойствамиХроническая гипоксия плода занимает важнейшее место среди разнообразных состояний риска для плода и новорожденного. В структуре перинатальной смертности в 40-70% случаев она является причиной мертворождений и смерти детей в раннем неонатальном периоде. Перинатальная гипоксия в 31-88% случаев становится причиной повреждения центральной нервной системы, столь чувствительной к кислородной недостаточности. Как следствие перенесенной гипоксии у новорожденных нарушается соматическое и нервно-психическое развитие, затрудняющее в последствии их социальную адаптацию. В возникновении и развитии гипоксии плода роль отводится гестозу, частота которого составляет до 20% по отношению к числу родов (Redman С, Roberts J., 1993).
В основе гестоза лежат метаболические нарушения, характеризующиеся накоплением недоокисленных продуктов обмена веществ в условиях ацидоза и избыточной липопероксидации, а также повреждение диффузионных и перфузионных процессов в маточно-плацентарно-плодовом комплексе (Шанин Ю. Н. и др., 2003). Одним из пусковых механизмов развития гестоза является инвазия трофобласта в спиральные артерии, которые остаются нерасширенными и не имеют типичных гестционных изменений. Трофобласт, будучи в состоянии гипоперфузии, оказывает выраженное влияние на весь плацентарный комплекс. Предполагается, что высвобождение свободных радикалов трофобластом в условиях недостаточности АТФ индуцирует процессы ПОЛ в плодово-плацентарных сосудах, а активация эндотелиоцитов матери элементами трофобласта, в свою очередь, запускает процессы избыточной липопероксидации в маточно-плацентарном, а затем и в системном кровотоке матери. Важную роль в развитии гестоза играет патология эндотелия сосудов, приводящая к сужению их просвета. Характерными морфологическими изменениями являются гломерулярный эндотелиоз, несвойственный другой патологии, а также ультраструктурные изменения в плацентарном ложе и пограничных сосудах матки.
Резюмируя, следует подчеркнуть, что ведущая роль в патофизиологических механизмах развития этой патологии все же принадлежит антиоксидантной недостаточности и избыточной интенсификации процессов липопероксидации. Выраженность клинических проявлений зависит от соотношения между интенсивностью и длительностью воздействия патогенных факторов риска и состоятельностью системы антиоксидантной защиты, определяющей адаптивные возможности беременной и плода.
Многосторонний и, главным образом, неспецифический характер этих нарушений позволил нам в совместной работе с Г.Б. Рябининым с лечебной целью использовать в составе комплексной терапии метапрот и оценить его действие на состояние плода, новорожденного, клиническое течение родов и послеродового периода. Исследование выполнено на базе клиники акушерства и гинекологии Военно-медицинской академии МО РФ и родильного дома № 9 г. Санкт-Петербурга. В исследование было включено 157 беременных женщин и их плодов. Пациентки были разделены на группы: 1 -я — 50 женщин, без признаков внутриутробного страдания плода составили контрольную группу; 2-я — 60 женщин с осложненной гестозом беременностью, получавшие общепринятую комплексную терапию составили группу сравнения; 3-я — 47 беременных женщин с гипоксией плода получали в дополнение к комплексной терапии метапрот. Метапрот назначался курсом продолжительностью 5 дней перорально в суточной дозе 10 мг/кг массы тела, в 3 приема. Средний возраст пациенток составил 24,7±2,1 года. По анамнестическим данным группы беременных были сопоставимы по социальному статусу, семейному положению, материально-бытовым условиям.
Следует отметить, что гипоксия плода чаще всего осложняла течение беременности у первородящих женщин. В группах женщин с гестозом наблюдались такие осложнения, как ранний токсикоз, анемия беременных, угроза прерывания беременности. Течение гестоза сопровождалось усилением процессов липопероксидации и снижением активности антиоксидантных систем, что регистрировалось по изменению соответствующих показателей в крови и ткани плаценты беременных. Включение метапрота в комплекс лечебных мероприятий нормализовывало антиоксидантный статус организма. В крови беременных женщин по сравнению с исходным состоянием (до лечения) снижалось в 2,2 раза содержание малонового диальдегида и в 1,7 раза содержание диеновых конъюгатов (рис. 9).
На фоне действия метапрота возрастала активность каталазы в 2 раза и супероксиддисмутазы в 1,4 раза, увеличивалось содержание восстановленного глутатиона в 1,3 раза (рис. 10). Показатели в группе пациентов, получавших метапрот, также выгодно отличались от соответствующих значений в группе женщин, получавших традиционную терапию. Так, содержание МДА было ниже в 2 раза, диеновых конъюгатов в 1,4 раза, восстановленного глутатиона возрастала в 1,2 раза, активность каталазы увеличивалась в 1,9 раза, а каталазы — в 1,8 раза.
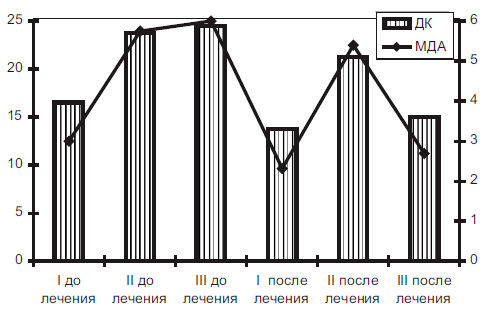 Рисунок 9. Влияние метапрота на содержание продуктов переписного окисления липидов в крови беременных ЦК- диеновые коньюгаты (мкмоль/л); МДА - малоновый диальдегид (мкмоль/л). | 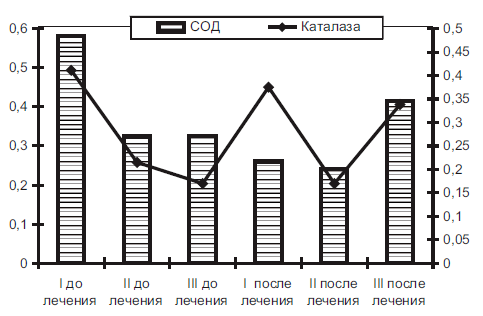 Рисунок 10. Влияние метапрота на активность анти-оксидантной системы в крови беременных СОД - супероксиддисмутаза (А/мг белка) |
В ткани плаценты беременных с гестозом на фоне приема метапрота также снижалось содержание продуктов перекисного окисления липидов и увеличивалась активность антиоксидантных ферментов и содержание восстановленного глутатиона. Наряду с антиоксидантными эффектами метапрот нормализовал уровень лактата и пирувата в крови и плаценте пациенток, что препятствовала развитию лактацидоза и способствовало стабилизации углеводного обмена.
Состояние плода оценивали с помощью фетального мониторинга по изменениям показателей его сердечной деятельности в условиях нестрессового теста. Включение метапрота в схему лечения гестоза уже через сутки приводило к улучшению состояния плода по сравнению с общепринятой терапией, что регистрировалось по бальной системе шкалы Е. R. Lyons и соавторов (1979).
Состояние новорожденных на 1-й и 5-й минуте жизни оценивали по шкале V. Apgar (1953). В плазме крови, полученной из сосудов пуповины сразу после рождения ребенка, определяли показатели ПОЛ и антиоксидантной системы, содержание лактата и пирувата. Об адаптационных возможностях новорожденных судили по динамике неврологического и соматического статуса в неонатальном периоде, длительности пребывания детей в стационаре. Гестационный возраст новорожденных во всех группах находился в пределах от 37 до 42 недель. В группе рожениц, получавших традиционную терапию, 25% детей имели оценку 6 и менее баллов и нуждались в проведении реанимационных мероприятий. В группе женщин, получавших метапрот в дополнение к традиционной терапии, таких новорожденных было в 2,9 раз меньше. На 5-й минуте жизни 10% новорожденных, перенесших гипоксию, имели оценку по шкале V.Apgar 6 и менее баллов, что является плохим прогностическим признаком (табл. 27)
Таблица 27. Характеристика групп новорожденных
| Группы, показатели | 1-я (контроль, n = 50) | 2-я (с гипоксией плода, n = 60) | 3-я (с гипоксией, получавшие метапрот, n = 47) |
|---|---|---|---|
| Масса тела, г | 3418±137 | 3209±183 | 3250±179 |
| Оценка по V. Apgar На 1-й мин На 5-й мин | 7,95±0,24 8,93±0,20 | 6,66±0,32 7,89±0,29 | 7,62±0,26* 8,74±0,29* |
| Частота неврологических нарушений, % | 8,0 | 43,3 | 27,7* |
| Примечание. * — р В группе женщин, получавших метапрот, таких детей не было, а средняя оценка по шкале V. Apgar на 1-й и 5-й минуте жизни детей была достоверно выше, чем в других группах. У этих новорожденных в 1,6 раза реже наблюдались поражения центральной нервной системы, да и те носили более легкий характер. Таким образом, улучшение состояния новорожденных на фоне приема матерями метапрота приводило к сокращению сроков их пребывания в клинике. Включение метапрота в комплексную терапию матерей с гестозом и гипоксией плода приводило к нормализации оксидативного статуса новорожденных. При общепринятом лечении гипоксии плода у новорожденных наблюдались метаболические нарушения. По сравнению с контрольной группой в крови новорожденных увеличивалось в 1,6 раза содержание диеновых конъюгатов, в 1,9 раза содержание МДА. У этих детей отмечалось снижение в 2,3 раза активности супероксиддисмутазы и в 1,4 раза каталазы, в 1,2 раза содержания восстановленного глутатиона, возрастало в 2,3 раза величина отношения лактата к пирувату. В результате приема метапрота содержание продуктов перекисного окисления липидов уменьшалось по сравнению с группой пациенток, получавших общепринятую терапию. Так, содержание МДА снизилось в 1,7 раза, а диеновых конъюгатов в 1,8 раз. На фоне метапрота в крови новорожденных увеличивалось в 1,3 раза содержание восстановленного глутатиона и в 1,6 раз активности супероксиддисмутазы (рис. 11).
Наряду с этим в 1,8 раз снижалось содержание лактата и величина отношения лактата к пирувату в 1,7 раз. Применение метапрота привело к улучшению функционального состояния плода и новорожденного, уменьшению в 1,6 раза частоты и тяжести перинатальных энцефалопатии, к уменьшению в 2,2 раза частоты оперативного родоразрешения и некоторых осложнений родового акта. Это свидетельствует о патогенетической обоснованности включения метапрота в комплекс терапии хронической гипоксии плода при гестозе. Таким образом, включение беременным женщинам в комплексную терапию хронической гипоксии плода при гестозе метапрота приводит к нормализации патологических изменений в системах ПОЛ/антиоксидантная система, сохранению показателей углеводного обмена на уровне, характерном для здоровых женщин. Применение метапрота улучшает функциональное состояние плода и новорожденного, снижает частоту и тяжесть перинатальных энцефалопатии. Наряду с этим снижается частота оперативного родоразрешения и слабости родовой деятельности, кровотечений в родах и раннем послеродовом периоде. При хронической гипоксии плода, обусловленной гестозом, беременным в комплекс лечебных мероприятий целесообразно включать метапрот, назначая его курсом 5 дней в суточной дозе 10 мг/кг массы тела, разделенной на 3 приема. Клиническая фармакология метапрота, нового противоастенического препарата с психоактивирующими свойствами | |||
Комментарии
ПРАКТИКА ПЕДИАТРА