Новейшие основанные на мелатонине методы терапии: потенциальные преимущества в терапии большой депрессии
СтатьиNovel melatonin-based therapies: potential advances in the treatment of major depression
Ian B Hickie, Naomi L Rogers. Lancet 2011; in press
Published Online May 18, 2011 DOI: 10.10l6/S0140-6736(11)60095-0 Brain & Mind Research Institute, The University of Sydney, Camperdown, NSW, Australia (Prof IB Hickie MD, NL Rogers PhD); and School of Management and Marketing, Institute for Health and Social Science Research, Central Queensland University, Mackay, QLD, Australia (NL Rogers) Адрес для корреспонденции: Prof Ian B Hickie, Brain & Mind, Research Institute, 94 Mallett Street, Building F, Level 4, Camperdown, NSW 2050, Australia. ian.hickie@sydney.edu.au
Большая депрессия относится к ведущим причинам преждевременной смертности и инвалидизации. Несмотря на определенную эффективность современные препараты имеют существенные недостатки. Последние достижения в изучении фундаментальных связей между хронобиологией и аффективными расстройствами, а также в разработке новых препаратов, нацеленных на циркадианную систему, изменили приоритеты в этой области. В этой обзорной статье мы обобщили данные о связи между хронобиологическими нарушениями и большой депрессией и осветили новые стратегии терапии антидепрессантами, нацеленные на циркадианную систему. Прежде всего мы представили агомелатин, агонист рецепторов мелатонина и селективный антагонист серотонинергических рецепторов 5-HT2C, который обладает хронобиотическим, антидепрессивным и анксиолитическим эффектами. В кратковременных исследованиях агомелатин был сопоставим по антидепрессивной эффективности с венлафаксином, флуоксетином и сертралином, а при длительной терапии снижал частоту рецидивов (23,9%) в сравнении с плацебо (50,0%). Пациенты с депрессией, получавшие терапию агомелатином, сообщали об улучшении качества сна и облегчении засыпания. Поскольку агомелатин не повышает уровни серотонина, он не вызывает типичных для многих других антидепрессантов побочных эффектов - гастроинтестинальных, половых и метаболических.
Введение
Большая депрессия является главной причиной преждевременной смертности и инвалидизации.[1,2] Несмотря на спорность терапевтических преимуществ антидепрессантов при легких депрессиях,[3,4] в целом клиническая польза препаратов и психотерапии для пациентов с депрессией не вызывает сомнений. Положительные эффекты лечения включают снижение частоты самоубийств, повышение работоспособности, редукцию вторичного злоупотребления алкоголем и другими психоактивными веществами, снижение риска сердечнососудистой патологии и, благодаря более регулярному и широкому использованию адекватных медицинских служб, дестигматизацию депрессии и тревоги.[5,6]
Длительная терапия антидепрессантами часто является ключевым компонентом лечения пациентов с тяжелой депрессией, что стимулирует разработку препаратов с улучшенными профилями безопасности. Хотя новейшие антидепрессанты имеют клинически значимые различия в эффективности в эффективности и переносимости, в разработке большинства препаратов основным направлением было воздействие на одни и те же моноаминовые мишени (например, серотонин, норадреналин, или дофамин). В последнее время значительно пополнились наши знания о биологии циркадианной системы, клиническом значении нарушений суточных ритмов, неблагоприятном влиянии многих антидепрессантов на циркадианные циклы и архитектуру сна, а также механизмах, за счет которых литий оказывает глубокое влияние на циркадианную биологию. В свете разработки аналога мелатонина с подтвержденным антидепрессивным эффектом, агомелатина, эти достижения привели к смещению приоритетов на потенциальную клиническую пользу манипуляций циркадианной системой [8-10].
Циркадианная система и цикл сон-бодрствование
Циркадианная система является центральным звеном в поддержании суточного цикла сон-бодрствование и общего благополучия. Эта система координирует ключевые физиологические функции, включая цикл сон-бодрствование, терморегуляцию, эндокринную, имунную, сердечнососудистую и метаболическую системы [11] (рисунок 1). Хотя циркадианные ритмы нарушаются при многих нейропсихических расстройствах (например, психотические расстройства, постинфекционные заболевания, состояния хронической слабости и хроническая боль), их нарушения приобретаю фундаментальный характер при большой депрессии, атипичной депрессии и сезонном аффективном расстройстве.[10] Значительные флуктуации также тесно связаны с разными фазами биполярного аффективного расстройства.[15]
Циркадианные нарушения при депрессии
Установлены тесные связи между циркадианными нарушениями и некоторыми наиболее типичными симптомами клинической депрессии, включая задержку начала сна, беспокойный сон, ранние утренние пробуждения, слабость в дневное время, уплощение или реверс утренних пиков субъективного настроения, энергии и бдительности.[10] Профили циркадианных нарушений варьируют в широких пределах: у некоторых пациентов наблюдается смещение фазы на более раннее время (проявляется ранним засыпанием, ранним пробуждением и смещением на более раннее время ритмов секреции мелатонина, кортизола и норадреналина; рисунок 1B), тогда как у других выявляется задержка фазы (позднее засыпание, отставленное утреннее пробуждение; рисунок 1C).
Стратегии поиска и критерии отбора
Данная статья не является систематическим обзором. Мы выполнили поиск статей в системе PubMed используя следующие ключевые слова: "мелатонин", "аналоги мелатонина", "агомелатин", "рамелтеон", "тазимелтеон", "PD-6735", "депрессия", "антидепрессанты", "циркадианные нарушения", "циркадианные ритмы", "хронотерапия", "хронобиотики" и "сон". Мы анализировали только англоязычные статьи и резюме. Сроки выхода публикаций ограничивались периодом с 1948 г. по февраль 2011 г. Поиск по ключевому слову "агомелатин" дополнялся информацией, доступной на веб-сайте US National Institutes of Health Clinical Исследования.gov (Национальный институт клинических исследований здоровья США), веб-сайте International Standard Randomised Controlled Trial Number Register (Номерной регистр международных стандартных контролируемых исследований) и веб-сайте European Medicines Agency (Европейское медицинское агентство). Данный поиск также дополнялся информацией от производителя агомелатина (Servier Laboratories) и предполагал дополнительные источники от рецензентов данной статьи.
Рисунок 1: Циркадианная ритмичность у субъектов с нормальным ритмом (A), смещением фазы на более раннее время (B), задержкой фазы (C) или внутренней десинхронизацей (D).
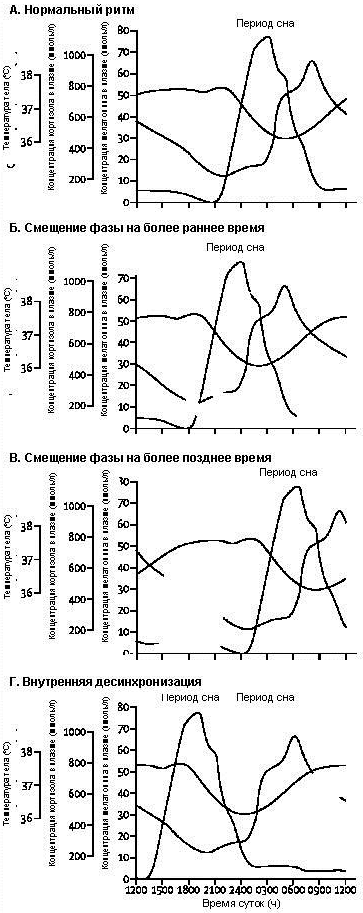
Периоды сна отмечены серым фоном с указанием времени суток по оси абсцисс. (A) Нормальный ритм: начало секреции мелатонина примерно за 2 часа до начала сна и непосредственно перед ночным снижением температуры тела. Плазменные концентрации кортизола достигают надира вечером и пика утром, вскоре после окончания сна. (B) Смещение фазы на более раннее время: временные соотношения между циркадианные ритмами температуры тела, плазменными концентрациями мелатонина и кортизола и сроками сна сохраняются; однако все они смещаются на более ранние часы относительно нормального ритма. (C) Задержка фазы: временные соотношения между циркадианные ритмами температуры тела, плазменными концентрациями мелатонина и кортизола и сроками сна сохраняются; однако все они смещаются на более поздние часы относительно нормального ритма. (D) Внутренняя десинхронизация: временные соотношения между циркадианные ритмами температуры тела, плазменными концентрациями мелатонина и кортизола и сроками сна смещаются относительно друг друга и не совпадают по фазе. По данным Rogers и соавт.[12-14]
Также отмечается снижение амплитуды суточных колебаний других ключевых параметров, включая температуру тела и плазменные концентрации кортизола.[10,11,15-19]
В условиях внутренней внутренняя десинхронизация (рисунок 1D) несколько циркадианных ритмов (например, температура тела, плазменные концентрации мелатонина и кортизола, сон-бодрствование) утрачивают соответствие по фазе как друг с другом, так и с окружающей средой.[11] На наш взгляд такое нарушение внутренних связей между ключевыми физиологическими циклами сна, настроения, когнитивных функций и др. приводит к формированию полифазных профилей сна, чрезмерной сонливости или слабости в состоянии бодрствования, депрессивному настроению и нарушениям нейрокогнитивных функций.
У большинства пациентов с депрессией отмечается увеличение латентности сна и высокая частота пробуждений в течение ночи. Соответственно развивается выраженная гиперсомния, слабость в дневное время или дремота.[20] Кроме того, у пациентов с депрессией выявляются полисомнографические изменения архитектуры сна, включая сокращение времени медленноволнового сна, редукцию периодов парадоксального (REM) сна, сокращение латентности первого эпизода REM сна и увеличение количества 1 и 2 стадий сна.[21] Если не-REM сон (стадия 1, стадия 2 и медленноволновый сон) регулируется преимущественно гомеостатической системой, то REM сон регулируется циркадианной системой. [22] Целью терапии антидепрессантами является не только восстановление нормального профиля цикла сон-бодрствование, но также ресинхронизация циркадианно зависимой биологии и ее связей с внешней средой.
Нарушение циркадианной функции как причина нейропсихических расстройств
Накапливается все больше доказательств того, что нарушения циркадианной функции могут быть главным фактором риска нейропсихических расстройств. В этом контексте нарушения циркадианных ритмов (независимо от клинического диагноза) реализуются в фенотипе, который характеризуется депрессивным настроением, слабостью в дневное время, снижение концентрации, скелетно-мышечными болями и аномальными суточными колебаниями в субъективных оценках уровня энергии.[23] Первичные циркадианные расстройства и первичные аффективные расстройства имеют общие генетические факторы риска (таблица 1) и одинаковые детерминанты окружающей среды. Значимые внешние факторы включают длительное нарушение режима сна, злоупотребление алкоголем и другими психоактивными веществами, путешествия с пересечением меридианов или сменная работа, другие общемедицинские заболевания (например, острая инфекция). Поведенческие или фармакологические методы терапии, направленные на нормализацию циркадианной функции, способствуют не только значительному улучшению настроения, но и существенному улучшению когнитивных функций и редукции слабости в дневное время.[28,29]
Циркадианные недостатки современных средств терапии большой депрессии
На протяжении более 50 лет мишенью терапии большой депрессии были моноаминергические системы. Многие трициклические антидепрессанты прошлого поколения оказывают благоприятное влияние на засыпание и длительность сна (преимущественно через гистаминергические механизмы), но при этом подавляют REM сон. Более того, способность подавлять REM сон раньше рассматривалась как облигатное свойство антидепрессантов.[30] Наиболее широко используемые в современной практике селективные ингибиторы обратного захвата серотонина часто нарушают медленноволновый сон и циклы REM сна (как минимум при кратковременной терапии) и не всегда восстанавливают нормальную циркадианную функцию.[31] Эти побочные эффекты новых антидепрессантов часто приводят к необходимости сопутствующей терапии седативными средствами. Для современной терапии тяжелой депрессии типично присоединение антипсихотиков второго поколения с выраженными седативными или нормотимическими свойствами (например, оланзапин или кветиапин). Снотворные средства, которые просто сокращают время засыпания или число ночных пробуждений, не лечат депрессию. Сходным образом, чистые седативные препараты лишь в ограниченной степени способны корректировать хронобиологические нарушения, а их длительное применение сопряжено с риском развития толерантности и зависимости. [32] Нормализация хронобиологии все чаще рассматривается как маркер эффективности терапии антидепрессантами. Неудача в попытках нормализации ритмов сопряжена с повышением риска резидуальных симптомов или ранних рецидивов.[33] Циркадианная направленность терапии антидепрессантами
Циркадианная направленность терапии депрессии предусматривает не только восстановление нормальных суточных колебаний в пределах цикла сон-бодрствование, но также восстановление и ресинхронизацию других ключевых нейрогормональных (например, колебания плазменных концентраций мелатонина и кортизола), физиологических (например, температура тела) и нейрокогнитивных (например, бдительность) функций. Предпосылкой такого подхода служит перенастройка циркадианной системы под влиянием стимулов внешней среды. Разработано несколько стратегий достижения этой цели, включая адекватный распорядок воздействия ярким белым18 или голубым [34] светом, терапия мелатонином [35] и перестройка распорядка сна и бодрствования. В одном из исследований установлен положительный эффект комбинации психофармакотерапии и циркадианных методов терапии (например, депривация сна, воздействие ярким светом и смещение фазы сна на более раннее время) в редукции депрессивных симптомов у пациентов с биполярным расстройством.[36] У пациентов, которым в результате рандомизации была назначена дополнительная циркадианная терапия (n=32), отмечался достоверно более выраженный антидепрессивный эффект через 48 часов после начала лечения (размер эффекта 0,56, p=0.03), который стойко сохранялся до 7-й недели терапии (0,51, p=0.02), в сравнении с пациентами, которые получали только фармакотерапию (n=17).
Недавно было разработано несколько аналогов мелатонина, которые, как и ожидалось, продемонстрировали хронобиотические эффекты. [37] Некоторые из препаратов, которые традиционно используются в терапии аффективных расстройств, также влияют на ключевые компоненты регуляции циркадианной системы. Стабилизатор настроения литий вызывает задержку фазы [38] и может увеличивать циркадианный период.[38,39] Недавно было показано, что хронобиотические эффекты лития могут быть связаны с воздействием на гликоген синтаза киназу 3ß,[40] которая является центральным регулятором эндогенных циркадианных часов.[41]
Поведенческие манипуляции циркадианной системой.
Несколько методов поведенческой терапии предусматривают манипуляции циркадианной системой и связанными с ней системами цикла сон-бодрствование. Главной мишенью обычно становится фаза сна, тогда как меньше внимания уделяется повышению активности в дневное время (особенно в утренние часы) или редукции дремоты в дневное время. Тотальная или парциальная депривация во второй половине ночи оказывают кратковременный антидепрессивный эффект.[42] Антидепрессивный эффект депривации сна исчезает после эпизодов сна, а повторные сеансы депривации сна приводят к накоплению дефицита сна.[43] Такой эффект негативно влияет на состояние бодрствования в дневное время, нейрокогнитивные функции и безопасность (например, управление автомобилем или механизмами).[43]
Хроническое ограничение сна (7-14 дней) с сокращением времени в постели до 6 часов за ночь приводит к прогрессирующему снижению нейрокогнитивной продуктивности.[44,45] Негативные эффекты ограничения сна на нейрокогнитивные функции компенсируются после восстановления нормальной длительности сна. В других исследованиях установлены сходные эффекты менее длительного ограничения сна[43] наряду с изменениями многих физиологических функций, включая секрецию мелатонина[12] и метаболические параметры.[46]
Хотя терапия ярким светом может редуцировать депрессивные симптомы, этот метод применяется преимущественно у пациентов с сезонным аффективным расстройством (также известным как зимняя депрессия).[42] Предполагается, что эффективность воздействия ярким светом связана с резким подавлением мелатонина в дневное время, которое в отдаленном периоде приводит к смещению фазы и восстановлению адекватной синхронизации с окружающей средой. Однако несмотря на то, что большинство исследований терапии ярким светом выполнено у пациентов с сезонным аффективным расстройством, в ряде кратковременных исследований с малыми выборками показана эффективность терапии ярким светом при не сезонной депрессии.[47-49] По данным мета-анализа Cochrane [48] терапия ярким светом, как отдельно, так и в комбинации с антидепрессантами или депривацией сна, оказывает некоторые умеренные эффекты. недавно установлено, что циркадианная система наиболее чувствительна к спектру голубого света (460 нм) [34], что предполагает возможность применения менее интенсивного света для эквивалентного смещения фазы.
Мелатонин
Мелатонин обладает высоким аффинитетом к двум типам рецепторов (MT1 и MT2), которые расположены в головном мозге, включая супрахиазматическое ядро гипоталамуса, черную субстанцию (substantia nigra), гиппокамп, мозжечок, вентральную тегментальную область (ventral tegmental area) и прилежащее ядро (nucleus accumbens).[35,50] Эти области головного мозга участвуют в регуляции различных гомеостатических систем, включая цикл сон-бодрствование и терморегуляцию. Роль этих G-протеин-связывающихся рецепторов окончательно не установлена, а пропорция их экспрессии может иметь значение для эффектов мелатонина.[51] Изменения в количестве и пропорции MT1 и MT2 рецепторов в головном мозге выявляются при нейродегенеративных расстройствах (например, при болезни Альцгеймера),[52] сходные изменения также зафиксированы после длительной терапии антидепрессантами.[50,51] Выделен третий участок связывания мелатонина(MT3), [53] однако аффинитет мелатонина к этим рецепторам намного ниже, а их роль менее ясна.
Мелатонин вырабатывается и секретируется в эпифизе. У здоровых субъектов без хронобиологических нарушений и без депрессии секреция мелатонина наиболее интенсивна в ночное время, тогда как днем выявляются лишь незначительные концентрации мелатонина в крови.[35] Мелатонин играет важную роль в системе циркадианной ритмичности связываясь с рецепторами в супрахиазматическом ядре и другими клетками и системами в разных областях организма.[54,55] Связывание мелатонина с рецепторами супрахиазматического ядра оказывает два эффекта: подавление нейрональной активности в супрахиазматическом ядре и настройка или смещение фазы циркадианных ритмов.[35] Кроме того ночное повышение плазменных концентраций мелатонина связано с увеличением потребности заснуть, снижением температуры тела и снижением уровня бдительности.[35,50]
Экзогенный мелатонин в терапии
Сегодня мелатонин широко используется в США как пищевая добавка. Разные лекарственные формы мелатонина продаются по всему миру, включая формы немедленного и замедленного высвобождения. Прием мелатонина в адекватное время суток оказывает хронобиотическое действие и может способствовать смещению фазы циркадианной системы (при монотерапии или, что происходит чаще, в комбинации с воздействием светом).[35] наряду с хронобиотическими эффектами мелатонин также повышает потребность заснуть, сокращает латентность сна, снижает уровень бдительности и нейрокогнитивные функции, уменьшает температуру тела. Такие эффекты желательны в ночное время, но могут рассматриваться как побочные эффекты, если мелатонин применяется в дневное время.[35]
Является ли мелатонин антидепрессантом?
Экзогенный мелатонин оказывает некоторые подобные антидепрессивным эффекты на моделях у животных.[56] Ежедневное введение мелатонина компенсирует неблагоприятные эффекты хронического стресса у мышей.[57] С другой стороны монотерапия мелатонином у человека по всей видимости не является эффективной стратегией лечения депрессии.[58] Хотя мелатонин может корректировать распорядок цикла сон-бодрствование и увеличивать длительность сна у пациентов с большим депрессивным расстройством, он не оказывает более специфичных антидепрессивных эффектов.[59] Однако добавление хронобиотических препаратов, таких как мелатонин, к современным антидепрессантам может повысить эффективность терапии.[33,51]
Хотя некоторые антидепрессанты улучшают некоторые показатели сна, включая эффективность сна и увеличение количества REM сна, другие (например, трициклические антидепрессанты и селективные ингибиторы обратного захвата серотонина) оказывают негативное влияние на архитектуру сна, сокращают длительность REM сна и увеличивают латентность REM сна.[60] Поскольку REM сон регулируется циркадианной системой, увеличение его латентности скорее свидетельствует об изменениях в циркадианной системе, нежели в гомеостатической системе сна. Нарушения других параметров, связанных с циркадианной системоы, включая мелатонин, температуру тела и кортизол, также типичны для пациентов с депрессией, поэтому терапия антидепрессантами должна быть нацелена и на эти аспекты депрессивного расстройства. Подобных эффектов следует ожидать от препаратов, связывающихся с мелатонинергическими рецепторами.
Аналоги мелатонина
Наряду с большинством представленных на рынке лекарственных форм мелатонина разработка специфичных аналогов мелатонина означает, что мы получаем доступ к веществам, которые систематически изучаются в контексте фармакологических и поведенческих свойств. Хотя все аналоги мелатонина исследовались на предмет промотирующих сон эффектов, они различаются по химической структуре и степени аффинитета к MT1 и MT2 рецепторам. Кроме того создан еще один препарат - агомелатин - также связывается с 5-HT2B и 5-HT2C рецепторами и более интенсивно исследуется как антидепрессант. В таблице 2 перечислены свойства аналогов мелатонина. Rajaratnam и соавторы [37] представили подробный анализ результатов исследований этих веществ на животных.
Циркадин
Мелатонин в форме Циркадина действует так же, как эндогенный мелатонин на MT1 и MT2 рецепторы. Циркадин сокращает время засыпания, улучшает качество сна и уровень бодрствования в утреннее время у лиц старше 55 лет, страдающих инсомнией.[61,67]
Рамелтеон
Рамелтеон обладает высоким аффинитетом к MT1 и MT2 рецепторам и слабым аффинитетом к MT3 участкам связывания.[68] В исследованиях транзиторной и хронической инсомнии с участием пациентов взрослого и пожилого возраста, рамелтеон оказывал умеренный эффект на латентность сна и общее время сна.[64,69-73] В этих исследованиях пациенты распределялись в зависимости от времени отправления ко сну; соответственно увеличение общего времени сна под действием рамелтеона было связано с уменьшением времени засыпания. Рамелтеон одобрен в US Food и Drug Administration (FDA) для терапии инсомнии, особенно в случаях задержки начала сна.
Тазимелтеон
Этот препарат обладает высоким аффинитетом к MT1 и MT2 рецепторам и вызывает сопоставимое с действием мелатонина смещение фазы на моделях у животных. У человека получены доказательства улучшения латентности начала сна и непрерывности сна при попытке более ранней, чем в норме, фазы сна (в первые часы после полудня).[65] Кроме того отмечается значительное смещение фазы после терапии тазимелтеоном с дозозависимым смещением на более раннее время фазы начала секреции мелатонина с наступлением сумерек в условиях 5-часового смещения на более раннее время фазы цикла свет-темнота.[65]
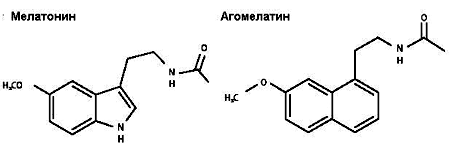
Рисунок 2. Структура мелатонина (N-ацетил-5-метокситриптамин) и агомелатина (N-[2-(7-метокси-1 -нафтил)этил] ацетамид).
PD-6735
Это вещество действует как селективный агонист MT1 и MT2 рецепторов и обладает выраженными хронобиотическими и снотворными свойствами. У пациентов с хронической первичной инсомнией отмечалась редукция латентности сна в рамках исследования ранжированных доз препарата.66 После 9-часового смещения на более раннее время фазы цикла свет-темнота PD-6735 ускорял перенастройку ряда циркадианных ритмов, включая колебания температуры тела и плазменных концентраций кортизола, калия, натрия и ионов хлора.[66]
Агомелатин
Агомелатин является уникальным препаратом, поскольку действует как селективный агонист MT1 и MT2 рецепторов и антагонист 5-HT2B и 5-HT2C рецепторов.[62] На рисунке 2 представлены химические структуры агомелатина и мелатонин. Агомелатин быстро всасывается: время до максимальной концентрации в крови составляет 45-90 мин после однократной пероральной дозы 25-50 мг.[75] После приема внутрь агомелатин подвергается интенсивному первичному печеночному метаболизму, который соучаствует в значительной вариабельности межиндивидуальной биодоступности.[76] Дополнительные факторы, влияющие на биодоступность, включают пол, прием пероральных контрацептивов и курение.[75] В циркулирующей крови агомелатин в большей части связывается протеинами плазмы (>90%) и почти полностью метаболизируется (до 80% дозы выводится с мочой в форме метаболитов). Средний период полужизни составляет 140 минут. Агомелатин повышает концентрации дофамина и норадреналина в префронтальной коре вследствие антагонизма к 5-HT2C рецепторам.[62]
Наряду с ожидаемыми на основании механизма действия хронобиотическими эффектами агомелатин также является клинически значимым антидепрессантом [77,78] и обладает анксиолитическими свойствами [79]. Предполагается, что эти психотропные эффекты обусловлены синергизмом между мелатонинергическими (MT1, MT2 рецепторы) и моноаминергическими (5-HT2C рецепторы) эффектами. Антидепрессивный эффект агомелатина также может быть связан с другими не циркадианными механизмами, такими как стимуляция выработки нейротрофического фактора головного мозга.[80]
Назначение агомелатина молодым мужчинам за 5 часов до сна приводит к смещению на более раннее время циркадианной фазы ритмов температуры тела и мелатонина, а также более раннему снижению частотоы сердечных сокращений. [63] Также отмечается смещение на раннее время окончания периода сна и REM сна в отсутствие других изменений в показателях сна. Выраженные эффекты смещения фазы также зафиксированы в другом исследовании с участием здоровых пожилых мужчин - смещение на более раннее время ритмов температуры тела и кортизола под действием агомелатина, вновь без влияния на параметры сна.[82]
Подобные антидепрессивным эффекты агомелатина подтверждены в исследованиях на животных.[83] У человека выполнена экстенсивная программа рандомизированных контролируемых исследований.[84-86] Стандартные терапевтические дозы агомелатина в этих исследованиях составили 25-50 мг. В качестве препаратов сравнения использовались известные антидепрессанты, включая флуоксетин, пароксетин, сертралин и венлафаксин (таблица 3 и таблица 4). В трех опубликованных плацебо-контролируемых исследованиях, выполненных для регистрации препарата,[87-89] абсолютное различие в долях респондеров (пациенты с минимум 50% редукцией стартового суммарного балла 17-пунктовой Шкалы депрессии Гамильтона балл) между агомелатином и плацебо составило 14,8% (95% CI 1,5-27,4),[89] 15,2% (3,3-26,4),[87] и 19,0% (6,5-31,5).[88]
Однако, доступные сегодня данные еще большего числа исследований агомелатина отражают более общую проблему оценки новых антидепрессантов — недостаточное отличие от плацебо.[3,4] Как и другие антидепрессанты агомелатин более эффективен у пациентов с более тяжелой депрессией.[84,95] Является ли агомелатин более эффективным у пациентов со специфичными аномальными изменениями циркадианной функции или более тяжелых нарушениях сна, еще предстоит выяснить.
В исследованиях с активными препаратами сравнения агомелатин (25-50 мг) был сопоставим по эффективности с венлафаксином (75-150 мг; форма замедленного высвобождения 150 мг)[93,94] и превосходил по эффективности флуоксетин (20-10 мг)95 и сертралин (50-100 мг).[92] Достоверно более выраженное улучшение показателей сна, включая повышение качества сна (среднее различие 5,63, 95% CI 0,85-10,41, p=0-021), редукцию ночных пробуждений (4,86, 0,23-9,49, p=0-040) и инсомнии (0,37, 0,01-0,72, p=0-044) отмечалось при терапии агомелатином в сравнении с венлафаксином.[93]
В длительном исследовании профилактики рецидивов депрессии[98,99] частота рецидивов на 24 неделе при терапии агомелатином составила 20,6% в сравнении с 41,4% для плацебо (разница в 20,8% [95% CI 11-0-30-0]), а через 10 месяцев исследования - 23,9% для агомелатина против 50,0% для плацебо (разница в частоте рецидивов 26,4% [95% CI 12-7-39-0]). В двух других исследованиях профилактики рецидивов не обнаружено превосходства агомелатина над плацебо (таблица 4). Наконец, в отличие от пароксетина, агомелатин не вызывает симптомы отмены.[97] Поскольку агомелатин не повышает уровни серотонина, он не вызывает побочных эффектов, типичных для других новых антидепрессантов (прежде всего, гастроинтестинальные расстройства, головные боли, половые дисфункции, психомоторная ажитация, прибавка в весе), а также серьезных нежелательных явлений (таких как серотониновый синдром или серотониновые симптомы отмены).[101-104] Тошнота, головокружение и головная боль были наиболее частыми нежелательными явлениями у пациентов, получавших терапию агомелатином, однако частота этих побочных эффектов была такой же, как у пациентов, получавших плацебо (таблица 5).[105]
Профиль побочных эффектов агомелатина не отличается от профиля плацебо по показателям многих типичных для антидепрессантов нежелательных явлений, включая прибавку в весе, половые дисфункции и эффекты отмены (таблица 5).[101]
Заключение
Аналоги мелатонина обладают новым и эффективным механизмом, обеспечивающим смещение фазы у человека. Хотя эти препараты исследовались преимущественно при расстройствах сна, они имеют потенциал для применения в качестве главных или дополнительных средств терапии широкого круга нейропсихических расстройств, сопровождающихся стойкими циркадианными нарушениями. Важно, что только агомелатин (который также связывается с 5-HT2C рецепторами) оказывает клинически значимый антидепрессивный эффект. Благодаря благоприятному профилю побочных эффектов и безопасности и способности восстанавливать нормальную циркадианную функцию между депрессивными эпизодами, этот препарат может занять уникальное место в терапии некоторых пациентов с тяжелой депрессией и другими развернутыми аффективными расстройствами.
Участники
Оба автора принимали участие в разработке концепции и написании данной статьи, в рассмотрении и одобрении ее финальной версии.
Конфликты интересов
IBH выполнял ранее обязанности главного исполнительного дирекора и клинического консультанта в Австралийской национальной нициативе по депрессии (Australian National Depression Initiative). Он возглавлял проекты для медицинских специалистов и населения при поддержке государства, коммерческих агентств и фармакологических компаний (Wyeth, Eli Lily, Servier, Pfizer, AstraZeneca), направленные на выявление и терапию депрессии и тревоги. Он участвовал в экспертных советах фармакологических компаний по отдельным антидепрессантам, включая нефазодин, дулоксетин и дезвенлафаксин, а также принимал участие в мультицентровом клиническом исследовании эффектов агомелатина на архитектуру сна при депрессии. IBH также получал помощь от National Health and Medical Research Council Australian Medical Research Fellowship. Он является участником аудита семейной практики по нарушениям сна и большой депрессии при поддержке Servier, производителя агомелатина. NLR получала гранты от Vanda Pharmaceuticals, Servier, Pfizer и Cephalon, а также гонорары за лекции от Pfizer, CSL Biotherapies и Servier. Ранее она также получала научную финансовую поддержку от Vanda Pharmaceuticals, производителя тазимелтеона. Она также получает неограниченный образовательный грант от Servier. научные исследования, выполненные IBH и NLR, спонсировались преимущественно из NHMRC проектов и программных грантов.
Выражение благодарности
Мы благодарим Bradley Whitwell, Tracey Davenport и Georgina Luscombe за их помощь в редактировании и оформлении диаграмм.
Таблица 1. Генетический перекрест между циркадианной системой и аффективными расстройствами.
| Эффект | Другие замечания | |
| GSK3B | Биполярное расстройство | Мишень для лития; центральный регулятор циркадианных часов |
| CLOCK | Биполярное расстройство | T3111C SNP: CC генотип связан с более выраженной инсомнией у пациентов, получающих терапию антидепрессантами, а также более выраженной инсомнией и снижением потребности в сне у пациентов с биполярным расстройством |
| ARNTL (также известен как BMAL1 или MOP3) | Биполярное расстройство | Данные исследований с анализом SNP и гаплотипа |
| PER3 | Биполярное расстройство, сезонное аффективное расстройство | Данные по биполярному расстройству из исследований с анализом гаплотипа |
| TIMELESS (также известен как TIM1) | Биполярное расстройство | Данные из исследований с анализом SNP |
| PER2, NPAS2, ARNTL | Сезонное аффективное расстройство | Комбинация этих генов приводит к дополнительным эффектам и дополнительно повышает риск развития сезонного аффективного расстройства |
Таблица 2. Эффекты мелатонина и аналогов мелатонина
| Торговые названия | Одобрение | Связывание* | Эффекты на сон | Хронобиотические эффекты | Антидепрессивные эффекты | |
| Гормон | ||||||
| Мелатонин [37] | MT1, MT2, MT3 | Промотирует засыпание, особенно в течение биологического дня (т.е. при низких концентрациях эндогенного мелатонина) | Смещение фазы на более раннее время и задержка фазы; настройка циркадианной системы | Синергические эффекты при добавлении к антидепрессантам и при монотерапии у животных | ||
| Мелатонин (Neurim Pharmaceuticals)[61] | Циркадин | EMA 2007 | MT1, MT2, MT3 | Имитирует профиль эндогенного мелатонина, постепенно высвобождая мелатонин в течение 8-10 часов | Смещение фазы на более раннее время | Нет данных |
| Аналоги | ||||||
| Агомелатин (Servier)[62,63] | Вальдоксан, Мелитор, Тиманакс | EMA 2009 | MT1, MT2, 5-HT2B (антагонист), 5-HT2C (антагонист) | Значимый терапевтический эффект у пациентов с депрессией | Смещение фазы на более раннее время; настраивает циркадианную систему | Да: большое депрессивные расстройство у взрослых |
| Рамелтеон (Takeda Pharmaceutical Company)[64] | Розерем | FDA 2005 | MT1, MT2 | Снижение латентности сна, повышение общего времени сна у пациентов с инсомнией, редукция медленноволнового сна | Смещение фазы на более раннее время | Нет данных |
| Тазимелтеон (VEC-126; Vanda Pharmaceuticals)[65] | FDA клинические исследования 3 фазы завершены в 2010 г.; | MT1, MT2 | Промотирует засыпание и сон maintenance (tested during 5-h смещение на более раннее | Смещение на более раннее время фазы и задержка фазы | Нет данных | |
| orphan drug designation 2010 | время фазы) и concurrent shift in эндогенный циркадианные ритмы | |||||
| TIK-301 (PD-6735, LY-156, 735; Tikvah Pharmaceuticals)[66] | FDA phase 2 clinical trial since 2002; статус орфанного препарата (лекарство-сирота) в 2004 г. | MT1, MT2 | Снижение латентность сна у пациентов с инсомнией | Промотирует смещение фазы на более раннее время | Нет данных | |
Таблица 3. Результаты плацебо-контролируемых и сравнительных с активными препаратами исследований агомелатина у человека.
| n* | Балл HAM-D (стартовый) | Балл HAM-D (финальный) | Разница† | Балл CGI-S/I (стартовый) | Балл CGI-S/I (финальный) | Разница† | |
| CL2-014 [87] | |||||||
| Агомелатин 1 мг в сутки | 136 | 27,9 (3,0) | 13,2 (8,2) | 2,17 (NS) | 4,8 (0,7) | 2,9 (1,5) | 0,41 (NS) |
| Агомелатин 5 мг в сутки | 146 | 27,3 (2,6) | 14,7 (8,5) | 0,64 (NS) | 4,9 (0,7) | 3,1 (1,5) | 0,19 (NS) |
| Агомелатин 25 мг в сутки | 135 | 27,4 (2,7) | 12,8 (8,2) | 2,57 (p=0,034) | 4,7 (0,7) | 2,8 (1,4) | 0,42 (NS) |
| Пароксетин 20 мг в сутки | 144 | 27,3 (3,4) | 13,1 (8,4) | 2,25 (p=0,030) | 4,9 (0,7) | 2,8 (1,5) | 0,51 (p<0,05) |
| Плацебо | 136 | 27,4 (3,1) | 15,3 (8,9) | 5,0 (0,7) | 3,3 (1,5) | ||
| CL3-022§ [75] | |||||||
| Агомелатин 25 мг в сутки | 129 | 27,6 (2,9) | 14,5 (8,2) | 1,17 (p=0,193)‡ | 5,0 (0,5) | 3,3 (1,4) | 0,19 (NS) |
| Флуоксетин 20 мг в сутки | 133 | 27,5 (2,8) | 13,3 (7,6) | 2,55 (p=0,005)‡ | 5,0 (0,6) | 3,1 (1,4) | 0,38 (p<0,05) |
| Плацебо | 147 | 28,0 (3,6) | 15,9 (8,6) | 5,0 (0,6) | 3,5 (1,5) | ||
| CL3-023§ [75] | |||||||
| Агомелатин 25 мг в сутки | 141 | 25,7 (2,8) | 13,0 (8,0) | 0,63 (p=0,504) | 4,6 (0,7) | 2,9 (1,3) | 0,17 (NS) |
| Пароксетин 20 мг в сутки | 137 | 26,1 (2,9) | 12,2 (8,1) | 1,58 (p=0,095) | 4,6 (0,7) | 2,7 (1,3) | 0,37 (p<0,05) |
| Плацебо | 137 | 26,0 (2,7) | 13,8 (8,0) | 4,5 (0,6) | 3,1 (1,3) | ||
| CL3-024§ [75] | |||||||
| Агомелатин 25 мг в сутки | 148 | 26,4 (3,0) | 12,0 (8,2) | 0,90 (p=0,291) | 4,7 (0,7) | 2,9 (1,4) | 0,17 (NS) |
| Агомелатин 50 мг в сутки | 147 | 26,5 (3,4) | 13,4 (8,2) | 0,41 (p=0,629) | 4,8 (0,7) | 3,0 (1,4) | 0,02 (NS) |
| Флуоксетин 20 мг в сутки | 146 | 26,5 (3,4) | 12,5 (7,4) | 0,53 (p=0,538) | 4,7 (0,7) | 2,9 (1,3) | 0,11(NS) |
| Плацебо | 158 | 26,9 (3,4) | 13,4 (8,4) | 4,7 (0,7) | 3,0 (1,4) | ||
| CL3-026 (пожилые пациенты >60 лет)§ [75] | |||||||
| Агомелатин 25 мг в сутки | 109 | >24 (MADRS) | 10,6 (9,4) (MADRS) | 0,19 (p=0,89) | NR | NR | NR |
| Плацебо | 109 | >24 (MADRS) | 9,6 (8,7) (MADRS) | NR | NR | ||
| CL3-042 [88] | |||||||
| Агомелатин 25-50 мг в сутки | 116 | 27,4 (2,7) | 13,9 (7,7) | 3,18 (p=0,002) | 4,9 (0,7) | 3,1 (1,4) | 0,5 (p=0,006) |
| Плацебо | 119 | 27,2 (2,7) | 17,0 (7,9) | 4,9 (0,7) | 3,6 (1,4) | ||
| CL3-043 [89] | |||||||
| Агомелатин 25-50 мг в сутки | 106 | 26,5 (2,8) | 14,1 (7,7) | 2,3 (p=0,026)‡ | 4,8 (0,7) | 3,2 (1,3) | 0,44 (p=0,017)‡ |
| Плацебо | 105 | 26,7 (3,0) | 16,5 (7,4) | 4,8 (0,7) | 3,6 (1,3) | ||
| CAGO178A2302 (NCT00411242) [90] | |||||||
| Агомелатин 25 мг в сутки | 158 | 26,8 (SE 0,3) | 15,0 (SE 0,6) | 2,2 (p=0,010)‡ | Данные представлены только в диаграмме | NR (p=0,010)‡ | |
| Агомелатин 50 мг в сутки | 161 | 26,8 (SE 0,3) | 15,9 (SE 0,7) | 1,2 (p=0,144)‡ | Данные представлены только в диаграмме | NR (p=0,115)‡ | |
| Плацебо | 163 | 26,4 (SE 0,2) | 17,1 (SE 0,6) | ||||
| CAGO178A2301 (NCT00411099) [91] | |||||||
| Агомелатин 25 мг в сутки | 156 | 26,7 (SE 0,3) | 15,9 (SE 0,6) | 0,6 (p=0,505)‡ | NR | NR | NR (p=0,144) |
| Агомелатин 50 мг в сутки | 161 | 27,1 (SE 0,3) | 14,1 (SE 0,6) | 2,5 (p=0,004)‡ | NR | NR | NR (p=0,003) |
| Плацебо | 167 | 27,1 (SE 0,3) | 16,6 (SE 0,7) | NR | NR | ||
| CAGO178A2303 (NCT00463242)§ [75] | |||||||
| Агомелатин 25-50 мг в сутки | 162 | 27,2 (SE 0,3) | 17,1 (SE 0,6) | 0,5 (p=0,539)‡ | NR | NR | NR |
| Пароксетин 20-40 мг в сутки | 163 | 27,0 (SE 0,3) | 14,0 (SE 0,6) | 3,4 (p<0,001)‡ | NR | NR | NR |
| Плацебо | 158 | 26,9 (SE 0,3) | 17,3 (SE 0,6) | NR | NR | ||
Таблица 4. Результаты сравнительных исследований агомелатина с активными препаратами и исследований агомелатина в профилактике рецидивов у человека
| n* | Балл HAM-D (стартовый) | Балл HAM-D (финальный) | Разница† | Балл CGI-S/I (стартовый) | Балл CGI-S/I (финальный) | Разница† | |
| Исследования с активными препаратами сравнения
CL3-046 (ISRCTN49376288)[92] |
|||||||
| Агомелатин 25-50 мг в сутки | 150 | 26,1 (2,8) | 10,3 (7,0) | 1,68 (p=0,031) | 4,7 (0,7) | 2,5 (1,1) | 0,28 (p=0,043) |
| Сертралин 50-100 мг в сутки | 157 | 26,5 (3,0) | 12,1 (8,3) | 4,7 (0,7) | 2,8 (1,3) | ||
| CL3-035 [93] | |||||||
| Агомелатин 25-50 мг в сутки | 165 | 25,9 (3,2) | 9,9 (6,6) | 1,1 (p=0,154) | 3,2 (0,8) | 1,6 (0,7) | 0,32 (p=0,016) |
| Венлафаксин 75-150 мг в сутки | 167 | 26,0 (3,3) | 11,0 (7,4) | 3,6 (0,9) | 1,6 (0,8) | ||
| CL3-036 [94] | |||||||
| Агомелатин 50 мг в сутки | 137 | 27,9 (4,1) (MADRS) | 10,1 (7,8) (MADRS) | 0,3 (p=0,751) | 4,4 (NR) | NR | NR |
| Венлафаксин (замедленного высвобождения) 150 мг в сутки | 139 | 27,9 (4,6) (MADRS) | 9,8 (7,9) (MADRS) | 4,5 (NR) | NR | ||
| CL3-045 (ISRCTN19313268) [95] | |||||||
| Агомелатин 25-50 мг в сутки | 247 | 28,5 (2,7) | 11,1 (7,3) | 1,49 (p=0,024)‡ | 5,0 (0,6) | 2,6 (1,3) | 0,22 (p=0,059)‡ |
| Флуоксетин 20-40 мг в сутки | 257 | 28,7 (2,5) | 12,7 (8,5) | 5,0 (0,6) | 2,8 (1,4) | ||
| CL3-056 [96] | |||||||
| Агомелатин 25-50 мг в сутки | 71 | 26,1 (2,3) | NR | 1,46 (p=0,002) | 4,7 (0,6) | NR | NR |
| Эсциталопрам 10-20 мг в сутки | 67 | 26,0 (2,9) | NR | 4,7 (0,7) | NR | ||
| CL3-030 [97] | |||||||
| Агомелатин 25 мг в сутки | 88 | 22,6 (2,4) (MADRS) | 6,1 (3,5) (MADRS) | 0,9 (p=0,064) | 4,1 (0,8) | 1,6 (0,8) | 0,0 (p=1,000) |
| Пароксетин 20 мг в сутки | 104 | 22,9 (2,2) (MADRS) | 5,2 (3,2) (MADRS) | 4,2 (0,8) | 1,6 (0,7) | ||
| Исследования профилактики рецидивов или повторных эпизодов
CL3-041 (ISRCTN53193024) 24 недели [98] |
|||||||
| Агомелатин 25-50 мг в сутки | 165 | 6,1 (2,6) | 7,5 (7,0) | 3,13 (p<0,001) | 1,8 (0,8) | 2,1 (1,2) | 0,5 (p=0,009) |
| Плацебо | 174 | 6,0 (2,7) | 10,6 (8,4) | 1,8 (0,7) | 2,6 (1,5) | ||
| 44 недели [99] | |||||||
| Агомелатин 25-50 мг в сутки | 165 | 6,1 (2,6) | 7,8 (7,4) | 3,69 (p<0,001) | 1,8 (0,8) | 2,1 (1,3) | 0,6 (p=0,002) |
| Плацебо | 174 | 6,0 (2,7) | 11,5 (8,6) | 1,8 (0,7) | 2,7 (1,5) | ||
| CL3-021§ [75] | |||||||
| Агомелатин 25 мг в сутки | 185 | 6,0 (2,7) | 9,3 (7,4) | 0,32 (NS) | 1,8 (0,8) | 2,3 (1,5) | 0,0 (NS) |
| Плацебо | 179 | 6,2 (2,7) | 9,6 (7,5) | 1,8 (0,8) | 2,3 (1,5) | ||
| CAGO178A2304 (NCT00467402; профилактика повторных эпизодов)? [00] | |||||||
| Агомелатин 25 мг в сутки | 64 | 4,6 (3,6) | NR | OR = 0,90 (p=0,667) | NR | NR | X2(p=0,572) |
| Агомелатин 50 мг в сутки | 76 | 6,1 (3,4) | NR | NR | NR | ||
| Плацебо | 141 | 6,0 (3,3) | NR | ||||
Таблица 5. Побочные эффекты, связанные с агомелатином, в плацебо-контролируемых и сравнительных с активными препаратами исследованиях
| Доля пациентов с побочными эффектами (агомелатин)* | Доля пациентов с побочными эффектами (препарат сравнения)* | Побочные эффекты, связанные с агомелатином† | Побочные эффекты, достоверно чаще возникавшие при терапии агомелатином, чем препаратом сравнения | |
| Плацебо-контролируемые исследования | ||||
| Агомелатин 25 мг в сутки [87] | 51,1% (70 из 137) | 54,7% (76 из 139) | Головная боль (6,6%) | Нет |
| Агомелатин 25-50 мг в сутки [88] | 42,4% (50 из 118) | 42,5% (51 из 120) | Головная боль (5,1%), слабость (5,1%) | Нет |
| Агомелатин 25-50 мг в сутки [89] | 57,5% (61 из 106) | 62,9% (66 из 105) | Головокружение (9,3%), назофарингит (6,5%), грипп (6,5%) | Нет |
| Агомелатин 25-50 мг в сутки [90] | 70,3% (232 из 330) | 65,5% (108 из 165) | Головная боль (13,3%), сонливость (9,1%), головокружение (7,3%), диарея (7,3%), тошнота (6,1%), слабость (5,8%), седация (5,2%), назофарингит (5,2%) | Нет |
| Агомелатин 25-50 мг в сутки [91] | 75,1% (244 из 325) | 74,6% (126 из 169) | Головная боль (16,3%), тошнота (12,0%), диарея (10,5%), головокружение (8,6%), сухость во рту (7,1%), сонливость (7,1%), седация (6,8%), слабость (5,2%), инсомния (5,2%) | Тошнота (p=0,05) |
| Исследования с активными препаратами сравнения | ||||
| Агомелатин 25-50 мг в сутки vs сертралин 50-100 мг в сутки [92] | 48,0% (73 из 152) | 49,1% (78 из 159) | Головная боль (8,6%), сухость во рту (5,3%) | Нет |
| Агомелатин 25-50 мг в сутки vs венлафаксин 75-150 мг в сутки [93] | 51,2% (85 из 166) | 57,1% (96 из 168) | Головная боль (9,6%), тошнота (6,0%) | Нет |
| Агомелатин 50 мг в сутки vs венлафаксин (замедленного высвобождения) 150 мг в сутки [94] | 20,4% (28 из 137)* | 38,1% (53 из 139)* | Тошнота (11,7%), головная боль (10,2%), инфекция верхних дыхательных путей (7,3%) | Нет |
| Агомелатин 25-50 мг в сутки vs флуоксетин 20-40 мг в сутки [95] | 57,2% (143 из 250) | 56,3% (148 из 263) | Головная боль (16,0%), тошнота (8,0%), сонливость (6,0%) | Нет |
| Профилактика рецидивов | ||||
| Агомелатин 25-50 мг в сутки vs плацебо (24 недель) [98] | 51,5% (85 из 165) | 52,3% (91 из 174) | Головная боль (7,9%),назофарингит (6,7%), боль в спине (5,5%) | Нет |
| Агомелатин 25-50 мг в сутки vs плацебо (44 недель) [99] | 59,4% (98 из 165) | 56,9% (99 из 174) | Головная боль (9,7%), назофарингит (9,1%), боль в спине (6,7%) | Нет |
Список использованной литературы
- Murray CJ, Lopez AD. Alternative projections of mortality and disability by cause 1990-2020: Global Burden of Disease Study. Lancet 1997; 349: 1498-504.
- Lopez AD, Mathers CD, Ezzati M, Jamison DT, Murray CJ. Global and regional burden of disease and risk factors, 2001: systematic analysis of population health data. Lancet 2006; 367: 1747-57
- Kirsch I, Deacon BJ, Huedo-Medina TB, Scoboria A, Moore TJ, Johnson BT. Initial severity and antidepressant benefits: a meta-analysis of data submitted to the Food and Drug Administration. PLoS Med 2008; 5: e45.
- Turner EH, Matthews AM, Linardatos E, Tell RA, Rosenthal R. Selective publication of antidepressant trials and its influence on apparent efficacy. N Eng J Med 2008; 358: 252-60.
- Hickie I. Is depression overdiagnosed? No. BMJ 2007; 335: 329.
- Hall WD, Mant A, Mitchell PB, Rendle VA, Hickie IB, McManus P. Association between antidepressant prescribing and suicide in Australia, 1991-2000: trend analysis. BMJ 2003; 326: 1008.
- Cipriani A, Furukawa TA, Salanti G, et al. Comparative efficacy and acceptability of 12 new-generation antidepressants: a multiple-treatments meta-analysis. Lancet 2009; 373: 746-58.
- Wirz-Justice A. Diurnal variation of depressive symptoms. Dialogues Clin Neurosci 2008; 10: 337-43.
- Monteleone P, Maj M. The circadian basis of mood disorders: recent developments and treatment implications. Eur Neuropsychopharm 2008; 18: 701-11.
- Germain A, Kupfer DJ. Circadian rhythm disturbances in depression. Hum Psychopharmacol 2008; 23: 571-85.
- Czeisler CA, Buxton OM, Khalsa SBS. The human circadian timing system and sleep-wake regulation. In: Kryger MH, Roth T, Dement WC, eds. Principles and practice of sleep medicine, 4th edn. Philadelphia: WB Saunders, 2005: 375-94.
- Rogers NL, Dinges DF. Interaction of chronic sleep restriction and circadian system in humans. J Sleep Res 2008; 17: 406-11.
- Rogers NL, Price NJ, Mullington JM, Szuba MP, Van Dongen HPA, Dinges DF. Plasma cortisol changes following chronic sleep restriction. Sleep 2000; 23: A70-71.
- Rogers NL, Price NJ, Szuba MP, Van Dongen HPA, Dinges DF. Effect of sustained caffeine on core body temperature during 88 hours of sustained wakefulness. Sleep 2001; 24: A172-73.
- Mansour HA, Monk TH, Nimgaonkar VL. Circadian genes and bipolar disorder. Ann Med 2005; 37: 196-205.
- Moore RY. Organization and function of a central nervous system circadian oscillator: the suprachiasmatic hypothalamic nucleus. Fed Proc 1983; 42: 2783-89.
- Miller JD, Morin LP, Schwartz WJ, Moore RY. New insights into the mammalian circadian clock. Sleep 1996; 19: 641-67.
- Duffy JF, Wright KP Jr. Entrainment of the human circadian system by light. J Biol Rhythms 2005; 20: 326-38.
- Souetre E, Salvati E, Belugou JL, et al. Circadian rhythms in depression and recovery: evidence for blunted amplitude as the main chronobiological abnormality. Psychiatry Res 1989; 28: 26378.
- Kaplan KA, Harvey AG. Hypersomnia across mood disorders: a review and synthesis. Sleep Med Rev 2009; 13: 275-85.
- Roberts RE, Shema SJ, Kaplan GA, Strawbridge WJ. Sleep complaints and depression in an aging cohort: a prospective perspective. Am J Psychiatry 2000; 157: 81-88.
- Dijk DJ, Czeisler CA. Contribution of the circadian pacemaker and the sleep homeostat to sleep propensity, sleep structure, electroencephalographic slow waves, and sleep spindle activity in humans. J Neurosci 1995; 15: 3526-38.
- Hickie I, Davenport T, Wakefield D, et al, and Dubbo Infection Outcomes Study Group. Post-infective and chronic fatigue syndromes precipitated by viral and non-viral pathogens: prospective cohort study. BMJ 2006; 333: 575.
- McClung CA. Circadian genes, rhythms and the biology of mood disorders. Pharmacol Ther 2007; 114: 222-32.
- Partonen T, Treutlein J, Alpman A, et al. Three circadian clock genes Per2, Arntl, and Npas2 contribute to winter depression. Ann Med 2007; 39: 229-38.
- Wulff K, Gatti S, Wettstein JG, Foster RG. Sleep and circadian rhythm disruption in psychiatric and neurodegenerative disease. Nat Rev Neurosci 2010; 11: 589-99.
- Mansour HA, Talkowski ME, Wood J, et al. Association study of 21 circadian genes with bipolar I disorder, schizoaffective disorder, and schizophrenia. Bipolar Dis 2009; 11: 701-10.
- Hickie I, Davenport T. A behavioural approach based on reconstructing the sleep-wake cycle. Cogn Behav Pract 1999; 6: 442-50.
- Frank E. Interpersonal and social rhythm therapy: a means of improving depression and preventing relapse in bipolar disorder. J Clin Psychol 2007; 63: 463-73.
- Vogel GW, Buffenstein A, Minter K, Hennessey A. Drug effects on REM sleep and on endogenous depression. Neurosci Biobehav Rev 1990; 14: 49-63.
- Dumont GJH, de Visser SJ, Cohen AF, van Gerven JM, on behalf of the Biomarker Working Group of the German Association for Applied Human Pharmacology. Biomarkers for the effects of selective serotonin reuptake inhibitors (SSRIs) in healthy subjects. Br J Clin Pharmacol 2005; 59: 495-510.
- Touitou Y, Bogdan A. Promoting adjustment of the sleep-wake cycle by chronobiotics. Physiol Behav 2007; 90: 294-300.
- Wirz-Justice A. From the basic neuroscience of circadian clock function to light therapy for depression: on the emergence of chronotherapeutics. J Affect Dis 2009; 116: 159-60.
- Lockley SW, Brainard GC, Czeisler CA. High sensitivity of the human circadian melatonin rhythm to resetting by short wavelength light. J Clin Endocrinol Metab 2003; 88: 4502-05.
- Wright KP Jr, Rogers NL. Endogenous versus exogenous effects of melatonin. In: Pandi-Perumal SR, Cardinali DP, eds. Melatonin: from molecules to therapy. New York: Nova Science Publishers, 2007: 547-69.
- Wu JC, Kelsoe JR, Schachat C, et al. Rapid and sustained antidepressant response with sleep deprivation and chronotherapy in bipolar disorder. Biol Psychiatry 2009; 66: 298-301.
- Rajaratnam SM, Cohen DA, Rogers NL, et al. Melatonin and melatonin analogues. Sleep Med Clin 2009; 4: 179-93.
- Klemfuss H. Rhythms and the pharmacology of lithium. Pharmacol Ther 1992; 56: 53-78.
- Johnsson A, Pflug B, Engelmann W, Klemke W. Effect of lithium carbonate on circadian periodicity in humans. Pharmakopsychiatr Neuropsychopharmakol 1979; 12: 423-25.
- Quiroz JA, Gould TD, Manji HK. Molecular effects of lithium. Mol Interv 2004; 4: 259-72.
- Iitaka C, Miyazaki K, Akaike T, Ishida N. A role for glycogen synthase kinase-3beta in the mammalian circadian clock. J Biol Chem 2005; 280: 29397-402.
- Wirz-Justice A, Benedetti F, Berger M, et al. Chronotherapeutics (light and wake therapy) in affective disorders. Psychol Med 2005; 35: 939-44.
- Dinges DF, Rogers NL, Baynard MD. Chronic sleep deprivation. In: Kryger MH, Roth T, Dement WC, eds. Principles and practice of sleep medicine, 4th edn. Philadelphia: WB Saunders, 2005: 67-76.
- Belenky G, Wesensten NJ, Thorne DR, et al. Patterns of performance degradation and restoration during sleep restriction and subsequent recovery: a sleep-dose response study. J Sleep Res 2003; 12: 1-12.
- Van Dongen HPA, Maislin G, Mullington JM, Dinges DF. The cumulative cost of additional wakefulness: dose-response effects on neurobehavioral functions and sleep physiology from chronic sleep restriction and total sleep deprivation. Sleep 2003; 26: 117-26.
- Spiegel K, Leproult R, Van Cauter E. Impact of sleep debt on metabolic and endocrine function. Lancet 1999; 354: 1435-39.
- Golden RN, Gaynes BN, Ekstrom RD, et al. The efficacy of light therapy in the treatment of mood disorders: a review and meta-analysis of the evidence. Am J Psychiatry 2005; 162: 656-62.
- Tuunainen A, Kripke DF, Endo T. Light therapy for non-seasonal depression. Cochrane Database Syst Rev 2004; 2: CD004050.
- Even C, Schroder CM, Friedman S, Rouillon F. Efficacy of light therapy in nonseasonal depression: a systematic review. J Affect Dis 2008; 108: 11-23.
- Pandi-Perumal SR, Trakht I, Srinivasan V, et al. Physiological effects of melatonin: role of melatonin receptors and signal transduction pathways. Prog Neurobiol 2008; 85: 335-53.
- Hirsch-Rodriguez E, Imbesi M, Manev R, Uz T, Manev H. The pattern of melatonin receptor expression in the brain may influence antidepressant treatment. Med Hypoth 2007; 69: 120-24.
- Brunner P, Sozer-Topcular N, Jockers R, et al. Pineal and cortical melatonin receptors MT1 and MT2 a decreased in Alzheimer's disease. Eur J Histochem 2006; 50: 311-16.
- Spadoni G, Bedini A. Advances on the development of subtype selective melatonin ligands. In: Pandi-Perumal SR, Cardinali DP, eds. Melatonin: from molecules to therapy. New York: Nova Science Publishers, 2007: 33-45.
- Weaver DR. Melatonin and circadian rhythmicity in vertebrates. Physiological roles and pharmacological effects. In: Turek FW, Zee PC, eds. Regulation of sleep and circadian rhythms. New York: Dekker, 1999: 197-262.
- von Gall C, Stehle JH, Weaver DR. Mammalian melatonin receptors: molecular biology and signal transduction. Cell Tissue Res 2002; 309: 151-62.
- Rogers NL, Dinges DF, Kennaway DJ, Dawson D. Potential action of melatonin in insomnia. Sleep 2003; 26: 1058-59.
- Kopp C, Vogel E, Rettori MC, Delagrange P, Misslin R. The effects of melatonin on the behavioural disturbances induced by chronic mild stress in C3H/He mice. Behav Pharmacol 1999; 10: 73-83.
- Carman JS, Post RM, Buswell R, Goodwin FK. Negative effects of melatonin on depression. Am J Psychiatry 1976; 133: 1181-86.
- Dalton EJ, Rotondi D, Levitan RD, Kennedy SH, Brown GM. Use of slow-release melatonin in treatment-resistant depression. J Psychiatry Neurosci 2000; 25: 48-52.
- Srinivasan V, Pandi-Perumal SR, Trakht I, et al. Pathophysiology of depression: role of sleep and the melatonergic system. Psychiatry Res 2009; 165: 201-14.
- Lemoine P, Nir T, Laudon M, Zisapel N. Prolonged-release melatonin improves sleep quality and morning alertness in insomnia patients aged 55 years and older and has no withdrawal effects. J Sleep Res 2007; 16: 372-80.
- Millan MJ, Gobert A, Lejeune F, et al. The novel melatonin agonist agomelatine (S20098) is an antagonist at 5-hydroxytryptamine2C receptors, blockade of which enhances the activity of frontocortical dopaminergic and adrenergic pathways. J Pharmacol Exp Ther 2003; 306: 954-64.
- Krauchi K, Cajochen C, Mori D, Graw P, Wirz-Justice A. Early evening melatonin and S-20098 advance circadian phase and nocturnal regulation of core body temperature. Am J Physiol 1997; 272: R1178-88.
- Roth T, Seiden D, Sainati S, Wang-Weigand S, Zhang J, Zee P. Effects of ramelteon on patient-reported sleep latency in older adults with chronic insomnia. Sleep Med 2006; 7: 312-18.
- Rajaratnam SM, Polymeropoulos MH, Fisher DM, et al. Melatonin agonist tasimelteon (VEC-162) for transient insomnia after sleep-time shift: two randomised controlled multicentre trials. Lancet 2009; 373: 482-91.
- Nickelsen T, Samel A, Vejvoda M, Wenzel J, Smith B, Gerzer R. Chronobiotic effects of the melatonin agonist LY 156735 following a simulated 9h time shift: results of a placebo-controlled trial. Chronobiol Int 2002; 19: 915-36.
- Wade AG, Ford I, Crawford G, et al. Efficacy of prolonged release melatonin in insomnia patients aged 55-80 years: quality of sleep and next-day alertness outcomes. Curr Med Res Opin 2007; 23: 2597-605.
- Kato K, Hirai K, Nishiyama K, et al. Neurochemical properties of ramelteon (TAK-375), a selective MT1/MT2 receptor agonist. Neuropharmacology 2005; 48: 301-10.
- Roth T, Stubbs C, Walsh JK. Ramelteon (TAK-375), a selective MT1/MT2-receptor agonist, reduces latency to persistent sleep in a model of transient insomnia related to a novel sleep environment. Sleep 2005; 28: 303-07
- Zammit G, Schwartz H, Roth T, Wang-Weigand S, Sainati S, Zhang J. The effects of ramelteon in a first-night model of transient insomnia. Sleep Med 2009; 10: 55-59.
- Erman M, Seiden D, Zammit G, Sainati S, Zhang J. An efficacy, safety, and dose-response study of Ramelteon in patients with chronic primary insomnia. Sleep Med 2006; 7: 17-24.
- Zammit G, Erman M, Wang-Weigand S, Sainati S, Zhang J, Roth T. Evaluation of the efficacy and safety of ramelteon in subjects with chronic insomnia. J Clin Sleep Med 2007; 3: 495-504.
- Roth T, Seiden D, Wang-Weigand S, Zhang J. A 2-night, 3-period, crossover study of ramelteon's efficacy and safety in older adults with chronic insomnia. Curr Med Res Opin 2007; 23: 1005-14.
- Vachharajani NN, Yeleswaram K, Boulton DW. Preclinical pharmacokinetics and metabolism of BMS-214778, a novel melatonin receptor agonist. J Pharm Sci 2003; 92: 760-72.
- European Medicines Agency. Evaluation of medicines for human use—CHMP assessment report for Valdoxan. http : //www.ema.europa.eu/docs/en GB/document Jibrary/EPAR - Public assessment report/human/000915/WC500046226.pdf (accessed March 14, 2011).
- Therapeutic Goods Administration, Department of Health and Ageing. Australian public assessment report for agomelatine. http://www.tga.gov.au/pmeds/auspar/ausparvaldoxan.pdf (accessed Feb 22, 2011).
- Dubovsky SL, Warren C. Agomelatine, a melatonin agonist with antidepressant properties. Expert Opin Investig Drugs 2009; 18: 1533-40.
- de Bodinat C, Guardiola-Lemaitre B, Mocaer E, Renard P, Munoz C, Millan MJ. Agomelatine, the first melatonergic antidepressant: discovery, characterization and development. Nat Rev Drug Discov 2010; 9: 628-42.
- De Berardis D, Di Iorio G, Acciavatti T, et al. The emerging role of melatonin agonists in the treatment of major depression: focus on agomelatine. CNS Neurol Dis Drug Targets 2011; 10: 119-32.
- Paizanis E, Renoir T, Lelievre V, et al. Behavioural and neuroplastic effects of the new-generation antidepressant agomelatine compared to fluoxetine in glucocorticoid receptor-impaired mice. Int J Neuropsychopharmacol 2010; 13: 759-74.
- Cajochen C, Krauchi K, Mori D, Graw P, Wirz-Justice A. Melatonin and S-20098 increase REM sleep and wake-up propensity without modifying NREM sleep homeostasis. Am J Physiol 1997; 272: R1189-96.
- Leproult R, Van Onderbergen A, L'hermite-Baleriaux M, Van Cauter E, Copinschi G. Phase-shifts of 24-h rhythms of hormonal release and body temperature following early evening administration of the melatonin agonist agomelatine in healthy older men. Clin Endocrinol 2005; 63: 298-304.
- Zupancic M, Guilleminault C. Agomelatine: a preliminary review of a new antidepressant. CNS Drugs 2006; 20: 981-92.
- Kennedy SH, Rizvi SJ. Agomelatine in the treatment of major depressive disorder: potential for clinical effectiveness. CNS Drugs 2010; 24: 479-99.
- ClinicalTrials.gov. Agomelatine search. http://clinicaltrials.gov/ct2/ results?term=agomelatine (accessed March 14, 2011).
- International Standard Randomised Controlled Trial Number Register. Agomelatine search. http:/ /www.controlled-trials.com/isrctn/search.html?rch=agomelatine&sort=3&dir=desc&max=10&Submit=SUBMIT (accessed March 14, 2011).
- Loo H, Hale D'haenen H. Determination of the dose of agomelatine, a melatoninergic agonist and selective 5-HT(2C) antagonist, in the treatment of major depressive disorder: a placebo-controlled dose range study. Int Clin Psychopharmacol 2002; 17: 239-47.
- Olie JP, Kasper S. Efficacy of agomelatine, a MT1/MT2 receptor agonist with 5-HT2C antagonistic properties, in major depressive disorder. Int J Neuropsychopharmacol 2007; 10: 661-73.
- Kennedy SH, Emsley R. Placebo-controlled trial of agomelatine in the treatment of major depressive disorder. Eur Neuropsychopharm 2006; 16: 93-100.
- Stahl SM, Fava M, Trivedi MH, Caputo A, Shah A, Post A. Agomelatine in the treatment of major depressive disorder: an 8-week, multicenter, randomized, placebo-controlled trial. J Clin Psychiatry 2010; 71: 616-26.
- Zajecka J, Schatzberg A, Stahl S, Shah A, Caputo A, Post A. Efficacy and safety of agomelatine in the treatment of major depressive disorder: a multicenter, randomized, double-blind, placebo-controlled trial. J Clin Psychopharmacol 2010; 30: 135-44.
- Kasper S, Hajak G, Wulff K, et al. Efficacy of the novel antidepressant agomelatine on the circadian rest-activity cycle and depressive and anxiety symptoms in patients with major depressive disorder: a randomized, double-blind comparison with sertraline. J Clin Psychiatry 2010; 71: 109-20.
- Lemoine P, Guilleminault C, Alvarez E. Improvement in subjective sleep in major depressive disorder with a novel antidepressant, agomelatine: randomized, double-blind comparison with venlafaxine. J Clin Psychiatry 2007; 68: 1723-32.
- Kennedy SH, Rizvi S, Fulton K, Rasmussen J. A double-blind comparison of sexual functioning, antidepressant efficacy, and tolerability between agomelatine and venlafaxine XR. J Clin Psychopharmacol 2008; 28: 329-33.
- Hale A, Corral R-M, Mencacci C, Ruiz JS, Severo CA, Gentil V. Superior antidepressant efficacy results of agomelatine versus fluoxetine in severe MDD patients: a randomized, double-blind study. Int Clin Psychopharmacol 2010; 25: 305-14.
- Quera-Salva M-A, Hajak G, Keufer-Le Gall S, Nutt D. Efficacy and safety of agomelatine in patients with major depressive disorder compared to escitalopram: a randomized, double-blind study. Int J Neuropsych 2010; 13: P03-43.
- Montgomery SA, Kennedy SH, Burrows GD, Lejoyeux M, Hindmarch I. Absence of discontinuation symptoms with agomelatine and occurrence of discontinuation symptoms with paroxetine: a randomized, double-blind, placebo-controlled discontinuation study. Int Clin Psychopharmacol 2004; 19: 271-80.
- Goodwin GM, Emsley R, Rembry S, Rouillon F, for the Agomelatine Study Group. Agomelatine prevents relapse in patients with major depressive disorder without evidence of a discontinuation syndrome: a 24-week randomized, double-blind, placebo-controlled trial. J Clin Psychiatry 2009; 70: 1128-37.
- Goodwin GM, Rouillon F, Emsley R. Long-term treatment with agomelatine: prevention of relapse in patients with major depressive disorder over 10 months. Eur Neuropsychopharmacol 2009; 18: S338-39.
- Novartis clinical trial results database. Agomelatine search. http: //www.novctrd.com/ctrdwebapp/clinicaltrialrepository/displayfile.do?trialresult=3420 (accessed March 14, 2011).
- Kasper S, Hamon M. Beyond the monoaminergic hypothesis: agomelatine, a new antidepressant with an innovative mechanism of action. World J Biol Psychiatry 2009; 10: 117-26.
- Montejo AL, Prieto N, Terleira A, et al. Better sexual acceptability of agomelatine (25 and 50 mg) compared with paroxetine (20 mg) in healthy male volunteers. An 8-week, placebo-controlled study using the PRSEXDQ-SALSEX scale. J Psychopharmacol 2010; 24: 111-20.
- Racagni G, Popoli M. The pharmacological properties of antidepressants. Int Clin Psychopharmacol 2010; 25: 117-31.
- Llorca P-M. The antidepressant agomelatine improves the quality of life of depressed patients: implications for remission. J Psychopharmacol 2010; 24: S21-26.
- Valdoxan product information. http:/ /www.medicines.org.au/files/ sepvaldx.pdf (accessed Feb 22, 2011).
