Применение вакцины Ваксигрип у детей с патологией
Статьи
 Хроническая патология - показание к вакцинации
Хроническая патология - показание к вакцинации
№6 (6) Ноябрь-декабрь 1999
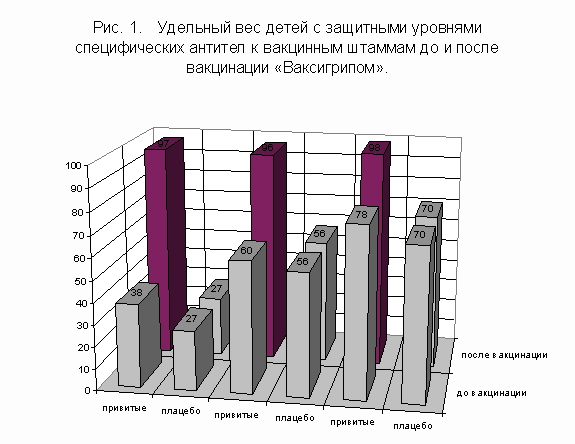
Е.И. Бурцева, О.В. Шамшева, А.Н. Слепушкин, И.Н. Новикова, В.Ф. Учайкин. Применение вакцины "Ваксигрип" у детей с патологией НИИ вирусологии им. Д.И. Ивановского РАМН, РГМУ, ООО "Диавакс" (Диагностика и вакцины), Москва В России одним из основных специфических средств в борьбе с гриппозной инфекцией является вакцинопрофилактика с использованием живых и инактивированных вакцин [1]. Гриппозные вакцины эффективны не только в плане снижения уровня заболеваемости, но и также в предупреждении развития постгриппозных осложнений и обострений хронических форм сопутствующих заболеваний со стороны сердечно-сосудистой и легочной систем [3,5]. В последние годы в России прошла регистрацию и широко используется гриппозная сплит-вакцина "Ваксигрип", производства фирмы "Пастер Мерье Коннот", Франция. Технология производства вакцины, включающая высокую степень очистки, в отличие от ряда других зарегистрированных в России вакцин, позволяет применять ее начиная с 6-месячного возраста [2]. Результаты предыдущего исследования по изучению специфической активности и защитного эффекта вакцины "Ваксигрип" у детей с соматической патологией в сезоне 1997-98 гг.. сообщались ранее [2,4]. Опыт показал, что двукратное введение вакцины в дозе 0.25 мл создавало защиту от всех трех вакцинных штаммов – A(H1N1), A(H3N2) и В, составив по числу сероконверсий – 78,0%, 71,0% и 81,0% соответственно, а по защищенности – 80,0%, 78,0% и 98,0% при кратности приростов средних геометрических титров антител 7,3, 7,2 и 8,4 соответственно. Кроме того, вакцинация значительно снижала частоту другой инфекционной патологии и обострений хронических заболеваний. Цель настоящего исследования заключалась в оценке прививочных свойств и профилактического эффекта двукратной вакцинации "Ваксигрип" у детей в дозе 0.5 мл. Вакцину "Ваксигрип" изучали в сезоне 1998-99 гг.. в детских домах г.Москвы у детей с поражением ЦНС и нарушениями психического развития в возрасте от 3 лет и старше. Под наблюдением находилось 73 ребенка, привитых вакциной, и 72 контрольной группы. Среди основных диагнозов: задержка психического развития (34 и 51 соответственно), олигофрения (36 и 16 соответственно) и ДЦП (1 и 2 соответственно). С сопутствующими заболеваниями наибольшую группу составили дети, в анамнезе которых был атопический дерматит (15 и 13 соответственно), функциональные изменения со стороны сердечно-сосудистой системы (4 и 5 соответственно), инфекция мочевыводящих путей (7 и 2 соответственно), а также хронические заболевания почек, ЖКТ, легких и др. Практически здоровыми были признаны 2 ребенка в группе привитых и 3 – в контрольной группе. "Ваксигрип" – очищенная инактивированная расщепленная вакцина производства фирмы Пастер Мерье Коннот (Франция) в одной прививочной дозе (0,5 мл) содержит по 15 мкг гемагглютининов вирусов гриппа А/Пекин/262/95 (H1N1), А/Сидней/5/97 (H3N2) и В/Харбин/7/94, рекомендованных ВОЗ для включения в состав гриппозных вакцин в сезоне 1998-99 гг. Вакцину вводили по 0,5 мл внутримышечно двукратно с интервалом 4 недели. Реактогенность вакцины оценивали путем учета общих и местных реакций в течение 4 дней после введения препарата. Об общей реакции судили по повышению температуры тела и изменению общего самочувствия. Среди местных реакций учитывали размеры гиперемии, припухлости и болезненность в месте введения вакцины, а также состояние регионарных лимфоузлов. Иммуногенную активность вакцины оценивали при титровании парных сывороток, взятых до и после вакцинации, в реакции торможения гемагглютинации (РТГА) микрометодом по общепринятой методике. В реакции были использованы антигены из штаммов вирусов гриппа, аналогичные, входящим в состав вакцины – А/Пекин/262/95 (H1N1), А/Сидней/5/97 (H3N2), В/Пекин/184/93. Реакцию ставили с 0,75% взвесью эритроцитов 0(I) группы крови человека. Оценку антигенной активности вакцины проводили по приросту титров антител (в 4 раза и более), динамике уровня средних геометрических титров антител (СГТ), а также уровню иммунологической защиты путем определения удельного веса лиц с титрами специфических антител 1:40 и выше до и после вакцинации. Профилактический эффект вакцинации оценивали путем учета заболеваний, вызванных группой респираторных вирусов, а также обострений хронически протекающих заболеваний в течение 3 месяцев после окончания вакцинации (с 20.12.98-20.03.99). Обработку полученных результатов проводили с использованием методов вариационной статистики. Достоверность различий полученных показателей подтверждали определением критерия Стъюдента (t), считая достоверно значимыми различия при to3 (1). В период наблюдения за переносимостью вакцины после первой вакцинации в группе привитых были зарегистрированы 3 случая жалоб на болезненность в месте инъекции (4,0%) и 1 температурная реакция средней степени выраженности (1,8%). При повторном введении вакцины через 4 недели было отмечено нарушение общего состояния в виде вялости и недомогания у 1 (1,8%) ребенка. При этом отмеченные реакции были непродолжительными и не превышали 1-2 дней. Оценка исходного иммунного ответа к вирусам гриппа А и В до вакцинаций показала, что больше половины обследуемых детей уже имели защитные уровни титров антител (>1:40) к вирусам гриппа А(H3N2) и В (56,0-78,0%). К вирусу гриппа А(H1N1) эти исходные показатели были значительно ниже и составили – 27,0-38,0% (рис. 1). Это связано с различием сроков активизации и начала циркуляции этих штаммов в качестве эпидемических: вирус гриппа А/Сидней/5/97 (H3N2) – с 1997 года, В/Пекин/184/93 – с 1993 года. Вирус гриппа А/Пекин/262/95 (H1N1) в предыдущие годы вызывал эпидемические подъемы заболеваемости только в странах Юго-Восточной Азии, а также спорадические случаи и небольшие вспышки в некоторых странах мира. Таким образом, по своей эпидемической значимости и распространенности он отличался от двух других вирусов. Было выявлено, что двукратная вакцинация стимулировала активную выработку специфических антител таким образом, что число детей с защитными уровнями титров антител к вакцинным вирусам составило 96,0-98,0% при отсутствии такой положительной динамики в контрольной группе, где сравниваемые показатели остались на исходных уровнях (27,0-70,0%). Детальная характеристика антигенных свойств вакцины "Ваксигрип" после двукратного введения представлена в табл. 1. При сравнительной оценке числа сероконверсий в группах серонегативных (1:10 и ниже) и детей с исходно высокими титрами антител 1:20-1:320 не было обнаружено статистически значимых различий между показателями. В целом по группе детей была зарегистрирована сероконверсия в 99,0% к вирусу гриппа А(H1N1), 90,0% к вирусу гриппа А(H3N2) и 92,0% к вирусу гриппа В. По-видимому, второе введение препарата через 4 недели обусловило усиление индивидуальной иммунологической памяти, приведшей к выработке достаточно значимого количества специфических антител. Так, у детей с высокими исходными титрами антител к вакцинным вирусам (1:640-1:1280) прироста не регистрировали, т.к. титрование сывороток в РТГА проводили только до титра 1:1280. В контрольной группе лишь в 2 случаях наблюдали прирост титров к вирусам гриппа А(H1N1) и В, что по-видимому обусловлено перенесенным заболеванием и в целом не влияло на достоверность различий между группами. Анализ динамики уровней СГТ антител и кратности их прироста также подтверждает высокую антигенную активность вакцины "Ваксигрип". В группе привитых отмечали достоверное нарастание титров антител ко всем трем вакцинным штаммам, при наибольшем показателе (32 раза) к новому эпидемическому варианту А(H1N1) и относительно сравнимых к А(H3N2) и В (12 и 8 раз соответственно). В контрольной группе уровни СГТ оставались в период наблюдения практически на исходных уровнях и составили соответственно 11.3-12.1 к вирусу гриппа A(H1N1), 39-34 к вирусу гриппа А(H3N2) и 56-56 к вирусу гриппа В. В целом из 69 привитых детей, обследованных серологически, только в одном случае не было зарегистрировано иммунологических сдвигов (1,4%), в то время как у 54 детей наблюдалось наличие специфических антител ко всем трем вакцинным вирусам (78,3%) и у 14 – к двум из вакцинных штаммов ( 20,3%). Результаты учета заболеваемости детей в течении 3-х месяцев после окончания вакцинации представлены в табл. 2. В группе привитых за весь период было зарегистрировано 6 случаев заболевания (8,2%) с гриппоподобными симптомами (ринит, бронхит, конъюнктивит и др.), в то время как в контрольной группе грипп и ОРВИ перенесли 28 (38,8%) детей. Таким образом, индекс профилактического эффекта (ИЭ) вакцинации был достаточно высоким и составил 4,7, а коэффициент эффективности (КЭ) – 79%. Разница показателей статистически достоверна. Необходимо отметить, что антигенная структура вакцинных штаммов "Ваксигрип" был аналогична циркулирующим эпидемическим вирусам гриппа, два из которых были наиболее активны в сезоне 1998-99 г – А/Сидней/5/97 (H3N2) и В/Пекин/184/93. Таким образом, результатом двукратной вакцинации явилось формирование коллектива с практически 100% иммунной прослойкой. Удельный вес лиц с защитными уровнями титров антител (1:40 и выше) среди привитых составил 96.0-98.0%. Сравнительная оценка прививочных свойств вакцины "Ваксигрип" у детей от 3 лет и старше при введении разной антигенной нагрузки (двукратно по 0.25 мл и двукратно по 0.5 мл) показала более высокую иммуногенную активность 2-ой схемы по числу сероконверсий, кратности прироста титров антител при отсутствии развития дополнительных побочных реакций. ЛИТЕРАТУРА
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||