Отдельные ингибиторы протонного насоса и исходы двойной антитромбоцитарной терапии у пациентов с ишемической болезнью сердца: систематический обзор
Статьи Американская кардиологическая ассоциация/ Американская ассоциация по изучению инсульта
Оригинальное исследование
Matthew W. Sherwood, врач, магистр валеологии;
Chiara Melloni, врач, магистр валеологии;
W. Schuyler Jones, врач;
Jeffrey B. Washam, доктор фармакологических наук;
Vic Hasselblad, кандидат наук;
Rowena J. Dolor, врач, магистр валеологии
Отделения сердечно-сосудистой медицины (M.W.S., C.M., W.S.J.) и терапевтическое отделение (R.J.D.),
Кардиологический центр при университете Дьюка (J.B.W.) и Отделение биостатистики и биоинформатики (V.H.),
Медицинский центр при университете Дьюка, Дарем, Нью-Йорк.
Краткая информация - По итогам наблюдательных исследований по оценке возможного взаимодействия между ингибиторами протонного насоса (ИПН) и клопидогрелом были получены неоднозначные результаты. Нами был проведен систематический обзор по сравнению безопасности отдельных ИПН у пациентов с ишемической болезнью сердца, принимающих клопидогрел.
Методы и результаты - Для включения в обзор отбирали исследования, проводившиеся с января 1995 года по декабрь 2013 года. Получали данные и оценивали качество 34 потенциальных исследований. Выполняли мета-анализ исследований, в которых было проведено сравнение периодов последующего наблюдения, исходов и многофакторной поправки. Скорректированное отношение шансов или отношение рисков для комбинированных исходов смертности по причине сердечно-сосудистых заболеваний или по всем причинам, инфаркта миокарда и инсульта по истечении 1 года были указаны в 6 наблюдательных исследованиях с данными по отдельным ИПН. Мета-анализ случайных эффектов в 6 исследованиях выявил повышенный риск нежелательных сердечно-сосудистых явлений у пациентов, принимающих пантопразол (отношение рисков 1.38; 95% ДИ: 1.12-1.70), лансопразол (отношение рисков 1.29; 95% ДИ: 1.09-1.52) или эзомепразол (отношение рисков 1.27; 95% ДИ: 1.02-1.58), по сравнению с пациентами, не принимающими ИПН. Данная связь не была значимой для омепразола (отношение рисков 1.16; 95% ДИ: 0.93–1.44). Анализы чувствительности для популяции пациентов с ишемической болезнью сердца (острый коронарный синдром или смешанная) и исключение одного исследования ввиду гетерогенности опубликованных результатов не оказали значительного влияния на оценку эффекта любого ИПН.
Заключения - Некоторые часто применяемые ИПН, ранее считавшиеся безопасными для одновременного применения с клопидогрелом, ассоциированы с повышенным риском нежелательных сердечно-сосудистых явлений. Несмотря на то, что данные получены по результатам наблюдений, они указывают на необходимость проведения рандомизированных, контролируемых исследований для оценки безопасности одновременного применения ИПН и клопидогрела у пациентов с ишемической болезнью сердца.
(J Am Heart Assoc. 2015;4:e002245 doi: 10.1161/JAHA.115.002245)
Ключевые слова: нежелательные сердечно-сосудистые исходы, клопидогрел, ишемическая болезнь сердца , лекарственное взаимодействие, ингибитор протонного насоса
Двойная антитромбоцитарная терапия (ДАТТ), подразумевающая комбинацию аспирина и ингибитора P2Y12, улучшает сердечно-сосудистые (СС) исходы и рекомендована национальными руководствами к применению в течение одного года после первичной госпитализации у пациентов с острыми коронарными синдромами (ОКС).1,2 Клопидогрел, теперь доступный в форме генерического препарата, остается наиболее широко применяемым ингибитором P2Y12 среди амбулаторных пациентов, перенесших ОКС. Клопидогрел является неактивным лекарственным препаратом, переход которого в активную форму зависит от цитохрома P450 или печеночных ферментов системы CYP. Ввиду повышенного риска кровотечения из желудочно-кишечного тракта (ЖКТ), обусловленного клопидогрелом и ДАТТ, многие пациенты, перенесшие ОКС, также начинают принимать ингибитор протоннного насоса (ИПН) или антагонист Н2-рецепторов. Препараты ИПН (наиболее часто назначаемые препараты для снижения риска кровотечения из ЖКТ) также вступают во взаимодействие с печеночными ферментами системы CYP и, тем самым, могут ингибировать превращение клопидогрела в его активный метаболит и оказать потенциальное негативное воздействие на его эффективность.
Некоторые наблюдательные исследования были проведены с целью оценки возможного лекарственного взаимодействия между ИПН и ДАТТ и его связи с сердечно-сосудистыми исходами.3-6 По итогам проведения данных исследований были получены неоднозначные результаты: некоторые свидетельствовали о потенциальном взаимодействии между клопидогрелом и ИПН, на фоне которого было отмечено ухудшение сердечно-сосудистых исходов, в других связь с исходами отсутствовала. Доступно очень мало данных рандомизированных исследований, чтобы ответить на данный вопрос. По результатам недавно проведенного мета-анализа по данной проблеме был сделан вывод, что результаты наблюдательных и рандомизированных исследований по ИПН расходятся.7
Несмотря на конфликт данных и возможное равенство сил в данной области, Управление по контролю качества пищевых продуктов и лекарственных средств США выпустило особое предостережение в черной рамке о применении клопидогрела одновременно с препаратами ИПН, в частности, омепразолом и эзомепразолом, по которым получено больше всего данных. В случае с омепразолом данные получены по итогам как наблюдательных, так и рандомизированных, контролируемых исследований. Остается неопределенность относительно связи с другими ИПН, поскольку отмечается вариативность эффективности между препаратами данного класса. Каждый ИПН оказывает различное воздействие на метаболизм CYP и, тем самым, влияние на метаболизм клопидогрела и последующие сердечно-сосудистые исходы могут не совпадать. В недавно проведенных мета-анализах были объединены все ИПН, вероятно, для большей мощности, с целью оценки взаимосвязи между ИПН, клопидогрелом и сердечно-сосудистыми исходами.8 Тем не менее, на основании фармакологических данных, могут быть отмечены различные взаимодействия между отдельными ИПН и клопидогрелом. Целью настоящего исследования является установление взаимосвязи между отдельными препаратами ИПН и нежелательными сердечно-сосудистыми явлениями у пациентов с острой и стабильной ишемической болезнью сердца (ИБС), принимающих клопидогрел.
Методы
Систематический обзор был проведен для оценки имеющейся на данный момент литературы, а также сбора и объединения доступных данных. Данный анализ был проведен в рамках более обширного систематического обзора по оценке эффективности и безопасности антитромбоцитарных и антикоагулянтных лекарственных препаратов, применяемых в терапии пациентов с нестабильной стенокардией и инфарктом миокарда (ИМ) без подъема сегмента ST.9 Финансовую поддержку при проведении более обширного систематического обзора оказало Агентство по исследованиям и качеству в здравоохранении.
Нами были использованы ключевые обозначения Медицинских предметных рубрик Национальной медицинской библиотеки. В область поиска для включения в настоящее исследование входили систематические обзоры в период с 1 января 1995 года по 30 декабря 2013 года в базах данных PubMed, Embase и Cochrane. Поиск релевантных статей для включения в наш анализ также осуществлялся по «серым» литературным источникам, включая реестры, аннотации материалов конференций и завершенные исследования (ClinicalTrials.gov, Всемирная организация здравоохранения, Международная платформа реестров клинических исследований, указатель материалов конференций ProQuest).
Популяция исследования
Дизайны исследования включали когортное исследование (проспективное и ретроспективное), исследование случай-контроль и перекрестное исследование. Было доступно незначительное количество данных, полученных из рандомизированных контролируемых исследований, однако их включение в обзор представлялось нецелесообразным по статистическим и концептуальным причинам. В обзор включали исследования на английском языке, в которых было проведено сравнение одновременного применения клопидогрела и ИПН в рамках терапии пациентов с ОКС после выписки или у пациентов, подвергающихся чрескожному коронарному вмешательству в связи с сердечно-сосудистыми исходами, и последующее наблюдение в течение, как минимум, 1 года. В рамках данных исследований также должен был быть проведен анализ ИПН по отдельности, в том числе омепразола, эзомепразола, пантопразола, лансопразола и рабепразола. Исследования исключали, если в них не был проведен анализ исходов для отдельных ИПН, если период последующего наблюдения составлял менее 12 месяцев, или если в них не было проведено многофакторное моделирование со скорректированным отношением шансов (ОШ) или отношением рисков (ОР). Исходы, представляющие интерес, включали комбинированные сердечно-сосудистые исходы смертности по причине сердечно-сосудистых заболеваний и/или по всем причинам, ИМ без смертельного исхода, инсульт, повторную госпитализацию и реваскуляризацию.
Отбор исследований
Качество исследований определяли по качеству предоставленных данных. Двумя исследователями (C.M. и J.W.) был проведен независимый обзор статей, третий исследователь (R.D.) выступал в роли арбитра в случае расхождения. Исследования включали на основании указанных ранее критериев включения, а затем изучали для извлечения данных.
Статистические методы
Извлечение данных
Для получения и обобщения исходных данных были созданы формы извлечения данных и таблицы подтверждающих данных. В таблицы вносили информацию о популяции исследования, отдельных препаратах ИПН, включенных в исследование, оцениваемых исходах, времени последующего наблюдения и нескорректированной и скорректированной точечной оценке. Первоначальное извлечение данных проводил один исследователь, анализ полноты и ошибок выполнял второй исследователь.
Обобщение данных
Первичную литературу обобщали посредством извлечения ОШ и ОР, указанных авторами. Нами предполагалось, что на искажение взаимосвязи между омепразолом и нежелательными сердечно-сосудистыми явлениями могли оказать влияние многочисленные факторы, преимущественно такие факторы риска, как кровотечение из ЖКТ и риск развития сердечно¬сосудистых явлений. В их число входили: возраст, пол, масса тела, функция почек и другие медицинские сопутствующие заболевания, включая возникавшее ранее кровотечение из ЖКТ.
Данные факторы, как правило, учитывались в логистической регрессии с множеством независимых переменных или модели склонности для исследований, включенных в наш анализ. По возможности мы оценивали каждое исследование с точки зрения включения информации о применении соответствующих сопутствующих препаратов для вторичной профилактики ИБС.
Первоначально для анализа рассматривали нескорректированные и скорректированные ОШ и ОР. Использовали модель случайных эффектов. В ходе мета-анализов выполняли прямое сравнение, если исходы и периоды последующего наблюдения были признаны сопоставимыми. Оценка систематической погрешности, связанной с предпочтительной публикацией положительных результатов исследований, посредством построения воронкообразного графика выборки, нанесения на план численности выборки исследования в сравнении с ОШ или ОР (логарифмическая шкала), была запланирована при достаточном количестве исследований (т.е. >10). Анализы чувствительности были проведены вместе с испытаниями на возможные эффекты гетерогенности (статистический показатель Q) только при включении пациентов с ОКС в сравнении с пациентами смешанной популяции (стабильная ИБС и ОКС). При получении несопоставимых данных для одного исследования проводили анализ чувствительности для данного исследования с целью установления значительного изменения результатов. Все статистические анализы совокупных деидентифицированных данных были проведены в Институте клинических исследований при Университете Дьюка с использованием пакета программ Comprehensive Meta-Analysis версия 2 (Biostat).
Результаты
Первоначальный поиск по литературным источникам выявил 36 потенциальных исследований для дальнейшей оценки. После применения указанных выше критериев исключения (Рисунок 1) были исключены 2 исследования как дублирующие и 4 рандомизированных контролируемых исследования. Впоследствии были исключены 24 исследования ввиду отсутствия данных о последующем наблюдении в течение 1 года и исходах применения отдельных ИПН. Итоговая выборка исследований включала 6 наблюдательных исследований, 5 из которых имели высокое качество и 1 - среднее качество, при участии более 41 000 пациентов4-6,10-12 (Таблица 1). В указанных исследованиях нашей выборки были доступны данные об исходах для омепразола, эзомепразола, пантопразола, лансопразола и рабепразола. Ввиду ограниченности доступных данных для объединения рабепразол был исключен из дальнейшего анализа. Нами также было установлено отличное применение сопутствующих препаратов (>75%), включая аспирин, бета-блокаторы и статины, а также более разнообразное использование ингибиторов ангиотензин-превращающего фермента и блокаторов ангиотензиновых рецепторов в исследованиях, предоставляющих эти данные (все за исключением исследования, проведенного Kreutz et al10).
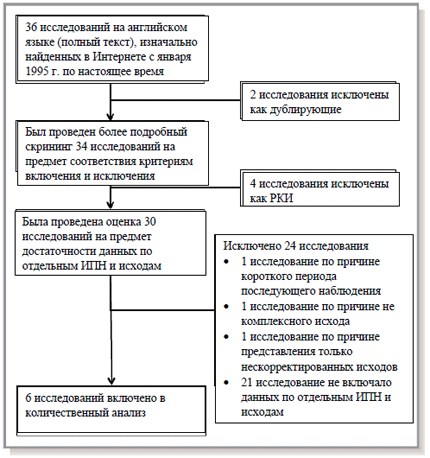
Рисунок 1. Блок-схема выборки для выбора исследований, отображающая результаты
проведенного нами поиска в литературе с последующим исключением исследований из количественного анализа.
ИПН обозначает ингибиторы протонного насоса; РКИ – рандомизированное, контролируемое исследование.
Омепразол
В ходе шести наблюдательных исследований при участии 10 201 пациента была проведена оценка действия омепразола при его добавлении к ДАТТ у пациентов со стабильной ИБС и пациентов с ОКС после выписки по комбинированной конечной точке смертности по причине сердечно-сосудистых заболеваний или по всем причинам, ИМ без смертельного исхода и инсульта спустя 1 год.4-6,10-12 Результат представляли в виде рассчитанного ОР 1,16 (95% ДИ: 0,93-1,44) (Рисунок 2А). Были получены данные о выраженной гетерогенности (показатель Q 28,70 для 5 df, P2 составлял 82,58.
Пантопразол
В ходе шести наблюдательных исследований при участии 15 620 пациентов была проведена оценка действия пантопразола при его добавлении к ДАТТ у пациентов со стабильной ИБС и пациентов с ОКС после выписки по комбинированной конечной точке смертности по причине сердечно-сосудистых заболеваний или по всем причинам, ИМ без смертельного исхода и инсульта спустя 1 год.4-6,10-12 Результат представляли в виде рассчитанного ОР 1,38 (95% ДИ: 1,12-1,70) (Рисунок 2В). Были получены данные о выраженной гетерогенности (показатель Q 36,50 для 5 df, P2 составлял 86,30.
Лансопразол
В ходе пяти наблюдательных исследований была проведена оценка действия лансопразола при его добавлении к ДАТТ у 4 681 пациента со стабильной ИБС, перенесшего ОКС, по комбинированной конечной точке смертности по причине сердечно-сосудистых заболеваний или по всем причинам, ИМ без смертельного исхода и инсульта спустя 1 год.4-6,10,11 Результат представляли в виде рассчитанного ОР 1,29 (95% ДИ: 1,09-1,52) (Рисунок 2С). Данные о выраженной гетерогенности (показатель Q 5,89 для 4 df, P2 составлял 32,07.
Эзомепразол
В ходе шести наблюдательных исследований при участии 11 200 пациентов была проведена оценка действия эзомепразола при его добавлении к ДАТТ у пациентов со стабильной ИБС и пациентов с ОКС после выписки по комбинированной конечной точке смертности по причине сердечно-сосудистых заболеваний или по всем причинам, ИМ без смертельного исхода и инсульта спустя 1 год.4-6,10-12 Результат представляли в виде рассчитанного ОР 1,27 (95% ДИ: 1,02-1,58) (Рисунок 2D). Были получены данные о выраженной гетерогенности (показатель Q 27,28 для 5 df, P2 > составлял SUP 81,67.
Таблица 1. Характеристика исследований
| Исследование; популяция; качество | Общий размер выборки* ИПН в сравнении с «без ИПН» Выборки | ИПН, кол-во (%) | Исходы/Период времени | Количество исходов | Ковариаты для скорректированного ОШ/ОР |
|---|---|---|---|---|---|
| Kreutz, 201010; общая популяция с ИПН; высокое | Всего: 16 690 ИПН: 6 828 Без ИПН: 9 862 | Омепразол, 2 307 (34%) Пантопразол, 1 653 (24%) Лансопразол, 785 (11%) Эзомепразол, 3 257 (48%) | Комбинированная сердечно-сосудистая смертность в течение 1 года, ИМ без смертельного исхода, инсульт, реваскуляризация | Всего: 3 476 ИПН: 1 766 Без ИПН: 1 710 | Возраст, пол, госпитализация, стентирование, СД, АГ, ЗСН, ХПН, HL, сопутствующие лекарственные препараты |
| Ray, 20105; смешанная популяция с ИПН; высокое | Всего: 20 596 ИПН: 7 226 Без ИПН: 8 995 | Омепразол, 683 (9%) Пантопразол, 4 708 (62%) Лансопразол Эзомепразол Рабепразол | Комбинированная сердечно-сосудистая смертность в течение 1 года, ИМ без смертельного исхода, инсульт, внезапная сердечная смерть | Всего: 1 041 ИПН: 580 Без ИПН: 461 | Возраст, пол, страхование здоровья, АКШ, ЧКВ, сопутствующие лекарственные препараты, ЗСН, инсульт, БПА |
| Simon, 201111; FAST-MI, популяция с ИМ; высокое | Всего: 2 744 ИПН: 1 449 Без ИПН: 900 | Омепразол, 993 (69%) Пантопразол, 99 (7%) Лансопразол, 46 (3%) Эзомепразол, 311 (22%) | Комбинированная сердечно-сосудистая смертность в течение 1 года, ИМ без смертельного исхода, инсульт | Всего: 225 ИПН: 100 Без ИПН: 125 | Шкала GRACE, пол, курение, HL, АГ, СД |
| Van Boxel, 201012; смешанная популяция с ИБС; среднее | Всего: 18 139 ИПН: 5 734 Без ИПН: 12 405 | Омепразол, 1 826 (32%) Пантопразол, 2 618 (46%) Эзомепразол 1 092 (19%) Рабепразол, 133 (2%) | Комбинированная сердечно-сосудистая смертность в течение 1 года, ИМ без смертельного исхода, инсульт, НС | Всего: 1 584 ИПН: 830 Без ИПН: 754 | Возраст, пол, сопутствующие лекарственные препараты, ЗСН, ИМ, ССЗ, ХОБЛ, ХПН, СД, ЯБ |
| Charlot, 20106; вся популяция с ИМ; высокое | Всего: 56 406 ИПН: 6 753 Без ИПН: 17 949 | Омепразол, 2 717 (17%) Пантопразол, 4698 (30%) Лансопразол, 2 798 (18%) Эзомепразол 5316 (34%) | Комбинированная сердечно-сосудистая смертность в течение 1 года, ИМ, инсульт | Всего: 2 564 ИПН: 1 506 Без ИПН: 1 058 | Возраст, пол, доход, шок, СД, ЯБ, ЧКВ, отек легких, ССЗ, рак, аритмия, ХПН, ОПН, сопутствующие лекарственные препараты |
| O’ Donoghue 20094; TRITON-TIMI 38, популяция с ОКС; высокое | Всего: 13 608 ИПН: 4 529 Без ИПН: 9 079 | Омепразол, 1 675 (37%) Пантопразол, 1 844 (41%) Лансопразол, 441 (10%) Эзомепразол, 613 (14%) | Комбинированная сердечно-сосудистая смертность в течение 1 года, ИМ, инсульт | Всего: 781 ИПН: 526 Без ИПН: 255 | Возраст, пол, этническая принадлежность, АГ, HL, СД, курение, инициальное событие, возникший ранее ИМ, АКШ, ССЗ, БПА, КК, DES, сопутствующие лекарственные препараты, ИМТ, гемоглобин, АД, ЧСС |
| ОКС обозначает острый коронарный синдром; ИМТ - индекс массы тела; АД - артериальное давленние; АКШ - аортокоронарное шунтирование; ИБС - ишемическая болезнь сердца; ЗСН -застойная сердечная недостаточность; ХОБЛ - хроническая обструктивная болезнь легких; КК -клиренс креатинина; ХПН - хроническая почечная недостаточность; СС - сердечно-сосудистый; ССЗ - сердечно-сосудистое заболевание; DES - стент, выделяющий лекарственный препарат; СД - сахарный диабет; Hgb - гемоглобин; ОР - отношение рисков; АГ - артериальная гипертензия; meds - сопутствующие лекарственные препараты; ИМ - инфаркт миокарда; ОШ - отношение шансов; БПА - болезнь периферических артерий; ЧКВ - чрезкожное коронарное вмешательство; ИПН - ингибитор протонного насоса; ЯБ - язвенная болезнь; НС - нестабильная стенокардия. *Для каждого исследования размер выборки также указан с учетом пациентов, принимающих клопидогрел. | |||||
Анализ чувствительности
Принимая во внимание гетерогенность наших результатов, нами было проведено несколько анализов чувствительности. Для изучения потенциальной гетерогенности в исследуемой выборке мы разделили исследования на группы: популяции только с ОКС в сравнении со смешанными популяциями или популяциями со стабильной ИБС. Как видно из Таблицы 2, значительные изменения в сводном резюме ОР (с более широким ДИ) в популяции только с ОКС или в смешанной популяции для любого отдельного ИПН отсутствовали.
Для дальнейшего изучения эффекта возможного исследования с резко отклоняющимися значениями мы повторили процедуру анализа сначала, исключив исследование Simon et al ввиду использования ОШ и маленькой численности выборки (Рисунок 3А и 3В). Как показано на Рисунке 3, значительные изменения в сводных расчетах ОР для любого отдельного ИПН или в расчете суммарного эффекта ИПН отсутствовали. Наконец, принимая во внимание от факт, что в количественный анализ было включено значительно меньше 10 исследований, анализ систематической погрешности, связанной с предпочтительной публикацией положительных результатов исследований, не был выполнен, поскольку мощность данных исследований не была достаточно высокой для обеспечения точной оценки погрешности при маленькой численности выборки.13,14
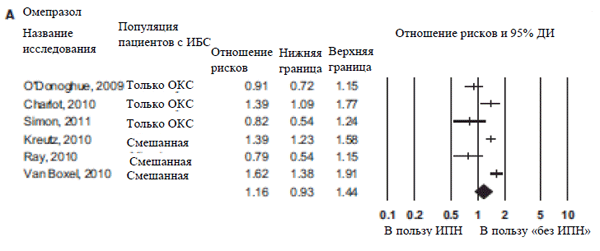
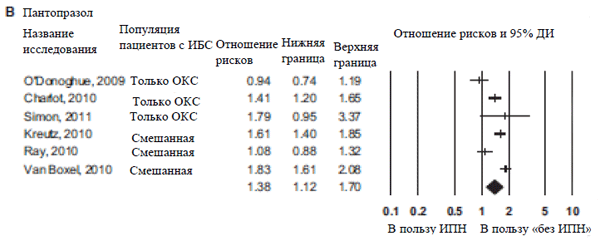
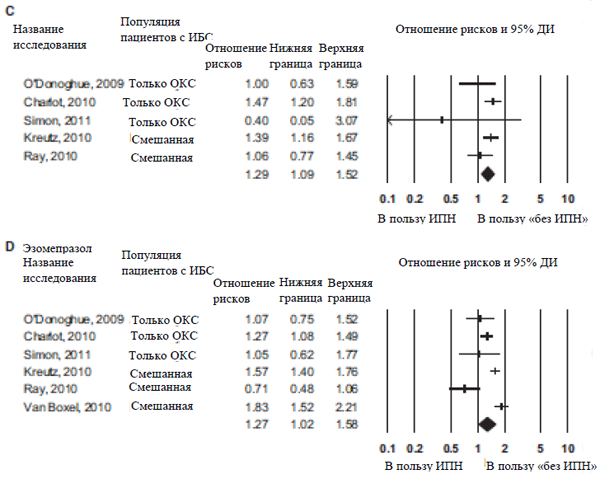
Рисунок 2. Результаты мета-анализов отдельных ИПП по данным включенных исследований:
(А) омепразол, (В) пантопразол, (С) лансопразол, (D) эзомепразол.
ОКС обозначает острые коронарные синдромы; ИБС – ишемическая болезнь сердца;
ИПН – ингибитор протонного насоса.
Таблица 2.
Анализ чувствительности для отдельных ИПН в популяции пациентов с ИБС
| Препарат | Популяция пациентов с ИБС | Исследования (кол-во) | Величина эффекта (95% ДИ) | Показатель Р гетерогенности |
|---|---|---|---|---|
| Омепразол | Только ОКС | 3 | 1,04 (0,76-1,41) | 0,31 |
| Смешанная | 3 | 1,28 (0,97-1,71) | ||
| Пантопразол | Только ОКС | 3 | 1,29 (0,89-1,77) | 0,45 |
| Смешанная | 3 | 1,49 (1,14-1,95) | ||
| Лансопразол | Только ОКС | 3 | 1,26 (0,91-1,74) | 0,96 |
| Смешанная | 2 | 1,24 (0,92-1,68) | ||
| Эзомепразол | Только ОКС | 3 | 1,15 (0,83-1,60) | 0,57 |
| Смешанная | 3 | 1,37 (1,01-1,85) | ||
| ОКС обозначает острый коронарный синдром; ИБС - ишемическая болезнь сердца | ||||
Обсуждение
В систематическом обзоре доступных данных наблюдательных исследований о связи отдельных ИПН с нежелательными сердечными исходами у пациентов с ИБС, принимающих клопидогрел, некоторые ИПН, ранее считавшиеся безопасными, были признаны опасными. Омепразол не продемонстрировал статистически значимой связи с нежелательными сердечно¬сосудистыми явлениями вне зависимости от статуса ИБС (ОКС в сравнении со стабильной ИБС), в то время как пантопразол, лансопразол и эзомепразол имели статистически значимую связь с нежелательными сердечно-сосудистыми исходами. Сохраняется потребность в проведении рандомизированных, контролируемых исследований или мета-анализов на уровне пациентов для оценки безопасности отдельных ИПН для одновременного применения с клопидогрелом у пациентов с ИБС.
Несмотря на то, что обилие наблюдательных данных по итогам отдельных исследований демонстрирует связь между ИПН (как группы) и нежелательными сердечно-сосудистыми исходами, имеются несколько правдоподобных объяснений полученных результатов. Наиболее убедительным аргументом остается то, что применение ИПН является маркером повышенного риска, а не причиной неблагоприятных сердечно-сосудистых исходов. Это хорошо продемонстрировали несколько исследований с применением клопидогрела и антагонистов P2Y12-рецепторов нового поколения. Goodman et al оценили воздействие ИПН на нежелательные сердечно-сосудистые явления у пациентов, перенесших ОКС, принимавших тикагрелор или клопидогрел в рамках исследования PLATO.15 Важным отличием является то, что, несмотря на блокирующее действие тикагрелора на P2Y12-рецептор, он является активным веществом и, таким образом, в отличие от клопидогрела, не требует метаболизма посредством системы CYP 2C19 для активации. В связи с этим, фармакокинетический механизм взаимодействия между ИПН и тикагрелором отсутствует. Авторы показали, что у пациентов, принимавших ИПН или другие не-ИПН препараты для лечения заболеваний ЖКТ, наблюдалась значительно более высокая частота возникновения нежелательных сердечно-сосудистых явлений как в группе пациентов, принимавших клопидогрел, так и в группе пациентов, получавших тикагрелор. Этапные анализы начала применения ИПН на момент рандомизации или в последующем в ходе исследования (2, 4, 9, 30, 60, 90 или 180 день) показали, что ИПН были лишь независимо связаны с нежелательными сердечными явлениями, когда пациенты начинали их принимать до или во время рандомизации. Эти авторы пришли к выводу, что наиболее правдоподобным объяснением полученных результатов будет являться то, что ИПН использовали в качестве маркера пациентов с повышенным риском сердечно-сосудистых явлений, и что взаимосвязь между явлениями и приемом ИПН у пациентов, принимавших клопидогрел и тикагрелор, была в значительной степени искажена. Dunn et al пришли к аналогичному выводу в ходе анализа результатов исследования CREDO при участии пациентов, принимавших и не принимавших ИПН.16

Рисунок 3. Анализы чувствительности общего эффекта ИПН (А) с и (В)
без исследования, проведенного Simon et al.11
Были предложены альтернативные механизмы объяснения взаимосвязи между ИПН и нежелательными сердечно-сосудистыми явлениями. В крупномасштабном исследовании по фармаконадзору Shah et al изучали применение ИПН в сплошной группе пациентов для оценки взаимосвязи ИПН с сердечно-сосудистыми явлениями и смертностью. По данным их исследования, вне зависимости от приема клопидогрела, у пациентов, принимавших ИПН, был отмечен повышенный риск возникновения ИМ (ОР 1,16; 95% ДИ: 1,09-1,24), а также в 2 раза более высокий риск общей смертности (ОР 2,00; 95% ДИ: 1,07-3,78; Р=0,031) по сравнению с пациентами, не принимавшими ИПН.17 Аналогичная взаимосвязь у пациентов, принимавших блокаторы Н2-рецепторов, не была установлена. Несмотря на то, что точный механизм воздействия ИПН на общую популяцию неизвестен, авторы указывают на ранее проводившиеся исследования на животных, в которых сообщалось, что применение ИПН может быть связано со снижением активности синтазы оксида азота, которая, в свою очередь, является известным маркером состояния сосудов и тромбоза. Несмотря на то, что данные результаты представляют интерес, их недостаточно для объяснения возможного взаимодействия между клопидогрелом и ИПН. Наиболее надежным методом оценки взаимосвязи между ИПН и клопидогрелом остается проведение рандомизированного, контролируемого исследования.
В настоящее время доступны незначительные данные рандомизированных контролируемых исследований для ответа на данный вопрос. Небольшие рандомизированные контролируемые исследования были проведены с применением пантопразола18 и омепразола19, в которых были оценены реактивность и функция тромбоцитов в качестве конечных точек. Данные исследования показали, что реактивность тромбоцитов выше у пациентов, одновременно принимавших клопидогрел и омепразол, по сравнению с пациентами, принимавшими клопидогрел отдельно или клопидогрел в комбинации с пантопразолом. Тем не менее, ни одно из указанных исследований не было достаточно масштабным и не обладало необходимой мощностью для изучения клинических исходов. Исследование COGENT было разработано для оценки воздействия омепразола в сравнении с плацебо на исходы тромбоза и кровотечения у пациентов, которым назначали ДАТТ клопидогрелом продолжительностью, как минимум, 12 месяцев.20 В исследование включали только тех пациентов, которые должны были получать ДАТТ (с клопидогрелом) в течение, как минимум, 12 месяцев и на момент включения не принимали ИПН, антагонисты Н2-рецепторов или другие антацидные препараты, применяемые при заболеваниях ЖКТ. К сожалению, исследование было преждевременно остановлено ввиду медленного набора пациентов и отсутствия финансирования. Тем не менее, несмотря на ограниченные численность выборки и период последующего наблюдения, у пациентов, принимавших омепразол и ДАТТ в сравнении с только ДАТТ, наблюдался аналогичный риск возникновения тромботических явлений и значительно сниженный риск кровотечения из ЖКТ. На данный момент приведенные данные являются самыми доступными относительно взаимосвязи между отдельными ИПН и нежелательными сердечно-сосудистыми исходами у пациентов с ИБС. Несмотря на представленные результаты, Управление по контролю качества пищевых продуктов и лекарственных средств США снова выпустило предостережение о применении омепразола или эзомепразола в комбинации с клопидогрелом на основании данных наблюдательных исследований.
Когда доступно мало данных рандомизированных, контролируемых исследований, исследователи зачастую пытаются объединить самые лучшие доступные источники данных для получения выводов. Систематические обзоры с мета-анализами позволяют исследователям и врачам-клиницистам использовать данные результаты во многих исследованиях и увеличивать мощность для ответа на важные клинические вопросы. Результаты нашего систематического обзора совпадают с проводившимся ранее рандомизированным, контролируемым исследованием20, в котором сообщается, что омепразол не связан с нежелательными сердечно- сосудистыми явлениями у пациентов с ИБС, одновременно принимающих клопидогрел. Для оставшихся отдельных ИПН, включая пантопразол, лансопразол и эзомепразол, наши наблюдательные результаты дополняют представленную ранее литературу, однако в узком смысле представляют гипотезу и указывают на необходимость дополнительных подтверждающих данных рандомизированных, контролируемых исследований по оценке эффективности и безопасности данных ИПН у пациентов с ИБС, одновременно принимающих клопидогрел. На данный момент нет четких доказательств, рекомендующих переход с одного ИПН на другой во избежание взаимодействия с клопидогрелом. В настоящее время ввиду противоречивости доступных данных следует рассмотреть вопрос об изменении рекомендаций для отражения текущей неопределенности.
Ограничения
Проведенное нами исследование имело некоторые ограничения. Во всех исследованиях отсутствовали данные о схеме приема препарата, продолжительности применения и явлениях кровотечения из ЖКТ. Наблюдалась вариативность в определении комбинированной конечной точки и ковариат для скорректированных ОШ и ОР, например, использование смертности по всем причинам в сравнении со смертностью по причине сердечно-сосудистых заболеваний, что могло внести некоторую неточность в нашу оценку эффекта. Кроме того, нами был проведен мета-анализ с учетом ОР и ОШ, что может вызывать вопросы в отношении статистической достоверности в случае высокой частоты возникновения явлений. Частота возникновения явлений была одинаковой (≤25%), анализы чувствительности были проведены, за исключением исследования Simon et al - единственного исследования с использованием ОШ - и показали весьма сходные результаты вне зависимости от использования указанных данных. Кроме того, отсутствие результатов отдельных конечных точек ограничили нашу возможность использовать регрессионный мета-анализ или метод косвенного сравнения. Наконец, все данные были основаны на наблюдательных исследованиях и могут быть искажены систематической ошибкой отбора: пациенты с худшим самочувствием и большим количеством сопутствующих заболеваний получают терапию ИПН и, следовательно, имеют повышенный риск нежелательных клинических исходов.
Заключения
Некоторые часто применяемые ИПН, ранее считавшиеся безопасными для одновременного применения с клопидогрелом, были связаны с повышенным риском нежелательных сердечно-сосудистых явлений. Несмотря на то, что данные получены по результатам наблюдений, они указывают на необходимость проведения рандомизированных контролируемых исследований или мета-анализов на уровне пациентов для оценки безопасности одновременного применения ИПН и клопидогрела у пациентов с ИБС.
Источники финансирования
Д-р Sherwood получил грант на обучение №5 T32 HL 7101-37 Национального института здравоохранения T-32. Jones: Гранты на научно-исследовательскую работу - Американской кардиологической ассоциации, компании AstraZeneca, Boston Scientific Corporation и Daiichi Sankyo.
Раскрытие информации
Отсутствует
Корреспонденцию направлять: Matthew W. Sherwood, врач, магистр валеологии, Институт клинических исследований при Университете Дьюка, 2400 Pratt Street, P.O. Box 17969, Durham, NC 27715. Список литературы 1. Jneid H, Anderson JL, Wright RS, Adams CD, Bridges CR, Casey DE Jr, Ettinger SM, Fesmire FM, Ganiats TG, Lincoff AM, Peterson ED, Philippides GJ, Theroux P, Wenger NK, Zidar JP, Anderson JL. 2012 ACCF/AHA Focused Update of the Guideline for the Management of Patients With Unstable Angina/Non-ST-Elevation Myocardial Infarction (Updating the 2007 Guideline and Replacing the 2011 Focused Update): A Report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. Circulation. 2012;126:875–910.
2. O’Gara PT, Kushner FG, Ascheim DD, Casey DE Jr, Chung MK, de Lemos JA, Ettinger SM, Fang JC, Fesmire FM, Franklin BA, Granger CB, Krumholz CB, Linderbaum JA, Morrow DA, Newby LK,
3. Ornato JP, Ou N, Radford MJ, Tamis-Holland JE, Tommaso JE, Tracy CM, Woo YJ, Zhao DX, Force CAT. 2013 ACCF/AHA Guideline for the Management of ST-elevation Myocardial Infarction: Executive Summary A Report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. Circulation. 2013;127:529–555.
4.Ho PM, Maddox TM, Wang L, Fihn SD, Jesse RL, Peterson ED, Rumsfeld JS. Risk of adverse outcomes associated with concomitant use of clopidogrel and proton pump inhibitors following acute coronary syndrome. JAMA. 2009;301:937–944.
5. O’Donoghue ML, Braunwald E, Antman EM, Murphy SA, Bates ER, Rozenman Y, Michelson AD, Hautvast RW, Ver Lee PN, Close SL, Shen L, Mega JL, Sabatine MS, Wiviott SD. Pharmacodynamic effect and clinical efficacy of clopidogrel and prasugrel with or without a proton-pump inhibitor: an analysis of two randomised trials. Lancet. 2009;374:989–997.
6.Ray WA, Murray KT, Griffin MR, Chung CP, Smalley WE, Hall K, Daugherty JR, Kaltenbach LA, Stein CM. Outcomes with concurrent use of clopidogrel and proton-pump inhibitors: a cohort study. Ann Intern Med. 2010;152:337–345.
7. Charlot M, Ahlehoff O, Norgaard ML, Jorgensen CH, Sorensen R, Abildstrom SZ, Hansen PR, Madsen JK, Kober L, Torp-Pedersen C, Gislason G. Proton-pump inhibitors are associated with increased cardiovascular risk independent of clopidogrel use: a nationwide cohort study. Ann Intern Med. 2010;153:378–386.
8. Melloni C, Washam JB, Jones WS, Halim SA, Hasselblad V, Mayer SB, Heidenfelder BL, Dolor RJ. Conflicting results between randomized trials and observational studies on the impact of proton pump inhibitors on cardiovascular events when coadministered with dual antiplatelet therapy: systematic review. Circ Cardiovasc Qual Outcomes. 2015;8:47–55.
9. Siller-Matula JM, Jilma B, Schror K, Christ G, Huber K. Effect of proton pump inhibitors on clinical outcome in patients treated with clopidogrel: a systematic review and meta-analysis. J Thromb Haemost. 2010;8:2624–2641.
10. Melloni C, Jones WS, Washam JB, Hasselblad V, Mayer SB, Halim S, Subherwal S, Alexander K, Kong DF, Heidenfelder BL, Irvine RJ, Wing L, Dolor RJ. Antiplatelet and Anticoagulant Treatments for Unstable Angina/Non-ST Elevation Myocardial Infarction. Rockville, MD: Agency for Healthcare Research and Quality (US); 2013 Nov. Report No.: 13(14)-EHC125-EF. AHRQ Comparative Effectiveness Reviews. AHRQ Comparative Effectiveness Reviews.
11. Kreutz RP, Stanek EJ, Aubert R, Yao J, Breall JA, Desta Z, Skaar TC, Teagarden JR, Frueh FW, Epstein RS, Flockhart DA. Impact of proton pump inhibitors on the effectiveness of clopidogrel after coronary stent placement: the clopidogrel medco outcomes study. Pharmacotherapy. 2010;30:787–796.
12. Simon T, Steg PG, Gilard M, Blanchard D, Bonello L, Hanssen M, Lardoux H, Coste P, Lefevre T, Drouet E, Mulak G, Bataille V, Ferrieres J, Verstuyft C, Danchin N. Clinical events as a function of proton pump inhibitor use, clopidogrel use, and cytochrome P450 2C19 genotype in a large nationwide cohort of acute myocardial infarction: results from the French Registry of Acute ST-Elevation and Non-ST-Elevation Myocardial Infarction (FAST-MI) registry. Circulation. 2011;123:474–482.
13. van Boxel OS, van Oijen MG, Hagenaars MP, Smout AJ, Siersema PD. Cardiovascular and gastrointestinal outcomes in clopidogrel users on proton pump inhibitors: results of a large Dutch cohort study. Am J Gastroenterol. 2010;105:2430–2436; quiz 2437.
14. Sterne JA, Gavaghan D, Egger M. Publication and related bias in meta-analysis: power of statistical tests and prevalence in the literature. J Clin Epidemiol. 2000;53:1119–1129.
15. Egger M, Davey Smith G, Schneider M, Minder C. Bias in meta-analysis detected by a simple, graphical test. BMJ. 1997;315:629–634.
16. Goodman SG, Clare R, Pieper KS, Nicolau JC, Storey RF, Cantor WJ, Mahaffey KW, Angiolillo DJ, Husted S, Cannon CP, James SK, Kilhamn J, Steg PG, Harrington RA, Wallentin L; Platelet Inhibition and Patient Outcomes Trial Investigators. Association of proton pump inhibitor use on cardiovascular outcomes with clopidogrel and ticagrelor: insights from the platelet inhibition and patient outcomes trial. Circulation. 2012;125:978–986.
17. Dunn SP, Steinhubl SR, Bauer D, Charnigo RJ, Berger PB, Topol EJ. Impact of proton pump inhibitor therapy on the efficacy of clopidogrel in the CAPRIE and CREDO trials. J Am Heart Assoc. 2013;2:e004564 doi: 10.1161/JAHA.112.004564.
18. Shah NH, LePendu P, Bauer-Mehren A, Ghebremariam YT, Iyer SV, Marcus J, Nead KT, Cooke JP, Leeper NJ. Proton Pump Inhibitor Usage and the Risk of Myocardial Infarction in the General Population. PLoS One. 2015;10:e0124653.
19. Cuisset T, Frere C, Quilici J, Poyet R, Gaborit B, Bali L, Brissy O, Morange PE, Alessi MC, Bonnet JL. Comparison of omeprazole and pantoprazole influence on a high 150-mg clopidogrel maintenance dose the PACA (Proton Pump Inhibitors and Clopidogrel Association) prospective randomized study. J Am Coll Cardiol. 2009;54:1149–1153.
20. Gilard M, Arnaud B, Cornily JC, Le Gal G, Lacut K, Le Calvez G, Mansourati J, Mottier D, Abgrall JF, Boschat J. Influence of omeprazole on the antiplatelet action of clopidogrel associated with aspirin: the randomized, double-blind OCLA (Omeprazole Clopidogrel Aspirin) study. J Am Coll Cardiol. 2008;51:256–260.
21. Bhatt DL, Cryer BL, Contant CF, Cohen M, Lanas A, Schnitzer TJ, Shook TL, Lapuerta P, Goldsmith MA, Laine L, Scirica BM, Murphy SA, Cannon CP. Clopidogrel with or without omeprazole in coronary artery disease. N Engl J Med. 2010;363:1909–1917.
