Превосходство агомелатина в сравнении с флуоксетином в антидепрессивной эффективности у пациентов с тяжелым БДР: рандомизированное двойное-слепое исследование
Статьи Superior antidepressant efficacy results of agomelatine versus fluoxetine in severe MDD patients: a randomized, double-blind studyAnthony Halea, Ricardo-Marcelo Corralb, Claudio Mencaccic, Jeronimo Saiz Ruizd, Cristina Albarran Severoe, Valentim Gentilf
a Trust Headquarters, St Martin's Hospital, Canterbury, UK, b Centro de Neuro Psiquiatria Cervino, Buenos Aires, Argentina, c Azienda Ospedaliera Fatebenefratelli e Oftalmico, Dipartimento di Salute Mentale, Milan, Italy, d Servicio de Psiquiatria, Hospital Ramon y Cajal, Madrid, Spain, e IRIS, Division Therapeutique de Neuropsychiatrie, Courbevoie, France u f Departamento e Instituto de Psiquiatria HCFMUSP, Sao Paulo, Brazil
Адрес для корреспонденции: проф. Anthony Hale, MBBS, PhD, FRCPsych, Trust Headquarters, St Martin's Hospital, Littlebourne Road, Canterbury, Kent, CT1 1AZ, UK
International Clinical Psychopharmacology 2010
Целью этого международного 8-недельного рандомизированного двойного-слепого исследования было подтверждение превосходства антидепрессивной эффективности агомелатина, первого антидепрессанта, действующего как агонист MT1/MT2 рецепторов и антагонист 5-HT2C рецепторов, в сравнении с флуоксетином у амбулаторных пациентов, соответствующих критериям Диагностического и статистического руководства по психическим расстройствам - том IV-TR для большого депрессивного расстройства тяжелой степени, с суммарным стартовым баллом Шкала депрессии Гамильтона (HAM-D17) не менее 25 и стартовым баллом шкалы CGI-Тяжесть заболевания не менее 4. Пациенты получали агомелатин 25-50 мг/сут (n = 252) или флуоксетин 20-40 мг/сут (n = 263) в течение 8 недель. Главным показателем эффективности был суммарный балл HAM-D17 (изменение стартового балла на момент последней послестартовой оценки). Дополнительными показателями эффективности были баллы Шкалы общего клинического впечатления (CGI), тяжесть (CGI-S), тревоги (HAM-A) и нарушений сна (пункты HAM-D для оценки сна). Средняя редукция суммарного балла HAM-D17 за 8 недель терапии была достоверно более выраженной при терапии агомелатином в сравнении с флуоксетином, различия между группами составили 1.49 балла (95% доверительный интервал, 0.20-2.77; P=0.024). Процент респондеров на момент последней послестартовой оценки был выше при терапии агомелатином по показателям шкалы HAM-D17 (снижение стартового суммарного балла > 50%; 71.7% агомелатин против 63.8% флуоксетин; P=0.060) и шкалы CGI-Улучшение (балл 1 или 2; 77.7 против 68.8%; P=0.023). Установлены достоверные различия между группами величиной в 0.37 балла (95% доверительный интервал, 0.060.68) по субшкале сна HAM-D в пользу агомелатина (P=0.018). Редукция баллов шкалы HAM-A при терапии агомелатином и флуоксетином была одинаковой. Оба препарата были безопасными и хорошо переносились пациентами. Таким образом в данном исследовании агомелатин превосходил флуоксетин по антидепрессивной эффективности в 8-недельной терапии пациентов с тяжелым эпизодом большого депрессивного расстройства, обнаруживая при этом благоприятный профиль переносимости.
Ключевые слова: агомелатин, антидепрессант, тревога, флуоксетин, большое депрессивное расстройство, сон
Введение
Агомелатин является первым мелатонинергическим антидепрессантом и действует как агонист MT1/MT2 рецепторов и антагонист 5-HT2C рецепторов (Yous et al., 1992; Audinot et al., 2003). Агомелатин открывает новый фармакологический подход, поскольку не влияет на внеклеточные уровни 5-HT (Millan et al., 2005). Показано, что агомелатин ресинхронизирует нарушенные циркадианные ритмы на моделях депрессии у животных (Fuchs et al., 2006) и у здоровых добровольцев (Krauchi et al., 1997; Leproult et al., 2005) и нормализует циркадианные ритмы у пациентов с депрессией на ранних этапах терапии (Quera Salva et al., 2007; Kasper et al., 2010), которые часто нарушаются при депрессии (Souetre et al., 1989; Peeters et al., 2006; Emens et al., 2009). Антидепрессивная эффективность агомелатина при кратковременной терапии пациентов с депрессией подтверждена в масштабных рандомизированных двойных-слепых плацебо-контролируемых исследованиях (Loo et al., 2002; Kennedy и Emsley, 2006; Olie и Kasper, 2007). Стойкость антидепрессивного эффекта агомелатина при длительной терапии показана в специальном рандомизированном исследовании симптомов отмены (Goodwin et al., 2009).
Антидепрессивная эффективность агомелатина также верифицирована в сравнении с активными препаратами в двух рандомизированных двойных-слепых исследованиях у пациентов с большим депрессивным расстройством (БДР), в которых антидепрессивный эффект был дополнительным показателем. По уровню антидепрессивной эффективности в рамках 6-недельной терапии агомелатин 25-50 мг/сут был сопоставим с селективным ингибитором обратного захвата серотонина и норадреналина (ИОЗСН) венлафаксином 75-150 мг/сут в соответствии с баллами Шкалы депрессии Гамильтона (HAM-D) (различие 0.92, NS) (Lemoine et al., 2007). В этом исследовании с участием 344 пациентов антидепрессивная эффективность агомелатина была связана с улучшением ночного сна, бдительности и функционирования в дневное время, а также достоверным изменением баллов Шкалы общего клинического впечатления (CGI-I) (Lemoine et al., 2007). В другом 6-недельном очном сравнительном исследовании с селективным ингибитором обратного захвата серотонина (СИОЗС) сертралином 50-100 мг/сут с участием 313 пациентов с депрессией установлены достоверные различия в пользу агомелатина в показателях относительной амплитуды цикла отдых-активность/сон-бодрствование по завершении 1 недели терапии и достоверно более выраженная редукция депрессивных симптомов в группе агомелатина в сравнении с сертралином в соответствии с динамикой суммарных баллов HAM-D через 6 недель лечения (различия 1.68, P<0.05) (Kasper et al., 2010).
Агомелатин также был эффективен в терапии пациентов с депрессией со стартовым суммарным баллом 17-пунктовой шкалы HAM-D (HAM-D17) не менее 25 (Montgomery и Kasper, 2007). Такие более тяжелые депрессии представляют особенно важную мишень для терапии, поскольку уровень нарушений функционирования и суицидальный риск значительно возрастают по мере утяжеления депрессивного состояния (Montgomery и Lecrubier, 1999). Более того, подтверждение эффективности при тяжелой депрессии является доказательством истинного антидепрессивного эффекта. Целью этого очного сравнительного исследования было подтверждение превосходства агомелатина 25-50 мг/сут в сравнении с СИОЗС флуоксетином 20-40 мг/сут в эффективности терапии пациентов с тяжелой депрессией с верификацией тяжести состояния на основании стартового суммарного балла шкалы HAM-D17. Кроме того предусматривалась оценка эффективности в коррекции нарушений сна и тревоги, а также переносимости.
Рисунок 1. Дизайн исследования. Включение и рандомизация проводились на одном и том же визите (неделя 0). Катамнестический визит назначался по завершении 8-й недели или после преждевременной отмены терапии.
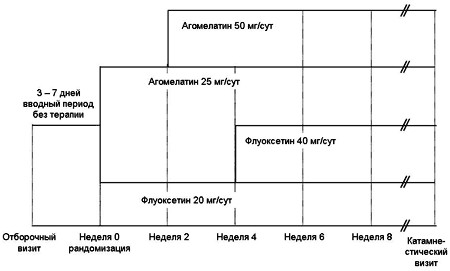
Методы
Дизайн исследования
Данное международное мультицентровое двойное-слепое рандомизированное с параллельными группами сравнительное исследование проводилось с 2005 по 2008 год в 41 клиническом центре в 5 странах (Аргентина, Бразилия, Италия, Испания и Великобритания) на амбулаторных пациентах с единичным или рекуррентным тяжелым БДР, требующим назначения терапии антидепрессантами. Исследование проводилось в соответствии с принципами Качественной клинической практики (Good Clinical Practice E6) Международной конференции по гармонизации (CPMP/ICH/135/95) и Хельсинской декларации, Финляндия, 1964 (пересмотр в Токио, 2004). Исследование было одобрено соответствующими местными этическими комитетами; в исследование включались только пациенты, давшие письменное информированное согласие.
Дизайн исследования представлен на рисунке 1. Через 3-7-дневного периода отмывки (в зависимости от периода полужизни препаратов предыдущей терапии) пациенты рандомизировались для терапии агомелатином (25 мг/сут) или флуоксетином (20 мг/сут) в течение 8 недель, визиты проводились через каждые 2 недели. В случае недостаточного клинического эффекта в соответствии с заранее определенными критериями доза агомелатина повышалась до 50 мг/сут по завершении первых 2-х недель терапии, а доза флуоксетина - до 40 мг/сут по завершении первых 4-х недель терапии в согласии с действующими инструкциями по применению этих антидепрессантов. Выбор доз флуоксетина определялся действующими инструкциями по применению флуоксетина в данной популяции пациентов (Reynolds, 1996). После такого повышения дозы препаратов оставались неизменными на протяжении всего периода терапии в исследовании.
Ни исследователи, ни пациенты не знали критериев неудовлетворительного эффекта и не были осведомлены о повышении дозы, которое проводилось централизованно с помощью интерактивной голосовой системы. На всем протяжении исследования все пациенты принимали по 2 капсулы препарата внутрь утром и 1 капсулу вечером, независимо от назначенной терапии и суточной дозы. В соответствии с действующими рекомендациями агомелатин назначался вечером, а флуоксетин - утром. Оба препарата были имели идентичный внешний вид и вкус на протяжении всего периода исследования. Упаковки и маркировки также были одинаковыми.
В качестве исследователей привлекались квалифицированные специалисты, прошедшие специальное обучение процедурам исследования до начала исследования для минимизации вариабельности оценок. До начала исследования и в ходе исследования также проводился тренинг исследователей по диагностике депрессии и измерениям по шкале HAM-D17 с помощью видеозаписей клинических интервью пациентов.
Выборка исследования
В исследование включались амбулаторные пациенты мужского и женского пола в возрасте от 18 до 65 лет, страдающие тяжелым БДР в соответствии с критериями Диагностического и статистического руководства по психическим расстройствам - том IV-TR (American Psychiatric Association, 2000), подтвержденными оценками по Краткому международному нейропсихиатрическому вопроснику (Mini-International Neuropsychiatry Interview; Sheehan et al., 1997). Для включения пациента требовалось, чтобы на отборочном визите суммарный балл шкалы HAM-D17 был не менее 25, балл Шкалы общего клинического впечатления-тяжесть (CGI-S) - не менее 4, а также присутствовало минимум 7 симптомов из пунктов A1-A9 диагностических критериев большого депрессивного эпизода (выраженное нарушение профессионального функционирования, привычной социальной активности или межличностных отношений) и был диагностирован единичный или рекуррентный эпизод длительностью не менее 4 недель. В интервале между отборочным визитом и визитом включения суммарный балл HAM-D17 не должен был снижаться более чем на 20%. При включении требовалось, чтобы суммарный балл по пунктам 1 (депрессивное настроение), 2 (чувство вины), 5 (средняя инсомния), 6 (поздняя инсомния в утренние часы), 7 (работа и другая активность), 8 (заторможенность), 10 (психическая тревога) и 13 (общие соматические симптомы) составлял не менее 55% от общего суммарного балла шкалы HAM-D17 для гарантии включения в выборку пациентов с предполагаемой тяжестью депрессии (Ruhe et al., 2005), а также было необходимо, чтобы суммарный балл HAM-D17 был не менее 25 и балл шкалы CGI-S -не менее 4.
Предусматривались следующие критерии исключения, касающиеся характеристик депрессивного эпизода: сезонность, психотические признаки и приуроченность манифестации к послеродовому периоду. Также исключались пациенты с выраженными суицидальными намерениями и/или отчетливыми суицидальными тенденциями в рамках текущего эпизода (4 балла по пункту 3 шкалы HAM-D17 или мнение исследователя), биполярным расстройством, симптомами тревоги, такими как панические атаки, обсессивно-компульсивным расстройством, посттравматическим стрессовым расстройством, злоупотреблением или зависимостью от психоактивных веществ, резистентностью текущего эпизода к флуоксетину, а также пациенты, получавшие электросудорожную терапию или формализованную психотерапию в течение последних 3-х месяцев или начавшие курс светотерапии в пределах последних 2-х месяцев. Исключались пациенты, не обнаружившие эффекта предыдущей терапии двумя разными антидепрессантами, назначенными в адекватных дозах (включая флуоксетин) с длительностью курсов терапии не менее 4-х месяцев для лечения текущего или предыдущих депрессивных эпизодов. Пациенты с неврологическими расстройствами (деменция, судорожные состояния и инсульт), либо тяжелыми или некомпенсированными органическими расстройствами (новообразование, кардиологическая, пульмонологическая, гастроэнтерологическая патология, нестабильный диабет 1 или 2 типа) не могли участвовать в исследовании. Запрещались для применения другие антидепрессанты, гипнотики, анксиолитики и нейролептики на протяжении всего периода исследования и в течение определенного периода до начала исследования в зависимости от периода полужизни препарата. В частности требовалась отмена терапии гипнотиками или анксиолитиками не позднее отборочного визита, однако при необходимости разрешалось применение золпидема в течение первых 2-х недель исследования (максимальная доза 10 мг/сут).
Показатели эффективности
Эффективность препаратов исследования в лечении депрессии оценивалась исследователями на каждом 2-недельном визите с помощью шкалы HAM-D17 (Hamilton, 1967) и шкал CGI-S и CGI-I (Guy, 1976). Главным критерием эффективности было изменение стартового суммарного балла HAM-D17 на момент последней послестартовой оценки. Суммарный балл HAM-D17 использовался для верификации тяжести депрессии и оценки динамики депрессивных симптомов. Дополнительными критериями эффективности были баллы шкал CGI-S и CGI-I, нарушений сна (по пунктам HAM-D для оценки инсомнии) и тревоги (общий суммарный балл шкалы HAM-A и суммарные баллы по подшкалам психической и соматической тревоги шкалы HAM-A). Шкала CGI-S использовалась для верификации тяжести психических расстройств, тогда как шкала CGI-I - для оценки общего улучшения состояния пациентов, начиная с 2-й недели терапии. В соответствии с показателями шкалы HAM-D17 респондерами считались пациенты с редукцией стартового суммарного балла не менее чем на 50%, а ремиссия квалифицировалась у пациентов с суммарным баллом не более 6. По показателям шкалы CGI-I респондерами считались пациенты с баллом 1 или 2, при этом пациенты с 1 баллом считались достигшими ремиссии. Эффекты препаратов исследования на симптомы тревоги оценивались исследователями по шкале HAM-A (Hamilton, 1959) на 8-й неделе (стартовая оценка на неделе 0) или ранее в случае преждевременного исключения. В рамках post-hoc анализов оценивалась эффективность коррекции нарушений сна по суммарным баллам инсомнии по шкале HAM-D (сумма баллов по пунктам 4, 5 и 6 шкалы HAM-D), а также эффект терапии на суммарный балл HAM-D17 за исключением пунктов инсомнии.
Показатели безопасности и комплаентность
Сообщаемые пациентами нежелательные явления регистрировались на каждом визите. Оценивались и регистрировались все соматические симптомы, сообщенные пациентами спонтанно или выявленные целенаправленными вопросами. В таких случаях исследователи по возможности определяли диагноз и регистрировали дату начала, исход, предпринятые меры и дату ремиссии или стабилизации нежелательных явлений. Исследователи также оценивали нежелательные явления в категориях тяжести, связи с терапией исследования и серьезности. Индекс массы тела, артериальное давление и частота сердечных сокращений в положении сидя, электрокардиограмма регистрировались на неделе 0, затем на неделе 8 или раньше в случае преждевременного исключения из исследования. Биохимические и гематологические анализы крови проводились на неделе 0, затем на неделе 8 или раньше в случае преждевременного исключения из исследования. Комплаентность оценивалась подсчетом количества возвращенных капсул на каждом визите, начиная со 2-й недели исследования, общая комплаентность рассчитывалась за 8-недельный период.
Статистический анализ
Было предусмотрено три выборки для статистических анализов. Выборка рандомизации включала всех включенных пациентов, прошедших рандомизацию (через интерактивную голосовую систему). Полная выборка (FAS) (формировалась по принципу общей выборки терапии [intention to treat]) включала пациентов из выборки рандомизации, которые приняли минимум одну дозу препарата исследования, прошли стартовую (неделя 0) оценку и минимум одну послестартовую оценку главного показателя эффективности за весь период от недели 0 до недели 8. Выборку безопасности составили все включенные пациенты, принявшие минимум одну дозу препарата исследования.
Все анализы эффективности проводились в выборке FAS с использованием метода замещения недостающего значения предыдущим (на основании последнего послестартового зарегистрированного показателя), достоверность статистических тестов была установлена на уровне 0.05 (двусторонние тесты). Главный анализ предусматривал оценку изменений стартового суммарного балла HAM-D17 на момент последней послестартовой оценки в течение 8 недель методом двустороннего ковариационного анализа по факторам терапии и центра (центр как случайный эффект) с использованием стартовых показателей в качестве ковариант, без взаимодействия. В качестве анализа чувствительности проводился нескорректированный анализ последних послестартовых измерений, основанный на t-тесте Стьюдента для независимых выборок. Кроме того изучались различия между агомелатином и флуоксетином в показателях терапевтического эффекта и ремиссии (Post-hoc анализ) на основании баллов шкалы HAM-D17 с учетом последних послестартовых значений и с помощью теста х . В анализе показателей шкалы CGI использовался t-тест Стьюдента для независимых выборок с целью сравнения терапевтических групп по баллам CGI-S и CGI-I на момент последней оценки и баллам CGI-S на 2-й неделе исследования (Post-hoc анализ). Терапевтические группы также сравнивались по процентам респондеров и пациентов в ремиссии по критериям CGI-I на момент последней оценки с помощью теста х2 (Post-hoc анализ).
Терапевтические группы сравнивались по изменениям суммарных баллов по трем пунктам инсомнии шкалы HAM-D и общим суммарным баллам шкалы HAM-D17 за исключением пунктов инсомнии на момент последней послестартовой оценки с помощью t-теста Стьюдента (Post-hoc анализ). Для сравнительного анализа терапевтических групп по общим суммарным баллам HAM-A, а также суммарным баллам подшкал психической и соматической тревоги HAM-A использовались методы дескриптивной статистики.
Дескриптивная статистика применялась для анализа данных по безопасности в обеих терапевтических группах за весь 8-недельноый период исследования.
Планируемый размер выборки рассчитывался на основании прогнозируемых финальных суммарных баллов HAM-D17 за 8-недельный период терапии в контексте различий между группами агомелатин и флуоксетина в рамках FAS с помощью двустороннего t-теста Стьюдента для независимых выборок на 5% уровне ошибки I типа. Установлено, что по 247 пациентов в каждой терапевтической группе обеспечит возможность выявления различий между группами с 85% мощностью для стандартного отклонения 7.4 баллов.
Рисунок 2. Диаграмма CONSORT.
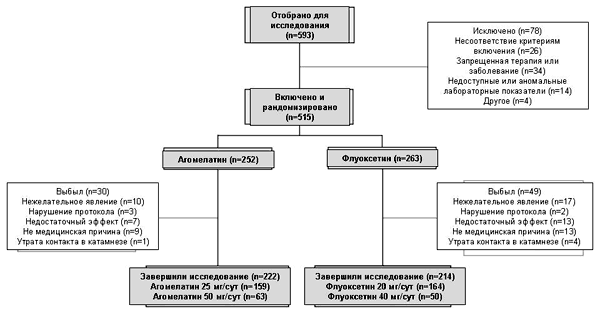
Результаты Пациенты
Диаграмма распределения пациентов в исследовании CONSORT представлена на рисунке 2. Из 593 пациентов, отобранных для исследования, 515 пациенты были включены и рандомизированы для терапии агомелатином (252 пациенты) или флуоксетином (263 пациенты) в течение 8 недель (выборка рандомизации). Выборку FAS составили 247 пациентов в группе агомелатина и 257 пациентов в группе флуоксетина (97.9% от выборки рандомизации), а выборку безопасности составили 250 пациентов в группе агомелатина и 263 пациента в группе флуоксетина.
Основные демографические характеристики и показатели заболевания представлены в таблице 1. Средний возраст пациентов в выборке составил 42.3 ±11.6 лет (от 18 до 65 лет), 77.7% были женского пола. В соответствии с критериями Диагностического и статистического руководства по психическим расстройствам - том IV-TR, 484 (94.0%) пациентов страдали тяжелым эпизодом БДР без психотических симптомов и 31 (6.0%) пациент - умеренным эпизодом БДР. Среднее число депрессивных эпизодов составило 2.5±2.1, включая текущий эпизод (медиана 2.0 эпизода, разброс от 1 до 20 эпизодов), при средней продолжительности заболевания 7.6±9.2 лет (медиана 4.3 лет) и a среднее duration of the current эпизод of 4.9 ± 3.9 месяцев (медиана 3 месяцев, разброс от 0-22 месяцев). Средний суммарный балл HAM-D17 составил 28.6±2.6 (разброс от 24 до 39). Средний балл CGI-S равен 5.0±0.6 (разброс от 4 до 6), что соответствует понятию «значительно болен». Средний суммарный балл HAM-A составил 26.1±7.0, средний балл психической тревоги равен 15.7±3.5, средний балл соматической тревоги равен 10.3±4.4. До начала исследования психофармакотерапию получали 239 (46.4%) пациентов, преимущественно СИОЗС (25.2%) и производные бензодиазепина (22.9%). Клинически значимых различий в стартовых показателях между терапевтическими группами в выборке рандомизации не установлено. Стартовые показатели в выборках FAS и выборке рандомизации были одинаковыми (таблица 1).
Таблица 1. Основные демографические данные и характеристики БДР на момент отбора или включения в выборку рандомизации.
| Агомелатин (n = 252) |
Флуоксетин (n=263) |
Все (n = 515) |
|
| Демографические характеристики | |||
| Возраст (лет) | 41.8 ±11.2 | 42.7 ±11.9 | 42.3 ±11.6 |
| Женский пол, n (%) | 194 (77.0) | 206 (78.3) | 400 (77.7) |
| Характеристики депрессии | |||
| Диагноз БДР, единичный эпизод по DSM-IV-TR, n (%) | 89 (35.3) | 99 (37.6) | 188 (36.5) |
| Умеренный, n (%) | 1 (0.4) | 7 (2.7) | 8 (1.6) |
| Тяжелый без психотических симптомов, n (%) | 88 (34.9) | 92 (35.0) | 180 (35.0) |
| Диагноз БДР, рекуррентный эпизод по DSM-IV-TR, n (%) | 163 (64.7) | 164 (62.4) | 327 (63.5) |
| Умеренный, n (%) | 13 (5.2) | 10 (3.8) | 23 (4.5) |
| Тяжелый без психотических симптомов, n (%) | 150 (59.5) | 154 (58.6) | 304 (59.0) |
| Число депрессивных эпизодов | 2.5±2.1 | 2.4±2.2 | 2.5±2.1 |
| Длительность заболевания (лет) | 8.2 ±9.6 | 7.0±8.8 | 7.6 ±9.2 |
| Длительность текущего эпизода (месяцев) | 5.0±3.9 | 4.8 ±3.8 | 4.9 ±3.9 |
| HAM-D17 суммарный балл | 28.5±2.7 | 28.7 ±2.5 | 28.6 ±2.6 |
| CGI-S | 5.0±0.6 | 5.0±0.6 | 5.0±0.6 |
| HAM-A | 25.9 ±7.0 | 26.3 ±7.0 | 26.1 ± 7.0 |
| Предыдущая психофармакотерапия, n (%) | 119 (47.2) | 120 (45 6) | 239 (46.4) |
| СИОЗС, n (%) | 63 (25.0) | 67 (25.5) | 130 (25.2) |
| Производные бензодиазепина, n (%) | 63 (25.0) | 55 (20.9) | 118 (22.9) |
| Антипсихотики, n (%) | 4 (1.6) | 6 (2.3) | 10 (1.9) |
| Литий, n (%) | 1 (0.4) | 2 (0.8) | 3 (0.6) |
| Карбамазепин, n (%) | - | 1 (0.4) | 1 (0.2) |
| Вальпроевая кислота, n (%) | 1 (0.4) | - | 1 (0.2) |
CGI-S, Шкала общего клинического впечатления - тяжесть; DSM-IV, Диагностическое и статистическое руководство по психическим расстройствам; HAMA-A, тревога; HAM-D, Шкала депрессии Гамильтона; БДР, большое депрессивное расстройство; СИОЗС, селективный ингибитор обратного захвата серотонина.
В сумме доза повышалась у 123 пациентов: 70 из 241 (29.0%) в группе агомелатина и 53 из 230 (23.0%) в группе флуоксетина. За 8-недельный период исследования преждевременно выбыли 30 пациентов в группе агомелатина (11.9%) в сравнении с 49 в группе флуоксетина (18.6%). Частота преждевременного исключения из-за нежелательных явлений и недостаточной эффективности была меньше при терапии агомелатином, чем флуоксетином, но различия не достигали уровня статистически достоверных (нежелательные явления, 4.0 против 6.5%, соответственно, P = 0.204; недостаточная эффективность, 2.8 против 4.9%, соответственно, P = 0.204).
Средняя длительность терапии в выборке рандомизации составила 53.4 ± 13.3 дней (медиана 57.0 дней), без значимых различий между терапевтическими группами. Общая комплаентность составила 94.5 ± 15.9% и была одинаковой в обеих группах.
Эффективность
В выборке FAS терапия агомелатином сопровождалась более выраженным снижением суммарного балла HAM-D17 (среднее изменение -17.3 ±7.3) в сравнении с флуоксетином (среднее изменение -16.0± 8.4) от недели 0 до последней до последней послестартовой оценки (таблица 2). Агомелатин статистически достоверно превосходил флуоксетин с различиями между группами E (SE) равными 1.49 (0.66) (P= 0.024). Эти результаты были подтверждены анализом чувствительности (нескорректированный анализ), в котором различия между группами в пользу агомелатина на момент последней послестартовой оценки составили 1.54 (0.71) (P= 0.030). На неделе 8 снижение стартового суммарного балла HAM-D было одинаковым в обеих группах: -18.4± 6.3 при терапии агомелатином и -18.1 ± 6.9 при терапии флуоксетином. В ходе анализа с поправкой на прием психофармакотерапии в анамнезе, стартовый суммарный балл HAM-D17 и центр подтверждены приведенные выше результаты и установлены статистически достоверные различия в пользу агомелатина в сравнении с флуоксетином в 1.57 (0.64) балла [95% доверительный интервал (CI), 0.31-2.83, P =0.015]. Процент респондеров по шкале HAM-D17 на момент последней послестартовой оценки составил 71.7% при терапии агомелатином и 63.8% при терапии флуоксетином, с тенденцией к статистической достоверности [E (SE), -7.85 (4.15), 95% CI, -15.98 - 0.28; P = 0.060] (таблица 3). Доля пациентов в ремиссии по шкале HAM-D17 на момент последней послестартовой оценки составила 32.0% в группе агомелатина в сравнении с 28.4% в группе флуоксетина [E (SE), -3.58 (4.09), 95% CI, -11.59 to 4.44; P= 0.381] (таблица 3).
Таблица 2. Сравнение агомелатина и флуоксетина за 8 недель исследования по главному критерию эффективности - суммарный балл HAM-D17, и дополнительным критериям эффективности: суммарный балл пунктов инсомнии HAM-D (сумма по пунктам 4, 5 и 6), суммарный балл HAM-D17 за исключением пунктов инсомнии, балл CGI-S и баллы HAM-A в полной выборке анализа (FAS).
| Агомелатин (n=247) |
Флуоксетин (n=257) |
|
| HAM-D17 суммарный балл | ||
| Стартовый показатель (неделя 0) | ||
| Среднее ±SD | 28.5±2.7 | 28.7 ±2.5 |
| Мин-макс | 24-39 | 25-38 |
| Последняя послестартовая оценка | ||
| Среднее ±SD | 11.1 ±7.3 | 12.7 ±8.5 |
| Мин-макс | 0-34 | 0-40 |
| Последняя послестартовая оценка - неделя 0 | ||
| Среднее ±SD | -17.3±7.3 | -16.0±8.4 |
| Мин-макс | -31 to 6 | - 38 to 8 |
| Различия между группами (главный анализ) | ||
| E(SE) | 1.49 (0.66) | |
| 95% CI | 0.20-2.77 | |
| P (ANCOVA) | 0.024 | |
| HAM-D балл по пунктам инсомнии | ||
| Стартовый показатель (неделя 0) (среднее ±SD) | 4.9±1.3 | 4.9±1.3 |
| Последняя послестартовая оценка (среднее ± SD) | 1.4±1.7 | 1.8 ±1.9 |
| Различия между группами | ||
| E (SE) | 0.37 (0.16) | |
| 95% CI | 0.06-0.68 | |
| P (t-тест Стьюдента) | 0.018 | |
| HAM-D17 без пунктов инсомнии | ||
| Стартовый показатель (неделя 0) (среднее ±SD) | 23.6 ±2.6 | 23.8±2.4 |
| Последняя послестартовая оценка (среднее ± SD) | 9.7 ±6.3 | 10.9 ±7.2 |
| Различия между группами | ||
| E (SE) | 1.17 (0.61) | |
| 95% CI | - 0.03 to 2.36 | |
| P (t-тест Стьюдента) | 0.055 | |
| CGI-S балл | ||
| Стартовый показатель (неделя 0) (среднее ±SD) | 5.0±0.6 | 5.0±0.6 |
| Последняя послестартовая оценка (среднее ± SD) | 2.6 ±1.3 | 2.8 ±1.4 |
| Различия между группами | ||
| E (SE) | 0.22 (0.12) | |
| 95% CI | -0.01 | to 0.45 |
| P (t-тест Стьюдента) | 0.059 | |
| HAM-A суммарный балл | ||
| Стартовый показатель (неделя 0) (среднее ±SD) | 26.0±7.0 | 26.4±7.0 |
| Последняя послестартовая оценка (среднее ± SD) | 11.1 ± 8.1 | 12.3±10.0 |
| Последняя послестартовая оценка - неделя 0 (среднее ± SD) | -14.7±9.5 | -14.2±10.3 |
| HAM-A балл психической тревоги | ||
| Стартовый показатель (неделя 0) (среднее ±SD) | 15.6 ±3.6 | 16.0±3.4 |
| Последняя послестартовая оценка (среднее ± SD) | 6.9 ±4.8 | 7.4±5.5 |
| Последняя послестартовая оценка - неделя 0 (среднее ± SD) | -8.6 ±5.5 | -8.7 ±5.6 |
| HAM-A балл соматической тревоги | ||
| Стартовый показатель (неделя 0) (среднее ±SD) | 10.4±4.3 | 10.3±4.5 |
| Последняя послестартовая оценка (среднее ± SD) | 4.2 ±3.9 | 4.9 ±5.0 |
| Последняя послестартовая оценка - неделя 0 (среднее ± SD) | -6.1 ±4.9 | -5.5±5.4 |
ANCOVA, ковариационный анализ; CGI-S, Шкала общего клинического впечатления - тяжесть; HAMA-A, Шкала тревоги Гамильтона; HAM-D, Шкала депрессии Гамильтона.
За период между неделей 0 и последней послестартовой оценкой средний балл CGI-S снизился в обеих группах выборки (таблица 2); установлены статистически достоверные различия между группами в пользу агомелатина (P = 0.059). Результаты post-hoc анализа на 2-й неделе свидетельствуют, что уже на этом визите стартовый средний балл CGI-S редуцировался в достоверно большей степени в группе агомелатина (4.2 ± 0.9 для агомелатина против 4.4 ± 0.9 для флуоксетина) [E (SE), 0.17 (0.08), 95% CI, 0.010.32; P= 0.035]. Сходным образом на момент последней послестартовой оценки средний балл CGI-I был ниже при терапии агомелатином чем при терапии флуоксетином, при этом различия были статистически достоверными [1.9 ± 1.0 против 2.1 ± 1.2; E (SE), 0.18 (0.10), 95% CI, -0.01 to 0.38; P = 0.063]. Процент респондеров на терапию по критерию шкалы CGI-I (балл 1 или 2) на момент последнего измерения за 8-недельный период составил 77.7% при терапии агомелатином и 68.8% при терапии флуоксетином (P = 0.023) (таблица 3). Различий в долях пациентов в ремиссии по критерию шкалы CGI-I (балл 1) не обнаружено (39.3 против 39.8%, соответственно, P= 0.896) (таблица 3).
Таблица 3. Сравнение эффективности агомелатина и флуоксетин на момент последней послестартовой оценки за 8 недель терапии по процентным долям респондеров и пациентов в ремиссии по критериям шкал HAM-D17 и CGI-I в полной выборке анализа.
| Агомелатин (n=247) |
Флуоксетин (n=257) |
|
| Шкала HAM-D17 | ||
| Респондеры на терапию на момент последней послестартовой оценки, n (%) | 177 (71.7) | 164 (63.8) |
| Различия между группами | ||
| E (SE) | -7.85 (4.15) | |
| 95% CI | -15.98 to 0.28 | |
| P (x2 тест) | 0.060 | |
| Пациенты в ремиссии на момент последней послестартовой оценки, n (%) | 79 (32.0) | 73 (28.4) |
| Различия между группами | ||
| E (SE) | -3.58 (4.09) | |
| 95% CI | -11.59 to 4.44 | |
| P (x2 тест) | 0.381 | |
| CGI-I балл | ||
| Респондеры на терапию на момент последней послестартовой оценки, n (%) | 192 (77.7) | 176 (68.8) |
| Различия между группами | ||
| E (SE) | -8.98 (3.92) | |
| 95% CI | -16.67 to 1.294 | |
| P (x2 тест) | 0.023 | |
| Пациенты в ремиссии на момент последней послестартовой оценки, n (%) | 97 (39.3) | 102 (39.8) |
| Различия между группами | ||
| E (SE) | 0.57 (4.36) | |
| 95% CI | -7.97 to 9.12 | |
| P (x2 тест) | 0.896 | |
Агомелатин оказывал достоверно более выраженное влияние на симптомы инсомнии. Средние баллы HAM-D по пунктам инсомнии (сумма баллов по пунктам инсомнии 4, 5 и 6 шкалы HAM-D) представлены в таблице 2. Установлены различия между группами E (SE) в 0.37 балла (0.16) в пользу агомелатина на момент последней послестартовой оценки (95% CI, 0.06-0.68; P =0.018, post-hoc анализ). Кроме того по результатам post-hoc анализа редукция суммарного балла HAM-D17 за исключением пунктов инсомнии была достоверно более выраженной в группе агомелатина с различиями между группами E (SE) в 1.17 балла (0.61) (95% CI, -0.03 to 2.36; P= 0.055) (таблица 2).
Оба препарата одинаково эффективно редуцировали симптомы тревоги. В выборке FAS зафиксирована сопоставимая редукция среднего суммарного балла HAM-A, а также баллов психической тревоги и соматической тревоги в периоде между неделе 0 и последней после-стартовой оценкой (таблица 2). На момент последней послестартовой оценки средний суммарный балл HAM-A снизился на 11.1±8.1баллов при терапии агомелатином и на 12.3±10.0 баллов при терапии флуоксетином. Безопасность
Не обнаружено значимых различий между группами в процентных долях пациентов в выборке безопасности, у которых отмечалось минимум одно нежелательное явление в периоде исследования (57.2% при терапии агомелатином и 56.3% при терапии флуоксетином). Случаев смерти не зафиксировано. В обеих терапевтических группах частота нежелательных явлений не зависела от дозы. Наиболее частыми нежелательными явлениями в соответствии с классификацией по органам и системам были гастроинтестинальные расстройства (26.4% для агомелатина и 26.6% для флуоксетина) и нарушения функции нервной системы (24.0 и 20.2%). Психические расстройства отмечались у 4.4% пациентов в группе агомелатина в сравнении с 7.6% пациентов в группе флуоксетина.
Наиболее частыми нежелательными явлениями были головная боль, тошнота и сонливость (таблица 4). Процент пациентов с минимум одним нежелательным явлением, расцененным как связанное с терапией, составил 38.4% в группе агомелатина и 41.1% в группе флуоксетина (P = 0.538, NS). Доли пациентов с минимум одним тяжелым нежелательным явлением равнялись 4.0% при терапии агомелатином и 5.3% при терапии флуоксетином (P= 0.478, NS). У большинства пациентов с нежелательными явлениями наблюдалась полная их редукция (93.0% при терапии агомелатином против 92.4% при терапии флуоксетином).
Таблица 4. Наиболее частые нежелательные явления (возникавшие у более 2% пациентов) за 8 недель терапии в выборке безопасности (все включенные пациенты, принявшие минимум одну дозу терапии исследования)
| Агомелатин (n = 250) | Флуоксетин (n=263) | |||
| N | n (%) | N | n (%) | |
| Головная боль | 43 | 40 (16.0) | 33 | 30 (11.4) |
| Тошнота | 20 | 20 (8.0) | 32 | 30 (11.4) |
| Сонливость | 15 | 15 (6.0) | 9 | 9 (3.4) |
| Верхняя абдоминальная боль | 11 | 11 (4.4) | 7 | 7 (2.7) |
| Назофарингит | 10 | 10 (4.0) | 2 | 2 (0.8) |
| Сухость во рту | 9 | 8 (3.2) | 8 | 8 (3.0) |
| Запор | 8 | 8 (3.2) | 3 | 3 (1.1) |
| Головкружение | 7 | 7 (2.8) | 9 | 9 (3.4) |
| Диарея | 7 | 7 (2.8) | 7 | 7 (2.7) |
| Грипп | 6 | 6 (2.4) | 7 | 7 (2.7) |
| Рвота | 5 | 5 (2.0) | 7 | 7 (2.7) |
Средние показатели массы тела, артериального давления и частоты сердечных сокращений оставались стабильными в обеих терапевтических группах и на каждой дозе за весь 8-недельный период терапии. Несмотря на отсутствии различий между терапевтическими группами в медианах значений показателей печени у 5 пациентов (n=4 в группе агомелатина против n=1 в группе флуоксетина) отмечалось повышение уровней ферментов печении более чем в 3 раза превосходящее верхнюю границу нормы. Ни в одном из этих случаев повышение трансаминаз не сопровождалось какими либо клиническими признаками и полностью редуцировалось у всех пациентов (на фоне продолжающейся терапии). Не обнаружено клинически значимых различий между терапевтическими группами или подгруппами разных доз препаратов в изменениях гематологических или биохимических параметров крови.
Обсуждение
Выполнено первое сравнительное исследование эффективности агомелатина и флуоксетина в терапии амбулаторных пациентов с тяжелым БДР. Полученные результаты свидетельствуют, что агомелатин превосходит флуоксетин по уровню антидепрессивной эффективности ( P= 0.024): различия между группами средних суммарных баллах HAM-D17 за 8 недель терапии составили 1.49 балла. Следует отметить, что в изученной выборке пациентов с тяжелой депрессией улучшение баллов шкалы CGI-S при терапии агомелатином начиналось уже на 2 неделе терапии (P= 0.035 в сравнении с флуоксетином) и это преимущество агомелатина сохранялось вплоть до финальной оценки через 8 недель лечения ( P = 0.059), что согласует с данными предыдущих публикаций о раннем развертывании терапевтического эффекта агомелатина (Loo et al., 2002). Приведенное наблюдение подкрепляется различиями между группами в баллах шкалы CGI-I балл, которые достигают уровня статистически достоверных на момент последней оценки (P= 0.063). Доли респондеров также были выше в группе агомелатина в сравнении с флуоксетином по критериям как шкалы HAM-D17 (71.7 против 63.8%, P = 0.060), так и шкалы и CGI-I (77.7 против 68.8%, P= 0.023). Эти результаты свидетельствуют, что агомелатин является ценной альтернативой флуоксетину в терапии тяжелой депрессии. Показатели частоты ремиссии (32.0% при терапии агомелатином и 28.4% при терапии флуоксетином) могут выглядеть низкими, однако следует учитывать кратковременность исследования и более строгий, а именно - на 1 балл ниже, чем обычно, критерий ремиссии по шкале HAMD (< 6 баллов).
Антидепрессивная эффективность агомелатина у пациентов с более тяжелой депрессией (HAM-D > 25) доказана результатами анализов данных 3-х двойных-слепых рандомизированных плацебо-контролируемых исследований (Loo etaZ, 2002; Kennedy и Emsley, 2006; Olie и Kasper, 2007), а также мета-анализа объединенных данных этих исследований (Montgomery и Kasper, 2007). Результаты нашего исследования, в котором принимались специальные меры для исключения пациентов, более чувствительных к одному препарату, чем к другому, подтверждают стойкость антидепрессивного эффекта агомелатина у пациентов с тяжелой депрессией.
Полученные данные о превосходстве агомелатина в сравнении с флуоксетином могут рассматриваться как противоречащие результатам другого плацебо-контролируемого исследования, в котором флуоксетин использовался в качестве валидатора и достоверно отличался от плацебо, тогда как агомелатин не обнаруживал отличий от плацебо (European Medicines Agency, 2009). Однако в указанном исследовании предусматривалось подтверждение антидепрессивного эффекта агомелатина в сравнении с плацебо, но не сравнение агомелатина с флуоксетином, а флуоксетин использовался лишь как средство измерения чувствительности исследования; соответственно это исследование не имело достаточной мощности для сравнительной оценки агомелатина и флуоксетина. Подобные неоднозначные результаты довольно типичны для плацебо-контролируемых исследований с тремя терапевтическими группами и, как правило, объясняются методологическими проблемами (Committee for Proprietary Medicinal Products, 2002). Действительно, плацебо-контролируемые исследования могут в одинаковой степени вызывать тревогу у пациентов и исследователей, что может быть причиной существенного искажения в отборе депрессивных пациентов для выборки исследования (Melander et al., 2008). Следовательно более адекватным представляется непосредственное сравнение антидепрессантов без плацебо, что повышает валидность сравнительных оценок эффективности. Более того, данные о превосходстве одного препарата над другим по главному показателю эффективности, полученные в очном сравнительном исследовании, считаются наиболее убедительными (Montgomery et al., 2007).
Клиническая значимость различий между терапевтическими группами в баллах шкалы HAM-D представляется спорной. В свою очередь данные о превосходстве одного препарата над другим, полученные на большом числе пациентов представляются клинически убедительными, но редко встречаются в литературе. Более того, различия в 1.5 балла в суммарных баллах HAM-D17 в пользу агомелатина в сравнении с флуоксетином могут расцениваться как клинически значимые, особенно с учетом отличий активных препаратов от плацебо в 2-3 балла в позитивных плацебо контролируемых исследованиях СИОЗС/ИОЗСН (Khan et al., 2000; Kirsch et al., 2002). Считается, что различия в половину от величины различий с плацебо, т.е. 1.5 балла, могут быть обоснованным критерием сравнения активных препаратов. Ранее сообщалось, что агомелатин 25-50 мг/сут статистически достоверно превосходит по эффективности СИОЗС, как было показано в сравнительном исследовании с сертралином 50100 мг/сут (Kasper et al., 2010). Агомелатин также сравнивался с ИОЗСН венлафаксином 75150 мг/сут, который он превосходил по эффективности в соответствии с показателями шкалы CGI-I, а также отличался более быстрым эффектом и более высокой эффективностью в улучшении активности и функционирования в дневное время, а также субъективных показателей сна (Lemoine et al, 2007). В обоих указанных исследованиях антидепрессивная эффективность была дополнительным критерием сравнения. Соответственно результаты нашего исследования можно считать более вескими с научной точки зрения, поскольку именно антидепрессивная эффективность была главным критерием сравнения препаратов.
Данные о том, что агомелатин превосходит по эффективности флуоксетин, сертралин и венлафаксин, следует рассматривать с учетом печально известных затруднений в установлении значимых различий между антидепрессантами второго поколения (Hansen etaZ, 2005; Nemeroff и Thase, 2007). В недавно опубликованном анализе, в котором использовались данные очных и опосредованных сравнений 12 антидепрессантов новых поколений, сертралин и эсциталопрам выделены как препараты с наилучшим балансом эффективности и переносимости (Cipriani et al., 2009). Также получены доказательства превосходства венлафаксина при его сравнении с СИОЗС как классом, а также непосредственно с флуоксетином (Hansen et al., 2005; Papakostas et al., 2007; Nemeroff et al,2008). Эти данные представляются особенно важными учитывая клинически достоверные преимущества агомелатина в сравнении с сертралином, венлафаксином и флуоксетином (Kennedy и Rizvi, 2010).
Результаты анализа дополнительных показателей эффективности в нашем исследовании свидетельствуют, что антидепрессивный эффект агомелатина может быть связан с воздействием на симптомы сна и тревоги. Влияние агомелатина на нарушения цикла сон-бодрствование хорошо известно (Lemoine et al., 2007; Quera Salva et al., 2007; Kasper et al, 2010). По данным некоторых исследований флуоксетин также оказывает благоприятное влияние на сон (Stephenson et al., 2000). Нарушения сна составляют важный компонент депрессии, поэтому их коррекция представляется важным условием терапии антидепрессантами пациентов с БДР (Ohayon и Roth, 2003). Пункты 5 (средняя инсомния) и 6 (поздняя инсомния) шкалы HAM-D отражают типичные симптомы нарушений сна при депрессии и считаются столь же чувствительными к эффектам терапии антидепрессантами, как шесть пунктов HAM-D, формирующих подшкалу Бека HAM-D6 (Santen et al., 2008). Более выраженное улучшение сна при терапии агомелатином может быть частично связано с общим превосходством агомелатина над флуоксетином, установленным по суммарным баллам HAM-D17, хотя различия между этими препаратами сохраняются и после удаления пунктов сна из общего балла шкалы HAM-D17 (P = 0.055). В нашем исследовании симптомы тревоги редуцировались в одинаковой степени при терапии агомелатином и флуоксетин. Эти данные подтверждают результаты других исследований терапии пациентов с депрессией с применением агомелатина (Loo et al., 2002; Kasper et al., 2010) и флуоксетина (Spalletta et al, 2002).
В нашем исследовании также получены дополнительные доказательства благоприятного профиля переносимости агомелатина. Частота нежелательных явлений в нашем исследования была низкой, а доли пациентов с преждевременной отменой терапии за весь период исследования боли одинаковыми в обеих терапевтических группах. В течение исследования не наблюдалось никаких клинически значимых изменений витальных показателей и биологических параметров за исключением аномального повышения ферментов печение у 5 пациентов, получавших агомелатин, и 1 пациента в группе флуоксетина. Эти данные согласуются с результатами других исследований агомелатина (Loo et al., 2002; Kennedy и Emsley, 2006; Lemoine et al., 2007; Olie и Kasper, 2007; Goodwin et al., 2009; Kasper et al., 2010; Kennedy и Rizvi, 2010), в которых переносимость агомелатина была сопоставима с переносимостью плацебо и фиксировалась низкая частота преждевременной отмены терапии. Кроме того показано, что прекращение приема агомелатина не приводит к развитию симптомов отмены (Montgomery et al., 2004). В сочетании с высоким антидепрессивным эффектом это ключевое преимущество агомелатина может способствовать приверженности пациентов длительной терапии, успешной поддерживающей терапии и, в конечном итоге, высокому качеству ремиссии (Goodwin et al., 2009).
Полученные нами данные подтверждают предположение о том, что антидепрессивный эффект агомелатина реализуется редукцией всего широкого спектра симптомов депрессии (Dubocovich, 2006). Так, при терапии агомелатином улучшение настроения сопровождается редукцией сопутствующей тревоги и нормализацией циркадианных ритмов, включая цикл сон-бодрствование. Способность агомелатина воздействовать на все компоненты БДР в сочетании с хорошей переносимостью обеспечивают успех терапии у широкого круга пациентов с депрессией, включая тяжелые депрессии. Подобные свойства обусловлены инновационным механизмом действия агомелатина относительно других антидепрессантов, так как агомелатин является агонистом MT1/MT2 рецепторов и антагонистом 5-HT2C рецепторов (Papp et al., 2003; Bertaina-Anglade et al., 2006; Soumier et al., 2009).
В числе возможных ограничений нашего исследования можно указать относительно высокий стартовый балл HAM-D17, требовавшийся для включения пациентов выборку исследования, что привело к накоплению в выборке пациентов с тяжелой депрессией, в связи с чем выборку исследования нельзя считать полностью репрезентативной относительно всей популяции больных депрессией в клинической практике. Тем не менее известно, что агомелатин полностью сопоставим с СИОЗС и ИОЗСН, такими как сертралин и венлафаксин, в терапии пациентов с умеренными и тяжелыми большими депрессивными эпизодами в соответствии со стартовыми суммарными баллами HAM-D17, равными 20 или 22 (Lemoine et al., 2007; Kasper et al., 2010).
Другим недостатком нашего исследования могут быть различия в сроках повышения стартовых доз сравниваемых антидепрессантов: доза агомелатина повышалась через 2 недели, а доза флуоксетина - через 4 недели после начала терапии. Однако такой распорядок повышения стартовых доз полностью соответствует официальным инструкциям по применению этих двух препаратов. Более того, более раннее повышение дозы в группе флуоксетина могло негативно сказаться на результатах лечения вследствие возможно повышения частоты преждевременной отмены терапии.
Таким образом, результаты проведенного исследования свидетельствуют о превосходстве агомелатина над флуоксетином в эффективности терапии пациентов с тяжелой депрессией. В феврале 2009 года агомелатин был одобрен Комитетом по медицинским продуктам для применения у человека (Committee for Medicinal Products for Human Use ) при Европейском медицинском агентстве (European Medicines Agency) для терапии БДР. Учитывая явную эффективность и благоприятный профиль переносимости можно считать агомелатин оптимальным средством терапии для всех пациентов с депрессией, включая больных, страдающих тяжелой депрессией.
Конфликт интересов
Данное исследование проводилось при поддержке компании Сервье. Авторы получали от Сервье гонорары и/или исследовательские гранты. Кроме заявленных выше авторы не имеют никаких других значимых профессиональных или финансовых отношений с какими либо организациями, конфликтующих с предметом и материалами данной публикации.
Список использованной литературы
