Пятидесятилетний опыт в производстве противогриппозных вакцин
Статьи ВведениеМасштабы бедствия
Грипп - это острое инфекционное заболевание, передающееся воздушно-капельным путем и поражающее верхние дыхательные пути. Заболевание вызывается вирусом, относящимся к семейству миксовирусов.
По своей социальной значимости грипп находится на первом месте среди всех болезней человека.(3). Заболеваемость гриппом и острыми респираторными вирусными инфекциями (ОРВИ) превышает суммарную заболеваемость всеми остальными инфекциями: в период эпидемии гриппа на их долю приходится10-50% временной нетрудоспособности населения, а в остальное время года - более 80% всей инфекционной патологии, до 40% всех заболеваний взрослых и более 60% заболеваний детей.
Интерес к возникновению новых вирусов гриппа возрос в связи с угрозой пандемии после вспышки гриппа в Гонконге в 1997 г.‚ сотрудничестве со всемирной организацией здравоохранения (ВОЗ) Европейская рабочая группа по изучению гриппа разработала план действий, призванных помочь странам адекватно реагировать при возникновении в будущем опасности пандемии (14).
Пандемии, развившиеся в 1918, 1957 и затем в 1968 годах, стоили жизни многим миллионам людей во всем мире, причем знаменитая "испанка" (в 1918 г.) унесла больше жизней, чем первая мировая война. Удары, наносимые гриппом в настоящее время, конечно же, менее драматичны, и, возможно, именно по этой причине грипп недооценивается, хотя так или иначе он продолжает собирать свою скорбную жатву каждый год.
ВОЗ прогнозирует появление нового варианта вируса гриппа, что может привести к пандемии гриппа, аналогичной пандемии 1918-1920 гг., когда умерло более 20 млн. человек.
Вирус гриппа
Вирус гриппа самостоятельно внедряется в мерцательный эпителий, выстилающий внутреннюю поверхность воздухоносных путей. Попав туда, он размножается в клетках, поглощая содержащиеся в них субстанции, так что к тому времени, когда образуются новые вирусы, все эти клетки оказываются полностью разрушенными.
Размножение вирусов протекает с исключительно высокой скоростью: через 24-48 часов после проникновения в клетки отдельных вирусных частиц образуется такое количество новых вирусов, которого достаточно для поражения всего эпителия легких. Следствием этого является то, что эпителиоциты респираторного тракта разрушаются иногда до базального слоя.
Физиологической функцией мерцательного эпителия является очищение дыхательных путей от пыли, бактерий и т. д. Если мерцательный эпителий разрушается, он уже не может в полной мере выполнять свои функции, и бактерии с большей легкостью проникают в легкие. Поврежденный эпителий содержит множество лазеек для бактерий, и таким образом появляется опасность развития бактериальной суперинфекции.
Описанная выше активность вируса гриппа объясняет основное различие между гриппозной инфекцией и другими острыми респираторными заболеваниями (ОРЗ), которые не всегда сопровождаются подобного рода поражениями или вообще не вызывают их.
Вирус гриппа обладает способностью видоизменяться. Ежегодно он мутирует и дает новые штаммы.

Рис. 1. Схематическое изображение вируса гриппа.
Различают три типа вируса гриппа - А, В и С:
- А вызывает крупные эпидемии и пандемии, характеризуется быстрым распространением, высокой инфекционностью (заболеваемость - смертность) и лабильностью антигенной структуры (мутации).
- В обладает постоянством антигенной структуры: менее подвержен мутациям.
- С обладает постоянством антигенной структуры, малозначим в патологии человека.
Медико-социальные последствия гриппа
Заболеваемость и смертность
Тяжелые клинические осложнения, развивающиеся после гриппа, такие как пневмония, бронхиты, вторичные бактериальные инфекции верхних дыхательных путей (отиты, синуситы), осложнения со стороны нервной и сердечно-сосудистой систем или обострение основного заболевания (сахарного диабета, сердечной недостаточности, хронических обструктивных бронхопневмопатий и т.д.), весьма часты и опасны среди престарелых и ослабленных людей.
Во время эпидемии гриппа 1989 г. количество случаев пневмонии, среднего отита и острого бронхита возросло в Англии и Уэльсе соответственно на 70%, 25% и 26%. В тот же период было зарегистрировано и увеличение показателя смертности, которое составило 30% (7). В Нидерландах вследствие осложнений, обусловленных гриппом, в период с 1967 по 1989 г. в среднем ежегодно умирало 2000 человек (16, 17). В настоящее время грипп является второй после пневмококковой инфекции причиной смерти от инфекционных заболеваний.
В России грипп и другие ОРВИ в структуре заболеваемости инфекционными болезнями составляют 95%. Ежегодно регистрируется смертность от гриппа.
Грипп - самая важная сегодня проблема среди рутинной инфекционной патологии, регистрируемой в России, и по экономическим потерям, и по тому урону, который он наносит здоровью популяции.
В 2000 г. в России гриппом переболело от 4% до 9% населения (на 27% больше, чем в 1999 г.). Ежегодно экономический ущерб от респираторных инфекций и гриппа составляет в среднем 10-12 млрд. руб.(4).
"Отношение населения к проблеме гриппа - традиционно поверхностное. Это объясняется псевдолегкостью течения: несколько дней человек потемпературил, полежал, а то и перенес заболевание на ногах. В результате - тяжелые осложнения, которыми и опасен грипп: страдают сердечно-сосудистая, другие жизненно важные системы организма. Ежегодно мы регистрируем 3-5 млн. случаев гриппа в нашей стране, десятки миллионов случаев ОРЗ. И все из-за того, что недооцениваем реальную опасность этого заболевания. Стратегия и тактика нашей специфической борьбы против гриппа - вакцинопрофилактика" (3).
Социально-экономический ущерб
Основные затраты на медицинскую помощь во время эпидемий гриппа составляют расходы на стационарное лечение, тем или иным образом связанное с гриппом. Число стационарных больных из групп повышенного риска увеличивается во время эпидемий гриппа в 2-5 раз. Это соответствует приблизительно 800 дополнительным случаям госпитализации на 100 000 жителей, относящихся к группам повышенного риска. Если экстраполировать эти данные и принять во внимание, что 20% всего населения входит в группы повышенного риска, это составит более 1600 дополнительных случаев госпитализации в период эпидемии на 1 миллион жителей.
Дополнительные расходы в Соединенных Штатах Америки в период каждой эпидемии гриппа только на стационарное лечение составляют более 300 миллионов долларов. Во время эпидемий бывают особенно высоки потери рабочих дней по нетрудоспособности. Как, например, в США в этот период регистрируется 52 миллиона случаев респираторных заболеваний, связанных гриппом, со средней продолжительностью 11,4 дня, следовательно, число потерянных рабочих дней составляет свыше 600 миллионов (10, 18). Таким образом, любая страна несет значительные убытки, связанные со снижением эффективности производства, а также дополнительными расходами на амбулаторное и стационарное лечение (10).
Не заболеть гриппом экономически выгодно не только стране в целом, но и отдельно каждому человеку. Как минимум грипп нарушает планы семьи, что может повлечь за собой экономический и моральный урон. В случаях осложнений после гриппа экономические потери семьи возрастают во много раз. Каковы неблагоприятные последствия заболевания ребенка: это ослабление организма, отставание в школе, возможность заражения членов семьи, тяжелые осложнения, которые чаще встречаются у детей, больничный лист для родителей.
Последствия заболевания гриппом в рабочее время
Возникновение проблем со здоровьем у работников может иметь множество негативных последствий для компании, в которой они работают. Это связано с невыходом на работу, потерей производительности и даже преждевременной смертью работников.
Основным аспектом проблемы гриппа является невыход на работу: больной, как правило, бывает вынужден оставаться в постели от 3 до 5 дней и утрачивает работоспособность в среднем на 5-10 дней (в случае осложнений - до 1 мес). В связи с этим происходит значительное снижение уровня производства и стагнация в сфере услуг.
Точно так же грипп нарушает порядок работы больниц, транспортных предприятий, гостиниц и других институтов, обладающих высокой социальной значимостью. Независимо от мер, принимаемых с целью ограничения экономических последствий, эти проблемы в конечном итоге приводят к потере производительности или увеличению издержек. Издержки в связи с заболеванием всегда следует подразделять на прямые, которые представляют собой собственно медицинские издержки (оплату труда медицинских работников, лекарственных средств, госпитализации и т.д.) и косвенные, которые главным образом связаны с затратами компании (невыход сотрудников на работу, снижение производительности и т.д.). При этом косвенные издержки, как правило, составляют половину всех затрат, связанных с болезнью.
Последствия для работодателя:
- Спад производства, который может быть компенсирован только увеличением расходов.
- Невыполнение планов и обязательств в срок.
- В некоторых странах работодатель обязан оплачивать отсутствующему на работе сотруднику определенное время невыхода на работу, несмотря на его бездействие.
- Для того чтобы поддержать общую производительность компании, работодатель вынужден находить временную замену отсутствующему сотруднику, либо просить его коллег работать сверхурочно, причем и в том и в другом случае возникают дополнительные затраты.
- Снижение эффективности труда вследствие повышенной нагрузки на здоровый персонал.
- Если не будут приняты такие компенсирующие меры, рентабельность компании может пострадать.
Последствия для сотрудника:
- Как минимум финансовые потери выражаются в уменьшении дохода за период утраты трудоспособности.
- Увеличение расходов на медицинское обслуживание (необходимость консультации врача и приобретения лекарственных средств).
- Повышенная нагрузка на работе после болезни (необходимо "наверстать упущенное").
- Повышение риска потерять работу.
Медицинские преимущества
Вакцинация является наиболее эффективной мерой, обеспечивающей профилактику гриппа и установление контроля над этим заболеванием (19).
В 1950 г. доктор А.Й.Клейн и доктор Э.Херцбергер опубликовали в журнале "Philips Technicзl Review" статью, в которой дается описание иммунизации населения с применением вакцины: "Благодаря иммунизации мы уже практически в течение 10 лет можем бороться с вирусом гриппа. Заболевание гриппом часто протекает в более или менее безобидных формах, а потому основная часть населения склонна недооценивать серьезность этого заболевания. В связи с этим позволим себе напомнить об ужасной эпидемии гриппа 1918-1919 гг., которая поразила все население планеты и, по оценкам, унесла жизни 20 миллионов человек. Это демонстрирует также, насколько важны меры профилактики этого заболевания. Было бы, однако, ошибкой оценивать серьезность данной инфекции только на основе показателей смертности. Эпидемии гриппа даже без значительного числа смертельных случаев постоянно вспыхивают раз в год или чаще, нанося большой урон экономике государства, так как в течение нескольких недель значительная часть работающего населения не может нормально выполнять свои производственные обязанности. Имеющиеся в настоящее время в нашем распоряжении возможности иммунизации отдельных групп или всего населения следует рассматривать и с медицинской, и с социально-экономической точки зрения как важное достижение".
Приведенные слова докторов Клейна и Херцбергера и спустя 50 лет по-прежнему сохраняют свою актуальность.
Грипп - это острое респираторное вирусное заболевание, единственная инфекционная болезнь, дающая пандемии с острым течением, великое бедствие планеты, но от него можно надежно предохраниться при помощи вакцинации. Министерства здравоохранения, специалисты-медики, представители фармацевтической промышленности и другие работники здравоохранения различных стран мира отмечают высокую надежность и безопасность вакцинопрофилактики гриппа (3).
Для того чтобы создать вакцину из актуального штамма, существует система мониторинга, патронируемая ВОЗ. Через лаборатории ВОЗ, расположенные по всему миру, выделяется изолят актуальных штаммов, доводится до вакцинного штамма и распространяется по фармацевтическим компаниям, производящим вакцину.

Система мониторинга
Безопасность современных вакцин, отвечающих международным стандартам очистки и эффективности, не подвергается сомнению. Эффективность вакцинации наглядно демонстрируется на примере лиц, входящих в группы повышенного риска. У людей пожилого возраста она существенно снижает частоту случаев пневмонии, госпитализации и смерти, обусловленных гриппом. Вакцинация значительно уменьшает уровень заболеваемости гриппом, а у заболевших "смягчает" клиническое течение болезни, сокращает ее длительность и предупреждает смертельные исходы (11).

Рис. 2. Оценка эффективности вакцинации против гриппа - результаты мета-анализа 20 исследований.
Группы лиц, которым рекомендуется целенаправленно проводить ежегодную вакцинацию против гриппа*(12, 13).
Группы повышенного риска развития осложнений и увеличения летальности вследствие гриппа
- Все лица старше 60 лет.**
- Находящиеся в стационарных медицинских учреждениях или страдающие хроническими заболеваниями и вынужденные постоянно посещать медицинские учреждения.
- Взрослые и дети, страдающие заболеваниями почек, сахарным диабетом, хроническими легочными, сердечно-сосудистыми заболеваниями, включая больных бронхиальной астмой.
- Взрослые и дети с иммунной недостаточностью, в том числе‚ ВИЧ-инфицированные и лица, получающие иммунодепрессанты.
- Дети и подростки (от 6 месяцев до 18 лет), получающие длительное лечение ацетилсалициловой кислотой (аспирин) и поэтому подверженные риску развития синдрома Рея.
- Беременные женщины, относящиеся к группам повышенного риска.
*В странах Европы существуют разные рекомендации относительно групп населения, которым следует проводить вакцинацию. Рекомендации большинства европейских стран согласуются с рекомендациями, действующими в США.
** Возраст лиц, которым рекомендуется активно проводить вакцинацию, составляет в Европе и в США 60 лет.
Лица, которые могут передавать вирус гриппа другим людям, входящим в группы повышенного риска:
- Врачи, медицинские сестры и другой персонал стационарных медицинских учреждений; стационарные больные или хронически больные, вынужденные постоянно посещать медицинские учреждения.
- Медицинские работники и иные служащие, оказывающие помощь на дому лицам, относящимся к группам повышенного риска.
- Члены семей больных, относящихсяк группам повышенного риска (включая детей).
Вакцинация лиц из групп повышенного риска преследует двойную цель - она защищает данных пациентов и препятствует заражению других людей.
Следует особо подчеркнуть важность вакцинации всех лиц, занятых в сфере здравоохранения. Необходимость вакцинации медицинских работников объясняется следующими причинами: она защищает привитых, препятствует распространению гриппа и, наконец, обеспечивает достаточное количество медицинского персонала на случай развития эпидемии.
Экономические преимущества
Исследования, проведенные в Соединенных Штатах Америки, демонстрируют соотношение "стоимость-эффективность" для вакцинопрофилактики гриппа у лиц старше 65 лет, входящих или не входящих в группы повышенного риска. Эти исследования показывают необходимость неограниченной вакцинации лиц старческого возраста, входящих в группы повышенного риска.
В ходе исследования, проведенного в Канаде, было подсчитано, что стоимость вакцинопрофилактики гриппа составляет 7,45 доллара на человека. Преимущества вакцинации лиц старческого возраста состоят в снижении расходов на стационарное лечение, консультации врачей и медикаменты. Получаемая экономия достигает 11,4 доллара, а чистая прибыль составляет 3,86 доллара (8).
Кроме того, анализ соотношения "издержки-прибыль", проведенный в Европе во время последних трех крупных эпидемий, показал, что в результате вакцинации к прямой экономии денежных средств добавляется еще и косвенные преимущества, заключающиеся в уменьшении затрат вследствие сокращения количества дней нетрудоспособности и снижения эффективности производства (9).
Современные вакцины
В настоящее время в России существует три поколения инактивированных вакцин для профилактики гриппа, а именно: цельновирионные, вакцины из расщепленных вирусов и субъединичные вакцины.
Эффективность различных вакцин
Можно привести множество данных, подтверждающих эффективность вакцинопрофилактики гриппа, которая в настоящее время не вызывает сомнений.
В то же время сравнение различных вакцин является весьма деликатным делом. Полномасштабное сравнение требует обследования больших групп населения и должно проводиться во время эпидемии. Ко всем этим трудностям добавляется еще и то обстоятельство, что состав вакцин изменяется каждый год. Кроме того, эффективность вакцины в отношении одного определенного штамма не может быть экстраполирована на другие штаммы. Более того, титр антител, достигаемый посредством вакцинации, зависит от множества факторов:
- факторы, относящиесяк больному, - возраст, состояние здоровья, предыдущие прививки;
- содержание в вакцине актуальных штаммов вируса гриппа;
- методы измерения (титрование антител).
 |
Вакцины первого поколения - цельновирионные вакцины - обеспечивают достаточный иммунный ответ, но их применение сопровождается повышенным риском побочных эффектов. |
 |
Вакцины второго поколения - так называемые вакцины из расщепленных вирусов - содержат фрагментированные и очищенные частицы, включая поверхностные белки и другие компоненты вируса. |
 |
Вакцины третьего поколения - субъединичные вакцины - содержат только поверхностные антигены гемагглютинин и нейраминидазу и лишены других компонентов вируса. Субъединичные вакцины обеспечивают иммунный ответ, равный таковому цельновирионных вакцин и вакцин из расщепленных вирусов, и характеризуются более низкой частотой местных и системных реакций. |
Указанные трудности были правильно поняты руководящими органами здравоохранения, и они приняли решение установить минимум критериев для оценки эффективности вакцин.
Для оценки иммуногенности (достигаемые титры антител) и реактогенности (нежелательные реакции на вакцинацию) субъединичных вакцин и сравнения этих показателей с таковыми у вакцин из расщепленных вирусов и цельновирионных вакцин был выполнен обзор литературы за период с 1975 по 1995 г.
Были выбраны 22 публикации, описывающие рандомизированные клинические испытания, проведенные на материале 5416 серологических наблюдений, 2858 зарегистрированных случаев местных реакций и 2990 случаев системных реакций. В испытаниях участвовали представители всех возрастных групп - от детей до лиц пожилого возраста. Для сравнения вакцин вычисляли абсолютные значения разности показателей защиты и частоты реакций. Их обрабатывали методом мета-анализа, что давало интегральные значения разности этих показателей и обеспечивало доверительный интервал на уровне 95% (6).
Иммуногенность вакцин
Данные, суммирующие результаты 22 исследований иммуногенности вакцин различных типов, наглядно показывают, что все вакцины эквивалентны в отношении индукции антител в актуальной эпидемической ситуации (рис.3).
Различие между показателями иммуногенности вакцин разных типов не является статистически достоверным (tкр < 2,9).
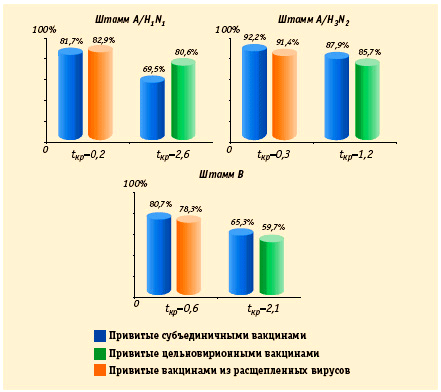
Рис.3. Мета-анализ результатов сравнения протективных титров, обеспечиваемых цельновирионными вакцинами, вакцинами из расщепленных вирусов и субъединичными вакцинами. Статистически достоверным является tкр=2,9.
Реактогенность вакцин
Реактогенность вакцин складывается из местных и системных реакций. Мета-анализ результатов 22 исследований, посвященных изучению иммуногенности и реактогенности различных вакцин, подтверждает меньшую реактогенность субъединичных вакцин по сравнению с вакцинами из расщепленных вирусов и цельновирионными вакцинами (рис.4).
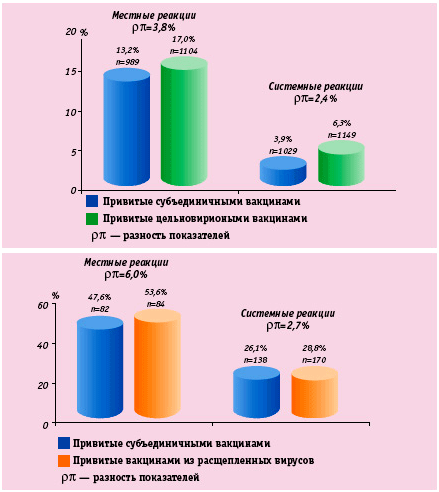
Рис. 4. Сравнение местных и системных реакций в группах привитых:
* субъединичными и цельновирионными вакцинами
* субъединичными вакцинами и вакцинами из расщепленных вирусов.
Эпизоды нежелательных реакций после введения любой из трех видов вакцин протекали в легкой форме и носили временный характер; вместе с тем, субъединичные вакцины характеризовались более низкой частотой местных и системных реакций.
Поскольку главной причиной, по которой отдельные больные отказываются от прививок против гриппа, является боязнь побочных эффектов, совершенно очевидно, что вакцина, обладающая хорошей переносимостью, должна быть особенно привлекательна именно для тех больных, которые испытывают страх перед поствакцинальными реакциями.
Производство субъединичной вакцины
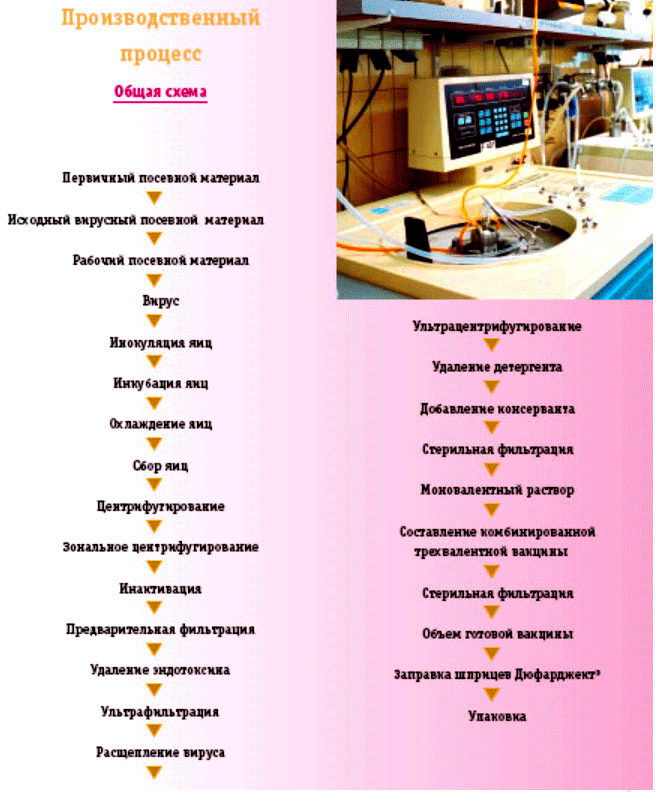
На схеме представлены этапы технологического цикла производства противогриппозной вакцины Инфлювак, выпускаемой компанией Солвей Фарма по стандарту GMP. После завершения в феврале в Женеве очередного заседания ВОЗ немедленно предоставляет определенное количество штамма нового вируса ("первичный посевной материал") в распоряжение производителей, которые выращивают из него запас "рабочего посевного вирусного материала". В последующем полученный материал используют для инокуляции яиц в объеме, необходимом для промышленного производства. После инфицирования вирусом яйца хранят в течение нескольких дней при температуре 33-35 ° С, а затем из них отсасывают содержащую вирусные частицы аллантоисную жидкость. Концентрированную вирусную суспензию получают путем последовательного выполнения различных операций центрифугирования. После инактивации вирусных частиц формальдегидом последовательно выполняют операции фильтрации и очистки. Затем вирусную суспензию обрабатывают детергентом, что позволяет отделить от вирусных частиц поверхностные клеточные белки гемагглютинин и нейраминидазу.
После добавления к субчастицам небольшого количества стабилизатора или консерванта их подвергают процедуре ультрацентрифугирования, в результате чего получают большое количество концентрированной моновалентной субъединичной противогриппозной вакцины. Приведенную выше процедуру повторяют для трех вакцин, каждая из которых направлена против конкретного штамма. Как только производители получат из Лондона самые последние реагенты, необходимые для определения концентрации гемагглютинина в моновалентной вакцине, три моновалентные вакцины комбинируют в одну трехвалентную вакцину.
На заключительном этапе массу трехвалентной вакцины стерилизуют методом фильтрации, после чего ею заправляют шприцы (0,5 мл/доза).
Заправленные шприцы проходят заключительную проверку, в ходе которой подтверждают соответствие вакцины всем стандартам качества. Результаты проверки заносят в специальный бланк контроля выпускаемой продукции (для внутреннего пользования), после чего выборочные образцы из каждой партии направляют в Национальную лабораторию инспекции, где производят внешний осмотр и выдают разрешение на выпуск продукции. В соответствии с согласованными европейскими странами процедурами регистрации всю продукцию, получившую разрешение на выпуск от Национальной лаборатории инспекции какой-либо страны Европейского сообщества, допускают к применению во всех остальных странах Сообщества.
В России каждая серия вакцины проходит контроль качества в Государственном институте стандартизации и контроля медицинских биологических препаратов им. Л.А. Тарасевича и получает сертификат качества соответствующей серии вакцины.
Солвей Фарма - 50-летний опыт вакцинопрофилактики гриппа
"Первая противогриппозная вакцина появилась в Нидерландах 50 лет назад. Сегодня Солвей Фарма - одна из самых крупных в мире компаний по производству противогриппозной вакцины. Грипп является чрезвычайно легко передающимся заболеванием, в результате которого производство ежегодно несет потери из-за невыхода на работу своих сотрудников, во многих случаях больные гриппом госпитализируются, а по всему миру фиксируются тысячи смертельных случаев. Число последних, как правило, недооценивается. По-прежнему вакцинация остается самым эффективным способом борьбы с гриппом, особенно, если учесть, что выпускаемые вакцины, включая и нашу вакцину Инфлювак®, доказали свою безопасность и эффективность. Это, однако, не снижает значимости работ по усовершенствованию вакцины. Компания Солвей Фарма намерена в ближайшее время начать выпуск новой вакцины, которая позволит еще более повысить уровень защиты от гриппа. Помимо этого, для производства противогриппозной вакцины нами разработана новая более гибкая технология. Уже в прошлом хорошо зарекомендовавшая себя вакцина Инфлювак® открывает благодаря таким инновационным разработкам обещающие перспективы на будущее".
Юрген Эрнст
Генеральный директор международной компании Солвей Фарма
"Всех нас очень вдохновляют открывающиеся перспективы. Солвей Фарма намерена строить свою политику на основе инновационных технологий и выпуске новых продуктов. Это позволит нам по-прежнему играть одну из ведущих ролей в борьбе с гриппом. Мы с оптимизмом смотрим в новое 50-летие!"
Абрахам Палаш
Университет Эразма, Роттердам
Компания Солвей Фарма производит субъединичную вакцину Инфлювак® уже более 15 лет и в настоящее время является одним из крупнейших производителей противогриппозной вакцины в мире. За эти годы выпущено более 150 миллионов доз.
Инфлювак® - это современная субъединичная противогриппозная вакцина, cодержащая только очищенные поверхностные антигены гемагглютинин и нейраминидазу, которые получены из определенных вакцинных штаммов вируса гриппа. Антигенный состав вакцины ежегодно обновляется в соответствии с последними рекомендациям ВОЗ.
Вакцина Инфлювак® к 2001 г. зарегистрирована и применяется в 39 странах мира.
Инфлювак®
Показания
Высокая иммуногенность и очень низкая реактогенность вследствие высокотехнологичного производства вакцины Инфлювак® позволяют проводить профилактику гриппа у взрослых и детей с 6-месячного возраста.
Применение во время беременности и в периоде лактации
Имеющийся опыт показывает, что Инфлювак® можно применять без каких-либо опасений в отношении плода во время беременности, а также в периоде лактации. Однако вакцинация беременных остается на усмотрение врача.
Взаимодействие с другими вакцинами
Инфлювак® можно применять одновременно с другими вакцинами. При этом их следует вводить в разные конечности, помня о теоретической возможности усиления побочных действий. У больных с уже известными реакциями такого рода рекомендуется раздельное введение препаратов с интервалом не менее трех недель.
Меры предосторожности
Вакцинация больных откладывается до окончания острых проявлений болезни и обострения хронических заболеваний. При нетяжелых ОРВИ, острых кишечных и других заболеваниях вакцинацию проводят сразу же после нормализации температуры.
Способ применения и дозы
- Доза для взрослых и подростков (с 14 лет): 0,5 мл однократно
- Доза для детей с 6 мес до 3 лет: 0,25 мл
- Доза для детей с 3 до 14 лет: 0,5 мл
Детям с 6 месяцев до 14 лет, ранее не болевшим гриппом и не вакцинированным, рекомендуется вводить 2 дозы вакцины соответственно возрасту с интервалом 4 недели.
Больным с иммунодефицитом рекомендуется вводить 2 дозы вакцины с интервалом 4 недели.
Иммунизацию проводят каждую осень. Вакцину вводят внутримышечно или глубоко подкожно.
Категорически запрещается вводить препарат внутривенно!
Клинические данные и исследования, проведенные в России
Иммуногенность и реактогенность вакцины Инфлювак®
Высокая иммуногенность вакцины и более низкая частота местных и системных реакций по сравнению с вакцинами первого и второго поколений доказана 15-летним опытом клинического применения и результатами исследований, проведенных в разных странах.
В России государственные регистрационные испытания МЗ РФ и изучение эффективности вакцины Инфлювак® проводились на базе Государственного института стандартизации и контроля медицинских биологических препаратов им. Л.А. Тарасевича.
Основными задачами регистрационного испытания являлись:
- оценка характера и интенсивности местных и общих реакций на введения вакцины Инфлювак®;
- определение безопасности препарата (клинико-лабораторное обследование привитых, анализ аллергической, инфекционной и соматической заболеваемости у привитых в течение 5 месяцев после вакцинации);
- определение иммуногенности вакцины.
Испытания проводили по следующей методике:
- случайность выборки при формировании опытной и контрольной групп;
- шифровка вакцин и плацебо;
- шифровка сывороток;
- постановка серологических реакций в независимой лаборатории;
- расшифровка материалов исследования после окончательного сбора всех данных эпидемиологического опыта.
Результаты исследования иммуногенности вакцины Инфлювак® приведены в таблице 1 и на рисунках 5-7. Результаты исследования реактогенности вакцины Инфлювак® представлены в таблицах 2 и 3.
1. Процент лиц с защитным титром антител (больше 40) до и через 28 дней после вакцинации Инфлювак®
| Штаммы вируса гриппа | Препараты | Число обследованных | Из них с титрами больше 40 | |
до вакцинации (%) |
через 28 дней (%) |
|||
A/H1N1 |
Инфлювак® |
69 |
53,6±6,0 |
100 |
Плацебо |
71 |
64,8±5,7 |
56,9±5,9 |
|
A/H3N2 |
Инфлювак® |
69 |
62,3±5,8 |
94,2±2,8 |
Плацебо |
71 |
60,6±5,8 |
53,5±5,9 |
|
B |
Инфлювак® |
69 |
68,1±5,6 |
100 |
Плацебо |
71 |
67,8±5,6 |
50,7±5,9 |
|
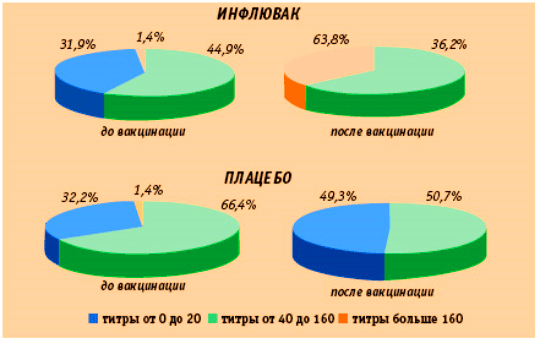
Рис. 5. Частота выявления антител к штамму вируса гриппа A/H1N1 в группе привитых вакциной Инфлювак® и плацебо до и через 28 дней после вакцинации.
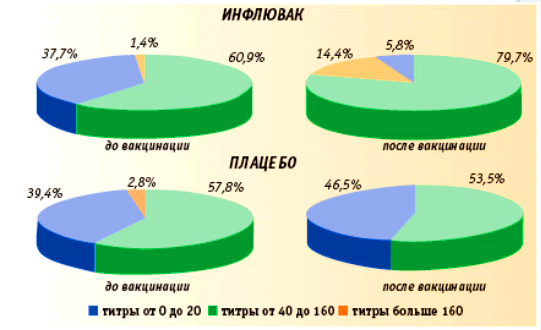
Рис.6. Частота выявления антител к штамму вируса гриппа A/H3N2 в группе привитых вакциной Инфлювак® и плацебо до и через 28 дней после вакцинации.
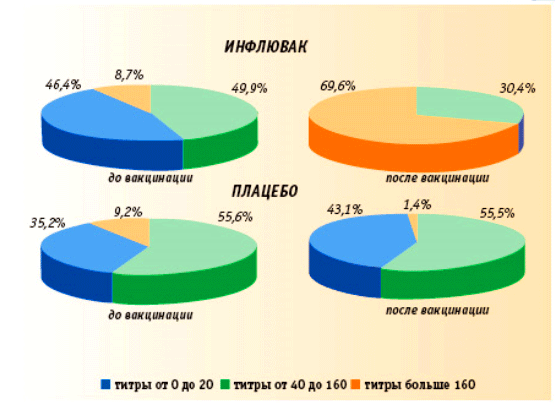
Рис.7. Частота выявления антител к штамму вируса гриппа В в группе привитых вакциной Инфлювак® и плацебо до и через 28 дней после вакцинации.
2. Частота нарушений общего и местного характера у привитых вакциной Инфлювак® и в контрольной группе
| Состояние привитых | Инфлювак® | Плацебо | |||
Абс. |
%±m |
Абс. |
%±m |
||
| Характер нарушений общего состояния | |||||
| Неудовлетворительное самочувствие (слабость) | 0 |
2 |
2.6±1.8 |
||
|
1 |
1.3±1.3 |
0 |
||
| Головная боль | 1 |
1.3±1.3 |
0 |
||
| Всего | 2 |
2.6±1.8 |
2 |
2.6±1.8 |
|
| Всего находилось под наблюдением | 77 |
77 |
|||
3. Частота температурных реакций у привитых вакциной Инфлювак® и в контрольной группе
| Температурная реакция | Инфлювак® | Плацебо | ||
Абс. |
%±m |
Абс. |
%±m |
|
| Сильная (38,6°С и выше) | 0 |
0 |
||
| Средняя (37,6°С- 38,5°С) | 2 |
2,6 ±1,8 |
0 |
|
| Слабая (37,1°С - 37,5°С) | 11 |
14,3±4,0 |
4 |
5,2±2,5 |
| Нормальная температура | 64 |
83,1±4,3 |
74 |
96,1±2,2 |
Результаты проведенных клинических испытаний в условиях строго контролируемого эпидемиологического опыта показали, что вакцина Инфлювак® обладает слабой реактогенностью и выраженной антигенно-имуногенной активностью в отношении вирусов А и В.
Это позволило зарегистрировать вакцину в РФ.
Регистрационный номер: П-8-242-№ 010306/08.07.98 г.
Профилактическая и противоэпидемическая эффективность вакцины Инфлювак®
Задачей исследования являлось определение профилактической (количественная оценка активности) и противоэпидемической (реализация свойства вакцины предотвращать развитие эпидемии при тех или иных условиях) эффективности вакцины Инфлювак® при массовом ее применении, а также изучение побочных эффектов и поствакцинальных осложнений.
В исследование, проводившееся в период предсезонного и сезонного подъема заболеваемости гриппом и ОРЗ (1999-2000 г.), были включены 3154 здоровых мужчины в возрасте 18-24 лет, не имеющие противопоказаний к вакцинации и давшие информированное согласие на ее проведение. Из них были сформированы 3 группы: основная (иммунизированные против гриппа вакциной Инфлювак®; n=1268) и две контрольные, одна из которых вакцинирована против другой инфекции (1-я контрольная группа; n=1264), а другая по условиям эпидемиологического опыта оставлена невакцинированной (2-я контрольная группа; n=622). Вакцинацию проводили в октябре - ноябре 1999 г. слепым методом, т.е. участники исследования не имели информации о том, какой вакциной их иммунизировали. Для оценки эффективности вакцины Инфлювак® определяли показатели (индекс К и коэффициент Е) профилактической и противоэпидемической защиты (эффективности вакцины) на основании данных о заболеваемости гриппом и ОРЗ среди иммунизированных вакциной Инфлювак® и невакцинированных участников исследования.
Результаты исследования приведены на рисунке 8 и в таблицах 4 и 5 (1).
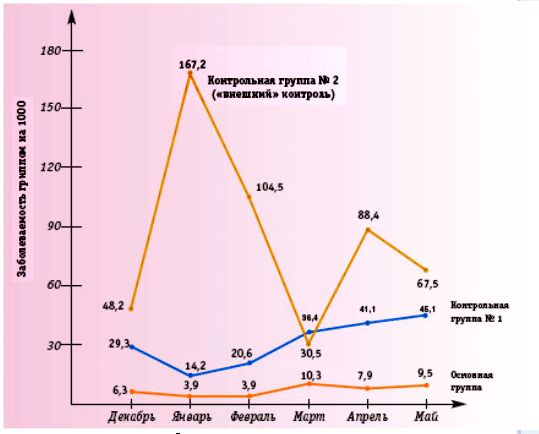
Рис. 8. Динамика заболеваемости гриппом у иммунизированных вакциной Инфлювак® и в контрольных группах (за период наблюдения с декабря 1999г. по май 2000г.).
4. Заболеваемость гриппом и ОРЗ в исследуемых группах за период сезонного подъема с ноября 1999г. по май 2000г.
| Группа | Число участников | Число заболевших гриппом и ОРЗ | Заболеваемость гриппом на 1000 участников (с учетом серологического подтверждения диагноза) | |
Абс. |
На 1000 наблюдений |
|||
| Основная (иммунизированные вакциной Инфлювак®) | 1268 |
460 |
362,8±13,5* |
41,7±5,6* |
| 1-я контрольная (не вакцинированные против гриппа) | 1264 |
630 |
498,4±14,1* |
186,9±10,9* |
| Всего (с 50% иммунной прослойкой) | 2532 |
1090 |
430,5±9,8* |
114,1±6,3* |
| 2-я контрольная ("внешний контроль") | 622 |
840 |
1350,1 |
506,3±20,0 |
Примечание. *- различие показателей по сравнению с показателями во 2-й контрольной группе статистически значимо (р < 0,05).
5. Соматическая и инфекционная заболеваемость (исключая грипп и ОРЗ) в группах вакцинированных и не вакцинированных против гриппа с ноября1999г. по май 2000г.
| Заболевания | Заболеваемость на 1000 участников | ||
иммунизированные вакциной Инфлювак® (основная группа; n=1268) |
не вакцинированные против гриппа (1-я контрольная группа; n=1264) |
||
| Острые воспалительные заболевания верхних дыхательных путей (кроме гриппа и ОРЗ) | 198,7± 11,2 |
206,5±11,4 |
|
| Инфекционные | 19,7±3,9 |
22,2±4,1 |
|
| Кожные | 57,6±6,5 |
49,1±6,1 |
|
|
5,5±2,1 |
6,3±2,2 |
|
|
6,3±2,2 |
5,5±2,1 |
|
| Желудочно-кишечные | 10,3±2,8 |
11,1±2,9 |
|
| Прочие | 2,4±1,9 |
2,4±1,9 |
|
| Всего | 300,5±12,8 |
303,0±12,9 |
|
Сезонный подъем заболеваемости гриппом и ОРЗ среди участников исследования был зарегистрирован с декабря по май. При анализе заболеваемости за весь период наблюдения отдельно в каждой группе выявлено, что статистически значимо (p < 0,05) более низкий (362,8 на 1000) уровень заболеваемости гриппом и ОРЗ был в основной группе по сравнению с 1-й (498,4 на 1000) и 2-й (1305,1 на 1000) контрольными группами. Параметры профилактической эффективности вакцины К и Е, полученные на основании показателей заболеваемости гриппом в 1-й контрольной и в основной группах, составили соответственно 4,5 и 77,7% , а на основании показателей заболеваемости гриппом во 2-й контрольной и основной группах С соответственно 12,1 и 91, 8%. Параметры противоэпидемической защиты К и Е в коллективе с 50% иммунной прослойкой и во 2-й контрольной группе соответственно составили 4,4 и 77,5%. При систематическом медицинском наблюдении в течение 8 месяцев за 1268 иммунизированными вакциной Инфлювак® ни в одном случае не выявлено необычных, редко встречающихся поствакцинальных реакций.
Таким образом, вакцина Инфлювак® обладает высокой профилактической и противоэпидемической эффективностью и низкой реактогенностью.
Вакцинопрофилактика гриппа у детей
Грипп опасен для каждого. Во время эпидемий погибают и вполне здоровые люди. Однако наибольшую угрозу грипп и его осложнения таят для маленьких детей. Дети становятся восприимчивы к гриппу начиная со второго полугодия жизни. В течение первых месяцев ребенок защищен полученными от матери противогриппозными антителами, так что возможность заболевания невелика. Но позже он эти антитела теряет, и вероятность заболеть гриппом становится очень высокой.
Переболев гриппом (обычно тяжело), ребенок приобретает антитела к нему, однако проблема состоит в том, что вирус гриппа все время меняется, так что антитела к варианту, циркулировавшему в прошлые годы, не в полной мере защитят от нового варианта вируса. Высокая восприимчивость к гриппу сохраняется у многих детей и в школьном возрасте; при тесном контакте между школьниками неудивительно, что грипп обусловливает взрывоподобные вспышки, часто являющиеся причиной распространения инфекции среди остального населения. Вакцинация детей способна защитить их от тяжелых последствий, связанных с гриппом. Особенно это касается детей с тяжелой соматической патологией.
Применение вакцины Инфлювак® для профилактики гриппа у детей с соматической патологией
На кафедре детских инфекционных болезней Российского государственного медицинского университета и Центра вакцинопрофилактики "Диавакс" было проведено изучение эффективности и реактогенности вакцины Инфлювак® у детей с тяжелой соматической патологией (в исследовании участвовало 127 детей: 71 ребенок был вакцинирован, 56 детей входили в контрольную группу) (5).
Иммуногенную активность вакцины определяли путем постановки реакции РТГА по общепринятой методике на основе результатов исследования порций крови, собранных через 28 дней после вакцинации.
Проведенные исследования свидетельствуют об отсутствии реактогенности у субъединичной вакцины Инфлювак® при применении у детей с различной соматической патологией. Вакцина оказалась высокоиммуногенной, что подтверждается высоким процентом 4-кратной сероконверсии после вакцинации в группах исходно серонегативных и серопозитивных лиц.
После введения препарата отмечено статистически достоверное увеличение процента детей с защитными титрами ко всем штаммам вируса гриппа. Наряду с этим, после иммунизации выявлено значительное уменьшение числа детей с низким уровнем титров антител одновременно со статистически достоверным увеличением числа детей с высоким уровнем титров антител, что также указывает на высокую иммуногенность вакцины.
6. Иммуногенность и сероконверсия в группе привитых вакциной Инфлювак®
| Штамм | Защитный титр антител (% случаев) | 4-х кратный прирост титров антител в группе серонегативных лиц (1:10 ® 1:40) |
4-х кратный прирост титров антител в группе серопозитивных лиц (1:40 и выше) |
А/Н1N1 |
82% |
90% |
100% |
A/H3N3 |
97% |
92,3% |
62% |
B |
99% |
83,3% |
61,5% |
Таким образом, проведенное исследование вакцины Инфлювак® подтвердило данные мета-анализа результатов сравнения иммуногенности и реактогенности субъединичных вакцин, цельновирионных вакцин и вакцин из расщепленных вирусов (Национальный центр по изучению гриппа ВОЗ), свидетельствующие об одинаковой иммуногенности субъедничных вакцин и вакцин из расщепленных вирусов у детей с соматической патологией.
Применение вакцины Инфлювак® для профилактики гриппа у детей с аллергическими заболеваниями
Вакцинация против гриппа в группах риска имеет свои особенности, так как возрастает опасность более тяжелого течения инфекции, развития осложнений и смертельных исходов. Иммунизация в группах риска, согласно рекомендациям, проводится субъединичными вакцинами, к которым относится вакцина Инфлювак®. Задачей настоящего исследования было изучение безопасности и эффективности применения вакцины Инфлювак® у детей с аллергическими заболеваниями (2).
В исследование были включены 100 детей в возрасте от 6 до 15 лет (44 мальчика и 56 девочек). У 15 детей в анамнезе был ложный круп, у 35 детей диагностирована риносинусопатия с сенсибилизацией к бактериальным и пыльцевым аллергенам, у 20 детей - бронхиальная астма легкого течения, у 30 детей выявлены аллергодерматозы (крапивница или атопический дерматит). Большинство детей имели сопутствующую сочетанную патологию. В анамнезе частые ОРВИ (более 6 раз в год), аденоидит (20 детей), хронический фарингит (30 детей), хронический отит (15 детей), хронический тонзиллит (20 детей).
Клинико-иммунологическое обследование проводили до вакцинации.
CD3 +-, CD4 +-, CD8 +-, CD19 +- клетки определяли с помощью моноклональных антител (фирма Becton-Dikinsen), сывороточные IgM, IgG, IgA - методом радиальной иммунодиффузии, IgA в слюне, общий и специфический IgE - методом ИФА, показатели хемилюминесценции - по стандартным методикам. Статистическую обработку результатов проводили с использованием компьютерных методов.
Иммунизацию осуществляли внутримышечно с помощью шприц-дозы однократно вакциной Инфлювак®. Ранее все дети болели гриппом. Перед вакцинацией они были осмотрены педиатром и аллергологом-иммунологом, прививку не проводили в период обострения заболеваний, в течение трех дней до и после вакцинации (суммарно 6 дней) дети получали кларитин в возрастных дозах один раз в день. В случае необходимости по клиническим показаниям (аллергодерматозы) применение кларитина было продолжено.
Результаты исследования приведены в таблицах 7-9.
7. Нарушения показателей иммунной системы у обследованных детей до вакцинации
| Иммунная система | Частота и характер нарушений |
| Т-клеточное звено | У 40% детей снижение количества CD3 +- или CD4 +- клеток |
| Макрофагальное звено | У 20% детей снижение показателя |
| Иммуноглобулины | У 20% детей снижение уровня IgG или IgA в крови; У 94% детей снижение уровня IgA в слюне |
| Звено естественных киллеров | У 15% детей снижение количества CD16 +- клеток |
| В-клеточное звено | У 15% детей снижение количества CD19 +- клеток |
По данным таблицы 7, иммунологические нарушения у больных до вакцинации затрагивали различные звенья иммунной системы, включая Т-клеточное, В-клеточное, макрофагальное звенья и звено естественных киллеров. У части детей выявлена гипоглобулинемия по IgG или IgA, у большинства отмечено снижение уровня IgA в слюне.
Анализ мазков из зева на микрофлору указывал на наличие хронической инфекции, обусловленной Staphylococcus aureus, Staph. epidermidis, Streptococcus viridаns и т.д. В 60-80% случаев выделенные стафилококки и стрептококки in vitro не были чувствительны к антибактериальным препаратам.
8. Уровень общего и специфического Ig E у детей с аллергическими заболеваниями до вакцинации против гриппа
| Показатели | Результаты |
| Уровень общего Ig E | У 25% детей 800-1000 МЕ/мл У 25% детей 200-300 МЕ/мл У 50% детей 50-190 МЕ/мл |
| Сенсибилизация к бытовым аллергенам | У 50% детей |
| Сенсибилизация к пыльцевым аллергенам | У 35% детей |
| Сенсибилизация к бактериальным или грибковым аллергенам | У 75% детей |
| Сенсибилизация к пищевым аллергенам | У 35% детей |
Вакцинация против гриппа была проведена в октябре-ноябре 2000г., и наблюдение проводили до апреля 2001г. После вакцинации у 10% детей выявлены местные реакции (болезненность в месте введения вакцины), у 4% детей отмечена системная реакция.
В течение 6 месяцев наблюдения после вакцинации зарегистрировано 5 эпизодов ОРВИ (5% детей), серологическую идентификацию возбудителей не проводили.
Таблица 9. Уровень IgE у детей с аллергическими заболеваниями, вакцинированных против гриппа
| Уровень общего IgE | Средние показатели | |
До вакцинации |
Через 1 месяц после вакцинации |
|
50-190 МЕ/мл |
157,6±3,3 |
154,6±2,5 |
200-300 МЕ/мл |
228±1,7 |
225±1,6 |
800-1000 МЕ/мл |
800±83 |
908±91 |
Обследуемая группа была разнородна по уровню общего IgE, после вакцинации не отмечалось достоверного нарастания данного показателя, что соответствует клиническим данным.
В последние годы большое внимание уделяется вакцинации групп риска, к которым относятся взрослые старше 50-60 лет и дети, отдельно выделены группа взрослых и детей, страдающих хроническими легочными заболеваниями, а также взрослые и дети с иммунной недостаточностью, в том числе ВИЧ-инфицированные лица, получающие иммунодепрессанты. К группам риска можно отнести около 20% населения. По последним данным, около 40% населения имеют те или иные проявления аллергических заболеваний.
Обследованная группа детей с аллергическими заболеваниями была неоднородна по иммунологическим нарушениям, при этом у части детей отмечены изменения в нескольких звеньях иммунной системы одновременно. У 50% детей уровень общего IgE был значительно повышен с наличием сенсибилизации к различным группам аллергенов, в частности у 75% выявлена сенсибилизация к бактериальным или грибковым аллергенам.
Наиболее общий признак - снижение уровня IgA в слюне, что указывает на нарушения в системе местного иммунитета, в первую очередь отвечающего за устойчивость к инфекциям носоглотки и респираторного тракта.
Проведенное исследование показало безопасность, слабую реактогенность и высокую эффективность субъединичной вакцины Инфлювак® у детей с аллергическими заболеваниями. Она может быть рекомендована для специфической профилактики гриппа в группе детей с аллергическими заболеваниями в сочетании с антигистаминными препаратами.
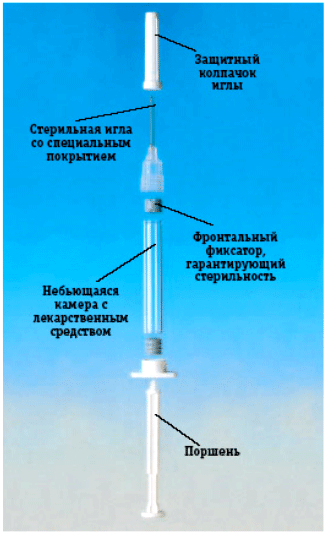
Дюфарджект®
В 1979 г. была разработана конструкция шприца Дюфарджект®. В ее основе лежит уникальное оригинальное устройство. При приведении шприца в действие специальная резиновая пробка продвигается вперед и попадает в отверстие, снабженное обводными каналами, что исключает попадание частиц резины в вакцину. Это всегда было неразрешимой проблемой в других шприцах. Компания Солвей Фарма получила патент на конструкцию шприца Дюфадрджект®. Игла фиксирована и имеет силиконовое покрытие. Шприц прост и готов к применению.
Дюфарджект® обеспечивает безопасное и безболезненное введение точной дозы вакцины Инфлювак®.
Присущее вакцине Инфлювак® соотношение между ожидаемым полезным эффектом и возможным риском весьма высоко оценивается в контексте профилактики гриппа и его осложнений.
Чистота вакцины Инфлювак® и ее безопасность, а также уникальный шприц Дюфарджект® создают все предпосылки для улучшения отношения населения к вакцинопрофилактике гриппа.
Безопасность применения вакцины Инфлювак®
С тех пор, как международная фармацевтическая компания Солвей Фарма приступила к производству противогриппозной субъединичной вакцины Инфлювак®, в многочисленных исследованиях была доказана ее безопасность и низкая реактогенность.
Тот факт, что за последние 5 лет было применено свыше 70 миллионов доз вакцины Инфлювак® (в т.ч. 800 тыс. в России в сезоны 1999-2000 и 2000-2001 гг.) и при этом не наблюдалось ни одного неизвестного побочного эффекта, который мог бы быть связан с ее действием, служит дополнительной гарантией безопасности вакцины Инфлювак®.
Список литературы
- Бектимиров Т.А., Ельшина Г.А., Горбунов М.А. и др. Результаты изучения эффективности гриппозной инактивированной субъединичной вакцины Инфлювак. Новые лекарственные средства и медицинские технологии, 2000, 9: 47-51.
- Маркова Т.В., Чувиров Д.Г. Применение вакцины Инфлювак® для профилактики гриппа у детей с аллергическими заболеваниями. В печати.
- Онищенко Г.Г. Состояние вакцинопрофилактики в России и перспективы ее развития. Российские мед.вести МЗ РФ, 1998, 4.
- Садовникова В.Н., Ясинский А.А. Инфекционная заболеваемость в Российской Федерации (1990-2000гг.). Эпидемиология и вакцинопрофилактика, №1/01.
- Шамшиева О.В., Учайкин В.Ф., Бурцева Е.Н. и др. Эффективность иммунопрофилактики гриппа субъединичной вакциной Инфлювак у детей с соматической патологией, Рос. Вестник перинатологии и педиатрии, 2000, 4:24-26.
- Beyer W.E.P. In press.
- Fleming D.M. The impact of three influenza epidemics on primary care in England and Wales. Pharmacoeconomics, 1996. In press.
- Gross P.A., Hermogenes A.W., Sacks H.S. et al. The efficacy of influenza vaccine in elderly persons. Ann. intern. Med., 1995, 123: 518-527.
- Levy E., Levy P. Influenza vaccination for an active population aged 25-64 years: a cost-benefit study. Rev. epidem. sante publ., 1992, 40:285-295.
- Milne R. Influenza vaccination warrants a greater share of healthcare resources. Pharmacoresources, 1995, 33:3-5.
- Nichol K.L., Margolis K.L., Wuorenma J., von Sternberg T. The efficacy and cost effectiveness of vaccination against influenza among elderly persons living in the community. N. Engl. J. Med., 1994, 331:778-84.
- Nicholson K.G., Snacken R., Palache A.M. Influenza immunisation policies in Europe and the United States. Vaccine, 1995, 13:365-369.
- Prevention and control of influenza. Recommendation of the Immunisation Practice Advisory Committee (ACIP). Morbidity Mortality Wkly Rep., 1994, 43: 1-13.
- Ruben F.L Who needs influenza vaccine in: Options for the control of influenza. Kendal A. P., Patriacra P.A. eds. New York: Alan R Liss, 1986, 139-154.
- Schoenbaum S.C. Economic impact of influenza: the individualIs perspective. Am. J. Med., 1987, 82 (suppl 6A): 26-30.
- Sprenger M.J.W. The impact of influenza: an epidemiological study of morbidity, direct mortality and related mortality. Thesis, Erasmus University, Rotterdam, 1990.
- Sprenger M.J. W., van Naelten M.A.M. G. et al. Influenza mortality excess deaths in the elderly, 1967-1982. Epidem. Inf., 1989, 103:633-641.
- Sullivan K.M. Health impact of influenza in the United States. Pharmacoeconomics, 1996. In press.
- WHO Memorandum from meeting in February 1995. Cell culture as a substrate for the production of influenza vaccines. Bull. WHO, 1995, 73:431-435.
