Влияние эбастина на концентрации катионного белка эозинофилов в сыворотке у пациентов с бронхиальной астмой
Статьи
Takahiko Horiguchi, Soichi Tachikawa, Junichi Kasahara, Mamoru Shiga, Rieko Kondo, Junichi Miyazaki, Masahiro Sugiyama, Yasushi Sasaki and Masahiro Hirose
Отделение заболеваний органов дыхания, Вторая клиническая база для медицинского образования, Медицинский университет Департамента здравоохранения Фуджита, Япония (Department of Respiratory Diseases, Second Hospital for Medical Education, Fujita Health University of Medicine, Nagoya, Aichi, Japan)
Аннотация
Цель: Настоящее исследование было посвящено оценке влияния эбастина на концентрации катионного белка эозинофилов (КБЭ) в сыворотке у пациентов с бронхиальной астмой.
Пациенты: В исследование были включены двадцать пациентов с бронхиальной астмой и низкой эффективностью текущей терапии (11 пациентов с атопической формой заболевания и девять – с неатопической формой).
Методы: В соответствии с открытым дизайном исследования все пациенты получали эбастин в дозе 10 мг/сутки в течение 4 недель, во время которых до и после применения препарата определялись концентрации КБЭ в сыворотке, количество эозинофилов в периферической крови, утренняя максимальная объемная скорость выдоха (МОСВ) и пороговые значения для гиперреактивности дыхательных путей (Dmin при астграфии).
Результаты: Было отмечено достоверное снижение концентраций КБЭ в сыворотке и количества эозинофилов в периферической крови. У пациентов с неатопической формой заболевания не было обнаружено достоверных изменений, в то время как у пациентов с атопической астмой было отмечено достоверное снижение (p<0,001) концентраций КБЭ в сыворотке. Более того, у пациентов с атопической формой заболевания не было выявлено существенных изменений Dmin, но отмечалось значительное (p<0,019) увеличение МОСВ.
Заключение: Эбастин не только подавляет аллергические реакции I типа, но также может ингибировать воспаление в дыхательных путях за счет снижения концентраций КБЭ в сыворотке, особенно у пациентов с атопической бронхиальной астмой.
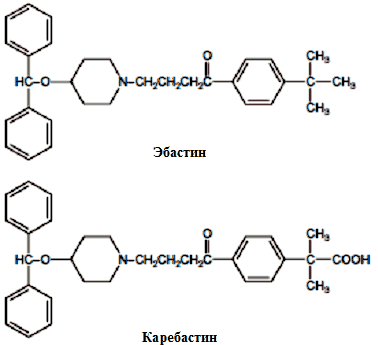
Эбастин (рисунок 1) представляет собой антагонист гистаминовых Н1 рецепторов, разработанный компанией Almirall Prodesfarma (Испания). Известно, что этот лекарственный препараты быстро метаболизируется в кишечнике и печени до активного соединения каребастина (рисунок 1), которое и сопровождается соответствующими эффектами препарата. Этот препарат характеризуется высоким аффинитетом к гистаминовым Н1 рецепторам, слабой центральной угнетающей и антихоленергической активностью и более длительным действием по сравнению с антигистаминами предыдущего поколения. Более того, было продемонстрировано, что эбастин обладает противоаллергической активностью, в частности ингибирует высвобождение гистамина из перитонеальных тучных клеток крысы и базофилов периферической крови человека и ингибирует возникновение экспериментальной астмы у морских свинок.[1,2]
Рисунок 1. Химические структуры эбастина и его активного карбоксикислого метаболита, каребастина.
Недавно было показано, что патогенез бронхиальной астмы заключается в хроническом персистирующем воспалении дыхательных путей с вовлечением эозинофилов, и участию воспалительных химических медиаторов уделяется все больше внимания.[3] Катионный белок эозинофилов (КБЭ) представляет собой один из белков эозинофильных гранул, и поскольку он активирует эозинофилы и индуцирует тяжелое повреждение тканей дыхательных путей, концентрация этого белка может считаться критерием оценки активности эозинофилов и маркером воспаления дыхательных путей при терапии бронхиальной астмы.[4-6] В настоящем исследовании мы применяли эбастин у 20 пациентов с бронхиальной астмой и изучали эффект препарата на концентрации КБЭ в сыворотке.
Пациенты и методы
Группа участников исследования состояла из 20 пациентов (10 мужчин и 10 женщин) с бронхиальной астмой взрослых, в возрасте от 23 до 72 лет, которые обратились или были госпитализированы в Отделение заболеваний органов дыхания Второй клинической базы для медицинского образования, Медицинского университета Департамента здравоохранения Фуджита (Department of Respiratory Diseases, Second Hospital for Medical Education, Fujita Health University of Medicine). Причиной госпитализации являлась низкая эффективность текущих методов терапии и необходимость в подборе новых методов терапии. Все пациенты предоставили информированное согласие на участие в настоящем исследовании.
Пациенты были разделены по типу заболевания на две группы: 11 пациентов с атопической формой заболевания и девять – с неатопической формой заболевания. В группу контроля вошли пять здоровых участников без анамнеза курения и без атопических заболеваний. В исследование были включены пациенты с бронхиальной астмой легкой или средней тяжести по критериям тяжести бронхиальной астмы Комитета Японского общества аллергологов,[7] а пациенты, у которых отмечались приступы длительностью до 2 дней или более до начала отбора в исследование, а также пациенты, получавшие стероиды и/или противоаллергические препараты, исключались из исследования.
Пациенты получали эбастин в дозе 10 мг/сутки в течение 4 недель, во время которых до и после применения препарата определялись концентрации КБЭ в сыворотке, количество эозинофилов в периферической крови, утренняя максимальная объемная скорость выдоха (МОСВ) и пороговые значения для гиперреактивности дыхательных путей (Dmin при астграфии). МОСВ определялась по общему из трех измерений с использованием пикфлоуметра Mini-Wright (Kere Kerement Clark, Великобритания), из которых использовалось максимальное значение. Допускалось применение пациентами теофиллина или ß-миметиков.
Забор анализов крови осуществлялся из локтевой вены утром в период с 9 часов до полудня. Для анализа был взят образец крови объемом три миллилитра в пробирку SST (Beckton Dickinson), которая отстаивалась при комнатной температуре в течение 60 минут, после чего центрифугировалась при 1500g в течение 10 минут. Полученная сыворотка хранилась при температуре -20°С или ниже. Концентрации КБЭ определялись с помощью набора для анализа RIA (Pharmacia). Одновременно определялось количество эозинофилов в периферической крови с использованием автоматического прибора для подсчета лейкоцитов (Technicon H-1). Кроме того, выполнялся тест на оценку гиперреактивности бронхов с использованием метахолина на аппарате астграф (Chest TLK-6000CV), а также определялось значение Dmin до и после применения эбастина.
Статистический анализ
Результаты представлены в виде средних ± стандартная ошибка (СКО). Для статистического анализа использовался парный t-критерий для сравнения значений, полученных до и после применения препарата, а также непарный t-критерий для сравнения двух групп. Статистически значимым было принято значение р<0,05.
Результаты
Сравнение концентраций КБЭ в сыворотке и количества эозинофилов в периферической крови до применения эбастина у пациентов с бронхиальной астмой и у здоровых участников
Концентрации КБЭ в сыворотке у пациентов с бронхиальной астмой и у здоровых участников до терапии эбастином представлены на рисунке 2. Концентрации КБЭ в сыворотке оказались значительно выше у пациентов с бронхиальной астмой, чем у здоровых участников (19,3±2,4 мг/л по сравнению с 6,7±0,4 мг/л) [p<0,001]. Количество эозинофилов в периферической крови также было достоверно выше у пациентов с бронхиальной астмой, чем у здоровых пациентов (390,0 ± 35,8/мм3 по сравнению с 124,0±5,1/мм3) [p<0,001].
Изменения концентраций КБЭ в сыворотке после применения эбастина
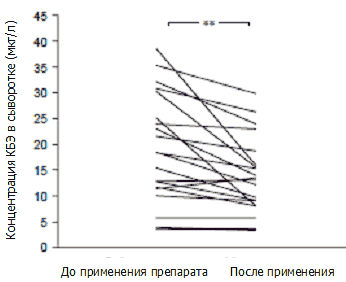
Изменения концентраций КБЭ в сыворотке до и после 4-недельной терапии эбастином у пациентов с бронхиальной астмой отображены на рисунке 3. Отмечалось достоверное снижение концентраций КБЭ в сыворотке с 19,3±2,4 мг/л до 14,0±1,7мг/л (p<0,014). У пациентов с неатопической формой заболевания не было обнаружено достоверных изменений (12,3±2,1 мг/л по сравнению с 11,2±1,9 мг/л), в то время как у пациентов с атопической формой астмы концентрации КБЭ в сыворотке, показанные на рисунке 4, значительно снизились с 25,0±3,0 мг/л до 16,3±2,4 мг/л (p<0,0014).
Рисунок 2. Концентрации катионного белка эозинофилов (КБЭ) в сыворотке у пациентов с бронхиальной астмой и у здоровых участников до применения эбастина. ** p<0,01.
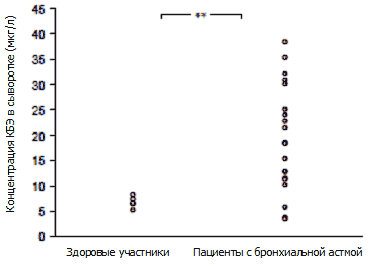
Рисунок 3. Изменение концентраций катионного белка эозинофилов (КБЭ) в сыворотке до и после 4 недель терапии эбастином у пациентов с бронхиальной астмой. ** p<0,01.
Изменения в количестве эозинофилов в периферической крови после применения эбастина
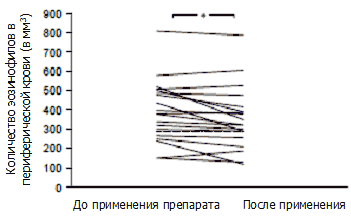
Изменения в количестве эозинофилов в периферической крови до и после 4 недель применения эбастина у пациентов с бронхиальной астмой показаны на рисунке 5. Количество эозинофилов в периферической крови значительно снизилось с 390,0±35,3/мм3 до 353,0±35,9/ мм3 (p<0,0105). У пациентов с неатопической формой заболевания не было обнаружено достоверных изменений (294,4±38,7/мм3 по сравнению с 274,4±43,7/мм3), но у пациентов с атопической формой астмы было отмечено значительное снижение количества эозинофилов 468,2±44,4/мм3 до 417,3±47,8/мм3 (p<0,0253).
Рисунок 4. Концентрации катионного белка эозинофилов (КБЭ) в сыворотке до и после 4 недель терапии эбастином у пациентов с бронхиальной астмой. ** p<0,01.
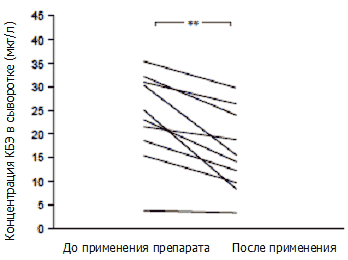
Рисунок 5. Изменение количества эозинофилов в периферической крови до и после 4 недель терапии эбастином у пациентов с бронхиальной астмой. * p<0,05.
Изменения утренней МОСВ после терапии эбастином
Изменения МОСВ до и после 4 недель терапии эбастином у пациентов с бронхиальной астмой отображены на рисунке 6. Отмечалось достоверное увеличение МОСВ с 385,5±16,9 л/мин до 402,5±18,4 л/мин (p<0,026). У пациентов с неатопической формой заболевания значимых изменений МОСВ отмечено не было (354,4±29,9 л/мин по сравнению с 356,7±27,4 л/мин), но у пациентов с атопической формой астмы было выявлено достоверное увеличение данного показателя с 410,9±16,1 л/мин до 440,0±19,1 л/мин (p<0,0189).
Рисунок 6. Изменение максимальной объемной скорости выдоха (МОСВ) до и после 4 недель терапии эбастином у пациентов с бронхиальной астмой. * p<0,05.

Изменения значения Dmin после терапии эбастином
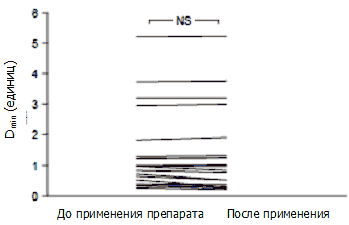
Изменения значения Dmin до и после 4 недель терапии эбастином у пациентов с бронхиальной астмой отображены на рисунке 7. Достоверных изменений значения Dmin отмечено не было (1,43±0,30 единиц по сравнению с 1,40±0,31 единиц). Точно так же не было выявлено значимых изменений в зависимости от формы заболевания.
Рисунок 7. Изменение пороговых значений гиперреактивности дыхательных путей (Dmin) до и после 4 недель терапии эбастином у пациентов с бронхиальной астмой.
Обсуждение
Патогенез бронхиальной астмы длительное время считался обусловленным преимущественно развитием реакций немедленного типа и как следствие сокращением гладкой мускулатуры бронхов, отеком слизистой оболочки дыхательных путей и повышением секреции в дыхательных путях, вызванных высвобождением химических медиаторов, таких как гистамин, из тучных клеток. Однако в последнее время в результате прогрессивного развития иммунологических и молекулярно-биологических исследований, особое внимание уделяется острому и хроническому аллергическому воспалению дыхательных путей, вторичному по отношению к аллергическим реакциям I типа, а также ингибированию воспалительного процесса в дыхательных путях как цели терапии.[8-10]
Считается, что КБЭ, белок эозинофильных гранул, оказывает повреждающее действие на эпителий дыхательных путей и играет значительную роль в развитии гиперреактивности дыхательных путей на фоне стимуляции других воспалительных клеток, при непосредственном влиянии на гладкую мускулатуру бронхов. Более того, КБЭ считается белком, отражающим активацию эозинофильного воспаления, эффектора аллергического воспаления.[4-6]
Эбастин представляет собой новый антагонист гистаминовых H1 рецепторов длительного действия, который специфично и активно антагонизирует гистаминовые H1 рецепторы и оказывает дозозависимый ингибирующий эффект на сужение дыхательных путей в модели экспериментальной астмы у морских свинок.[2]
В настоящем исследовании были изучены эффекты эбастина в отношении концентраций КБЭ в сыворотке, количества эозинофилов в периферической крови и значений МОСВ и Dmin у пациентов с бронхиальной астмой. После 4 недель применения эбастина у пациентов с бронхиальной астмой значения Dmin не изменились, однако, было отмечено достоверное снижение концентраций КБЭ в сыворотке и количества эозинофилов в периферической крови, а также значимое увеличение МОСВ по сравнению с исходными значениями этих параметров до применения препарата. Эти результаты демонстрируют, что изменения концентраций КБЭ в сыворотке и количества эозинофилов в периферической крови, а также МОСВ оказались более чувствительны, чем Dmin.
Таким образом, по результатам исследования было отмечено, что эбастин снижает концентрации КБЭ в сыворотке и количество эозинофилов в периферической крови, достоверно повышает МОСВ и ингибирует процесс воспаления в дыхательных путях у пациентов с бронхиальной астмой. При рассмотрении изменений концентраций КБЭ в сыворотке, количества эозинофилов в периферической крови и значений МОСВ в зависимости от формы заболевания никаких достоверных различий ни по одному из этих параметров до и после применения эбастина у пациентов с неатопической формой заболевания выявлено не было, в то время как у пациентов с атопической формой астмы были выявлены достоверные различия, что указывает на особо выраженный эффект эбастина на процесс воспаления в дыхательных путях у пациентов с атопической бронхиальной астмой.
Патогенез бронхиальной астмы можно грубо разделить на три фазы. Первая фаза включает реакции немедленного типа, возникающие в результате высвобождения химических медиаторов, таких как гистамин, из тучных клеток. Во вторую фазу происходит инфильтрация слизистой оболочки дыхательных путей воспалительными клетками, преимущественно эозинофилами, и повреждение эпителия дыхательных путей химическими медиаторами, такими как КБЭ, выделяемыми воспалительными клетками с последующим развитием нейрогенной воспалительной реакции. В третью фазу происходят репаративные процессы в тканях, подверженных воспалению и фиброзу вследствие нарушения равновесия регенерации, так называемое «ремоделирование». При бронхиальной астме в процесс аллергического воспаления вовлечены не множественные клеточные пролиферации, и в настоящее время осуществляется разработка лекарственных препаратов, ингибирующих соответствующие процессы.
Создается впечатление, что при аллергическом рините в развитие заложенности носа и эозинофильной инфильтрации слизистой оболочки носа отчасти вовлечены реакции второй фазы, т.е., реакции поздней фазы. В двойном слепом исследовании с участием пациентов с круглогодичным аллергическим ринитом было отмечено, что эбастин в значительной степени превосходит контрольный препарат, кетотифен, по эффекту в отношении заложенности носа.[11] Это соотносится с влиянием эбастина на процесс развития воспаления дыхательных путей.
У пациентов с бронхиальной астмой повреждающие ткани медиаторы, такие как КБЭ и MBP (главный основной белок), высвобождаются из активированных эозинофилов, что приводит к повреждению и слущиванию респираторного эпителия. Вследствие этого, чувствительные нервные окончания подвергаются воздействию и стимуляции гистамином с последующим высвобождением из нервных окончаний нейропептидов, таких как субстанция Р и нейрокинин А, что приводит к сужению (констрикции) дыхательных путей, отеку дыхательный путей, повышению сосудистой проницаемости и секрета слизи, что еще больше способствует развитию воспаления дыхательных путей.
Противоаллергические эффекты эбастина включают ингибирование пассивной кожной анафилактической реакции у морских свинок, уменьшение под действием препарата гистамин-индуцированного сокращения выделенной трахеи морской свинки и подавление реакций Шульца-Дейла в препаратах подвздошной кишки, выделенных у сенсибилизированных морских свинок. Все эти эффекты играют ингибирующую роль в процессе воспаления дыхательных путей. Таким образом, было сделано предположение о возможном снижении Dmin и уменьшении количества эозинофилов в периферической крови, вызванном применением эбастина вследствие подавления процесса воспаления дыхательных путей как результата упомянутых выше эффектов.
Специфические IgE антитела, вырабатывающиеся в ответ на аллерген, присутствующий в окружающей среде, могут быть выделены при атопической форме бронхиальной астмы, но не при неатопической форме. Однако между атопической и неатопической формами астмы не было отмечено различий по клинической картине воспаления дыхательных путей. Поэтому различия, выявленные в ходе настоящего исследования между атопической и неатопической формами бронхиальной астмы, требуют дальнейшего изучения в исследованиях с участием большего числа пациентов.
Заключение
В результате исследования было сделано заключение, что эбастин, разработанный как селективный антагонист гистаминовых Н1 рецепторов длительного действия, не только подавляет аллергические реакции I типа, но также помогает ингибировать воспаление в дыхательных путях за счет снижения концентраций КБЭ в сыворотке и количества эозинофилов в периферической крови, особенно у пациентов с атопической бронхиальной астмой.
Список использованной литературы
