Магниевые тайны библиотеки Кохрана: современный взгляд на проблему
Статьи Опубликовано в журнале:Российский Вестник Акушера-гинеколога 5, 2011
О.А. ГРОМОВА1,2, Е.Ю. ЛИСИЦЫНА1,2, И.Ю. ТОРШИН 1, О.Н. ГРАЧЕВА3
Magnesium secret of the Cochrane database: current view of the problem
O.A. GROMOVA, E.YU. LISITSYNA, I.YU. TORSHIN, O.N. GRACHEVA
Российский сателлитный центр института микроэлементов ЮНЕСКО, Москва; Ивановская государственная медицинская академия; 3Самарский государственный медицинский университет
Ключевые слова: библиотека Кохрана, применение магния в акушерстве, кохрановские метаанализы, магне B6. Key words: Cochrane database, use of magnesium in obstetrics, Cochrane metaanalyses, magne B6.
Доказательная медицина — это концепция современного клинического мышления, куда входят новые технологии сбора, анализа, синтеза и применения научной медицинской информации с целью выработки необходимых клинических решений, служащих, в первую очередь, для оптимизации лечебной тактики в отношении больного.
Однако не следует забывать, что «доказательная медицина» (англ. evidence-based medicine) — сравнительно новое течение в области медицины. И, как часто бывает во всяком новом направлении исследований, существует значительный дисбаланс в методологии [21, 48]. Например, методология современной доказательной медицины во многом опирается просто на формальную статистику клинических исследований и в настоящее время довольно редко принимает во внимание огромный корпус данных по фармакологии, молекулярной биомедицине и фундаментальной медицине [48, 49]. По словам одного из ведущих специалистов по доказательности биомедицинских исследований проф. Д. Иоаннидиса [40], цели и задачи молекулярной биомедицины и доказательной медицины во многом сходятся и не следует разделять важные результаты этих двух, на первый взгляд различных, областей современной медицины.
Биоинформатика в смысле информационного менеджмента биологических и медицинских исследований имеет огромное значение для интеграции доказательной медицины с другими областями биомедицины [6, 48, 49]. В контексте биоинформационного подхода доказательная медицина является лишь верхушкой айсберга, в основании которого лежат фундаментальные свойства ионов и молекул, молекулярно-биологические и биохимические исследования. Экспериментальная и клиническая фармакология служит инструментом, соединяющим вместе столь разнородные данные (рис. 1).
Рис. 1. В основе доказательности — фундаментальная биохимия молекул.
Но вернемся собственно к доказательной медицине и доказательности в том смысле, как эти термины понимаются в настоящее время большинством врачей. Эпидемиолог Арчи Кохран (Archie Cochrane) еще в 1972 г. предложил метод обобщения результатов клинических испытаний, который получил название метаанализа. Это статистический метод, объединяющий результаты нескольких независимых исследований, чаще всего для оценки клинической эффективности терапевтических вмешательств. С этой целью объединяют результаты двух и более рандомизированных контролируемых исследований.
Метаанализ предполагает изучение всех исследований, посвященных соответствующей проблеме, оценку неоднородности и определение информативности основных результатов путем анализа чувствительности [48]. Он включает определение основной цели анализа, выбор способов оценки результатов, систематизированный поиск информации, обобщение количественной информации, анализ ее с помощью статистических методов, интерпретацию результатов. При этом можно значительно увеличить количество анализируемых групп больных и соответственно число включенных в исследование пациентов, однако все исследования должны быть проведены в одинаковых условиях. Кохрановские обзоры по акушерству и гинекологии издаются и на русском языке [2].
Следует отметить, что ни в коем случае нельзя абсолютизировать результаты метаанализов, изложенные в так называемых кохрановских обзорах. Во-первых, как и любой другой метаанализ, кохрановские обзоры во многом отображают личный взгляд авторов или просто устоявшееся мнение [21]. Во-вторых, от 3 до 10% уже опубликованных кохрановских обзоров «отзываются» (метка «WITHDRAWN»), т.е. по тем или иным причинам результаты определенных обзоров считаются недействительными самими редакторами издания Cochrane Database Syst Rev. Например, в 2011 г. опубликовано 235 кохрановских обзоров (на начало мая 2011 г.), из них отозвано — 21; в 2010 г. опубликовано 736 обзоров, отозвано — 35.
В настоящей статье рассматривается доказательная база по использованию магния в акушерско-гинекологической практике прежде всего на основе публикаций кохрановской библиотеки. За более чем столетний опыт применения препаратов магния в акушерстве основными причинами для назначения были и остаются невынашивание беременности и эклампсия [7, 9, 10, 50].
Говоря о применении магния при беременности не следует смешивать две проблемы — применение магния как токолитика в виде сульфата магния, применение хлорида магния в растворах для внутривенных инфузий с целью купирования ургентных ситуаций и профилактическое применение магния (перорально) для нутриентной поддержки и оптимизации рационального питания [6]. Применение сульфата магния в акушерстве было разобрано нами ранее [6]. В настоящей работе уделяется основное внимание пероральному приему магния как одной из основ превентивной стратегии в практическом акушерстве. Повсеместное распространение в России дефицита магния и многих других микронутриентов [4, 5, 8] делает необходимым специальную нутриентную поддержку беременности на основе высокоусвояемых органических солей магния.
Следует иметь в виду, что дефицит магния может проявляться в виде так называемых быстрых или непосредственных проявлений (судороги, ком в горле, мышечные подергивания, аритмия) и отдаленных, преимущественно обменных, нарушений.
Непосредственные проявления дефицита. Чаще всего быстро развившийся недостаток магния в организме приводит к состоянию повышенной нервной возбудимости клетки. Это особенно заметно на мышечных клетках, у которых деполяризация является основной функцией. При дефиците магния они испытывают нарушение деполяризации, что проявляется в избыточности процессов сокращения по отношению к процессам расслабления. Клинически — это мышечные подергивания и судороги, чаще в икроножных мышцах, что является нередкой проблемой при беременности. Аритмия у беременных очень часто ассоциирована именно с дефицитом магния [50].
Отдаленные, преимущественно обменные, нарушения. В первую очередь они формируются под воздействием гипомагниемии в различных органах, биологических жидкостях и тканях, при этом происходит патологическая компартментализация(от англ. compartmentalization — отделение.) элементов [50].
Например, кальцификация плаценты (так называемый феномен старения плаценты), кальцификация суставов, связочного аппарата; старение кости, кальцификация атеросклеротических бляшек аорты и других сосудистых образований. Причем этот процесс потенцируется дефицитом пиридоксина, витамина В12, фолатов, витамина D. Нередко на фоне недостаточности магния в питании, особенно при сопутствующем накоплении токсичных элементов — антагонистов магния (Ni, Pb, Cd, Be, Al), формируются камни в желчных путях, в почках и мочевом пузыре, суставах [1]. К отдаленным последствиям дефицита магния относится развитие во время беременности артериальной гипертензии, в частности, у женщин с гиперальдостеронизмом. Все эти факторы значительно повышают риск невынашивания беременности, которое также является «отдаленным» последствием дефицита магния.
Далее в статье приведен краткий обзор кохрановских метаанализов, затем более подробно рассматриваются влияние препаратов магния на быстрые проявления дефицита магния (судороги при беременности), внутривенное использование сульфата магния в терапии эклампсии и профилактика отдаленных нарушений дефицита магния при беременности.
Несмотря на то что опубликовано всего несколько исследований по применению цитрата магния в акушерстве, данная органическая форма магния имеет большие перспективы применения в этой области. В первую очередь это относится к применению магния для терапии и профилактики преэклампсии, нефропатии беременных, мочекаменной болезни и других заболеваний почек у беременных. Безопасность цитрата магния и его высокая биоусвояемость делают актуальным его употребление беременными с целью профилактики и лечения нарушений функции почек.
Краткий обзор кохрановских метаанализов по применению препаратов магния
Всего было проведено 47 кохрановских метаанализов по изучению сульфата магния (2000—2011), суммарно включивших более 27 900 человек. В основном в данных работах изучали эффекты сульфата магния при осложнениях беременности — преэклампсии и эклампсии (более 20 000 женщин). Было проведено не менее 10 кохрановских метаанализов по изучению эффективности сульфата магния при лечении преэклампсии и эклампсии [24—35]. Данные по изучению применения органических солей магния (лактата магния, цитрата магния, аспартата магния) с целью профилактики преждевременных родов, профилактики рождения детей с низкой массой тела, задержкой внутриутробного развития, а также для профилактики и лечения судорог икроножных мышц у беременных также основаны на наблюдении за значительной когортой (более 11 000 женщин).
Негативные результаты кохрановских метаанализов относились к внутривенному пути введения сульфата магния и включали отсутствие эффектов в профилактике преждевременных родов [18, 37], терапии легочной гипертензии новорожденных [39], использовании комбинации кальция, магния и калия в лечении эссенциальной гипертонии [15]. Следует отметить три интересных направления использования сульфата магния в терапии, которые, хотя и не имеют прямого отношения к беременности, тем не менее указывают на доказательность его соответствия категориям «А» и «В» классификаций категорий риска лекарственных средств для плода и перспективу использования: применение сульфата магния при инсульте, бронхиальной астме и при остром инфаркте миокарда [43].
Вторичная ишемия мозга — частое осложнение субарахноидального кровотечения. Для лечения используются такие кальциевые антагонисты, как нимодипин и сульфат магния. В кохрановском метаанализе 16 исследований, включившем 3361 пациента, использование сульфата магния в дополнение к стандартному лечению нимодипином на 25% снижало риск осложнений (ОШ 0,75; 95% ДИ 0,57—1,00) и на 34% риск проявления клинических симптомов вторичной ишемии (ОШ 0,66; 95% ДИ 0,45— 0,96) [25].
Смертность от острого инфаркта миокарда остается высокой. Внутривенное введение сульфата магния является многообещающим терапевтическим воздействием. Кохрановский метаанализ рандомизированных исследований показал, что дополнение стандартной терапии сульфатом магния позволяет снизить раннюю смертность от острого инфаркта миокарда на 34%, риск желудочковой тахиаритмии на 55% (ОШ 0,45; 95% ДИ 0,31—0,66) и в том числе снизить риск тяжелой желудочковой тахиаритмии (ОШ 0,72; 95% ДИ 0,6—0,85) [42].
В кохрановском метаанализе 6 исследований, включившем 296 пациентов с бронхиальной астмой, было показано, что дополнение вдыханием сульфата магния терапии приступов бронхообструкции Ц-агонистами повышало эффективность лечения [16].
Кохрановские обзоры: магний и судороги икроножных мышц у беременных
Судороги мышц ног доставляют много беспокойства беременным женщинам, особенно с 16—20 нед беременности [36]. Распространенность судорог икроножных мышц у беременных достигает 45% случаев, причем в половине наблюдений они появляются после 25-й недели беременности. В 76% случаев женщины испытывают судороги до 2 раз в неделю и в подавляющем большинстве в ночное время. В целом судороги обременительны для женщины, так как ухудшают сон и самочувствие днем [51]. Дефицит магния у беременных провоцирует не только судороги икроножных мышц, но и аритмию; он меняет глюкозотолерантность тканей, повышает риск избыточной прибавки массы тела и гестационного диабета [38].
Чаще судороги у беременных развиваются по ночам, что совпадает с суточным ритмом концентрации магния и кальция: акрофаза концентрации кальция достигается в ночные часы (2—4 ч ночи) и совпадает с батифазой магния. Судорога чаще появляется при подъеме утром с постели, уменьшается при массаже и не повреждает икроножных мышц. Предполагается наличие венозного застоя, снижения тонуса вен, повышения внутрибрюшного давления, пищевых (витаминных, минеральных — магний, калий, кальций, и пр.) дефицитов, вызванных требованиями растущего плода, обезвоживания. Полагают, что боль вызывается избытком молочной кислоты, которая способствует непроизвольному сокращению мышц, особенно мышц ног.
Один из первых анализов исследований, соответствующих высоким требованиям доказательной медицины в отношении использования препаратов магния у беременных, был опубликован в 2002 г. в базе данных Cochrane в виде аналитического обзора «Interventions for leg cramps in pregnancy. Cochrane Database of Systematic Reviews 2002, Issue 1.», проведенного G. Young и D. Jewell [52]. В него вошли данные 5 исследований, включавших 352 беременных, которых на момент включения в исследование беспокоили судороги ног и которые применяли разнообразные медикаментозные средства. Данные исследования включили оценку эффекта лактата кальция без применения контрольной группы (M. Hammar, 1981); лактат кальция, применяемый внутрь, сравнивался с плацебо в виде аскорбиновой кислоты (M. Hammar, 1987); хлорид натрия и лактат кальция сравнивались между собой, а также с плацебо (Robinson, 1947); поливитаминные или полиминеральные добавки, в состав которых входили цинк, железо, лактат магния, аскорбиновая кислота, витамин B6, фолиевая кислота и др. сравнивались с плацебо (Thauvin, 1992); препараты магния (лактат и цитрат) сравнивались с плацебо в виде сорбитола, фруктозы и декстрозы [52].
Достоверно показан положительный эффект применения магния в работе L. Dahle и соавт. [20]. Исследование, проводившееся в двух различных центрах в Швеции, было проспективным, двойным слепым, плацебо-контролируемым, рандомизированным. В нем участвовали 73 женщины в различные сроки беременности (от 22 до 36 нед, средний срок — 29 нед). Оценивались сывороточные уровни магния (атомная абсорбционная спектрофотометрия) и клинические симптомы (с помощью вопросника: длительность и частота судорог). Интенсивность судорог определяли по визуальной аналоговой шкале. Пациентки также давали оценку эффективности лечения. В результате трехнедельной терапии установлено, что магний в виде органических солей — магния лактата и магния цитрата с высокой достоверностью уменьшает и в ряде случаев полностью купирует судороги икроножных мышц у беременных. Только у 23 из 34 женщин через 3 нед терапии судороги еще имели место по сравнению с почти полным их сохранением в контрольной группе (у 33 из 35). По оценке женщин, магний имел преимущество перед плацебо (p=0,0002). Также был показан хороший уровень безопасности применения лактата магния и цитрата магния у беременных: побочные реакции (тошнота) носили незначительный и редкий характер.
Таким образом, систематизация данных по применению солей магния, по данным обзора Кохрановской библиотеки [52], позволяет сделать заключение, что в клинических условиях признается хорошо доказанным фактом эффективность применения лактата магния или цитрата магния (в виде смеси лактата и цитрата магния 5 ммоль утром и 10 ммоль вечером) при судорогах икроножных мышц у беременных. В обзоре подчеркивается высокая безопасность применения лактата и цитрата магния у беременных в указанных дозах. В связи с этим терапия такими препаратами, как магне В6 (комбинация лактата магния и пиридоксина), приобрела особое значение во время беременности и в предродовом периоде.
Магнезиальная терапия преэклампсии (гестоза), эклампсии
Первое назначение магния было проведено французским акушером М. Бертраном для снятия судорог при эклампсии в 1906 г. Таким образом, применение магния в акушерстве перешагнуло 100-летний рубеж. Чем это обусловлено? Основными показаниями к применению магния у беременных все это время были невынашивание беременности и эклампсия — тяжелое полиорганное расстройство. Патогенез эклампсии сложен и включает эндотелиальную дисфункцию, нарушение реологии крови, генерализованную вазоконстрикцию. К механизмам положительного действия магния при эклампсии относятся угнетение синтеза тромбоксана A2, компенсация так называемого кальциевого спазма, что и позволяет магнию ослабить констрикцию сосудов и оптимизировать церебральную гемодинамику у беременной и кровообращение в системе мать—плацента—плод [11]. Введение магния пациенткам с эклампсией повышает уровень кальцитонина в сыворотке крови, существенно сниженный у женщин уже в период преэклампсии [14]. Хорошая эффективность магнезиальной терапии при лечении эклампсии и значимое снижение материнской смертности показаны в исследовании MAGPIE, в котором лечение магнием в 2 раза уменьшало риск развития эклампсии при отсутствии существенных побочных реакций [41].
В весьма показательном метаанализе 6 исследований (11 444 беременных) было установлено, что терапия сульфатом магния более чем в 2 раза шижает риск развития эклампсии (ОР 0,41; 95% ДИ 0,29—0,58), на 46% снижает материнскую смертность, но часто (24%) вызывает побочные эффекты (преимущественно горячие приливы во время капельного введения) [24, 29, 32].
В метаанализе [45] сравнивалась эффективность магнезиальной терапии и антиконвульсантов (диазепам, фенитоин, литические смеси) у 2241 женщины. Сульфат магния снижал риск развития эклампсии в большей степени, чем фенитоин (ОР 0,05; ДИ 0,00—0,84), но увеличивал риск кесарева сечения. Эффективность сульфата магния была сравнима или превосходила таковую антиконвульсантов при профилактике и лечении эклампсии. Кроме того, при использовании препаратов магния значительно реже наблюдались случаи перинатальной смерти, особенно при сравнении с литическими коктейлями. Выявлены также преимущества использования магния сульфата по сравнению с антагонистами кальция при преэклампсии умеренной степени, в то время как при тяжелой преэклампсии нимодипин в большей степени улучшал мозговое кровообращение, нежели магния сульфат. Известно, что низкий уровень внутриклеточного магния может способствовать развитию артериальной гипертензии у беременных. На этом основано применение магния при изолированной гипертензии беременных, хотя он не относится к препаратам для лечения артериальной гипертонии. Показано [46], что гипотензивная активность магния сопоставима с препаратом метилдопа.
Разные антиконвульсанты используются для терапии эклампсии. В кохрановском метаанализе 7 рандомизированных исследований, включившем 1396 женщин, исследовались эффекты диазепама и сульфата магния [17, 24, 29, 32]. Использование вливаний сульфата магния способствует снижению материнской смертности в среднем на 40% (1396 женщин, ОР 0,59; 95% ДИ 0,38—0,92) и также риска судорог (ОШ 0,43; 95% ДИ 0,33—0,55) по сравнению с диазепамом. В группе женщин, получавших сульфат магния, уменьшалось число новорожденных, имевших менее 7 баллов по шкале Апгар на 1-й минуте жизни (597 новорожденных; ОШ 0,75; 95% ДИ 0,65—0,87) и на 34% снижался риск нахождения ребенка в роддоме более 7 дней (3 исследования, 631 новорожденный; ОШ 0,66; 95% ДИ 0,46—0,96). Таким образом, внутривенное использование сульфата магния у беременных с эклампсией снижает и риск материнской смертности, и риск судорог. Сульфат магния оказывает нейропротективное действие на плод. Кохрановский метаанализ 5 рандомизированных исследований, суммарно включивший 6145 новорожденных, показал, что антенатальное применение сульфата магния значительно снижало риск развития детского церебрального паралича (на 32% ОШ 0,68; 95% ДИ, 0,54—0,87), а также тяжелых моторных дисфункций у новорожденных (ОШ 0,61; 95% ДИ 0,44—0,85) [22].
Однако, несмотря на очевидную пользу от внутривенного применения сульфата магния при эклампсии, данная процедура требует чрезвычайно внимательного отношения к дозировке магния. При передозировках сульфата магния уже в 2—3 раза чрезвычайно увеличивается риск для плода. Доказательная база по безопасности использования сульфата магния в акушерско-гинекологической практике разобрана нами в отдельной работе [6]. В кохрановском метаанализе 23 исследований, суммарно включившем более 2000 женщин, риск смерти новорожденного был почти в 3 раза выше при использовании сульфата магния (7 исследований, 727 новорожденных: ОШ 2,82; 95% ДИ 1,20—6,62) [18].
Общепринято только внутривенное введение сульфата магния. Дозы уточняют с учетом терапевтического эффекта и концентрации ионов магния в сыворотке крови. Обычно используется 20—25% раствор сульфата магния [3]. При преэклампсии и эклампсии в течение 20 мин вводится насыщающая доза (2—4 г), затем со скоростью 1—2 г/ч вводится поддерживающая доза в суммарном количестве не более 4 г. При тетании матки доза насыщения выше — 4 г в течение 20 мин, поддерживающая доза: сначала — 1—2 г/ч, затем — 1 г/ч (можно вводить капельно медленно в течение 24—72 ч).
С развитием клинической нутрициологии обозначилась другая сторона проблемы — хронический магниевый дефицит, часто встречаемый у женщин, и особенно у беременных. Использование пероральных органических препаратов магния и оптимизация питания хорошо компенсируют дефицит магния и показаны для профилактики возможных осложнений и повышения вероятности нормальных родов.
Доказательность использования органических солей магния для профилактики патологии беременности
В кохрановском метаанализе 2010 г. систематизированы данные 7 исследований (2689 женщин) по изучению влияния органических солей магния, назначаемых per os, на исход беременности и состояние беременной и плода [44]. По результатам этого объединенного анализа, имевшего кластерный дизайн, было выявлено, что прием магния до 25-й недели беременности (по сравнению с плацебо) снижает частоту преждевременных родов (ОР 0,73; 95% ДИ 0,57—0,94) и рождение детей с низкой массой тела (ОР 0,67; 95% ДИ 0,46—0,96). Более того, женщины, принимавшие органический магний внутрь, реже были госпитализированы (ОР 0,66; 95% ДИ 0,49—0,89) и у них реже наблюдались явления угрозы прерывания беременности (ОР 0,38; 95% ДИ 0,16—0,90) [44]. Результаты этого метаанализа представляют определенный практический интерес, поэтому остановимся на них подробнее. Отдельные исследования обозначаются далее с указанием года и страны (полные ссылки см. в списке литературы).
Важно отметить, что в 6 из 7 исследований, рассмотренных в метаанализе [44], использовались именно органические соли магния: цитрат (1 исследование), глюконат (2 исследования), аспартат (3 исследования). Цитрат магния рандомизированно назначался 530 беременным женщинам в количестве 15 ммоль цитрата магния (360 мг/сут в расчете на элементарный магний) ежедневно с начала до 25-й недели беременности (исследование «Австрия, 1997») [12, 13].
Эффекты глюконата магния изучались в 2 работах (исследование «Китай, 1997») [42] и (исследование «Миссисипи, 1992»). В исследовании 102 женщины были рандомизированы для приема глюконата магния в дозе 2 г/ сут с 28-й недели беременности по 30-ю неделю, а с 30-й недели беременности до родов — 3 г/сут (Китай, 1997). 54 женщины с высоким риском ранних родов были рандомизированы для приема 4 г/сут глюконата магния, начиная с 23-й недели беременности (216 мг в расчете на элементный магний) (Миссисипи, 1992).
Эффекты аспартата магния были изучены в 3 когортах: 985 женщин (15 ммоль/сут аспартата магния с 6—21-й недели до родов (исследование «Венгрия, 1988», 400 женщин (аспартат гидрохлорид магния, 365 мг/сут в расчете на элементарный магний с 13—24-й недели до родов (исследование «Мемфис, 1989») и в когорте из 568 женщин, которые были рандомизированы для приема 15 ммоль/сут аспартата гидрохлорида магния с 16 нед до родов (исследование «Цюрих, 1988».
Метаанализ этих исследований показал, что в большинстве работ прием магния приводил к значительному снижению риска преждевременных родов. В среднем по 5 исследованиям риск снижался на 27% (рис. 2).
Рис. 2. Снижение риска преждевременных родов по данным кохрановского метаанализа [44].
Здесь и далее горизонтальная линия отображает 95% достоверный интервал (95% ДИ), положение центрального квадрата — отношение шансов (ОШ), а размер квадрата показывает местонахождение 25—75% значений. Наблюдаемые эффекты тем сильнее, чем дальше от центральной линии расположены ОШ и 95% ДИ. 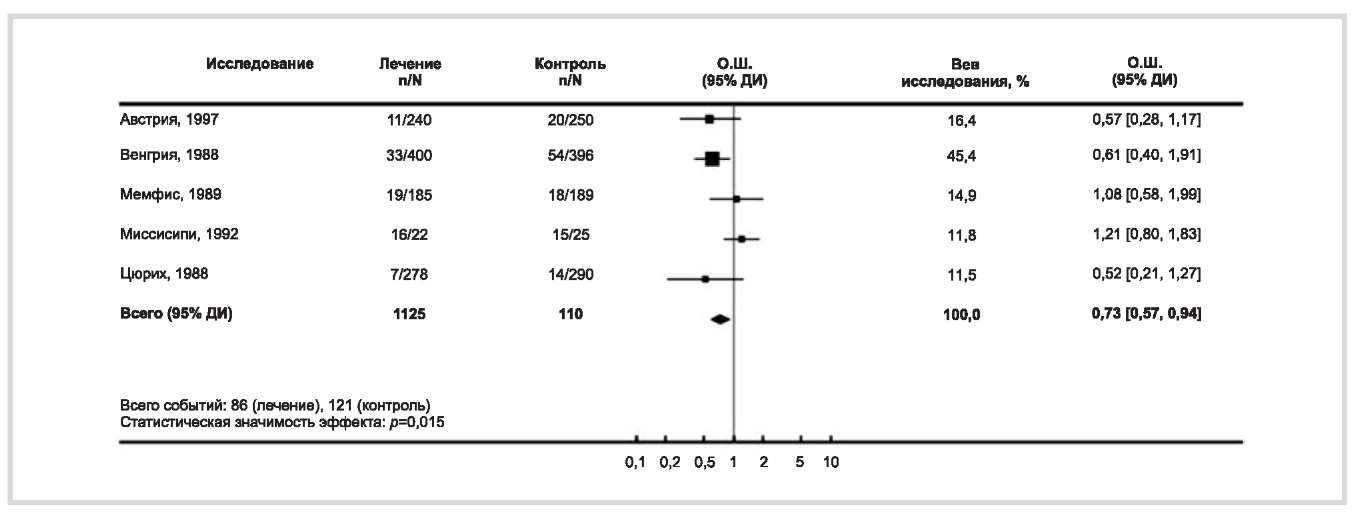
В 2 исследованиях (Австрия, 1997; Цюрих, 1988) было установлено, что пероральный прием органических солей магния снижал необходимость госпитализации матери на 34% (рис. 3) и, в частности, способствовал значительному (на 62%) снижению риска кровотечения в родах.
Рис. 3. Снижение риска необходимости госпитализации матери [44].
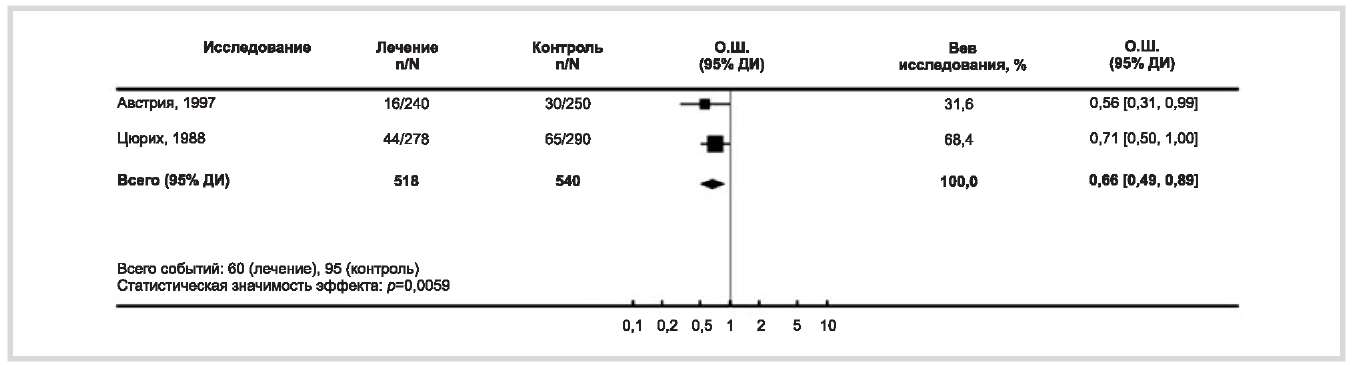
В 3 исследованиях показано, что прием внутрь органических солей магния способствовал профилактике низкой массы тела ребенка (менее 2500 кг) при рождении в среднем на 33% (рис. 4); в частности снижался риск рождения ребенка с очень низкой массой (менее 1500 г) на 48%. Следует отметить, что в 1 исследовании [19] использовался оксид магния, поэтому низкая результативность данного исследования неудивительна.
Показано, что доказательная база в отношении приема органических солей магния отнюдь не ограничивается цитированными выше исследованиями. Например, доказательная база по цитрату магния включает 54 исследования [47]. Систематический анализ мировой литературы по фармакологии и клиническим исследованиям цитрата магния показал, что практически полная утилизация цитрата делает его «экологически чистой тарой» для транспорта магния внутрь клеток. Имеющаяся доказательная база указывает на высокую эффективность цитрата магния, применяемого в терапии и для профилактики образования почечных камней, для компенсации гипомагнеимии, в лечении сосудистых заболеваний, для нормализации минеральной плотности костей, лечения синдрома беспокойных ног и бронхиальной астмы.
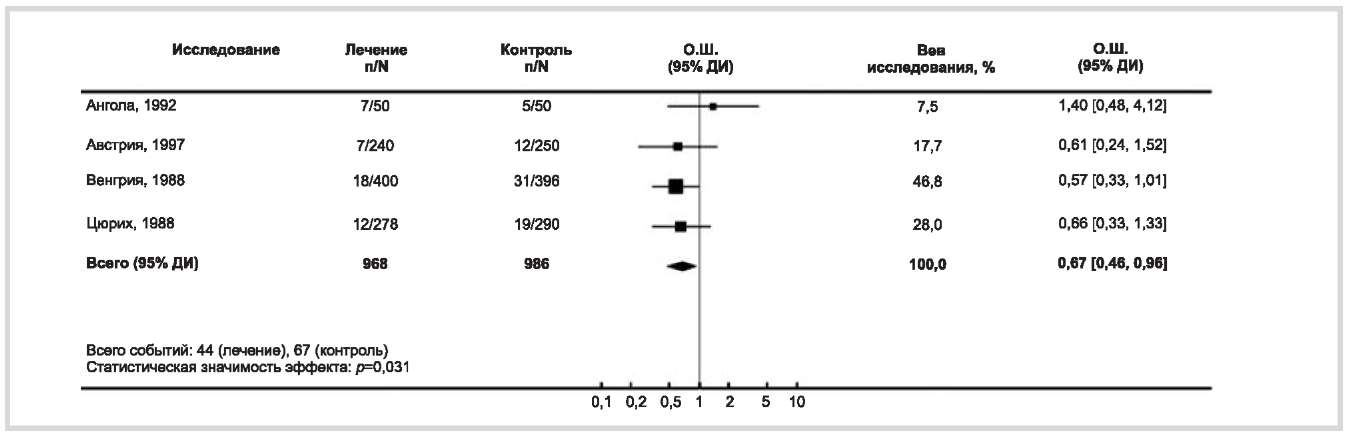
Рис. 4. Профилактика низкой массы ребенка при рождении органическими солями магния.
В исследовании (Ангола, 1992) использовался низкоусвояемый оксид магния, в остальных исследованиях — органические соли магния.
Коррекция дефицита магния при беременности. Принципы дозирования
Текущая физиологическая суточная потребность в магнии для взрослых составляет около 400 мг/сут, максимально до 800 мг/сут. При идеальном состоянии желудочно-кишечного тракта, эубиозе флоры кишечника, отсутствии полиморфизмов генома, связанных с нарушениями обмена магния, это можно обеспечить питанием (вода и пища). Необходимое количество рассчитывается, исходя из следующего показателя: 5 мг/кг/сут. Некоторым людям необходимо большее количество магния из-за значительных потерь. Детям требуется от 5 до 10 мг/ кг/сут; беременным женщинам (или кормящим матерям) — 10—15 мг/кг/сут; женщинам с установленным дефицитом магния также требуется 10—15 мг/кг/сут.
Парентеральная магнезиотерапия показана лишь в ургентных ситуациях магниевого дефицита. Обычная доза составляет 100 мг/ч внутривенно капельно или с помощью автоматических шприцев в течение 4—6 ч в сутки. При эклампсии допустимо медленное внутривенное введение 25% магния сульфата в дозе 10—20 мл. Быстрое введение магния чревато гипермагнезиемией. Парентеральная магнезиотерапия при острой необходимости должна проводиться лишь в стационарных условиях.
Препаратами выбора для долговременной профилактики и лечения дефицита магния являются лекарственные формы для приема внутрь. При этом органические соли магния не только значительно лучше усваиваются, но и легче переносятся больными. Они реже дают побочные эффекты со стороны пищеварительного тракта и лучше восполняют дефицит элемента. Существует несколько хорошо всасывающихся в кишечнике галеновых форм, выпущенных в виде препаратов: магния гидроксид; магния цитрат; магния глюконат; магния оротат; магния тиосульфат; магния лактат (в составе препарата магне В6 в
табл.) магния лактат и магния пидолат (в составе препарата магне В6 в форме раствора для питья). Содержание элементарного магния в лекарственных формах неодинаково. Например, магния гидроксид, таблетки жевательные — 130 мг; магния глюконат, табл. 0,5 г — 27 мг; магния цитрат, табл. шипучие 0,15 г — 24,3 мг; магния оротат, табл. 0,5 г — 32,8 мг; магния тиосульфат, табл. 0,5 г — 49,7 мг; магния лактат (в составе препарата магне В6 в табл. — 470 мг) — 48 мг.
Максимальный лечебный эффект коррекции дефицита магния достигается при пероральном приеме потенцированных органических форм магния: магне В6 (магния лактат, 48 мг/табл. в расчете на Mg++), магне В6, раствор для питья (магния пидолат и магния лактат, 100 мг/10 мл в расчете на Mg++), магне В6 форте (магния цитрат, 100 мг/ табл. Mg++), магния глицинат и др. Если применить данные цитированного выше кохрановского обзора [52], 1 ммоль магния соответствует 238 мг соли магния лактата. В одной таблетке магне В6 содержится 1,97 ммоль магния. Следует отметить, что такая дозировка (6—7 табл. магне В6 или 3 табл. магне В6 форте) нужна только в самом начале терапии судорог у беременных (1—2 недели). Уже со 2—3-й недели дозу магния можно понизить до 5—7,5 ммоль (3—4 таблетки магне В6 или 1—2 табл. магне В6 форте).
В цитированном ранее кохрановском метаанализе 7 рандомизированных исследований 2689 женщин, получавших пищевые добавки с магнием [44], положительные эффекты магния проявлялись при пероральном приеме органических солей магния (цитрат, глюконат, аспартат) в количествах 200—400 мг/сут в расчете на элементарный магний. Пероральный прием магния способствовал снижению преждевременных родов (ОШ 0,73; 95% ДИ 0,57— 0,94), малой массы тела ребенка при рождении (ОШ 0,67; 95% ДИ 0,36—0,96) и риска кровотечения в родах (ОШ 0,38; 95% ДИ 0,49—0,89).
Таким образом, представленные в настоящей статье данные обзоров библиотеки Кохрана однозначно показывают, что утверждения вроде «доказательность пользы приема магния — слабая», «по данным доказательной медицины, при дефиците магния у беременных эффективен только сульфат магния», «пероральные формы магния неэффективны» и т.д. находятся в прямом противоречии с реально имеющимися данными доказательной медицины. Индивидуумы, позволяющие себе такого рода высказывания, оперируют не данными доказательной медицины, а истеричными и манипулятивными методами желтой прессы. Нельзя исключить, что такого рода заявления могут являться частью программы вымогательства и шантажа, направленного против производителей фармацевтических препаратов... Терапия современными пероральными препаратами магния (такими, как магне В6) приобретает особое значение во время беременности и в предродовом периоде вследствие высокой биоусвояемости магния в этих препаратах, их высокой доказанной эффективности, значительного опыта их использования и высокой безопасности.
ЛИТЕРАТУРА
1. Авцын А.П., Жаворонков А.А., Риш М.А., Строчкова Л.С. Микроэлементозы человека: этиология, классификация, органопатология. М: Медицина 1994;496.
2. Беременность и роды. Кохрановское руководство. Под ред. Г.Т. Сухих. М: Логосфера 2010;560.
3. Видаль — справочник: Лекарственные препараты в России. М: АстраФармСервис 2011;1488.
4. Громова О.А. Магний и пиридоксин: основы знаний. М: ПротоТип 2006;234.
5. Громова О.А. Витамины и микроэлементы у беременных и кормящих: Обучающие программы ЮНЕСКО. М 2009;130.
6. Громова О.А., Торшин И.Ю., Серов В.Н. Магний в акушерстве и гинекологии: История применения и современные взгляды. Трудный пациент 2008;8:20—29.
7. Кошелева Н.Г. Роль гипомагниемии в акушерской патологии и методы ее коррекции. Вестн Рос ассоц акушгин 1999;1:42—46.
8. Орлова С.В. Распространенность алиментарнозависимых заболеваний в России. Юбилейный выпуск к 10-летию кафедры клинической нутрициологии. Вестн РУДН 2009;15—19.
9. Пособие для врачей: Программы ЮНЕСКО. Под ред. В.М. Сидельникова. М 2007;124.
10. Серов В.Н., Тютюнник В.Л., Твердикова Л.А. РМЖ: Акушерство 2011;19:5:3—7.
11. Adam B., Malatyalioglu E., Alvur M., Talu C. Magnesium, zinc and iron levels inpre-eclampsia. J Matern Fetal Med 2001;10:4:246—250.
12. Arikan G., Gucer F., Scholl W., Weiss PAM. Preterm labour during oral magnesium supplementation in uncomplicated pregnancies [Fruhgeburtlichkeit unter oraler magnesiumsubstitution beiunko-mplizierten schwangerschaften: eine randomisiert kontrolliert klinische studie]. Geburtshilfe und Frauenheilkunde 1997;57:491—495.
13. Arikan G., Panzitt T., Gaucer F. et al. Oral magnesium supplementation and the prevention of preterm labor. Am J Obstet Gynec 1997;176:1:Pt2:45.
14. Belfort M.A., Anthony J., Saade G.R., Allen J.C. A comparison of magnesium sulfate and nimodipine for the prevention of eclampsia. N Engl J Med 2003;348:4:304—311.
15. Beyer F.R., Dickinson H.O., Nicolson D.J. et al. Combined calcium, magnesium and potassium supplementation for the management of primary hypertension in adults. Cochrane Database Syst Rev 2006;3:CD004805.
16. BlitzM., Blitz S., Beasely R. et al. Inhaled magnesium sulfate in the treatment of acute asthma. Cochrane Database Syst Rev 2005;4:CD003898.
17. Bruno V. Antidegenerative effects of Mg2++-valproate in cultured cerebellar neurons. Funct Neurol 1995;10:3:121—130.
18. Crowther C.A., Hiller J.E., Doyle L.W. Magnesium sulphate for preventing preterm birth in threatened preterm labour. Cochrane Database Syst Rev 2002;4:CD001060.
19. DAlmeida A., Carter J.P., Antol A., Prost C. Effects of a combination of evening primrose oil (gamma linolenic acid) and fish oil (eicosapentaenoic + docosahexaenoic acid) versus magnesium, and placebo in preventing pre-eclampsia. Women and Health 1992;19:117—131.
20. Dahle L.O., Berg G., Hammar M. et al. The effect of oral magnesium substitution on pregnancy-induced leg cramps. Am J Obstet Gynec 1996;175:1:233—234.
21. Devisch I., Murray S.J. We hold these truths to be self-evident': deconstructing 'evidence-based' medical practice. J Eval Clin Pract 2009;15:6:950—954.
22. Doyle L.W., Crowther C.A., Middleton P. et al. Magnesium sulphate for women at risk of preterm birth for neuroprotection of the fetus. Cochrane Database Syst Rev 2009;1:CD004661. Review.
23. Dorhout-Mees S.M., Rinkel G.J., Feigin V.L. et al. Calcium antagonists for aneurysmal subarachnoid haemorrhage. Cochrane Database Syst Rev 2007;3:CD000277.
24. Duley L. Magnesium sulphate and other anticonvulsants for women with pre-eclampsia. Cochrane Database Syst Rev 2010;10:11:CD000025.
25. Duley L. Magnesium sulphate versus diazepam for eclampsia. Cochrane Database Syst Rev 2010;12:CD000127. Review.
26. Duley L. Magnesium sulphate and other anticonvulsants for women with pre-eclampsia. Cochrane Database Syst Rev 2010;11:CD000025. Review.
27. Duley L. Magnesium sulphate versus phenytoin for eclampsia. Cochrane Database Syst Rev 2010;10:CD000128. Review.
28. Duley L. Magnesium sulphate versus lytic cocktail for eclampsia. Cochrane Database Syst Rev 2010;CD002960. Review.
29. Duley L. Alternative magnesium sulphate regimens for women with pre-eclampsia and eclampsia. Cochrane Database Syst Rev 2010;8:CD007388. Review.
30. Duley L. Magnesium sulphate versus phenytoin for eclampsia.Co-chrane Database Syst Rev 2003;4:CD000128. Review. Update in: Cochrane Database Syst Rev 2010;10:CD000128.
31. Duley L. Magnesium sulphate versus diazepam for eclampsia. Co-chrane Database Syst Rev 2003;4:CD000127. Review. Update in: Cochrane Database Syst Rev 2010;12:CD000127.
32. Duley L. Magnesium sulphate versus diazepam for eclampsia.Co-chrane Database Syst Rev 2010;12:CD000127.
33. Duley L. Magnesium sulphate and other anticonvulsants for women with pre-eclampsia. Cochrane Database Syst Rev 2003;2:CD000025. Review. Update in: Cochrane Database Syst Rev 2010;11:CD000025.
34. Duley L. Magnesium sulphate versus phenytoin for eclampsia. Cochrane Database Syst Rev 2000;2:CD000128. Review.
35. Duley L., Henderson-Smart D. Magnesium sulphate versus diazepam for eclampsia. Cochrane Database Syst Rev 2000;2:CD000127. Review. Update in: Cochrane Database Syst Rev 2003;4:CD000127. Cochrane Database Syst Rev 2003;4:CD000128.
36. Frusso R., Zdrate M., Augustovski F., Rubinstein A. Magnesium for the treatment of nocturnal leg cramps: a crossover randomized trial. J Fam Pract 1999;48:11:868—871.
37. Han S., Crowther C.A., Moore V. Magnesium maintenance therapy for preventing preterm birth after threatened preterm labour. Cochrane Database Syst Rev 2010;7:CD000940.
38. Henriksen E.J. Exercise training and the antioxidant alpha-lipoic acid in the treatment of insulin resistance and type 2 diabetes. Free Radic Biol Med 2006;40:1:3—12.
39. Ho J.J., Rasa G. Magnesium sulfate for persistent pulmonary hypertension of the newborn. Cochrane Database Syst Rev 2007;3:CD005588.
40. Ioannidis J.P. Molecular evidence-based medicine: evolution and integration of information in the genomic era. Eur J Clin Invest 2007;37:5:340—349.
41. James M. Magnesium in obstetrics. Best Pract Res Clin Obst Gyn 2010;24:Iss. 3:327—337.
42. Li S., Tian H. Oral low-dose magnesium gluconate preventing pregnancy induced hypertension. Chunh-Hua-Fu-Chan-Ko-Tsa-Chih (Chinese Journal of Obstetrics and Gynaecology) 1997;32:613—615.
43. Li J., Zhang Q., Zhang M., Egger M. Intravenous magnesium for acute myocardial infarction. Cochrane Database Syst Rev 2007;2:CD002755.
44. Makrides M., Crowther C.A. Magnesium supplementation in pregnancy. Cochrane Database Syst Rev 2001;4:CD000937.
45. Manyemba J. Magnesium sulphate for eclampsia: putting the evidence into clinical practice. Cent Afr J Med 2000;46:6:166—169.
46. Morgan P.J., Kung R., Tarshis J. Nitroglycerin as a uterine relaxant: a systematic review. J Obstet Gynaec Can 2002;24:5:403— 409.
47. Roffe C., Sills S., Crome P., Jones P. Randomised placebo controlled trial of magnesium citrate in the treatment of chronic persistent leg cramps. Med Sci Monit 2002;8:5:CR326—330.
48. Torshin I.Yu. Bioinformatics in the post-genomic era: physiology and medicine. Nova Biomedical Books NY USA 2007;ISBN:1600217524;1—20.
49. Torshin I.Yu. Bioinformatics in the post-genomic era: sensing the change from molecular genetics to personalized medicine. Nova Biomedical Books NY USA 2009;In «Bioinformatics in the Post-Genomic Era» series, ISBN:978-1-60692-217-0.
50. Torshin I.Yu., Gromova O.A. Magnesium and pyridoxine: fundamental studies and clinical practice. NY: Nova Science 2009;ISBN-10:1-60741-704-9.
51. Valb0 A., B0hmer T. Leg cramps in pregnancy — how common are they? Tidsskr Nor Laegeforen 1999;119:11:1589—1590.
52. Young G.L., Jewell D. Interventions for leg cramps in pregnancy. Cochrane Database Syst Rev 2002;Issue 1. Art. No.:CD000121.
DOI: 10.1002/14651858. CD000121.
