Контролированное по плацебо рандомизированное исследование по применению интерферона бета-1 b в лечении второй, прогрессирующей фазы рассеянного склероза
СтатьиОпубликовано в журнале:
Международный Медицинский Журнал »» 4 / 2000 Европейская исследовательская группа по применению интерферона бета-1b в лечении второй, прогрессирующей фазы рассеянного склероза под руководством Людвига Каппоса
Отделение невропатологии, Университетская больница Базеля, Базель, Швейцария
Обоснование исследования.Благоприятное действие интерферона бета наблюдалось ранее только у пациентов в фазе чередования ремиссий и обострений рассеянного склероза (PC). Но до сих пор не оценивалась роль этого препарата при второй, прогрессирующей фазе данного заболевания (ВП-РС), эффективного лекарственного лечения которой до сих пор разработано не было.
Методы. В настоящем многоцентровом, с двойным сокрытием информации, контролированном по плацебо исследовании амбулаторные больные с баллом 3,0-6,5 по Расширенной шкале статуса инвалидности (Extended Disability Status Scale - EDSS) получали либо 8 млн. ME (IV) интерферона бета-1b подкожно через день, либо плацебо сроком до 3 лет. Эффективность лечения оценивалась, главным образом, по сроку до подтвержденного усугубления инвалидности величиной в 1,0 EDSS, которое сохранялось в течение 3 месяцев, либо величиной в 0,5 балла, если исходно EDSS составляла 6,0-6,5. Заранее запланированный промежуточный анализ безопасности и эффективности в популяции, получавшей лечение, был проведен после того, как все пациенты уже участвовали в исследовании, по крайней мере, 2 года.
Результаты. 358 больных с ВП-РС были распределены на получение плацебо, а 360 - на прием интерферона бета-1b; 57 пациентов (31 из группы плацебо и 26 из группы, получавшей интерферон бета-1b) были потеряны из наблюдения. Выявлено в высокой степени достоверное различие в пользу интерферона бета-1b по сроку до наступления подтвержденного усугубления инвалидности (р=0,0008). Интерферон бета-1b задерживал прогрессирование на 9-12 месяцев в период исследования 2-3 года. Соотношение различия для подтвержденного прогрессирования составило 0,65 (95% доверительный интервал 0,52-0,83). Этот благоприятный эффект наблюдался как при повторных рецидивах, так и при неуклонном прогрессировании заболевания без рецидивов. Положительные результаты были получены и судя по времени до прикованности к креслу-каталке, а также в отношении частоты и тяжести рецидивов, числа курсов стероидов, числа госпитализаций и данных магнитно-резонансной томографии. Применение препарата было безопасным, характер и частота побочных действий соответствовали предшествующему опыту с интерфероном бета-1b. Исследование было прекращено после того, как промежуточные результаты позволили ясно судить об эффективности.
Выводы. Терапия интерфероном бета-1b задерживает прогрессирование у больных с ВП-РС. Этот препарат представляет собой первое средство, оказывающее терапевтический эффект при ВП-РС.
Введение в 1993 году интерферона бета-1b в схемы лечения рассеянного склероза (PC) явилось значительным шагом вперед в помощи таким больным [I]. Имеется 3 препарата, содержащих интерферон бета, и испытания III фазы каждого из них показали снижение частоты рецидивов на 18-34% у больных с PC в фазе чередований рецидивов и ремиссий [1-3]. Такое уменьшение активности заболевания сопровождалось поразительным влиянием на патологические изменения, выявляемые при магнитно-резонансной томографии (МРТ), в особенности, на развитие новых участков поражения, накапливающих контрастное вещество.
У больных с PC и у их врачей большую озабоченность вызывает усугубление инвалидности, когда наступает вторая, прогрессирующая (ВП-РС) фаза заболевания. При ВП-РС беспомощность пациента становится доминирующим фактором, который определяет уровень и стоимость необходимого ухода [4]. Результаты трех исследований [1-3] указывают на то, что интерферон (3 задерживает усугубление инвалидности, но на основании их данных трудно достоверно судить об этом эффекте. Дело в том, что больные в этих работах были в ранней стадии заболевания с очень слабой степенью инвалидности или вообще без нее, что отражалось в низких баллах по Расширенной шкале статуса инвалидности (Extended Disability Status Scale - EDSS). При этом было маловероятно, что у этих больных инвалидность начнет нарастать в ближайшие 2-3 года. У пациентов с самыми низкими показателями EDSS (0-3,0), скорее, отражала легкие функциональные нарушения, а не инвалидность [5, 6]. В единственной работе, в которой срок до развития стойких изменений в EDSS использовался как главный показатель исхода, больные в начале исследования имели только самые низкие баллы EDSS, и длительность этой работы была минимальной.
Инвалидность при PC обусловлена двумя различными, хотя во многих случаях действующими одновременно механизмами: когда рецидив не проходит полностью (неполная ремиссия), или когда болезнь исподволь неуклонно прогрессирует. Эти механизмы, возможно, имеют в своей основе различные патоморфологические изменения [7]. При чередовании рецидивов и ремиссий неполное восстановление после рецидива - единственная причина нарастающей беспомощности пациента, в то время как у больных с вторичным прогрессирующим PC инвалидизация обусловлена как рецидивами, так и неуклонным, постепенным прогрессированием.
В 1994 году мы начали контролированное по плацебо, многоцентровое, европейское исследование для изучения эффекта интерферона бета-1b на прогрессирование заболевания у больных с ВП-РС [8]. Главные клинические результаты, полученные при промежуточном анализе, представлены в настоящей статье.
Методы Организация исследования
Настоящая работа - это европейское, многоцентровое, двойное-слепое, контролированное по плацебо исследование двух групп больных с ВП-РС, получающих лечение параллельно (одновременно). Предполагалось, что данное исследование будет состоять из 36-месячного периода терапии с последующим наблюдением без лечения в течение 3 месяцев. Посещения больных планировались в 1, 3, 5 и 15 дни 1-3 месяцев, а затем каждые 3 месяца до месяца 36 (то есть, до конца лечения), и еще раз - на 39 месяце (то есть, в конце периода наблюдения без лечения). Больные посещали врачей и вне этого графика - при возникновении рецидивов и других, не связанных с PC заболеваний, при этом диагнозы и проводимое лечение документировались. За пациентами наблюдали путем регулярных обследований до конца настоящей работы, за исключением тех больных, которые решали больше не участвовать в ней, или если связь с ними терялась по другим причинам.
Это исследование координировалось управляющим комитетом исследователей и представителей спонсоров. На протяжении всего времени проведения работы от них скрывались получаемые результаты. Обработка данных и весь статистический анализ производился во внешнем учреждении. Независимый консультативный комитет изучил результаты промежуточного анализа безопасности, который провели после того, как все пациенты уже участвовали в данном исследовании, по крайней мере, в течение 24 месяца.
Пациенты и лечение
Амбулаторные больные, подходящие для рандомизации, имели клинически или лабораторно подтвержденный диагноз PC [9]. Под вторичным прогрессированием подразумевали период ухудшения, независимого от рецидивов, который сохранялся, по крайней мере, в течение 6 месяцев, и следовал за периодом чередования рецидивов и ремиссий. Допускалось возникновение на этом фоне дополнительных рецидивов [10]. Возраст больных составлял 18-55 лет. Исходный балл EDSS колебался от 3,0 до 6,5 включительно. При этом у них за предшествующие 2 года были зарегистрированы либо ≥ 2 рецидивов, либо повышение балла EDSS на ≥ 1,0. Лечение иммунодепрессантами или иммуномодуляторами и другая мнимая терапия по поводу PC не позволялись в течение определенного времени до вступления в исследование. Полностью критерии включения больных в настоящую работу были опубликованы ранее [8]. Пациенты давали письменное согласие после соответствующего разъяснения.
По центральной схеме рандомизации назначали плацебо или интерферон бета-1b группам больных по 6 человек в соотношении 1/1. Согласно протоколу исследования, доступ к шифру был строго ограничен. Подкожно вводили через день 0,5 мл. интерферона бета-1b (4 млн. ME) или плацебо в течение первых 2 недель, с последующим повышением разовой дозы до 1,0 мл. (8 млн. ME интерферона бета-1b или плацебо). Интерферон бета-1b было невозможно отличить от плацебо. Лечение должно было прекращаться при неприемлемых побочных эффектах или при значительных отклонениях лабораторных показателей, при беременности, использовании запрещенных врачом медикаментов, или если шифр предавался огласке.
При появлении симптомов, сходных с таковыми при гриппе, а также при повышенной чувствительности больного к лихорадке назначались нестероидные противовоспалительные препараты или парацетамол. Системные стероиды применялись по стандартной схеме (1г. метилпреднизолона внутривенно в течение 3 дней с последующим оральным приемом преднизона, либо преднизолона с постепенным понижением дозы или без такого понижения), причем лечение этими препаратами проводилось только при рецидивах. За каждый год участия в исследовании пациент получал не более 3 курсов терапии стероидами.
Эффективность оценки и сокрытие информации
Подсчет баллов функциональных систем и EDSS проводился так, как было описано Kurtzke [5]. Эти баллы отражали работу отдельных неврологических систем: зрительной, пирамидальной, мозжечковой, стволовой, чувствительной, систем управления кишечником и мочевым пузырем, системы коры головного мозга (психической) и других. EDSS предусматривает оценку по 20 оценкам-баллам - от 0 (норма) до 10 (смерть от PC), при этом баллы считаются так: 0, 1 и далее баллы возрастают на 0,5 (1,5, 2,0 и т. д.) вплоть до 10; они основаны на сочетании оценки функциональных систем в баллах, а также на степени независимости больного при передвижении и в быту. Расплывчатость определений в первоначальных публикациях об этих системах привела к тому, что разные лица, проводившие оценку, давали разные результаты [II]. Поэтому врачи, вычислявшие EDSS в настоящем исследовании, прошли обучение в главном методическом центре по EDSS. Это обеспечило стандартные подходы в оценке отдельных функциональных систем, дальности передвижения и баллов EDSS [12].
Для более надежного обеспечения одинаковых подходов к оценке EDSS методический центр по EDSS проводил обучение специалистов до начала исследования и ежегодно во время него; им предоставляли видеопленки, учебники и пособия. Те специалисты, которые впервые приступали к оценке уже во время осуществления настоящей работы, обязательно сначала проходили подготовку в указанном методическом центре. Когда было возможно, один и тот же специалист, оценивающий EDSS, проводил все заранее определенные неврологические тесты у данного больного в течение всего срока настоящего исследования.
Чтобы избежать того, чтобы информация о характере лечения раскрывалась бы из-за весьма характерных побочных эффектов интерферона бета-1b [1, 2], назначаемые лечащие врачи отвечали только за общий медицинский уход, оценку безопасности лечения и за терапию рецидивов. В то же время, врачи, оценивающие EDSS осуществляли стандартизованные неврологические тесты; они не получали никакой потенциально раскрывающей информации от лечащих врачей; им позволяли разговаривать с больным только в той мере, насколько это было необходимо для проведения неврологических тестов. Во время оценки EDSS все возможные места инъекций были закрыты. Врачи, определявшие балл EDSS, отдельно хранили документацию по неврологическому обследованию, по баллам функциональных систем и по EDSS.
Для выяснения, насколько успешным было сокрытие информации, в конце исследования лечащих врачей, а также специалистов, оценивавших EDSS, и больных просили ответить на специальный вопросник.
Инвалидность
Главным критерием оценки служило время от начала исследования до первого запланированного ежеквартального посещения, при котором фиксировалось повышение EDSS, по крайней мере, на 1,0 (или на 0,5 при исходном EDSS 6,0-6,5), при условии, что такое повышение подтверждалось и при следующем запланированном посещении 3 месяца спустя (по крайней мере, через 70 дней). Посещение на 33 месяце было последним, после которого можно было получить подтверждение (на 36 месяце). Баллы EDSS, записанные во время рецидива, подтвержденного врачом-исследователем, рассматривались как ценные лишь в тех случаях, когда они были собраны после 90-го дня текущего рецидива.
Другим, связанным с EDSS показателем был срок, который проходил до прикованности больного к креслу-каталке (а именно, до достижения балла EDSS ≥ 7,0). Для этого критерия не требовалось подтверждения, поскольку ожидалось, что число больных при исходном EDSS £6,0, у которых EDSS достигнет ≥ 7,0, окажется гораздо меньше, и что это состояние будет происходить гораздо позднее, чем наступление ухудшения в EDSS, являвшегося главным критерием. Дополнительными показателями являлись: доля больных с подтвержденным прогрессированием, доля больных, которые становились прикованными к креслу-каталке, и балл EDSS при завершающем обследовании.
Показатели, связанные с рецидивами
Под рецидивом понимали острое или подострое возникновение, либо повторное возникновение неврологического нарушения, непосредственно перед которым в течение 30 дней неврологическое состояние не изменялось, улучшалось или медленно ухудшалось. Диагноз "рецидив" ставился, только если ухудшение держалось не менее 24 часов, при этом у больного должны были отсутствовать лихорадка и прочие признаки инфекции. Такой диагноз был правомочен только в то время, когда больному не проводили отмены стероидного препарата. Больных просили обращаться в центр по проведению исследования при возникновении любого симптома, подозрительного на рецидив. Лечащий врач проводил оценку рецидива, в том числе, записывал дату его начала, симптомы и степень тяжести (слабо выраженный, умеренный и тяжелый), а также исследовал состояние функциональных систем, вычислял баллы EDSS для рецидива. Только те рецидивы, которые были подтверждены лечащими врачами, считались пригодными для анализа эффективности терапии.
Изучались следующие показатели, связанные с рецидивом: ежегодная частота рецидивов (их число, разделенное на число дней в исследовании, умножалось на 365), срок до первого рецидива и доля больных с умеренным или тяжелым рецидивом.
Изучение других показателей
Оценивались связанные с PC применение стероидов и госпитализации. Ежегодно проводилась МРТ. У 125 больных (v 61 из группы, получавшей плацебо, и у 64, которым вводился интерферон бета-1b) МРТ выполнялась ежемесячно в период с 0 по 6 месяцы и с 18 по 24 месяцев, при этом обязательно использовались T1-взвешенные сканы с контрастированием гадолинием. Магнитно-резонансные томограммы анализировались в едином учреждении, причем каждый год оценивался объем поражения и появление новых активных патологических очагов.
При регулярных обследованиях у больных проводили анализ на нейтрализующие антитела к интерферону бета-1b с помощью теста с протеином МхА [13]; анализ считался положительным при двух последовательных титрах 1:20 или более.
О степени безопасности приема препарата судили по неблагоприятным реакциям, по функции жизненно важных органов, а также по данным физикального обследования и необходимости в назначении других препаратов. Стандартные лабораторные анализы проводились в центральной лаборатории при каждом очередном посещении врача. Электрокардиографию выполняли в начале и в конце исследования. При каждом ежеквартальном обследовании для оценки изменений настроения и риска суицида применялась шкала рейтинга депрессии по Montgomery и Asberg (Montgomery Asberg Depression Rating Scale - MADRS) [14], которая основывается на наблюдениях врача.
Статистический анализ
Общее количество больных, необходимое для исследования, было определено, исходя из допущения, что доля пациентов с подтвержденным прогрессированием в группе, получавшей плацебо, через 3 года составит 50%. Ожидалось, что терапевтическая разница 12,5% будет выявлена с помощью двустороннего логарифмического-рангового теста (log-rank test) при а=0,029 и мощности 80% при использовании метода Pocock для поправки на запланированный промежуточный анализ. Требовалось 355 больных на каждую группу, с учетом поправки на ожидаемые 20% потерь больных. Поправка а для промежуточного анализа эффективности позднее основывалась на адаптации по DeMets к "затратам a" [a spending] (а=0,048 для конечного анализа и а=0,0133 для промежуточного анализа, принимая за информационную фракцию 83% данных EDSS). Весь статистический анализ основывался на популяции, которую предполагалось пролечить, включая все данные о всех рандомизированных пациентах без каких-либо ограничений.
Исходные характеристики анализировались с помощью рангово-суммарного теста (rank-sum test) по Wilcoxon для сравнения порядковых (ordinal) и непрерывных показателей, и с помощью теста точности по Fisher для сравнения дихотомичных или непорядковых (non-ordinal) категорийных переменных.
Показатели эффективности анализировались посредством непараметрических методов, учитывающих нелинейность шкалы EDSS [6]. Основной метод оценки срока, прошедшего до подтвержденного прогрессирования, был анализ ковариации (covariапсе) [15] с поправкой на центр (т.е., на клинику, где проводилось исследование) и на исходный балл EDSS. Применялась также стратификационная поправка на центр. Логарифмические-ранговые баллы для оценки информации по наблюдению за больными после подтвержденного прогрессирования сравнивались между группами с использованием расширенного таста по Mantel-Haenszel со стратификационной поправкой на центр.
Производилась оценка выживаемости больных, при этом их группы, получавшие разные препараты, сравнивались между собой с помощью логарифмического-рангового теста Mantel-Cox, стратифицированного для исходных категорий EDSS (£3,5, 4,0-5,5 и ≥ 6). Соотношение различия оценивалось путем использования "кусочной" (piecewise) модели логистической регрессии, включающей факторы, кроме лечения: исходный балл EDSS, исследовательский центр и время [16]. В расширенные модели включались такие факторы, как продолжительность PC, возраст, пол и площадь поверхности тела, при этом проверялось их взаимодействие с лечением. Было также изучено прогрессирование, подтвержденное спустя 3 и 6 месяцев, независимо от сопутствующих рецидивов. Другие показатели эффективности анализировались по таким тестам, как тест Mantel-Haenszel, расширенный тест Mantel-Haenszel или логарифмический-ранговый тест Mantel-Cox с поправкой на исходный балл EDSS, а также на рецидив до начала исследования, исходную картину МРТ или на то, какой исследовательский центр наблюдал данного больного (таблица 1).
Продольный (longitudinal) анализ с обобщающими оценочными уравнениями применялся для того, чтобы ответить на вопрос, связано ли появление нейтрализующих антител с ослаблением эффекта лечения [17]. Как для построения таблиц, так и для проведения анализа использовалась программа SAS (версия 6,12).
Таблица 1. Основные статистические методы.
| Показатель эффективности | Статистические методы | Стратификация/ поправка на коварианты | Подтверждающее моделирование |
| Срок до подтвержденного прогрессирования | Непараметрический анализ ковариантов (первичный) Логарифмический-ранговый тест Mantel-Cox (вторичный) |
Центр/Исходная EDSS Исходная EDSS * | «Кусочная» (piecewise) логистическая модель |
| Срок до прикованности к креслу-каталке | Логарифмический-ранговый тест Mantel-Cox | Исходная EDSS * | |
| Доля больных, которые стали прикованными к креслу-каталке | Тест Mantel-Haenszel | Исходная EDSS * | «Кусочная» (piecewise) логистическая модель |
| Ежегодная частота рецидивов | Непараметрический анализ ковариантов | Центр/Рецидив в предыдущие годы | |
| Процентное изменения за год объема поражения на Т2 МРТ | Непараметрический анализ ковариантов | Центр/Исходный объем поражения | |
| Число новых активных поражений в месяцы 1-6 и 19-24 | Непараметрический анализ ковариантов | Центр/Исходное число поражений | |
| Доля больных с подтвержденным прогрессированием | Тест Mantel-Haenszel | Исходная EDSS * | Логистическая модель |
| Изменение EDSS относительно исходного уровня | Расширенный тест Mantel-Haenszel | Исходная EDSS * | |
| EDSS в конце исследования | Расширенный тест Mantel-Haenszel | Исходная EDSS * | |
| Срок до первого рецидива | Логарифмический-ранговый тест Mantel-Cox | Центр | |
| Доля больных с умеренным или тяжелым рецидивом | Тест Mantel-Haenszel | Центр | |
| Доля больных, применяющих стероиды | Тест Mantel-Haenszel | Центр | |
| Доля госпитализированных больных | Тест Mantel-Haenszel | Центр | |
| Число связанных с PC госпитализаций на 1 больного | Расширенный тест Mantel- Haenszel | Центр |
Как показано на схеме 1, 718 из 768 больных, выявленных в 32 европейских клинических центрах, рандомизированно распределялись на получение интерферона бета-1b (n[число больных]=360) или на прием плацебо (п=358). Среднее время наблюдения при промежуточном анализе равнялось 892 дням исследования в группе плацебо и 901 дню в группе интерферона бета-1b. Это составляло 85% информации по EDSS, которую ожидалось получить за 3 года проведения работы. Группы больных были сходны между собой по всем исходным показателям (таблица 2). Из них 57 пациентов (31 получавших плацебо [8,7%] и 26 принимавших интерферон бета-1b [7,2%]) вышли из исследования (таблица 3). Причины, по которым это произошло, существенно между группами не различались. В целом 130 больных (66 получавших плацебо и 64 принимавших интерферон бета-1b) прекратили лечение, но за ними продолжали наблюдение согласно протоколу (таблица 3). Суммарно 531 больной (группа плацебо 261 [72,9%], группа интерферона бета-1b 270 [75,0%] либо завершил 3 года терапии, либо все еще проходил лечение на момент промежуточного анализа (схема 1).
Cхема 1. Схема исследования.
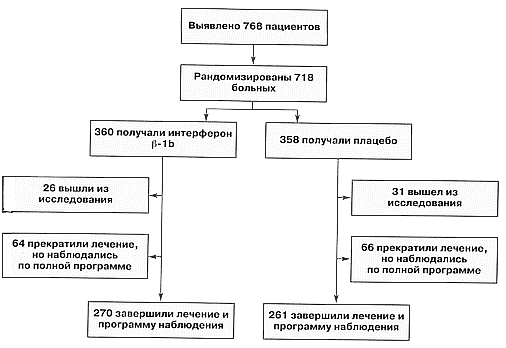
Больше отклонений от протокола зафиксировано в группе плацебо (73 пациентов [23,5%], чем в группе интерферона бета-1b (58 больных [17,2%]. Причины для отклонений от протокола были одинаково распределены между группами. Исключение составило существенно более частое использование запрещенных медикаментов в группе плацебо (33 по сравнению с 15 пациентами в группе интерферона бета-1b, р=0,0071), в том числе: избыточные дозы стероидов, лечение иммунодепрессантами или явное для пациента (с открытой этикеткой) применение интерферона бета. Только 11 отклонений от протокола были связаны с определением EDSS.
Группы существенно различались по следующим причинам прекращения лечения: неблагоприятные эффекты на фоне терапии (плацебо 15 [4,2%], интерферон бета-1b 45 [12,5%]); неохотное сотрудничество больного с врачами или его отказ от лечения (плацебо 19 [5,3%], интерферон бета-1b 8 [2,2%]); неэффективность испытуемого медикамента, по мнению врача или пациента (плацебо 44 [12,3%], интерферон бета-1b 23 [6,4%]) - таблица 3.
Таблица 2. Популяция больных (исходные характеристики).
| Плацебо (n=358)* | Интерферон бета-1b (n=360)* | |
| Средний возраст (СО, годы) | 40,9 (7,2) | 41,1 (7,2) |
| Женщины | 64,2% | 58,1% |
| Средняя продолжительность заболевания (СО, годы) | 13,4 (7,5) | 12,8 (6,6) |
| Средний срок после постановки диагноза PC с повышенным риском рецидивов (СО, годы) | 8,2 (6,1) | 8,1 (5,6) |
| Средний срок после появления признаков прогрессирующего ухудшения (СО, годы) | 3,8 (3,4) | 3,8 (2,7) |
| Средний срок после постановки диагноза ВП-РС (СО, годы) | 2,1 (2,2) | 2,2 (2,4) |
| Средняя исходная EDSS EDSS по категориям ≤ 3,5 4,0-5,5 ≥ 6,0 | 5,2(1,1) 47(13,1%) 142 (39,7%) 169 (47,2%) | 5,1(1,1) 67(18,6) 140 (38,9) 153 (42,5%) |
| Пациенты без рецидива в течение 2 лет перед исследованием** | 101 (28,2%) | 115(31,9%) |
** Данные отсутствуют у 7 пациентов (4 в группе плацебо, 3 в группе, пролеченной интерфероном бета-1b), которые были включены в подгруппу больных без рецидива. СО - стандартное отклонение.
Таблица 3. Причины выхода из исследования и прекращения лечения.
| Плацебо (n=358) | Интерферон бета-1b (n=360) | |
| Причины выхода из исследования | ||
| Неблагоприятный эффект, отклонение в лабораторных показателях | 4(1,1) | 5(1,4) |
| Прогрессирование заболевания | 10 (2,8) | 5(1,4) |
| Смерть* | 1 (0,3) | 3 (0,8) |
| Потеряна связь с больным | 4(1,1) | 8 (2,2) |
| Прочие | 12 (3,4) | 5(1,4) |
| Всего | 31 (8,7) | 26 (7,2) |
| Причины прекращения лечения (в том числе и с выходом из исследования) | ||
| Неблагоприятные эффекты** | 15(4.2) | 45(12,5) |
| Заболевание, независимое от медикаментов, получаемых в рамках исследования | 3 (0,8) | 0 |
| Больной не пожелал сотрудничать/отказался от лечения* | 19 (5,3) | 8(2,2) |
| Отклонения от протокола | 0 | 3 (0,8) |
| Неэффективность медикаментов, получаемых в рамках исследованиях*** | 44 (12,3) | 23 (6,4) |
| Смерть | 0 | 2 (0,6) |
| Беременность | 0 | 1 (0,3) |
| Прочие | 16(4,5) | 8(2,2) |
| Всего | 97(27,1) | 90 (25,0) |
** р<0,05 no двустороннему тесту точности Fisher.
*** Включает двух больных (1 в группе плацебо, 1 в группе, пролеченной интерфероном бета-1b), которые умерли после преждевременного прекращения лечения.
Показатели клинической эффективности
Что касается главного показателя эффективности -срока до подтвержденного неврологического ухудшения, непараметрический анализ ковариантов показал значительное различие между двумя группами (р=0,0008) в пользу интерферона бета-1b (схема 2, таблица 4).Из 358 пациентов, принимавших плацебо, у 178 (49,8%) было диагностировано прогрессирование (число дней до него [40% квантиля {quantile}] - 549, доверительный интервал [ДИ] 463-642). Из 360 пациентов, получавших интерферон бета-1b, прогрессирование было выявлено у 140 (38,9%) (число дней до него [40% квантиля] - 893, нижний предел ДИ 726, верхний предел невозможно было установить в днях в рамках данного периода исследования). Обычно дается 50% квантиля, но, поскольку она не достигалась обеими группами, мы взяли следующую квантилю, которая отражала бы самый длительный период наблюдения (40% квантиля).
Была получена достоверность различия (р=0,0016) и при поддерживающем (supportive) анализе, требующем двух подтверждений (включая оценки EDSS на 3 и 6 месяцах и баллы во время рецидива). Разница в главном показателе эффективности была подтверждена при дополнительном анализе у всех больных, которых собирались лечить, в том числе у тех, с кем была потеряна связь. Если при этом допускали, что у потерянных для наблюдения больных впоследствии развивалось прогрессирование, то показатель различия между группами составлял р=0,0012. Если же допускали, что к концу исследования у них прогрессирование не наступало, то этот показатель равнялся р=0,0014. При анализе по «кусочной» (piecewise) модели логистической регрессии были также подтверждены данные первичного анализа. При этом соотношение различия составило 0,65 (95% ДИ 0,52-0,83), и не было выявлено какого-либо взаимодействия между терапией и показателями, включенными в расширенную модель. То есть, эффект лечения с течением времени был весьма гомогенным.
Оценка вероятности отсутствия наступления рецидива (оценка показателей выживаемости без рецидивов) производилась для каждого квартала (3 месяца) на протяжении 33 месяцев (таблица 4). Эффект лечения стал заметен спустя 9 месяцев его проведения (р=0,059), он оставался значительным по истечении 12 месяцев от начала терапии (р=0,003), причем различие между группами сохранялось на достоверном уровне в каждом квартале в оставшийся срок исследования (33 месяцев, р=0,0015). Тот факт, что лечение задерживало наступление прогрессирования, можно выразить путем сравнения сроков, за которые достигается данная вероятность. Отсрочивание составляло от 9 до 12 месяцев для 65% и 60% вероятности оставаться свободным от прогрессирования (рисунок 1, таблица 4). Оценка квантилей срока, проходившего до наступления подтвержденного прогрессирования, с использованием метода Kaplan-Meier показала нарастание отсрочивания прогрессирования с течением времени с разницей в 344 дней в 40-й квантиле.
Рис. 1. Срок до подтвержденного прогрессирования, определенный по оценочному методу life-table.
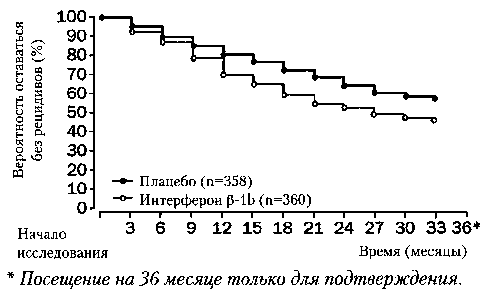
Таблица 4. Срок до подтвержденного прогрессирования: оценка по методу life-table вероятности оставаться без рецидивов.
| Период времени | Плацебо | Интерферон бета-1b | Р* | ||
| Доля больных без рецидива | Число с риском | Доля больных без рецидива | Числос риском | ||
| Месяцы 1-3 | 0,93 | 358 | 0,95 | 360 | 0,1962 |
| Месяцы 4-6 | 0,87 | 332 | 0,89 | 342 | 0,3830 |
| Месяцы 7-9 | 0,79 | 305 | 0,85 | 318 | 0,0591 |
| Месяцы 10-12 | 0,71 | 275 | 0,81 | 301 | 0,0031 |
| Месяцы 13-15 | 0,65 | 244 | 0,77 | 284 | 0,0009 |
| Месяцы 16-18 | 0,60 | 226 | 0,73 | 271 | 0,0003 |
| Месяцы 19-21 | 0,55 | 206 | 0,69 | 256 | 0,0002 |
| Месяцы 22-24 | 0,53 | 188 | 0,65 | 238 | 0,0012 |
| Месяцы 25-27 | 0,50 | 148 | 0,61 | 183 | 0,0015 |
| Месяцы 28-30 | 0,48 | 95 | 0,60 | 133 | 0,0013 |
| Месяцы 31-33 | 0,47 | 65 | 0,58 | 94 | 0,0015 |
За все время исследования подтвержденное прогрессирование наблюдалось у 49,7% пациентов в группе плацебо и только у 38,9% в группе лечения (р=0,0048), что означает относительное уменьшение на 21,7% доли больных с прогрессированием (таблица 5). Моделирование с помощью логистической регрессии показало, что у пациентов, получавших плацебо, вероятность прогрессирования была в 1,6 раз выше (соотношение различия 0,63, 95% ДИ [0,46-0,85]). Срок, проходящий до того, как пациент становился прикованным к креслу-каталке (то, есть, до того, как балл EDSS достигал 7,0) также был существенно удлинен (соотношение различия 0,66, 0,47-0,93; таблица 5); сравнение по методу life-table показало отсрочивание наступления такой беспомощности до 9 месяцев в группе интерферона бета-1b в сравнении с группой плацебо; различие было существенным на 12 месяце. Балл EDSS ≥ 7 был достигнут 88 пациентами (24,6%) в группе плацебо, и лишь 60 больными (16,7%) в группе интерферона бета-1b (р=0,0277). То есть, за время исследования за счет лечения удалось сократить на 32,1% долю больных, прикованных к креслу-каталке. Сравнение EDSS в конце исследования (при последнем посещении данного больного) между обеими группами не выявило сущесвтенного различия (р=0,075), но разности между конечными и исходными баллами достоверно отличались между группами в пользу интерферона бета-1b (р=0,0227).
Таблица 5. Результаты по вторичным и третичным показателем эффективности.
| Показатель эффективности | Плацебо (n=358) | Интерферон бета-1b (n=ЗбО) | Р |
| Доля больных с подтвержденным прогрес-сированием EDSS* | 49,7% | 38,9% | 0,0048 |
|
Потеря двигательных функций Срок до прикованности в креслу-каталке Оценка вероятности оставаться независимым от кресла-каталки Год 1 Год 2 Год З | 0,90 0,81 0,66 | 0,96 0,89 0,77 |
0,0133 0,0129 0,0094 0,0133 |
|
Средняя EDSS В конце исследования Изменение к концу исследования ** |
5,84 0,60 |
5,57 0,47 |
0,0750 0,0299 |
|
Средняя частота рецидивов по годам Всего Год 1 Год 2 Год З |
0,64 0,82 0,47 0,35 |
0,44 0,57 0,35 0,24 |
0,0002 0,0095 0,0201 0,1624 |
| Медиана срока до первого рецидива(дни) | 403 | 644 | 0,0030 |
| Доля больных с умеренным или тяжелым рецидивом | 53,1% | 43,6% | 0,0083 |
** Разность показателей в конце и в начале исследования.
Замедление прогрессирование, обусловленное лечением, не зависело от исходного балла EDSS или от рецидивов, присоединившихся до исследования или во время него, с относительным уменьшением частоты стойкого прогрессирования на 20% в группе, получавшей интерферон бета-1b (таблица 6).
Таблица 6.Доля больных с подтвержденным прогрессированием в зависимости от категории исходной EDSS и от того, возникали ли рецидивы до и после начала исследования.
| Плацебо (n=358) | Интерферон бета-1b (n=360) | ∆* | |||
| n | С подтвержденным прогрессированием | n | С подтвержденным прогрессированием | ||
|
Исходная EDSS ≤ 3,5 4,0-5,5 ≥ 6,0 |
47 142 169 |
20(42,6%) 73(51,4%) 85(50,3%) |
67 140 153 |
23(34,3%) 57(40,7%) 60(39,2%) |
-19,5% -20,8% -22,1% |
|
Рецидивы во время исследования Их не было Они были |
224 134 |
117(52,2%) 61(45,5%) |
194 166 |
81(41,8%) 59(35,5%) |
-19,9% -22,0% |
|
Рецидивы в течение 2 лет перед исследованием Их не было Они были |
257 101* |
128(49,8%) 50(49,5) |
245 115* |
94(38,4%) 46(40,0%) |
-22,9% -19,2% |
** 7 больных (4 на плацебо, 3 на интерфероне бета-1b) с отсутствующей информацией считались подгруппой больных без рецидивов. Средняя годовая частота рецидивов уменьшилась в группе лечения в целом примерно на 30% (0,64 в группе плацебо против 0,44 в группе интерферона бета-1b, р=0,002). Частота ежегодно падала в обеих группах (таблица 5), при этом эффект лечения с течением времени сохранялся, хотя на 3 году различие уже не было существенным. Срок до первого рецидива у больных, получавших интерферон бета-1b, был продлен (медиана 644 дней) в сравнении с таковым показателем у пациентов, принимавших плацебо (медиана 403 дня; р=0,0030). В группе интерферона бета-1b доля больных с умеренно выраженными и тяжелыми рецидивами была ниже (190 пациентов [53,1%] на плацебо и 157 больных [43, 6%] на интерфероне бета-1b, р=0,0083, таблица 5).
Активное лечение также позволило существенно уменьшить долю госпитализированных больных (189 пациентов [52,8%] на плацебо и 167 больных [46, 4%] на интерфероне p-lb, р=0,0435) и число связанных с PC госпитализаций на 1 больного (р=0,0003). Доля пациентов, применявших стероиды по поводу PC. была значительно ниже в группе, получавшей интерферон p-lb (53,6% против 67,9%, р<0,0001).
Заполненный вопросник, предназначенный для оценки эффективности сокрытия информации, был получен от 84-86% лечащих врачей, специалистов, оценивавших EDSS, и пациентов. Как и ожидалось, лечащие врачи часто правильно догадывались, получали ли больные плацебо (148 [48,4%] из 306) или интерферон бета-1b (176 [56,2%] из 313). В то же время, они не знали или неправильно угадали характер лечения, соответственно, у 225 (36,3%) из 619 и у 70 (11,3%) из 619 пациентов. Аналогично, 165 (54,3%) из 304 больных правильно догадались, что они получали плацебо, а 202 пациент (65,6%) из 308 - что им вводился интерферон бета-1b. Однако 71 (23, 4%) пациент их 304, получавших плацебо, думал, что он лечится интерфероном бета-1b; 36 (11,7%) больных из 308 группы интерферона бета-1b полагали, что им вводится плацебо, а 138 (22,5%) из 612 затруднились с ответом. Что было наиболее важно, врачи, оценивавшие EDSS, правильно угадали характер лечения только у 54 (18,6%) из 291 больных на плацебо и у 65 (20,8%) из 312 пациентов на интерфероне бета-1b. Эти врачи затруднились с ответом на вопрос о характере терапии у 401 (66,5%) из 603 больных.
Данные МРТ
Лечение интерфероном p-lb привело к значительному уменьшению среднего объема поражений на Т2 МТР: в группе на плацебо объем увеличился приблизительно на 8%, а у больных на интерфероне p-lb он сократился на 5% (р<0,0001). В когорте с частым проведением МТР (n=125) у пациентов, получавших интерферон бета-1b, в сравнении с пациентами на плацебо отмечено уменьшение на 65% количества новых активных поражений в месяцы 1-6 (р<0,0001) и на 78% в месяцы 19-24 (р=0,0008).
Нейтрализующие антитела к интерферону бета-1b
Из 100 (27,8%) больных были выявлены нейтрализующие антитела, причем у 66 эти антитела появились в первые 6 месяцев лечения. У 47 пациентов с нейтрализующими антителами впоследствии выявлялся, по крайней мере, один отрицательный титр, и у 37 из них титры остались негативными после такой реверсии (с позитивного на негативный статус по нейтрализующим антителам). Продольный (longitudinal) анализ с обобщающими оценочными уравнениями [17] показал существенное уменьшение терапевтического эффекта в отношении частоты рецидивов у больных с положительными анализами на нейтрализующие антитела. Но при этом не было выявлено уменьшения терапевтического эффекта, судя по параметрам, напрямую связанным с главным критерием (изменения EDSS с течением времени).
Безопасность
Наблюдались следующие распространенные, имеющие клиническое значение побочные эффекты, достоверно связанные с интерфероном бета-1b: осложнения в местах инъекций и гриппоподобные симптомы, которые были особенно распространены в ранней фазе лечения. Некроз в области введения интерферона бета-1b наблюдался у 4,7% больных. Другими, достоверно связанными с интерфероном бета-1b побочными эффектами явились мышечная гипертония (37,8% против 27,4%, р=0,0032) и артериальная гипертензия (3,9% против 0,8%, р=0,0117). Но не было выявлено достоверных различий между группами по тем изменениям, обнаруженным при неврологическом и терапевтическом обследовании, которые были связанны с мышечной гипертонией и гипертензией (таблица 7).
Таблица 7. Неблагоприятные эффекты, достоверно связанные с лечением интерфероном бета-1b.
| Система организма/ неблагоприятные эффекты | Плацебо (n=358) | Интерферон бета-1b (n=360) |
| Организм в целом Гриппоподобный синдром Лихорадка Озноб Боль в животе Озноб и лихорадка Гемопоэтическая и лимфатическая система Лейкопения |
133 (37,2%) 47(13,1%) 26 (7,3%) 23 (6,4%) 1 (0,3%) 18 (5,0%) |
213(59,2%) 142(39,4%) 79(21,9%) 38(10,8%) 13 (3,6%) 36(10,0%) |
| Сердечно-сосудистая система Артериальная гипертензия |
3 (0,8%) | 14 (3,9%) |
| Место инъекции Реакция Воспаление Некроз |
37 (10,3%) 15 (4,2%) 0 | 157 (43,6%) 180 (50,0%) 17 (4,7%) |
| Кожа и ее придатки Сыпь |
38(10,6%) |
77(21,4%) |
| Мышечно-скелетная система Миалгия |
32 (8,9%) |
82 (22,8%) |
| Нервная система Мышечная гипертония |
98 (27,4%) |
136 (37,8%) |
В группе, получавшей лечение интерфероном бета-1b, наблюдалась большая доля пациентов с патологическими значениями концентрации ферментов печени и лейкоцитарной формулы, как и прогнозировалось на основании результатов других исследований. Как правило, уровни ферментов печени нормализовались самопроизвольно или под влиянием снижения дозы, либо временного прекращения лечения. Имеющие клиническое значение лабораторные изменения возникали редко; из них только лимфопения была явно связана с интерфероном бета-1b.
В нашем исследовании было 4 смерти, 3 из которых произошли в группе, получавшей интерферон бета-1b. 2 пациентов (один на плацебо, второй на интерфероне бета-1b) совершили самоубийство, у 1 больного случилась остановка сердца, и у одного - массивная тромбоэмболия легочной артерии (через 55 дней после преждевременного прекращения приема интерферона бета-1b). У пациентов на фоне лечения интерфероном бета-1b не наблюдалось повышения частоты новых случаев депрессии или ее усугубления - ни по жалобам больных, ни по данным ежеквартального проведения оценки по шкале MADRS. Самоубийства или попытки самоубийства имели место у 5 больных на фоне приема плацебо и у 3, получавших интерферон бета-1b.
Обсуждение
Это исследование фазы III демонстрирует терапевтическую эффективность интерферона бета-1b при ВП-РС. Известно, что ВП-РС развивается у многих больных, и именно во время нее наиболее часто наступает необратимая инвалидность [17, 18].
Изученная когорта являлась репрезентативной для этой группы больных. Она включала пациентов с прогрессированием, которое сопровождалось или не сопровождалось рецидивами, и которому предшествовала начальная фаза чередования рецидивов и ремиссий [10]. Пациенты были в ранней стадии прогрессирования, которая начиналась приблизительно через 10 лет после первоначальной постановки диагноза PC, и у них имела место активная фаза заболевания в течение 2 лет до их включения в настоящую работу.
Главным показателем эффективности терапии в настоящем исследовании служило стойкое прогресси-рование инвалидности по данным EDSS. Хотя эту шкалу сильно критикуют, она остается наиболее признанной системой оценки прогрессирования PC [19]. Однако EDSS недостаточно детально отражает ухудшение состояния на определенных этапах PC, особенно при балле EDSS между 6,0 и 7,0. Обычно эти этапы относительно длиннее, чем другие, в это время больной постепенно утрачивает способность ходить. Поэтому в настоящем исследовании нарастание балла EDSS, начиная с исходного 6,0, мы считали не по 1,0, а по 0,5. Был предложен именно такой подход, поскольку на этой стадии заболевания каждая половина балла отражает существенное ухудшение в течении EDSS. Еще одно ограничение шкалы EDSS заключается в большой вариабельности оценок, которые, согласно: ней, дают разные исследователи. С этим недостатком мы боролись путем повторных, стандартизованных аудио-визуальных курсов обучения врачей, что привело к существенному повышению единообразия в оценках [12].
Высоко достоверное отсрочивание прогрессирования PC - до 12 месяцев за время исследования (р=0,0008) отмечено в группе, получавшей интерферон бета-1b, что видно по графикам, составленным по методу life-table. Эти результаты подтверждаются также столь же ясной пользой по данным вторичных и третичных показателей. Это дало основание независимому консультативному комитету рекомендовать досрочное прекращение исследования. Результаты любой работы неизбежно зависят от поведения группы плацебо. Процент неудач лечения и сроки до прогрессирования PC в группе плацебо настоящего исследования находились в тех же пределах, что и результаты предыдущих работ, в которых изучались и больные с ВП-РС [21, 22].
Данные вопросника, посвященного проблеме сокрытия информации, показали, что вполне эффективными оказались следующие мероприятия: врачи, проводившие оценку по EDSS, были отстранены от лечения пациентов, от них скрывалась вся клиническая информация; больным рекомендовали принимать противовоспалительные препараты; места инъекций закрывались при каждой оценке EDSS.
Интересно то, что в данном исследовании терапевтический эффект у сильно инвалидизированных больных оказался столь же значительным, как и у пациентов со слабой или умеренной степенью инвалидности. Ранее высказывалось предположение, что более детальная оценка ухудшения состояния у больных с исходной EDSS≥ 6,0, как описано выше, по существу, позволит опровергнуть зависимость неудач лечения от исходной EDSS [21].
Как и ожидалось по результатам предыдущих исследований с интерфероцом бета-1b, частота рецидивов была значительно ниже в группе лечения [1-3], причем в обеих группах этот показатель с течением времени снижался, что и можно было прогнозировать для ВП-РС [18]. Влияние на прогрессирование инвалидности оставалось значимым во все периоды исследования. Аналогичные эффекты терапии наблюдались независимо от возникновения рецидивов во время проведения работы. Таким образом, еще раз подтверждалось, что, интерферон бета-1b замедляет усугубление инвалидности, а не только понижает частоту рецидивов.
Эти данные затрагивают важные вопросы о механизмах прогрессировапия инвалидности при PC и о механизме действия интерферона бета. В настоящем исследовании наблюдался эффект на оба аспекта ухудшения - а именно, на неполное выздоровление от рецидива и на медленное, малозаметное прогрессирование. Первое из названных явлений, вероятно, связано с демиелинизацией и потерей аксонов вследствие острого воспаления, а второе может быть обусловлено непрерывным повреждением либо вялым воспалением, либо другим процессом. Возможны два механизма действия препарата: влияние на прогрессирование инвалидности путем подавления вялотекущего воспаления или, что менее вероятно, путем дополнительного, до сих пор не доказанного, защитного действия на миелин и аксоны.
Стероиды чаще применялись в группе плацебо. Это, возможно, отражает тот факт, что у больных в этой группе наблюдалась более высокая активность заболевания, что подтверждается меньшим числом госпитализаций по поводу PC в группе активного лечения. Однако стероиды не маскировали эффекта интерферона бета-1b.
В целом, характер побочных эффектов интерферона бета-1b в настоящем исследовании согласуется с уже известными данными о них и указывает на то, что длительное лечение этим препаратом в дозе 8 млн. ME (IU) при ВП-РС безопасно и, как правило, хорошо переносится. Как и в работе IFNB-1a [2, З], в настоящем исследовании не наблюдалось повышения частоты депрессии на фоне лечения интерфероном бета-1b. Мышечная гипертония выявлена у большей доли пациентов, но это не нашло отражения при детальном неврологическом обследовании.
Результаты настоящей работы убедительно свидетельствуют о том, что лечение интерфероном бета-1b отсрочивает стойкое неврологическое ухудшение у больных с ВП-РС. Достоверность этого вывода подтверждают дополнительный анализ прогрессирования заболевания, а также неизменное снижение частоты рецидивов и улучшение картины при МТР. Таким образом, терапия интерфероном бета-1b - это первый вид лечения, который оказался эффективным при ВП-РС.
Литература 1. IFNB Multiple Sclerosis Study Group. Interferon beta-1b is effective in relapsing-remitting multiple sclerosis. Neurology 1993,43: 655-61.
2. Jacobs LD, CookfairDL; Rudick RA; et al. Intramuscular interferon beta-la for disease progression in relapsing multiple sclerosis. Ann Neurol 1996; 39:285-94.
3. Ebers GC, Oger J, Paty D. The multiple sclerosis PRISMS study: prevention of relapses and disability by interferon beta-la subcutaneously in multiple sclerosis (abstr). Ann Neurol 1997; 42: 986.
4. Carton H, Laos R, PacoletJ, Versieck K, Vlietinck R. Utilisation and cost of professional care and assistance according to disability of patients with multiple sclerosis in Flanders (Belgium), J Neurol Neursurg Psychiatry 1998; 64:444-50.
5. KurtzkeJF. Rating neurological impairment in multiple sclerosis: an expanded disability scale (EDSS). Neurology 1983; 33:1444-52.
6. Willougbby EW, PatyDW. Scales for rating impairment in multiple sclerosis: a critique. Neurology 1988; 38: 1793-98.
7. Lucchinetti CF, Brack W, Rodriguez M, Lassmann H. Distinct patterns of multiple sclerosis pathology indicates heterogeneity in pathogenesis. Brain Pathol 1996; 6: 259-74.
8. Polman CH, Dahike F, Thompson AJ, et al. Interferon beta-lb in secondary-progressive multiple sclerosis: outline of the clinical trial. Mult Scler 1995; 1: 51-54 (suppl).
9. Poser СМ., Paty DW, Scheinberg L, et al.New diagnostic criteria for multiple sclerosis: guidelines for research protocols. Ann Neurol 1983; 13:227-31.
10. Lublin FD, Reingold SC. Defining the clinical course of multiple sclerosis: results of an international survey. Neurology 1996; 48: 907-11.
11. Noseworthy JH, Vandervoort MK, Wong CJ, Ebers GC, Canadian Cooperative MS Study Croup. Interrater variability with the Expanded Disability Status Scale (EDSS) and Functional Systems (FS) in a multiple sclerosis clinical trial. Neurology 1990; 40: 971-75.
12. Lechner-ScottJ, HuberS, Kappos L. Expanded disability status scale (EDSS) training for MS-iiiulticcntcr-trials.J Neurol 1997; 244 (suppr3): 25.
13. Lleonart R, NafD, Browning H, Weissmann C. A novel, quantitative bioassay for type I intereron using a recombinant indicator cell line. Biotechnology 1990; 8: 1263-67.
14. Montgomery S, Asberg M. A new depression scale designed to be sensitive to change. Br J Psychiatry 1979;134: 382-89.
15. PetkauJ. Statistical and design considerations for multiple sclerosis clinical trials. In: Goodkin DE, Rudick RA, eds. Advances in MS clinical trial design, treatment, and future perspectives. Heidelberg: Springer, 1996: 63-104.
16. Koch GG, Edwards S. Clinical effiacy trials with categorical data. In: Peace KE (ed). Biopharmaceutical statistics for drug development. New York: Marcel Dekker, 1988: 403-57.
17. Perkau.J and White R. Neutralizing antibodies and the efficacy of interferon beta-lb in relapsing-remitting multiple sclerosis (abstr). Mult Scler 1997, 3: 402.
18. WeinshenkerBG, Ebers GC. The natural history of multiple sclerosis. Can J Neurol Sci 198-7, 14: 255-61.
19. Rudick R, Antel J, Confavreux C, et al. Recommendations from the National Multiple Sclerosis Society Clinical Outcomes Assessment Task Force. Ann Neurol 1997; 42: 379-82.
20. The Multiple Sclerosis Study Group. Efficacy and toxicity of cyclosporine in chronic progressive multiple sclerosis: a randomised, double-blinded, placebo-controlled clinical trial. Ann Neurol 1990; 27: 591-605.
21. WeinshenkerBG, Issa M, BaskervilleJ. Meta-analysis of the placebo-treated groups in clinical trials of progressive MS. Neurology 1996, 46: 1613-19.
22. Canadian Cooperative Multiple Sclerosis Study Group. The Canadian cooperative trial of cyclophosphamide and plasma exchange in progressive multiple sclerosis. Lancet 1991; 337: 441-46.
Комментарии
ПРАКТИКА ПЕДИАТРА
