Особенности реканализации глубоких вен нижних конечностей у больных с тромбозом при пролонгированном лечении сулодексидом
Статьи Д.м.н., доц. А.С. Петриков, д.м.н., доц. В.И. Белых, д.м.н., проф. Я.Н. Шойхет
ГБОУ ВПО «Алтайский государственный медицинский университет» Минздрава России (ректор — д.м.н., проф. И.П. Салдан)
Изучена эффективность и безопасность сулодексида (СД) — Вессел Дуэ Ф (ВДФ, «Альфа Вассерманн», Италия), процесс реканализации вен у больных с тромбозом глубоких вен нижних конечностей (ТГВНК) при его пролонгированном применении в течение года. В открытом сравнительном проспективном исследовании больным с ТГВНК в основной группе (n=149; 62 женщины и 87 мужчин в возрасте от 18 до 69 лет) назначался ВДФ, в группе сравнения (n=126; 65 женщин и 61 мужчина в возрасте от 18 до 64 лет) — варфарин. Критерием включения являлся ТГВНК, документально подтвержденный при дуплексном сканировании в В-режиме, критериями исключения — онкологические заболевания, скелетные травмы и переломы, длительная иммобилизация, оперативные вмешательства, острые инфекции, возраст пациентов моложе 17 и старше 69 лет. Проводилось комплексное лабораторное и генетическое обследование больных, включающее определение основных клинико-биохимических показателей крови и системы гемостаза, содержания гомоцистеина и С-реактивного белка в сыворотке крови, аллельного полиморфизма 10 генов, кодирующих компоненты плазменного и тромбоцитарного гемостаза по стандартным методикам. Дуплексное сканирование (ДС) вен нижних конечностей выполнялось на современных ультразвуковых сканерах по стандартным методикам при госпитализации, на 10—14-е сутки перед выпиской и каждые 2 мес в течение года от начала лечения. В основной группе перевод больных на ВДФ (по 600 ЛЕ в/м 1 раз в сутки 10—14 дней) осуществлялся через 1,5—2 мес от начала лечения ТГВНК с последующим переходом на пероральный пролонгированный прием препарата (по 250 ЛЕ 2 раза в сутки 6—12 мес). Показаниями для назначения ВДФ являлись невозможность приема антагонистов витамина К, нарушения в системе протеина С, снижение уровня антитромбина III, развитие тромбоцитопении (в том числе гепарининдуцированной), а также выраженное угнетение фибринолиза и отсутствие, по данным дуплексного сканирования, динамики реканализации. Установлено, что пролонгированный прием СД в течение 12 мес не вызывал развития нежелательных побочных эффектов и аллергических реакций. В основной группе не наблюдалось развития кровотечений в течение года в отличие от больных группы сравнения (варфарин), у которых частота развития клинически значимых кровотечений составила 6,3% (р Ключевые слова: тромбоз глубоких вен нижних конечностей, сулодексид, реканализация вен.
Введение
Венозные тромбоэмболические осложнения (ВТЭО) считаются одними из основных причин заболеваемости и смертности у населения. Известно, что частота их развития составляет 1—2 случая в год на 1000 населения в общей популяции [46]. В России ежегодно когорта пациентов с ВТЭО увеличивается на 90—100 тыс. человек [16]. Перенесенный тромбоз глубоких вен нижних конечностей (ТГВНК) — причина развития посттромбофлебитического синдрома (ПТФС) в течение первых 3 лет у 35—69% больных, в первые 5—10 лет у 49—100% больных [8, 20]. ПТФС может наблюдаться у больных с тромбозом глубоких вен (ТГВ) голени в 25% случаев, поражением вен голени и бедра — в 46%, проксимальным венозным тромбозом (ВТ) — в 98% [35, 47].
У половины больных с острыми ВТ выше колена в течение первых 2—3 лет развиваются тяжелые трофические нарушения с формированием длительно не заживающих венозных язв [21].
При лечении ТГВНК важнейшими задачами являются купирование тромбообразования, предотвращение развития тромбоэмболии легочной артерии (ТЭЛА), предупреждение рецидива ВТ и восстановление проходимости венозного русла [1, 3, 4, 6, 9]. Поэтому неслучайно ключевая роль при ТГВНК отводится антитромботической терапии [13, 16, 20, 22]. Однако, несмотря на серьезные до казательные исследования в отношении режимов антикоагулянтной терапии при различных клинических ситуациях ВТЭО, сведения о подборе антикоагулянтной терапии, ее режимах с позиций эффективности и безопасности, особенно для пролонгированного применения у больных с ТГВНК, продолжают быть актуальной проблемой [5, 10, 11, 16].
В настоящее время нет однозначных рекомендаций в отношении продолжительного и пролонгированного назначения антикоагулянтов для лечения и вторичной профилактики ВТЭО с учетом факторов риска [9, 13, 22], поскольку результаты проведенных исследований часто противоречат друг другу [42]. Все это является основанием для активного поиска и изучения антикоагулянтов, которые могут применяться для пролонгированного лечения и профилактики ВТЭО, особенно в ситуациях, когда зачастую невозможно назначить больному антагонисты витамина К (АВК).
В последние годы широкое распространение получили препараты, способные корригировать процессы микроциркуляции на тканевом уровне и воздействовать на процессы системы гемостаза, — гепариноиды [7, 12, 28, 37]. Среди них особый интерес представляет сулодексид (СД) — Вессел Дуэ Ф (ВДФ, «Альфа Вассерманн», Италия). Имеется достаточное количество сообщений о его применении для лечения и профилактики кардиоваскулярных заболеваний и, в частности, ВТЭО [12, 28, 37, 38]. Благодаря наличию различных лекарственных форм и своим физико-химическим свойствам СД применяется и как антитромботический препарат [23, 25, 48]. Его антикоагулянтное действие проявляется за счет сродства к кофактору II гепарина, который инактивирует тромбин и связано с подавлением активированного X фактора, усилением синтеза и секреции простациклина (ПГI2) и снижением уровня фибриногена в плазме крови [19, 28, 30, 31, 33, 41, 48].
Профибринолитическое действие препарата обусловлено увеличением в крови содержания тканевого активатора плазминогена и снижением содержания его ингибитора [19, 27, 38].
Ангиопротективное действие СД (ВДФ) связано с восстановлением структурной и функциональной целостности клеток эндотелия сосудов, нормальной плотности отрицательного электрического заряда пор и нормальной толщины базальной мембраны сосудов. Кроме того, препарат восстанавливает структурную и функциональную целостность эндотелия сосудов (артерий, вен, капилляров) [19, 38, 41]. ВДФ оказывает разностороннее влияние на систему гемостаза, которое как качественно, так и количественно отличаются от действия нефракционированного и низкомолекулярного гепаринов (НФГ и НМГ). Его преимуществом по сравнению с НФГ и НМГ являются доказанная эффективность при пероральном приеме внутрь и простой контроль за лечением. Важно, что при пероральном применении препарата контроль за показателями системы гемостаза применяется редко [9, 48]. Присутствие СД в составе гепариноподобной фракции и дерматана сульфата обеспечивает дозозависимый синергический эффект его антитромботического потенциала при меньшем риске кровотечения в сравнении с гепаринами [29, 30], хотя антикоагулянтные его свойства несколько ниже [30, 31]. СД не обладает сродством к тромбоцитарному фактору 4 и не вызывает тромбоцитопении при длительном приеме [7, 19]. Он препятствует адгезии тромбоцитов к сосудистой стенке и умеренно снижает агрегационную функцию тромбоцитов благодаря поступлению в кровь из эндотелия простациклина, ослаблению продукции в лейкоцитах фактора стимуляции тромбоцитов.
Важным свойством препарата СД является его способность существенно стимулировать фибринолиз за счет снижения активности в крови PAI-I и увеличения выброса из эндотелия тканевого активатора плазминогена, уменьшать вязкость плазмы и улучшать микроциркуляцию за счет уменьшения в плазме фибриногена [24, 30, 31, 34, 39, 40, 48], а также оказывать умеренное венотоническое действие, поскольку уменьшение капиляро-венозного стаза играет важную роль в антитромботическое эффекте [33]. Все вышеуказанные эффекты ВДФ позволяют применять его не только для предупреждения роста и лизиса уже имеющихся тромбов, но и для вторичной профилактики ВТ, хронической венозной недостаточности и трофических язв [17, 18, 24, 34, 36, 37, 39, 40, 43—45].
К сожалению, работы, показывающие особенности процесса реканализации венозного русла у больных с перенесенным ТГВНК через 6 мес на фоне применения антикоагулянтов, в том числе СД, единичны [32]. Нет данных о пролонгированном применении СД у больных с ТГВНК, неизвестно, как происходит восстановление венозного русла в нижних конечностях у этих больных в течение года на фоне длительного применения СД. Все перечисленное обусловило проведение данного исследования.
Цель исследования — изучение эффективности и безопасности СД, процесса реканализации вен у больных с ТГВНК при его пролонгированном применении в течение года.
Материал и методы
В открытое сравнительное проспективное исследование включены 275 больных с ТГВНК. Основную группу составили 149 больных (62 женщины и 87 мужчин) в возрасте от 18 до 69 лет (средний возраст 40,4±1,9 года), которым назначался СД (ВДФ), группу сравнения — 126 больных (65 женщин и 61 мужчина) в возрасте от 18 до 64 лет (средний возраст 39,6±2,1 лет), которым назначался варфарин. Анализируемые группы были сопоставимы по полу и возрасту, характеру клинических проявлений и сопутствующей патологии. Критериями включения в исследование являлся документально подтвержденный при дуплексном сканировании в В-режиме ТГВНК, критериями исключения из исследования — онкологические заболевания, скелетные травмы и переломы, длительная иммобилизация, оперативные вмешательства, острые инфекции, возраст пациентов моложе 17 и старше 69 лет.
Комплексное лабораторное и генетическое обследование больных с ТГВНК включало определение основных клинико-биохимических показателей крови, системы гемостаза, содержания гомоцистеи-на (ГЦ) и С-реактивного белка в сыворотке крови, аллельного полиморфизма 10 генов, кодирующих компоненты плазменного и тромбоцитарного звеньев гемостаза по стандартным методикам. Доппле-рометрия и дуплексное сканирование (ДС) вен нижних конечностей выполняли на ультразвуковых сканерах Philips Envisor С, Acuson Antares и Acuson Aspen (Siemens, Германия), VIVID 3 и VIVID i (GE Medical Sistems, США), Toshiba Hario, Япония) в В-режиме с применением конвексного датчика 3,5 мГц и линейного датчика 5—10 мГц по стандартным методикам. ДС проводилось при госпитализации и накануне выписки из стационара на 10—14-е сутки, при амбулаторном наблюдении больных — 1 раз в 2 мес на протяжении года. В остром периоде лечение больных с ВТЭО велось с учетом последних клинических рекомендаций [16, 26]. При диагностике тромбофилических состояний использовались стандартные методики с учетом рекомендаций [11, 15]. В основной группе перевод больных на ВДФ осуществлялся через 1,5—2 мес от начала лечения ТГВНК амбулаторно. На момент включения в исследование другие антикоагулянты отменялись. Больным назначался СД по 600 ЛЕ в/м в течение 10—14 дней. Затем переходили на пероральный пролонгированный прием препарата 250 ЛЕ 2 раза в сутки.
Продолжительность приема ВДФ и варфарина составляла от 6 до 12 мес Показаниями для назначения ВДФ у больных являлись: невозможность приема АВК, нарушения в системе протеина С, снижение антитромбина III и развитие тромбоцитопе-нии (в том числе гепарининдуцированной), а также выраженное угнетение фибринолиза, отсутствие, по данным ДС, динамики реканализации,. Больным группы сравнения на 5—7-й день в стационаре назначался варфарин, подбор дозы которого осуществлялся по стандартным методикам с учетом значений международного нормализованного отношения (МНО). При достижении значений МНО более 2,0 прямые антикоагулянты отменялись. Консервативное лечение в обеих группах также включало обязательное применение компрессионного трикотажа и флеботоников (диосмин, кверцетин). По показаниям применялись антибиотикотерапия и нестероидные противовоспалительные препараты. После установления гипергомоцистеинемии больным назначался комбинированный лекарственный препарат, содержащий фолиевую кислоту, витамины В6 и В12, под динамическим контролем уровня ГЦ в сыворотке крови [14]. Точками исследования у больных с ТГВНК на фоне пролонгированного лечения СД являлись оценка переносимости препарата, частота развития кровотечений венозного тромбоза, процесс реканализации вен нижних конечностей в течение года. Полученные результаты обрабатывалась современными методами медико-биологической статистики с использованием программного пакета Statistica 6.0 и математических программ SPSS 19. Статистически значимыми различия (р) признавались при р Результаты и обсуждение
У всех больных основной группы пролонгированное применение ВДФ не вызывало развития нежелательных побочных эффектов и аллергических реакций. Переносимость препарата отмечена врачом и пациентом как отличная и хорошая.
На фоне пролонгированного лечения СД у 108 больных основной группы в течение года изучен процесс реканализации венозного русла нижних конечностей по данным ультразвукового исследования в динамике. Так как наблюдалось многоуровневое поражение венозного бассейна нижних конечностей, процесс реканализации вен оценивался по ДС отдельно для каждого сегмента — подвздошного (у 24 больных), бедренного (у 42), подколенного (у 38), берцового (у 20). Установлено, что через 2 мес на фоне лечения СД доля больных с окклюзионными формами подвздошного сегмента уменьшилась на 40,2% (p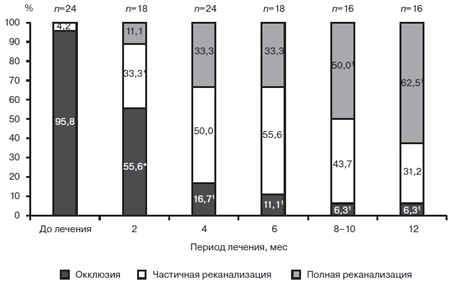
Рис. 1. Восстановление просвета подвздошных вен у больных с ТГВНК при лечении СД в течение года.
* — значимость различий по отношению к исходному значению (р
Аналогично отмечалась реканализация бедренного сегмента у больных с тромбозом бедренных вен. Уже через 2 мес применения СД доля больных с окклюзионным поражением бедренных вен уменьшилась на 75,5% (рЧерез 4 мес приема препарата отмечалось статистически значимое увеличение доли больных с полной реканализацией бедренного сегмента на 46,9% (р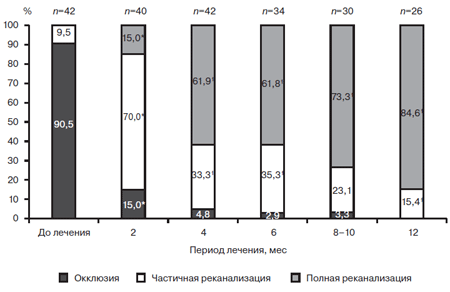
Рис. 2. Восстановление просвета бедренных вен у больных с ТГВНК при лечении СД в течение года.
* — значимость различий по отношению к исходному значению (р
Положительный клинический результат за счет восстановления просвета подколенной вены у больных с тромбозом при лечении СД наблюдался уже через 2 мес. Доля больных с окклюзионным поражением подвздошных вен через 2 мес лечения уменьшилась на 81,5% (р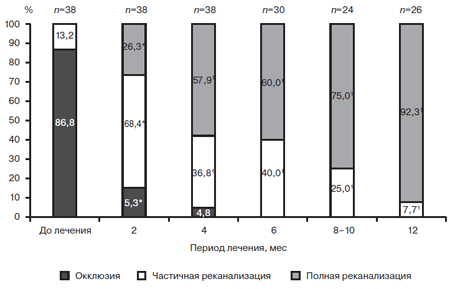
Рис. 3. Восстановление просвета подколенной вены у больных с ТГВНК при лечении СД в течение года.
* — значимость различий по отношению к исходному значению (р
Уже через 4 мес лечения СД отмечалось статистически значимый рост числа больных с полной реканализацией подколенной вены на 31,6% (p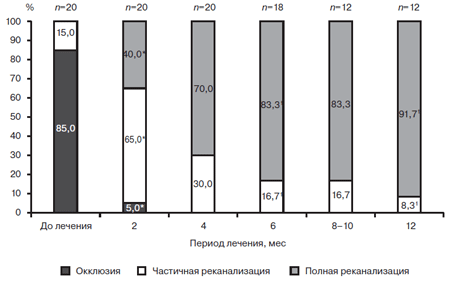
Рис. 4. Восстановление просвета берцовых вен у больных с ТГВНК при лечении СД в течение года.
* — значимость различий по отношению к исходному значению (р
Установлено, что через 2 мес применения СД у 95,0% больных с венозным тромбозом частично или полностью восстановился просвет берцовых вен. Окклюзионные формы сохранялись лишь у 5,0% больных, частичная реканализация наблюдалась у 55,0%, тогда как полная реканализация — у 40,0%. Окклюзионное поражение берцовых вен уже через 4 мес лечения СД не наблюдалась. Доля больных с частичной реканализацией берцовых вен была наибольшей через 2 мес лечения. В дальнейшем, на фоне лечения, она постепенно уменьшалась и через 12 мес лечения отмечалась у 8,3% больных. Полная ре-канализация берцовых вен на фоне непрерывного применения СД через 12 мес наблюдалась у 91,7% больных.
В группе сравнения применение варфарина в течение 6—12 мес у 8 пациентов (6,3% случаев) отмечено развитие клинически значимых кровотечений (почечное и мочевое — 3,1%, маточное — 2,4%, желудочное — 0,8%), тогда как у больных основной группы, принимающих СД, таких осложнений не наблюдалось (рПолученные данные согласуются с результатами зарубежных исследований, в которых показано, что применение СД в течение 6 мес для лечения и вторичной профилактики ВТЭО безопасно и не вызывает развития геморрагического синдрома, тогда как прием АВК сопровождается развитием различных кровотечений в 13,3—15,0% случаев [32, 36].
Заключение
Таким образом, существующие в литературе сравнительные исследования по эффективности и безопасности применения СД (ВДФ) для лечения и вторичной профилактики ВТЭО по отношению к антикоагулянтам (аценокумарол, гепаринсульфат, эноксапарин), традиционно используемым в различные периоды венозного тромбоза нижних конечностей и легочной эмболии, имели сопоставимые результаты, а по отношению к плацебо препарат оказывал статистически значимое влияние на систему гемостаза и фибринолиза, тромбоцитарное звено гемостаза и маркеры эндотелиальной дисфункции. Полученные результаты исследования и литературные данные показали эффективность и безопасность СД (ВДФ) для лечения и вторичной профилактики ТГВНК, в том числе у лиц среднего и пожилого возраста, включая различные формы тромбофилии, что позволяет рекомендовать его в качестве альтернативы антагонистам витамина К, избегая риска развития у пациентов геморрагических осложнений при пролонгированном приеме в течение года.
Оценка динамики реканализации просвета различных сегментов венозного русла нижних конечностей на фоне применения СД (ВДФ) в течение года позволяет сделать вывод о том, что его пролонгированное применение для лечения и профилактики тромботической опасности при ТГВНК является эффективным. При этом у больных с ТГВНК пролонгированное применение СД (ВДФ) в течение года способствует полной реканализации вен — подвздошных (62,5% случаев), бедренных (84,6%), подколенной (92,3%), а берцовых — в 91,7% случаев, что позволяет в дальнейшем предотвратить развитие тяжелых форм хронической венозной недостаточности и трофических язв. ЛИТЕРАТУРА 1. Аркадьева Г.В., Радзевич А.Э., Седов А.Н. Профилактика и лечение тромбозов и тромбоэмболий непрямыми антикоагулянтами при сердечно-сосудистой патологии. Российский кардиологический журнал. 2007;3:86-96.
2. Баркаган З.С., Момот А.П. Основы диагностики нарушений гемостаза. М. 1999.
3. Вавилова Т.В., Орловский П.И., Гриценко В.В. Терапия и профилактика тромбозов — клинические, лабораторные и организационные аспекты. Новые Санкт-Петербургские Врачебные ведомости. 2005;4:55-59.
4. Гавриленко А.В., Куклин А.В, Котов А.Э., Аликин Е.Ю. Антикоагулянты в сосудистой хирургии. Ангиология и сосудистая хирургия. 2008;14(4):33-40.
5. Грибаускас П.С. Антикоагулянты непрямого действия (применение, дозирование, показания и противопоказания, лабораторный контроль, осложнения и первая помощь). Українськ кардіологіч журнал. 2002;2:15-31.
6. Гринфельд Е.С. Современные подходы к лечению венозной тромбоэмболии. Русский медицинский журнал. 2010;18(3):131-135.
7. Жируев М.С., Шерстнов М.Ю., Ельсиновский В.И. Лечение тромбозов глубоких вен и тромбоэмболических осложнений в условиях Центра амбулаторной хирургии многопрофильной больницы. Амбулаторная хирургия. Стационарозамещающие технологии. 2005;18(2):57-60.
8. Кириенко А.И., Леонтьев С.Г., Лебедев И.С. Лечение тромбоза в системе нижней полой вены. Как избежать ошибок? Ангиология и сосудистая хирургия. 2007;13(4):99-102.
9. Кириенко А.И., Панченко Е.П., Андрияшкин В.В. Венозный тромбоз в практике терапевта и хирурга. М. 2012;336.
10. Козлова Т.В. Оценка риска геморрагических осложнений при длительном применении варфарина для профилактики рецидива венозного тромбоза. Вестник службы крови России. 2005;2: 18-22.
11. Козлова Т.В. Эффективность и безопасность длительной анти-коагулянтной терапии варфарином у больных с венозными тромбозами. Научно-практическая ревматология. 2005;4:53-57.
12. Немченко Л.Н. Сулодексид в лечении васкулярных заболеваний с риском тромбообразования. Сайт терапевтов, 2004. Доступно по: http: //www.therapiya.com/sulod_tromb.htm. Ссылка действительна по 15.04.2015.
13. Основы клинической флебологии. Под. ред. Шевченко Ю.Н., Стойко Ю.М. М.: Шико; 2013.
14. Петриков А.С., Шойхет Я.Н., Белых В.И., Костюченко Г.И. Фармакологическая коррекция гипергомоцистеинемии у больных с венозными тромбоэмболическими осложнениями. Флебология. 2012;6(4):24-28.
15. Руководство по гематологии. В 3 т. Под ред. Воробьева П.А. М.: Ньюдиамед; 2005;3.
16. Российские клинические рекомендации по диагностике, лечению и профилактике венозных тромбоэмболических осложнений. Флебология. 2010; 4(2):30-37.
17. Сулодексид. Механизмы действия и опыт клинического применения. Под ред. Светухина А.М., Баркагана З.С. М. 2000.
18. Суханова Г.А., Рудакова В.Е., Васильев С.А. Профилактика тромбоэмболических осложнений у лиц среднего и пожилого возраста. Клиническая геронтология. 2007;4:10-15.
19. Титова М.И., Амирасланов Ю.А., Земляной А.Б., Доронина Л.П., Руднева В.Г., Егорова В.В., Демидова В.С., Аскеров Н.Г. Программы антитромботической коррекции нарушений системы гемостаза при гнойной хирургической инфекции в до- и послеоперационном периоде. Вестник Национального медико-хирургического центра им. Н.И. Пирогова. 2013;8(2):119-124.
20. Савельев В.С., Гологорский В.А., Кириенко А.И. Флебология: руководство для врачей. М.: Медицина; 2001.
21. Шевченко Ю.Л. Основы клинической флебологии. М.: Медицина; 2005.
22. Явелов И.С., Кириенко А.И. Предупреждение рецидива венозных тромбоэмболических осложнений. Трудный пациент. 2012;10(14):6-10.
23. Adiguzel C, Iqbal O, Hoppensteadt D, Jeske W, Cunanan J, Litinas E, He Zhu, Walenga JM, Fareed J. Сomparative Anticoagulant and Platelet Modulatory Effects of Enoxaparin and Sulodexide. Сlinical and Applied Thrombosis/Hemostasis. 2009;15(5):501—511.
24. Agrati AM, Mauro M, Savasta C. A double-blind crossover placebo-controlled study of the profibrinolytic and antithrombotic effects of oral Sulodexide. Advances in Therapy. 1992;9(3):147-155.
25. Andreozzi GM. Sulodexide in the treatment of chronic venous disease. Am J Cardiovasc Drugs. 2012;1(2):73-81.
26. Kearon C, Akl АE, Comerota AJ, Prandoni P, Bounameaux H, Gold-haber SZ, Nelson ME, Wells PS, Gould MK, Dentali F, Crowther M, Kahn SR. American College of Chest Physicians. Antithrombotic therapy for VTE disease: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest. 2012;141:419-494.
27. Barbanti M, Guizzardi S, Calanni F, Marchi E, Babbini M. Anti-thrombotic and thrombolytic activity of sulodexide in rats. International Journal оf Clinical & Laboratory Research. 1992;22(3):179-184.
28. Borawski J, Dubowski M, Rydzewska-Rosolowska A, Mysliwiec M. Intravenous and oral sulodexide versus coagulation activation markers in humans. Clin Appl Thromb Hemost. 2009;5:596-598.
29. Buchanan M.R., Brister S.J., Ofosu F. Prevention and treatment of thrombosis: novel strategies arising from our understanding the healthy endothelium. Wien Klin Wochenschr. 1993;105(11):309-313.
30. Buchanan MR, Liao P, Smith LJ, Ofosu FA. Prevention of thrombus formation and growth by antithrombin III and heparin cofactor II-dependent thrombin inhibitors: importance of heparin cofactor II. Thromb Res. 1994;74(5):463-475.
31. Callas DD, Hoppensteadt W, Jeske W, Iqbal O, Bacher P, Ahsan A, Fareed J. Comparative pharmacologic profile of a glycosaminoglycan mixture, Sulodexide, and a chemically modified heparin derivative. Semin Thromb Hemost. 1993;1:49-57.
32. Cirujeda JL, Granado PC. A study on the safety, efficacy, and efficiency of sulodexide compared with acenocoumarol in secondary prophylaxis in patients with deep venous thrombosis. Angiology. 2006;57(1):53-64.
33. Coccheri S, Scondotto G, Agnelli G. Randomised, double blind, mul-ticentre, placebo controlled study of sulodexide in the treatment of venous leg ulcers. Thromb Haemost. 2002;87(6):947-952.
34. Crepaldi G, Rossi A, Coscetti G, Abbruzzese E, Calveri U, Calabro A. Sulodexide oral administration influences blood viscosity and fibrino-lysis. Drugs Exp Clin Res. 1992;18(5):189-195.
35. Hyers TM, Agnelli G, Hull RD, Weg JG, Morris TA, Samama M, Tapson V. Antithrombotic therapy for venous thromboembolism disease. Chest. 1998;114:561-578.
36. Lasierra J, Coronel P, Cuevas B. Is sulodexide an alternative treatment in the prophylaxis of thromboembolic disease? Journal of Thrombosis and Haemostasis. 2003;1(1):14-22.
37. Lasierra-Cirujeda J, Coronel P, Aza MJ, Gimeno M. Use of sulodex-ide in patients with peripheral vascular disease. J Journal of Blood Medicine. 2010;1:105-115.
38. Lauver DA, Lucchesi BR. Sulodexide: A Renewed Interest in This Gly-cosaminoglycan. Cardiovascular Drug Reviews. 2006;24(34):214-226.
39. Lunetta M, Salanitri T. Lowering of plasma viscosity by the oral administration of the glycosaminoglycan sulodexide in patients with peripheral vascular disease. Int Med Res. 1992;20:45-53.
40. Mannarino E, Pasqualini L, Ciuffetti G. Effect of oral administration of sulodexide on fibrinolysis and plasma viscosity: A pilot study. Drug Investigation. 1992;4:346-350.
41. Ofosu FA. Pharmacological actions of sulodexide. Seminars In Thrombosis аnd Hemostasis. 1998;24(2):127-138.
42. Ost D, Tepper J, Mihara H, Lander O, Heinzer R, Fein A. Duration of anticoagulation following venous thromboembolism: a meta-analysis. JAMA. 2005;294(6):706-715.
43. Penka M. Sulodexide in the treatment of venous thrombosis. Vnitni Lekarstvi. 1995;41(3):169-171.
44. Pinto A, Corrao S, Galati D, Arnone S, Licata A, Parrinello G, Maniscalchi T, Licata G. Sulodexide Versus Calcium Heparin in the Medium-Term Treatment of Deep Vein Thrombosis of the Lower Limbs. Angiology. 1997;48(9):805-811.
45. Romano F, Platania M, Costa A, Salaminitri T. The effect of sulodex-ide on blood viscosity in patients with peripheral vascular diseas. Eur J Clin Res. 2001;3:73-82.
46. Silverstein MD, Heit JA, Moor DN, Petterson TM, O’Fallon WM, Melton LJ. 3rd. Trends in the incidence of deep vein thrombosis and pulmonary embolism: a 25-year population-based study. Arch Int Med. 1998;158:585-593.
47. Stiegler H, Arbogast H, Nees S, Halder A, Grau A, Riess H. Throm-bectomy, lysis, or heparin treatment: concurrent therapies of deep vein thrombosis: therapy and experimental studies. Semin Thromb Hemost. 1989;15(3):250-258.
48. Thomas DP, Merton RE, Barrowcliffe TW. Relative efficacy of hepa-rin and related glycosaminoglycans as antithrombotic drugs. Ann NY Acad Sci. 1989;556:313-322.


