Мелатонин (Мелаксен) в неврологической практике
Статьи Опубликовано в:«CONSILIUM MEDICUM» »» ТОМ 14 № 2
Я.И.Левин
ГБОУ ВПО Первый МГМУ им. И.М.Сеченова Минздравсоцразвития РФ
XXI в. вполне уместно назвать веком мелатонина и мелатониномиметиков с учетом все возрастающей роли в современной медицине самого мелатонина и создания новых поколений гипнотиков и антидепрессантов, воздействующих на мелатониновые церебральные рецепторы.
Мелатонин N-ацетил-5-метокситриптамин) представляет собой индольное соединение и вырабатывается эпифизом, сетчаткой и кишечником. Его метаболизм представлен на рис. 1.
Рис. 1. Метаболизм мелатонина. 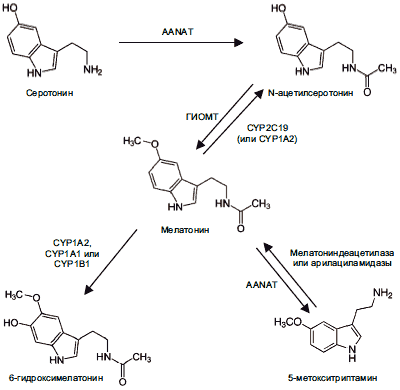
Хорошо изучены основные этапы биосинтеза мелатонина и временная динамика его образования (рис. 2). Синтез мелатонина осуществляется в эпифизе, его источником служит триптофан, который поступает в пинеалоциты из сосудистого русла и через 5-окситриптофан превращается в серотонин. Лимитирующим фактором в синтезе гормона служит активность фермента арилалкиламин-N-ацетилтрансферазы (AANAT), контролирующего образование предшественника - N-ацетилсеротонина, в дальнейшем при участии гидрокси-индол-О-метилтрансферазы (ГИОМТ), превращающегося в сам мелатонин. Принципиально важным является факт циркадианной (околосуточной) периодичности выработки в пинеалоците биологически активных соединений. Синтез мелатонина эффективно происходит только с наступлением темноты и резко снижается в светлую фазу суток - факт, впервые показанный R.Wurtman в 1960 г. Достаточно короткого светового импульса (силой 0,1-1 лк), чтобы подавить этот процесс. В дневные часы в ткани железы, напротив, накапливается серотонин.
Дневной ритм продукции мелатонина зависит от активности AANAT в сетчатке, которая в свою очередь зависит от ионов кальция, дофамина и γ-аминомасляной кислоты (ГАМК).
Сетчатка является независимым и важным местом продукции мелатонина, по содержанию которого она стоит на втором месте после эпифиза. По-видимому, сетчатке принадлежит определенная роль в поддержании уровня плазменного мелатонина в случае ослабления эпифизарной активности. Предполагается, что дофамин (биохимический аналог света) передает пигментному эпителию сигнал о свете, а мелатонин (биохимический аналог темноты) - о темноте, причем баланс между этими двумя нейрогормонами регулирует функцию пигментного эпителия при изменении адаптации.
На образовании мелатонина заметно сказывается целый ряд внешних и внутренних факторов. Особенно значима длина фотопериода, поскольку величина секреции находится в обратных отношениях с продолжительностью светового дня. В случае инверсии светового режима через несколько суток извращается и суточная динамика уровня мелатонина. Повреждение любого звена пути регуляции синтеза гормона, начиная с сетчатки, приводит к снижению ночной секреции мелатонина, распаду циркадианного ритма на отдельные ультрадианные составляющие. Из эндогенных факторов существенное значение могут иметь характер гормональной активности, особенно состояние гонад, а также возраст. Из-за возрастной инволюции железы наблюдается прогрессивное снижение амплитуды и величины секреции гормона на протяжении суток.
Мелатонин является многофункциональным гормоном, что определяется в том числе и значительной представленностью его рецепторов в разных образованиях головного мозга. Наиболее высоки уровень гормона и плотность мелатониновых рецепторов (МТ1, МТ2 и МТ3) в переднем гипоталамусе (преоптическая, медиобазальная области), за которыми следуют промежуточный мозг, гиппокамп, стриатум и неокортекс. Через эти рецепторы мелатонин способен ограничивать поведенческие нарушения, обусловленные стрессом, прямо вмешиваясь в работу эндокринных центров гипоталамуса и неэндокринных стрессорганизующих структур мозга. Мелатониновые рецепторы описаны в различных эндокринных органах, начиная с гонад, где их содержание особенно велико, и кончая надпочечниками. Значительная плотность специализированных рецепторов обнаружена и в клетках самого эпифиза. Повышение концентрации мелатонина в крови с наступлением темноты снижает у человека температуру тела, уменьшает эмоциональную напряженность, индуцирует сон, а также незначительно угнетает функцию половых желез, что отражается в задержке пролиферации опухолевых клеток молочной и предстательной желез. Мелатонин участвует в гормональном обеспечении околосуточного и сезонного периодизма поведенческой активности.
Рис. 2. Основные этапы биосинтеза мелатонина в эпифизе и нервные пути регуляции этого процесса (по Э.Б.Арушанян, 1991, с дополнениями).
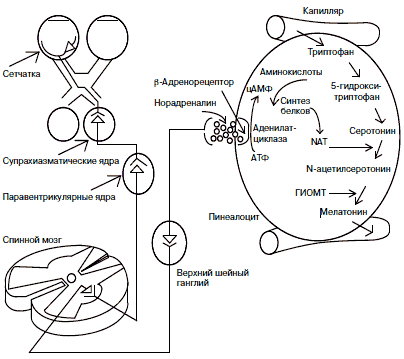
Мелатонин является одним из самых мощных эндогенных антиоксидантов, а также обладает протективными свойствами в отношении свободнорадикального поражения ДНК, белков и липидов. Мелатонин способен связывать свободные радикалы (гидроксил, свободный кислород, пероксинитрит и т.д.) и стимулировать активность антиоксидантной системы (ферменты супероксид дисмутаза, глутатион пероксидаза, глутатион редуктаза, глюкозо-6-фосфат дигидрогеназа). Мелатонин обеспечивает защиту клеток мозга по меньшей мере двумя способами: разложением пероксида водорода до воды и утилизацией свободных гидроксильных радикалов.
Доказанные биологические эффекты мелатонина многообразны: снотворный, гипотермический, антиоксидантный, противоопухолевый, адаптогенный, синхронизационный, антистрессовый, антидепрессантный, иммуномодулирующий.
В настоящее время роль мелатонина эпифиза в таких явлениях, как внутрисуточная и сезонная ритмика, сон-бодрствование, репродуктивное поведение, терморегуляция, иммунные реакции, внутриклеточные антиокислительные процессы, старение организма, опухолевый рост и психиатрические заболевания, -представляется несомненной.
Исходя из перечисленных биологических эффектов мелатонина, следует предположить его важную роль в терапии многих неврологических заболеваний.
Нарушения цикла «сон-бодрствование»
Первые прямые исследования действия мелатонина на сон человека с использованием полиграфической регистрации были выполнены в 1970-е годы. Испытуемым вводили внутривенно большие дозы мелатонина - от 50 мг до 1 г. Результаты таких исследований были противоречивы: вечернее внутривенное введение 50 мг мелатонина здоровым испытуемым вызывало приступ сонливости и значительно сокращало период засыпания без изменений структуры ночного сна; при утреннем и вечернем оральном приеме такой же дозы сонливость не наступала; вечерний пероральный прием 80 мг мелатонина на фоне инсомнии, вызванной предъявлением звукового шума, значительно улучшал структуру ночного сна. Ежедневный прием 1 г мелатонина в течение 6 дней увеличивал представленность II стадии медленного сна у здоровых испытуемых, снижал представленность IV стадии и увеличивал плотность быстрых движений глаз во время периодов быстрого сна.
В серии исследований P.Lavie и соавт. (1994, 1995 г.) мелатонин (5 мг) достоверно ускорял засыпание, увеличивал представленность II стадии в последующем сне независимо от времени его приема и удлинял продолжительность сна.
В наших исследованиях (А.М.Вейн, Я.И.Левин и соавт. 1998-1999) проведено изучение действия ежевечернего приема Мелаксена (содержит 3 мг мелатонина) в течение 5 дней на субъективную оценку качества ночного сна у 40 больных первичной инсомнией (возраст 25-75 лет). Считали себя «совами» ½ испытуемых и ½ - «жаворонками». Жаловались на трудности засыпания 90% человек, на частые ночные пробуждения -70%, на поверхностный сон - 60%, на трудности засыпания после пробуждения среди ночи - 50%, на ранние утренние пробуждения - 65%. В качестве причины инсомнии испытуемые чаще всего называли жизненные события и стресс, 2/3 из них уже имели опыт применения снотворных, как правило бензодиазепинов. За неделю до начала исследований все испытуемые прекращали прием любых снотворных и успокоительных препаратов. До и после применения Мелаксена пациенты заполняли анкеты субъективной балльной оценки сна. Полученные данные подвергались математическому анализу с применением методов непараметрической статистики. Обнаружено достоверное улучшение субъективных показателей сна по группе в целом, причем наиболее выражено - в ускорении засыпания. Это важный показатель эффективности Мелаксена в качестве снотворного, неоднократно ранее описанный в литературе. В целом эффективность Мелаксена как снотворного была оценена и врачами, и пациентами одинаково и составила по 5-балльной шкале 3,55. Безопасность Мелаксена оказалась очень высокой; ее также оценили одинаково в 4,9 балла, что означает, что Мелаксен практически не дает побочных эффектов и осложнений. При разделении испытуемых на 2 возрастные группы - до 40 лет (20 человек) и старше (20 человек) было обнаружено, что эффективность Мелаксена одинакова в 2 группах. При разделении испытуемых на 2 группы по эффекту воздействия Мелаксена на сон - «слабую» (медиана суммарной балльной оценки качества сна возросла не более чем на 3 единицы, 20 человек) и «сильную» (возрастание более чем на 3 балла, 20 человек) - обнаружено, что во 2-й группе достоверно преобладали испытуемые с исходно более резко выраженными субъективными нарушениями сна. Это означает, что чем хуже исходные субъективные показатели сна, тем сильнее положительное влияние Мелаксена.
Согласно гипотезе А.Борбели (Borbely) и соавт. (1988 г.), циркадный и гомеостатический «осцилляторы» являются независимыми друг от друга, так что состояние человека в каждый данный момент является результатом «алгебраического суммирования» воздействия этих двух механизмов. В настоящее время теория Борбели является общепризнанной для описания состояний бодрствования и медленного сна, хотя и остается неприменимой для описания быстрого - парадоксального сна.
В соответствии с этой концепцией и исходя из корреляции между субъективно ощущаемым и объективно подтвержденным ежевечерним нарастанием сонливости, с одной стороны, и началом роста уровня мелатонина в крови - с другой, предполагается, что циркадные осцилляции человека, его «биологические часы», определяются деятельностью двух реципрокных механизмов - выбросом мелатонина эпифизом и ритмической импульсацией нейронов супрахиазмального ядра (СХЯ). По мнению ряда авторов, роль мелатонина состоит скорее в открытии так называемых «ворот сна» (sleep gates), в создании «предрасположенности ко сну», в торможении механизмов бодрствования, чем в прямом воздействии на сомногенные структуры. Открытию «ворот сна» предшествует период повышенной активации человека - так называемый «запретный период» («запретная зона» - forbidden zone) для сна, который довольно резко сменяется «открытием ворот». Имеются некоторые свидетельства в пользу предположения о том, что эта «запретная временная зона» сна представляет собой пик ежедневного цикла бодрствования, поскольку сочетается с суточным пиком температуры тела. Начало секреции мелатонина у человека, приходящейся обычно на середину «запретного периода», способствует сглаженному, плавному переходу от бодрствования ко сну.
Однако возникает вопрос: связаны ли мягкие седативные и гипногенные эффекты мелатонина с его прямым воздействием на мозговые системы поддержания бодрствования и механизмы медленного сна или же они лишь отражают способность мелатонина вызывать фазовый сдвиг циркадного осциллятора? Похоже, что оба эффекта имеют место при введении физиологичных доз мелатонина, причем они могут алгебраически суммироваться друг с другом в зависимости от момента введения. Из-за высокой насыщенности СХЯ и прилежащих областей преоптической области высокоаффинными рецепторами мелатонина этот гормон наряду с рядом других физических (яркий свет) и биохимических факторов (в числе последних - нейромедиаторы глутаминовая кислота и серотонин, а также нейропептиды NPY - «нейропептид тирозин» и SP - «вещество П») способен оказывать мощные модулирующие воздействия на активность главного осциллятора в организме млекопитающих. Если мелатонин вводится в утренние часы, то он вызывает задержку циркадной фазы, а если в вечерние - то, наоборот, сдвиг фазы «вперед». Эти фазовые сдвиги у человека не превышают 30-60 мин/сут. Таким образом, путем ежедневного приема мелатонина можно добиться сдвига суточного цикла «активность-покой» на несколько часов в ту или другую сторону, что бывает необходимо при трансмеридиональных перелетах или сменной работе.
Инсульт
Мозговой инсульт, как правило, приводит к грубым расстройствам ночного сна. Эти расстройства проявляются изменениями как его структуры, так и циркадных характеристик. Если в первом случае имеют место качественные изменения, проявляющиеся серьезными нарушениями механизмов генерации и поддержания сна, то во втором - либо сон становится полифазным, либо происходит его инверсия (смещение цикла «сон-бодрствование»). Нами (А.М.Вейн, Я.И.Левин, РЛ.Гасанов, 2000) проведено изучение действия ежевечернего перорального приема Мелаксена в течение 10 дней на субъективную оценку качества ночного сна и его объективные характеристики у 15 больных в острейшем периоде ишемического инсульта. Их показатели сравнивались с таковыми у 15 здоровых добровольцев (контроль), соответственно подобранных по полу и возрасту. Все исследуемые прошли клинико-неврологическое обследование. Для объективизации динамики восстановления применяли также Скандинавскую шкалу инсульта. С помощью анкетных методов подробно уточняли сомнологический анамнез, субъективную оценку сна, уровень депрессии (опросник Бэка), личностной и реактивной тревоги (шкала Спилбергера). До и после 10-дневного приема препарата проводилась полисомнография c регистрацией электроэнцефалограммы, электроокулограммы и электромиограммы. Анализ структуры сна проводился с помощью программы Центра сомнологических исследований, где кроме стандартных параметров изучается сегментарная структура сна.
У всех больных регистрировались расстройства сна разной степени выраженности. Исследования показали, что в результате приема Мелаксена у больных отмечались: достоверное уменьшение длительности засыпания (с 35 до 21 мин), представленности I стадии -дремоты (с 12 до 8%), количества сегментов (с 89 до 66), увеличение времени II стадии - (с 32 до 44%). Индекс качества сна (интегративный показатель; чем он ниже, тем лучше структура сна) снижался с 29 до 24. Однако на фоне улучшения этих показателей сна имело место некоторое снижение длительности фазы быстрого сна (с 17 до 13%), при этом длительность глубокого медленного сна («дельта-сна») изменялась незначительно (с 18 до 20%). Особенностью Мелаксена являлось также то, что при инверсии сна (3 пациента) он восстанавливал нарушенный биоритм «сон-бодрствование». Отмечалось также достоверное снижение уровня депрессии. Личностная и реактивная тревожность оставалась без динамики. В неврологической картине динамики не наблюдалось, что, по-видимому, связано с недостаточностью этого срока для выявления положительных сдвигов. Сделан вывод, что Мелаксен оказывает положительное влияние на качество сна при его нарушениях, вызванных мозговым инсультом.
Но не только улучшение цикла «сон-бодрствование» делает Мелаксен интересным для применения у больных с инсультом. Целый ряд исследований (как экспериментальных, так и клинических) выявляет важнейшие свойства мелатонина для лечения этих пациентов:
- Мелатонин увеличивает церебральную реперфузию у крыс с экспериментальной артериальной окклюзией.
- Мелатонин уменьшает мозговой отек у крыс с экспериментальным инсультом.
- Мелатонин повышает нейропластичность в условиях стресса, вызванного экспериментальным инсультом.
- При врожденной гипоплазии эпифиза повышается риск мозгового инсульта и инфаркта миокарда
- Изменения иммунного статуса при инсульте, возможно, связано с нарушенной ночной секрецией мелатонина.
- Мелатонин повышает нейропластичность у пожилых.
Инсомния серьезным образом модифицирует и отягощает клинические проявления и течение хронической церебральной сосудистой недостаточности (ХЦСН) и требует специального лечения. С этой целью проведено российское многоцентровое (в 23 неврологических центрах) открытое несравнительное исследование эффективности и безопасности препарата Мелаксен, содержащего 3 мг мелатонина.
С помощью клинико-неврологических и анкетных (анкета балльной оценки субъективных характеристик сна; шкала сонливости - Epworth; анкета для скрининга синдрома апноэ во сне; госпитальная шкала тревоги и депрессии) методов и протокола нарушений сна (www.sleepmed.ru) обследованы 2063 пациента с ХЦСН и инсомнией [средний возраст пациентов - 55,7±9,0 года; женщины - 74,1% мужчины - 25,8%; продолжительность нарушений сна 49,7±56,2 мес (от 1 до 480 мес)] до, в процессе (14-й день) и после (28-й день) лечения Мелаксеном. Мелаксен назначался однократно за 40 мин до укладывания в постель в рамках стандартной комплексной терапии.
Исследованные пациенты характеризовались низким баллом по анкете сна (14,4 балла, норма - более 21), повышенной дневной сонливостью (8,2 балла, норма -5 и менее), субклинически выраженными тревогой и депрессией (9,6 и 8,3 балла соответственно). На трудности поддержания сна жаловались 93,8% пациентов, раннее утреннее пробуждение - 86,5%, нарушенное засыпание - 80%, дневную сонливость - 70% и на полное отсутствие сна (по мнению больных) - 8%.
На фоне лечения Мелаксеном уже во время 2-го визита суммарная балльная оценка субъективных характеристик сна возрастала на 36,6 и 57,7% по окончании лечения, составляя 22,7 балла. При этом уже ко 2-му визиту достоверно снижались баллы по шкалам дневной сонливости (6,4 балла), апноэ, тревоги (6,1) и депрессии (6,4). В конце лечения все перечисленные позитивные сдвиги усиливаются и нарастают. Все пациенты завершили курс терапии. Пациенты и врачи практически одинаково оценивали эффективность и безопасность препарата. Проведенное исследование демонстрирует эффективность Мелаксена для лечения нарушений сна по типу инсомнии у больных с ХЦСН в условиях амбулаторной и стационарной практики, он хорошо переносится и не создает проблем в комплексной терапии этих пациентов.
Эпилепсия
Достаточное количество исследований свидетельствует о снижении ночной секреторной активности эпифиза у больных эпилепсией, при этом отмечаются более низкие уровни мелатонина у больных с частыми приступами.
Исследование содержания мелатонина у взрослых больных эпилепсией с оценкой вечерней (за 1 ч до сна), ночной концентрации (утром) экскреции мелатонина у 54 больных фокальной симптоматической эпилепсией в возрасте от 21 до 47 лет показало, что эпилептические припадки провоцируют снижение концентрации мелатонина в организме. В отличие от здоровых субъектов пациенты обнаруживают также резкое усиление экскреции с мочой 6-сульфатоксимелатонина. Таким образом, в результате подобных сдвигов складывающаяся в организме недостаточность мелатонина может быть одной из причин повышенной генерации в мозговой ткани свободных радикалов, которая неизменно сопутствует эпилептическому процессу. Длительное применение противосудорожных препаратов повышает образование свободных радикалов, что ведет к оксидантному стрессу с последующей гибелью нейронов. Повышение концентрации свободных радикалов само по себе ведет к прогрессированию заболевания (дегенерация нейронов в результате перекисного окисления липидов и снижения синтеза глутатиона в эпилептическом очаге). С учетом описанных антистрессовых и антиоксидантных возможностей мелатонина становится понятной необходимость его применения у этих пациентов. Мелатонин необходимо добавлять к базисной противосудорожной терапии и в связи с наличием у него нейропротективных свойств как ингибитора глутаматных рецепторов и активатора ГАМК-рецепторов.
Паркинсонизм
При болезни Паркинсона ночная секреция мелатонина значительно снижается. У больных паркинсонизмом применяли мелатонин в рамках комплексной терапии. Выявлены улучшение ночного сна, повышение уровня дневного бодрствования и снижение уровня дневной сонливости, а также некоторое повышение двигательных возможностей и снижение уровня депрессии.
Болезнь Альцгеймера
Показано, что при болезни Альцгеймера ночная секреция мелатонина резко снижается. Ряд исследований позволяет предположить позитивное влияние мелатонина (в рамках комплексной терапии этих пациентов) на хронобиологические расстройства, такие как инверсия цикла «сон-бодрствование». Нарушение чувствительности МТ1-типа мелатонинергических рецепторов, возможно, участвует в снижении секреции таких нейропептидов, как вазопрессин и вазоинтестинальный пептид в центральной нервной системе при болезни Альцгеймера.
Фибромиалгия
Клиническая картина фибромиалгии складывается из мышечных болей, депрессии и инсомнии. Проведено изучение действия ежевечернего приема 1,5 мг мелатонина (Мелаксен) в течение 10 дней на субъективную
оценку качества ночного сна и его объективные характеристики у 11 больных фибромиалгией (А.М.Вейн, Я.И.Левин, И.Г.Ханунов, 1998-2000). Полисомнография подтвердила нарушения ночного сна в виде затрудненного засыпания, удлинения латентного периода поверхностного и парадоксального сна, подавления глубокого сна, уменьшения количества завершенных циклов сна, увеличения периодов бодрствования и движений во сне и т.д. После завершения курса лечения отмечалось субъективное улучшение сна, подтвержденное полиграфической регистрацией: облегчение засыпания, укорочение периодов бодрствования внутри сна и т.д. Отмечались также улучшение самочувствия, снижение уровня депрессии и улучшение тонкой моторики рук в дневное время. Сделан вывод, что мелатонин оказывает положительное влияние на качество сна при его нарушениях. У этих же пациентов несколько снизился уровень боли и депрессия.
Заключение
С учетом описанного многообразия биологических эффектов мелатонина ясно, что далеко не все его возможности активно используются в современной неврологии и его перспективы представляются оптимистичными.
Индекс лекарственных препаратов:
Список использованной литературы
Мелатонин: Мелаксен (ЮНИФАРМ, Инк.)
Комментарии
ПРАКТИКА ПЕДИАТРА
