Адаптогеннное действие ноотропных лекарственных средств при экспериментальном стрессе у животных
СтатьиВ.И. Ахапкина
Департамент экспериментальной и клинической фармакологии ОАО “Отечественные лекарства”, Москва
Многолетний опыт исследований и практического применения ноотропных препаратов в экстремальных условиях позволяет нам считать, что эта группа лекарственных средств наиболее полно отвечает требованиям, предъявляемых к нейротропным препаратам при их применении в осложненных условиях профессиональной деятельности человека.
Широкий спектр показаний к клиническому применению, чрезвычайно низкая токсичность и отсутствие отрицательных побочных эффектов делают ноотропные средства весьма привлекательными для применения в специальных областях медицины.
На молекулярном уровне препараты указанного типа оказывают в основном антигипоксическое и эрготропное (активизация энергетического обмена в клетках мозга) действие, с которым связаны их ноотропный (улучшение интеллектуально-мнестических функций), актопротекторный (повышение выносливости к физическим нагрузкам) и дезинтоксицирующий эффекты. На нейрональном уровне реализуются стимулирующее, депримирующее или нейростабилизирующее действие ноотропных препаратов, что может проявляться психостимулирующим, транквилизирующим, противосудорожным, противоукачивающим, эугипнотическим и другими эффектами.
Сочетание антигипоксического и эрготропного действия с одним или несколькими нейро-и психотропными эффектами значительно расширяет область применения представителей данного класса лекарственных средств. В практике экстремальной медицины ноотропные препараты полимодального действия используют как в качестве средств медикаментозной терапии при возникновении функциональных расстройств и заболеваний, так и с целью фармакологической коррекции утомления. Исходя из представлений о ведущей роли центральной нервной системы в регуляции адаптивной деятельности и учитывая специфические фармакологические свойства ноотропных препаратов, можно предположить, что их применение способно оказывать не просто стрессопротекторный, а именно адаптогенный эффект.
Задачей проведенного нами исследования было сравнительное изучение влияния ноотропных препаратов на стресс-реакцию у крыс.
Материалы и методы
Исследование проведено на 1050 крысах-самцах линии Вистар с массой тела 180–250 г; животные поступали из центрального питомника АМН “Столбовая”. До начала исследования животные адаптировались в течение 14 дней. В весенний период эксперименты не осуществлялись.
Была проведена сравнительная оценка 8 препаратов – Седуксена (диазепам), фенибута и его изомеров, Пантогама (гопантеновая кислота), Пиридитола (пиритинол), пирацетама и Фенотропила. Препараты вводились внутрибрюшинно один раз в сутки строго в одно и тоже время (± 5 минут). Исследования проводили двойным слепым методом. Контролем служили интактные крысы и животные, находившиеся в тех же экспериментальных условиях и получавших физиологический раствор (2 мл/100 г массы тела) или дистиллированную воду (1 мл/100 г массы тела).
Для оценки влияния препаратов на показатели стресс-реакции животных использовали три модели экспериментального стресса, получившие условные названия “болевого”, “эмоциогенного” и “антиортостатического” стресса [7, 8].
По окончании экспериментов животных забивали с помощью эфира и определяли массу тимуса, селезенки, надпочечников. Кроме того, исследовали желудок на наличие язв и геморрагических поражений [9].
На модели “антиортостатического” стресса определяли уровень кортизола в крови. В этой серии исследований животных забивали методом декапитации с помощью гильотины и забирали кровь для исследований.
Полученные результаты подвергали статистической обработке. Достоверность различий между сравниваемыми показателями оценивали с помощью t-критерия Стьюдента. За достоверные принимали различия на уровне значимости 95 % при р < 0,05.
Результаты и обсуждение
В условиях “болевого” стресса (иммобилизация с электрораздражением задних конечностей) защитное антистрессорное действие препаратов могло осуществляться за счет аналгезирующего или транквилизирующего эффектов. В ранее проведенных исследованиях на мышах нами было установлено, что ноотропные препараты повышают порог болевой чувствительности. Наибольший эффект оказывали фенибут и Фенотропил.
В условиях “эмоциогенного” стресса, у свободно перемещающихся на площадке с электродным полом попарно сгруппированных крыс для стимуляции использовали переменный ток, напряжение которого повышалось на 2 В каждые 15 секунд таким образом, чтобы поддерживать у животных состояние агрессии независимо от болевого порога. При применении этой методики возможность защитного антистрессорного действия препаратов за счет анальгезирующего эффекта была исключена, так как интенсивность электроболевого раздражения постоянно менялась, следуя за изменением эмоциональной реактивности животных. В результате 30-минутного сеанса раздражения у животных в течение 3 дней поддерживалась одинаковая степень эмоционального напряжения, проявляющегося в агрессии, направленной друг на друга.
При придании крысам антиортостатического положения с углом наклона головного конца -45° (антиортостатическая гипокинезия – АНОГ -45°) в течение 3 суток в тесных клетках-пеналах возможность защитного антистрессорного действия за счет анальгезирующего эффекта также была исключена, так как при этом варианте стресса болевой фактор отсутствовал.
При всех трех моделях стресса у контрольных животных (получавших физиологический раствор либо дистиллированную воду) наблюдались однотипные изменения: уменьшалась масса тимуса, увеличивалась масса надпочечников, возникали язвы желудка.
Показателем эффективности препаратов служил “защитный индекс”, который вычислялся как разность между интегральным показателем поражения слизистой оболочки желудка в контрольной группе животных, принятым за единицу, и аналогичным показателем в группе животных, получавших препараты. Максимальный защитный индекс мог быть равен единице. Нулевое значение индекса указывало на отсутствие эффекта, а отрицательное значение – на усиление поражения желудка под влиянием исследуемого препарата.
Защитный индекс пирацетама (рис. 1) для моделей “болевого”, “эмоциогенного” и “антиортостатического” стресса составлял 0,65, 1,0 и 0,52 соответственно. Таким образом, наибольший защитный эффект пирацетам оказывал при “эмоциогенном” варианте стресса.
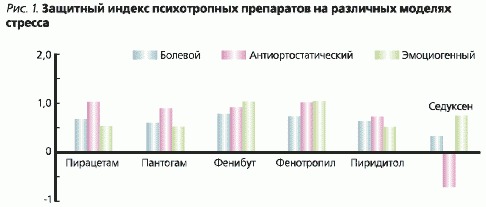
Пантогам по защитному эффекту приближался к пирацетаму (0,58, 0,87 и 0,50). Защитный индекс Пиридитола в моделях стресса был равен 0,62, 0,70 и 0,56; а у фенибута составлял 0,76, 0,89 и 0,99. Наибольшее защитное действие фенибут оказывал при “антиортостатическом” варианте стресса. Новый ноотропный препарат Фенотропил действовал аналогично фенибуту, но в более низких дозах. Его защитные индексы были равны 0,72, 0,99 и 1,0. Он полностью предупреждал нейрогенные поражения слизистой желудка при “антиортостатическом” варианте стресса и оказывал достаточно высокое защитное действие при “эмоциогенном” стрессе.
Защитный индекс Седуксена составлял при “болевом”, “эмоциогенном” и “антиортостатическом” вариантах стресса 0,31, -0,71 и 0,71 соответственно. Наибольший защитный эффект Седуксен оказывал при “антиортостатическом” стрессе [6], а на модели “эмоциогенного” стресса усугублял степень поражения слизистой оболочки желудка. Защитный эффект препарата выражался в уменьшении степени поражения слизистой оболочки желудка при иммобилизации в сочетании с ноцицептивным воздействием и при антиортостатической гипокинезии. В условиях “эмоциогенного” стресса, когда одним из экстремальных факторов становится физическая нагрузка, Седуксен усугублял выраженность деструктивных изменений в слизистой оболочке желудка. Причиной отсутствия защитного эффекта в последнем случае может быть центральное миорелаксирующее действие Седуксена, снижающее толерантность к физическим нагрузкам. Это совпадает с данными Г. Луханиной (1981 г.), в работах которой достаточно подробно изучалось влияние Седуксена на протекание стресс-реакции.
В условиях агрессивно-оборонительного поведения ноотропы проявляли однотипное защитное действие.
Защитное действие ноотропных препаратов в различных экстремальных условиях обусловлено, вероятно, сочетанием нейростабилизируюшего и адаптогенного эффектов, проявляющихся в предупреждении развития язв желудка при сохранении необходимого уровня активности нейрогуморальных механизмов адаптивной регуляции, обеспечивающих трофические функции нервной системы [1–3, 5].
На протяжении исследования масса тела животных во всех экспериментальных группах при АНОГ -45° достоверно снижалась, а в группе виварного контроля – несколько увеличивалась (табл.). Номера групп соответствовали исследуемым препаратам в следующем порядке: 1 – виварный контроль; 2 – контроль с физиологическим раствором; 3 – пирацетам 100 мг/кг; 4 – пирацетам 200 мг/кг; 5 – Фенотропил 25 мг/кг; 6 – Фенотропил 50 мг/кг; 7 – Фенотропил 100 мг/кг; 8 – фенибут 50 мг/кг; 9 – фенибут 100 мг/кг.
Таблица
Динамика массы тела крыс в 3-суточной АНОГ -45°
Группа |
До эксперимента, г |
Сутки эксперимента |
||
1 |
2 |
3 |
||
1 |
229,6 ± 3,8 |
235,1 ± 2,9 |
||
2 |
229,0 ± 3,6 |
201,0 ± 4,7 |
182,0 ± 4,3 |
160,0 ± 3,5 |
3 |
216,5 + 2,9 |
198,5 ± 2,7 |
177,8 ± 1,9 |
167,0 ± 2,4 |
4 |
224,5 ± 3,6 |
190,5 ± 3,2 |
173,0 ± 3,7 |
161,5 ± 3,5 |
5 |
230,0 ± 3,6 |
208,5 ± 4,7 |
183,5 ± 4,3 |
145,3 ± 1,4 |
6 |
234,5 ± 3,6 |
209,0 ± 4,7 |
196,0 ± 3,2 |
174,2 ± 3,4 |
7 |
236,5 ± 4,6 |
223,0 ± 4,5 |
208,0 ± 4,7 |
183,9 ± 3,6 |
8 |
232,4 ± 3,2 |
205,4 ± 4,7 |
188,0 ± 4,5 |
171,0 ± 2,3 |
9 |
229,0 ± 3,6 |
202,0 ± 4,7 |
187,0 ± 4,3 |
173,0 ± 3,7 |
Изучавшиеся ноотропные средства не предотвращали повышение уровня кортизола в крови по сравнению с виварным контролем, но достоверно снижали его по отношению к уровню кортизола в крови в группе животных, получивших только физиологический раствор (рис. 2).
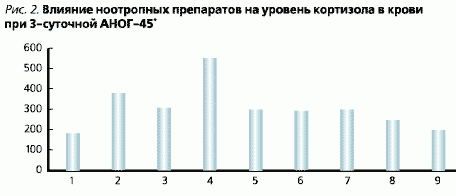
Согласно теории Г. Селье (1936 г.), под влиянием стресса активируется гипоталамус и продуцируются рилизинг-гормоны, стимулирующие синтез и высвобождение гормонов гипофиза (АКТГ, ТТГ и др.). Под влиянием АКТГ корковый слой надпочечников выделяет глюкокортикоиды, которые в больших количествах угнетают тимус и лимфатические узлы. В нашем исследовании также было отмечено значительное снижение массы тимуса у подвергнутых стрессу животных (рис. 3).
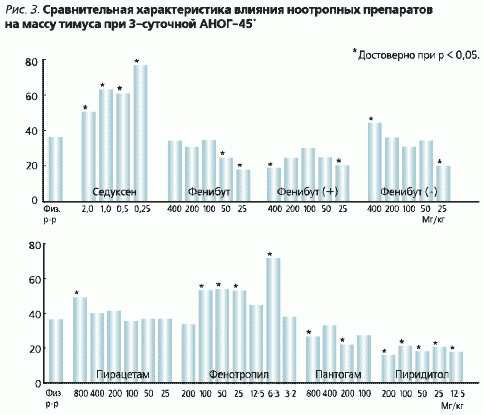
Фенибут предупреждал инволюцию тимуса только при “болевом” варианте стресса. В условиях АНОГ -45° он не влиял на массу этого органа, а его левовращающий изомер увеличивал массу тимуса на 7 % по сравнению с контрольной группой животных, получавших физиологический раствор. Пирацетам в дозе 800 мг/кг частично предотвращал инволюцию тимуса в условиях АНОГ (увеличение массы на 13,0 % по сравнению с контролем).
Наибольший эффект в условиях “антиортостатического” стресса оказал новый ноотропный препарат Фенотропил [*]. Он предотвращал в этой модели инволюцию тимуса в диапазоне доз от 6,3 до 100 мг/кг. Наибольший эффект препарат оказывал в дозе 6,3 мг/кг, предотвращая инволюцию тимуса на 36 % (рис.3).
Различным образом исследованные препараты влияли на массу селезенки, которая у животных, получавших физиологический контроль, уменьшалась на 34 % по сравнению с виварным контролем. Седуксен не предотвращал ее уменьшение по сравнению с физиологическим раствором (рис. 4). Фенибут увеличивал массу селезенки только в дозе 50 мг/кг (на 16 %). Фенибут (+) и фенибут (-) не влияли на уменьшение массы этого органа. Активность Фенотропила и Пантогама по этому показателю находилась на уровне фенибута. Пирацетам и Пиридитол в зависимости от дозы предотвращали инволюцию селезенки, а в дозе 25 мг/кг пирацетам увеличивал массу селезенки на 19 % по сравнению с виварным контролем.
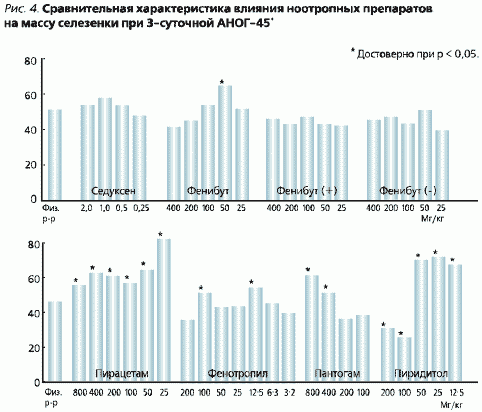
Данные о влиянии изучавшихся препаратов на гипертрофию надпочечников представлены на рис. 5. В условиях АНОГ эффект фенибута и его изомеров снижался с увеличением дозы. В дозе 25, 50 и 100 мг/кг фенибут снижал уровень гипертрофии надпочечников на 13, 32 и 9 % соответственно по сравнению с его уровнем у животных, получивших физиологический раствор. Фенибут (+) в дозах 50 и 100 мг/кг уменьшал этот показатель на 24 и 14 % соответственно. Фенибут (-) в этих дозах снижал уровень гипертрофии надпочечников на 19 %. Во всех остальных дозах он усиливал гипертрофию в среднем на 53 %. Пирацетам во всех дозах увеличивал гипертрофию надпочечников.
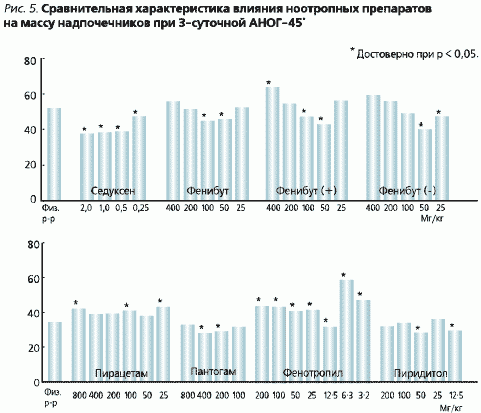
Седуксен полностью подавлял гипертрофию надпочечников. Особенность механизма действия Седуксена состоит в том, что не влияя на стабильные рефлексы, он угнетает образование нервных связей на начальных этапах формирования функциональной системы эмоционального регулирования в ответ на действие раздражителя. Не изменяя условно-рефлекторных реакций и восприятия сенсорных сигналов, Седуксен полностью подавляет тормозящие последствия эмоционального напряжения, улучшает точность условно-рефлекторного переключения [4]. В сравнении с другими транквилизаторами этот препарат характеризуется наибольшей универсальностью действия на вегетативные дисфункции центрального типа и вегетативные корреляты эмоционального стресса, не изменяя при этом адаптационные гемодинамические реакции (В.А. Белякова, 1980; Т.М. Высоковский, В.И. Куриленко, 1981).
Представленные в работе данные наглядно демонстрируют, что ноотропные препараты, обладающие различным спектром фармакологической активности, проявляют однотипное адаптогенное действие. В отличие от транквилизаторов они не подавляют ответ организма на стрессорное воздействие, а регулируют адекватность ответа на силу раздражителя, повышая тем самым устойчивость животных к стрессу. Адаптогенное действие ноотропных препаратов развивается уже после однократного применения. Эффект зависит от дозы. Необходимо также отметить, что к транквилизирующему или психостимулирующему компонентам действия ноотропных препаратов нельзя подходить исходя из общепринятых фармакологических и клинических принципов понимания этих эффектов. Это наглядно проявляется в действии фенибута, известного как транквилизатор, и Фенотропила, обладающего выраженным психостимулирующим компонентом действия. Однако оба препарата в зависимости от дозы и состояния организма проявляют как транквилизирующий, так и психостимулирующий эффект.
Есть основания предполагать, что адаптогенное действие ноотропных препаратов непосредственно связано с их ноотропным эффектом и может, по-видимому, рассматриваться в качестве одного из основных фармакологических тестов для этой группы лекарственных препаратов. Проведенные исследования позволяют разграничить понятия “стресс-протекторное” (антистрессорное) и “адаптогенное” действие. Подавление транквилизаторами ответа ЦНС на стресс-реакцию является классическим проявлением пассивной защиты, т. е. примером стресс-протекторного (антистрессорного) действия. Сохранение под влиянием ноотропных препаратов достаточного уровня мнестических функций мозга позволяет формировать “активную защиту” при стресс-воздействии, повышая тем самым устойчивость организма и его адаптационные возможности.
Адаптогенные эффекты Фенотропила являются дополнительным доказательством его ноотропных свойств, несмотря наличие у этого препарата выраженного психостимулирующего действия. Однако в отличие от психостимуляторов Фенотропил, как и другие классические ноотропы, способствует сохранению, а не истощению резервных возможностей организма при воздействии стресса и способен регулировать адекватность его реации в зависимости от силы стресса.
РЕФЕРАТ
В работе приведены результаты собственных экспериментальных исследований по оценке влияния ноотропных препаратов на показатели стресс-реакции у крыс на разных моделях стресса. Показано, что ноотропные препараты в отличие от классического стресс-протекторного препарата Седуксен не подавляют реакцию стресса, а оказывают адаптогенное действие, повышая устойчивость животных к экспериментальным воздействиям. Разграничиваются понятия “стресс-протекторного” и “адаптогенного” действия лекарственных препаратов.
ЛИТЕРАТУРА
- Ахапкина В.И. (Кaлоша В.И.), Станишевская А.В. и др. Всесоюзный съезд фармакологов // Тез. докл.: Ереван, 1982. С. 371–372.
- Ахапкина В.И..(Кaлоша В.И.), Полевой Л.Г. и др. VII Всесоюзная конференция по космич. биолог. и авиакосм. мед. // Тез. докл.: Калуга, 1982. С. 247.
- Ахапкина В.И. (Кaлоша В.И.), Полевой Л.Г. Биохимия, фармакология, медицинское применение производных витаминов и других предшественников коферментов: Сб. ст.: Иркутск, 1983, С. 194.
- Вальдман А.В., Козловская М.М., Медведев О.С. Фармакологическая регуляция эмоционального стресса. М., 1979. 358 с.
- Гончаров И.Б., Ахапкина В.И. XXIII Совещание постоянно действующей рабочей группы по космической биологии и медицине. Интеркосмос, Кошице, ЧСФР, 1990. С. 50.
- Зоря Л.В. Влияние седуксена на течение экспериментальной гипокинезии // Косм. биол. и авиакосм. мед. 1977. Т. 11. № 6. С. 68–73.
- Коваленко Е.А., Гуровский Р.Н. Гипокинезия. М., 1980. 320 с.
- Модели и методы изучения экспериментальных и эмоциональных стрессов. Волгоград, 1977. 130 с.
- Селье Г. Очерки об адаптационном синдроме. М., 1960. 253 с.
[*] Препарат запатентован в Российской Федерации в качестве ноотропного и антидепрессивного лекарственного средства, товарный знак ФЕНОТРОПИЛ (PHENOTROPIL) зарегистрирован в Российской Федерации и за рубежом.
Комментарии
ПРАКТИКА ПЕДИАТРА
