Доказательная медицина и ее применение в пульмонологии (диагностика и лечение бронхиальной астмы)
СтатьиОпубликовано в журнале:
Качественная клиническая практика »» 2 / 2002
А.Н. Цой1, В.В. Архипов1, А.Г. Чучалин2
1 - ММА им. И.М. Сеченова, г. Москва
2 - НИИ Пульмонологии МЗ РФ, г. Москва
Выбор источников достоверной информации имеет решающее значение для эффективной медицинской деятельности на всех ее уровнях. Качество имеющейся в распоряжении специалиста информации особенно важно при принятии решения относительно каждого конкретного клинического случая, при создании медицинских стандартов и формуляров, а также общем планировании деятельности здравоохранения [12]. Предложенная в начале 90-х гг. концепция доказательной медицины подразумевает добросовестное, точное и осмысленное использование лучших результатов клинических исследований для выбора лечения конкретного больного [2]. Подобный подход позволяет уменьшить уровень врачебных ошибок, облегчить процесс принятия решения для практических врачей, администрации лечебных учреждений и юристов, а также снизить расходы на здравоохранение и претворять в жизнь крупные социально-ориентированные медицинские проекты и инициативы [2].
Прошло почти 10 лет после появления первого международного руководства по диагностике и лечению бронхиальной астмы (БА) [I]. Российские врачи уже в 1996 г. имели возможность познакомиться с этим документом и применять его в своей практике. Имеется опыт создания аналогичных стандартов по лечению БА, ориентированных на отечественные условия и особенности системы здравоохранения в нашей стране [4]. Можно констатировать, что работа с подобными руководствами заставляет нас во многом пересмотреть вопросы обучения и самообразования практических специалистов, стимулирует отказ от рутинных и недостаточно эффективных методов диагностики и лечения и, в конечном счете, повышает уровень медицинской помощи больным БА.
Стандарты и протоколы по клинической практике предназначены, главным образом, для врачей широкого профиля (терапевты поликлиник и стационаров, врачи скорой помощи) и посвящены наиболее общим вопросам диагностики и лечения. Поэтому для этих руководств характерны строго ограниченный объем теоретических сведений и отсутствие описаний редких форм заболевания и новых экспериментальных методов лечения. Но благодаря этому они выполняют свою основную функцию — предоставляют врачам необходимую и точную информацию, позволяют оптимизировать лечебный процесс и обеспечить одинаково высокое качество медицинской помощи в любом из лечебных учреждений.
Первые руководства по клинической практике [1,3] строились по принципу консенсуса группы специалистов, однако в наши дни этого подхода явно недостаточно. Современный врач нуждается в строго взвешенных рекомендациях, основанных на данных наиболее качественно выполненных клинических исследований. Поэтому применение методов доказательной медицины, и в частности рейтинговой системы рекомендаций, на наш взгляд, более перспективно при подготовке будущих руководств по клинической практике и в дальнейшем обещает стать стандартом при подготовке подобных документов.
Цель настоящего обзора — ознакомить практических врачей с результатами использования концепции доказательной медицины на примере рекомендаций по лечению больных БА. При этом обоснование каждой из рекомендаций проводится с учетом уровня доказательности в соответствии с системой, принятой в доказательной медицине.
Уровень доказательности. Удобным механизмом, который позволяет каждому специалисту легко оценить качество каждого клинического исследования и достоверность полученных данных, является предложенная в начале 90-х гг. рейтинговая система оценки клинических исследований. Для непосредственной оценки исследования используются понятия — уровень доказательности. Обычно выделяют от 3 до 7 уровней доказательности [19], при этом с возрастанием порядкового номера уровня (обозначается латинскими числами) качество клинического исследования снижается, а результаты представляются менее достоверными или имеют только ориентировочное значение [II].
К I уровню в доказательной медицине принято относить хорошо разработанные, крупные, рандомизированные, двойные слепые, плацебоконтролируемые исследования. К этому же уровню доказательности принято относить данные, полученные в ходе мета-анализа нескольких рандомизированных, контролируемых исследований [2].
Небольшие рандомизированные и контролируемые исследования (в том случае, когда получить статистически корректные результаты, не удалось из-за малого числа больных, включенных в исследование) относят ко II уровню доказательности, а исследования «случай-контроль» или когортные исследования — к II или III уровню. Наконец, данные, содержащиеся в отчетах экспертных групп или консенсусах специалистов, принято относить к III или IV уровню [2].
В зависимости от мнения составителей (национальные общества доказательной медицины, общества специалистов) одно и то же исследование в различных рейтингах может относиться к разным уровням, однако общий порядок распределения исследований — практически везде одинаков. Так, в каждом из этих рейтингов первое место принадлежит крупным, рандомизированным, двойным слепым, плацебоконтролируемым исследованиям (как наиболее достоверным источникам информации), а завершается каждый рейтинг мнениями отдельных специалистов и данными крупных руководств по клинической практике.
В системе доказательной медицины отдельные практические рекомендации по диагностике и лечению различных заболеваний также имеют свой рейтинг — степень убедительности рекомендаций (обозначаются латинскими буквами). Система рейтинга рекомендаций в англоязычной литературе обозначается как сила рекомендаций (Strength of recommendation). При этом рекомендации, вытекающие из исследований I уровня, обозначаются как А, II уровня — В и т.д. Кроме того, к рекомендациям В относятся экстраполяции из исследований I категории доказательности, а рекомендации С строятся как на основании исследований III уровня доказательности, так и на экстраполяции данных исследований I и II уровня. Таким образом, рекомендации уровня А представляются вполне убедительными, так как опираются на веские доказательства, у рекомендаций уровня В — убедительность относительная, а для рекомендаций уровня С имеющихся доказательств недостаточно, но и эти рекомендации могут использоваться с учетом определенных обстоятельств. Положения, относимые к уровню D и Е, представляются доказанными недостаточно [2, II].
В настоящем обзоре была принята система оценки клинических исследований Canadian asthma consensus report (1999) [8]. При присвоении отдельным рекомендациям того или иного рейтингового уровня авторы опирались на мнение экспертов Великобритании и Канады [7, 18, 25].
Рекомендации по диагностике, оценке состояния больных и лечению бронхиальной астмы
Общие принципы лечения бронхиальной астмы в амбулаторных условиях
Бронхиальная астма характеризуется значительной вариабельностью тяжести течения. Поэтому для терапии бронхиальной астмы в конце 80-х гг. был предложен ступенчатый терапевтический подход, согласно которому каждой степени тяжести течения заболевания соответствует определенная схема лечения (рис. 1) [I].
Ступенчатый подход к лечению бронхиальной астмы
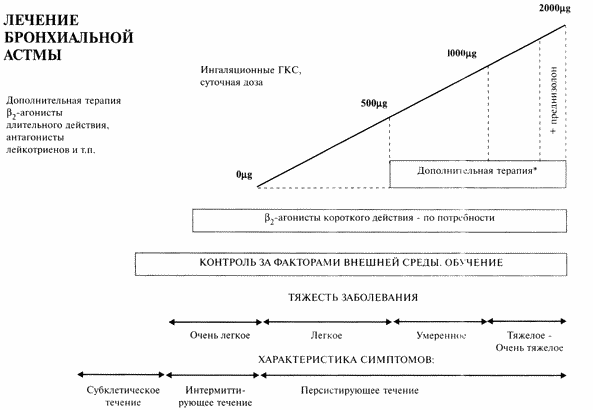
Первоначально было принято выделять четыре степени тяжести бронхиальной астмы (рис. 2) [ 1, 3]. Впоследствии показалось рациональным выделить группу больных с «очень тяжелым течением БА», т.е. тех, у кого адекватный контроль достигается только при применении пероральных глюкокортикостероидов (ГКС) [8]. К этой категории относят также пациентов с так называемой «трудной /тяжелой/ астмой» (аспириновый вариант астмы, ГКС-зависимая и ГКС-резистентная астма, лабильная астма) [10].
Общий алгоритм лечебного подхода к бронхиальной астме приведен на рис. 2. Он включает диагностический этап, выбор схемы первоначального лечения, подбор долговременной терапии заболевания и последующее наблюдение за больным. Так как бронхиальная астма является хроническим воспалительным заболеванием дыхательных путей [I], эффективность терапии оценивается не как полное излечение, а как адекватный контроль за течением заболевания, предотвращающий обострения ( табл. 1) [8]. Рис. 2
Алгоритм лечения бронхиальной астмы
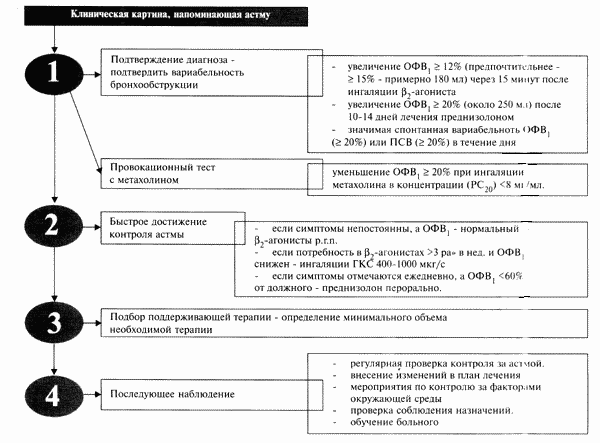
Диагностика и клиническая оценка бронхиальной астмы
Для подтверждения диагноза бронхиальной астмы и оценки тяжести состояния у всех больных с явлениями бронхообструктивного синдрома следует проводить исследование функции внешнего дыхания (С) [25]. К диагностическим критериям, специфичным для бронхиальной астмы, относятся (D) [1, 3]:
- - увеличение ОФВ1, >12% (предпочтительнее >15%, -т.е. примерно 180 мл) через 15 мин после ингаляции бета2-агониста;
- - увеличение ОФВ1 >20% (около 250 мл) после 10-14 дней лечения преднизолоном;
- - значимая спонтанная вариабельность ОФВ1.
При оценке ОФВ1, и ПСВ следует ориентироваться на среднестатистические нормы для данной популяции, а в идеале - на индивидуальный лучший показатель данного больного, измеренный в период стабильного состояния (С) [З].
Когда проведение спирометрии или бронхопрово-кационного теста недоступны, можно оценить вариа-бельный характер бронхообструкции (> 20%) при многодневном измерении ПСВ в домашних условиях, что также может указывать на наличие бронхиальной астмы (В) [8].
Для установления диагноза бронхиальной астмы используют бронхопровокационный тест с метахолином (С) [8].
Бронхиальная астма и факторы внешней среды
В целом, тяжесть симптомов астмы коррелирует со степенью чувствительности больного к аллергенам [I], хотя у целого ряда пациентов аллергия не играет ведущей роли в течении заболевания. Следует помнить, что увеличение объема медикаментозной терапии не должно заменять предотвращение контактна больного с аллергенами и ирритантами (С) [I].
Больным астмой также следует избегать контакта с табачным дымом (С) [1] и строго воздерживаться от курения (В) [25].
Больным с астмой следует избегать высокой концентрации ирритантов во вдыхаемом воздухе (С) [8], но до сих пор не имеется достаточных данных об эффективности применения для этих целей увлажнителей и других средств очистки воздуха (С) [8].
Все взрослые больные с первично возникшей астмой должны проходить обследования для исключения профессионального характера заболевания (В) [5, 8].
Мониторинг и обучение больных бронхиальной астмой.
Обучение пациентов является обязательным компонентом лечения астмы (А) [З]. Целью обучения является контроль за течением заболевания и выбор правильного поведения больного в различных ситуациях, связанных с заболеванием. Программа обучения не должна строиться только на ознакомлении больных с соответствующей литературой (А), а обучение больных необходимо проводить при каждом личном контакте медицинских работников с пациентами (В) [8], что требует хорошего контакта между медицинским работником и обучаемым (С) [З].
Таблица 1
Признаки контроля за течением астмы [8]
| Параметры | Их частота или характеристика |
| Дневные симптомы | < 4 дней в нед. |
| Ночные симптомы | < 1 ночи в нед. |
| Обострения | Легкие, редко |
| Физическая активность | Нормальная |
| Отсутствие на работе или учебе из-за заболевания | Нет |
| Потребность в бета2-агонистах короткого действия | < 4 доз в нед. |
| Величина ОФВ1 или ПСВ | > 85% от индивидуального лучшего показателя |
| Дневные вариации ПСВ* | < 15% |
Примечание:
Величина ОФВ1 - объем форсированного выдоха за 1 сек. ПСВ — пиковая скорость на выдохе.
*-(ПСВmax-ПСВmin)*100%/ПСВmax
Наиболее удобными и информативными средствами контроля за эффективностью лечения является наблюдение за функцией внешнего дыхания (спирогра-фия и пикфлоуметрия) (А) и определение потребности в бронхолитиках (А) [2, 15] в том случае, если пациент ежедневно фиксирует показатели ПСВ и симптомы своего заболевания в виде дневника (А) [8]. Постоянный мониторинг ПСВ может быть полезен у некоторых пациентов, особенно у больных со сниженным восприятием бронхообструкции (С) [8].
Для улучшения контроля за заболеванием для каждого пациента должен составляться письменный индивидуальный план лечения, основанный на самооценке симптомов (В) [З].
Иммунотерапия В общем случае проведение иммунотерапии не может быть рекомендовано для лечения бронхиальной астмы (В) [8]. Она не должна заменять проведение гипоаллергенного режима (С). Возможность иммунотерапии может рассматриваться в тех случаях, когда предотвращение контакта с аллергеном и фармакотерапия не приводят к адекватному контролю за активностью заболевания (А). Хорошо контролируемая астма не является противопоказанием к проведению иммунотерапии по поводу аллергического риноконъюнктивита и гиперчувствительности к яду насекомых (С) [8].
Ингаляционные ГКС
Ингаляционные ГКС эффективны при лечении БА (А) [5] и могут способствовать сокращению применения системных ГКС у больных с ГКС-зависимым течением БА (А) [7]. Назначение ингаляционных ГКС больным БА позволяет увеличить величину ПСВ и уменьшить потребность в бронхолитиках (А) [б]. Лучший уровень контроля за течением БА быстрее достигается при использовании более высоких доз ингаляционных ГКС (А) [б]. Позднее начало лечения ингаляционными ГКС в последующем бывает связано с более низкими результатами функциональных тестов (С) [8].
Все препараты из группы ингаляционных ГКС в эквивалентных дозах обладают одинаковой эффективностью (А) [З]. В проведенных исследованиях была доказана высокая эффективность ингаляционных ГКС при назначении два раза в день. При применении ГКС четыре раза в день эффективность лечения незначительно возрастает по сравнению с назначением той же дозы дважды в день (А) [7].
Ингаляционные ГКС следует рекомендовать тем больным, у которых обычная потребность в применении бета2-агонистов короткого действия составляет 2 или 3 раза в день и более (А) [7]. Первоначальная дневная доза ингаляционных ГКС обычно составляет 400-1000 мкг (беклометазона), при более тяжелом течении бронхиальной астмы можно рекомендовать более высокие дозы ингаляционных ГКС или начать лечение системными ГКС (С) [7]. Стандартные дозы ингаляционных ГКС (эквивалентные 800 мкг беклометазона) при неэффективности могут быть увеличены до 2000 мкг в пересчете на беклометазон (А) [7].
Если при лечении ингаляционными ГКС достигнут положительный результат, дозу ГКС следует постепенно снижать до минимальной, обеспечивающей контроль за проявлениями астмы (С) [З]. Снижение доз ингаляционных ГКС следует осуществлять постепенно, уменьшая дозу на 25-50 % от исходной, после того как состояние больного остается устойчивым в течение 3 мес (С) [7].
При обострениях бронхиальной астмы следует увеличить дозу ингаляционных ГКС в 2-4 раза (D) [8] или назначить преднизолон в дозе 0,5-1,0 мг/кг/сут (А) [3, 17]. Повышенная доза ГКС должна поддерживаться в течение 10-14 дней (С) [18].
Существенные опасения больных вызывает безопасность применения ГКС. Между тем, ингаляционные ГКС в низких и средних дозах сравнительно редко вызывают клинически значимые нежелательные эффекты и обладают очень хорошим отношением риск/польза (А) [8].
Пациентам, наследственность которых отягощена появлением глаукомы, повышением внутриглазного давления, через 5 дней регулярного приема ингаляционных ГКС должны пройти обследование окулиста, которое в дальнейшем следует регулярно повторять (D) [8]. Взрослым пациентам, получающим > 1000 мкг/сут в пересчете на беклометазон дипропионат, показано проведение денситометрии, в том случае если у них имеются факторы риска остеопороза (С) [8].
Больные, регулярно принимающие ингаляционные ГКС, должны после ингаляций полоскать полость рта водой для предотвращения системной адсорбции препарата (А) [З]. Применение спейсера также снижает риск нежелательного действия ингаляционных ГКС (D) [1, З].
Бета2-агонисты короткого действия
Бета2-агонисты короткого действия являются наиболее эффективными бронхолитическими средствами для купирования симптомов бронхиальной астмы (А) и профилактики астмы физического усилия (А) [3, 22]. Хотя применение бета2-агонистов короткого действия приводит к эффективному увеличению величины ПСВ (А) [18], эти препараты не должны рекомендоваться для постоянного применения в качестве базисной терапии (А) [I]. Наличие у больного потребности в ежедневном приеме бета2-агонистов является показанием к назначению противовоспалительной терапии (А) [1, З].
Если у больного бронхоспазм провоцируется физической нагрузкой, то до выполнения физических упражнений рекомендуется применять бета2-агонисты короткого действия (А) [I]. Например, сальбутамол более эффективен для предотвращения бронхоспазма, вызванного физической нагрузкой, чем хромогликат натрия (А) [7].
Пероральные бронхолитики следует рассматривать как препараты второго ряда после ингаляционных бронхолитиков (С) [З].
Бета2-агонисты длительного действия
Применение бета2-агонистов длительного действия является альтернативой увеличения доз ингаляционных ГКС при недостаточном контроле за течением астмы [13, 23]. Эти лекарственные средства могут применяться в качестве дополнительной терапии при умеренном и тяжелом течении астмы (А) [3, 8]. Не рекомендуется применять бета2-агонисты длительного действия для купирования острых приступов астмы (за исключением формотерола) и применять эти лекарственные средства при отсутствии противовоспалительной терапии (В). На фоне применения бета2-агонистов длительного действия должен быть продолжен прием препаратов с коротким действием для купирования симптомов (В) [З].
У большинства больных, получавших сальметерол, удается достигнуть удовлетворительного контроля за течением БА при назначении его по 50 мкг дважды в сутки (В) [13]. Сальметерол вызывает значимую бронходилатацию в течение 12 ч; при назначении препарата в суточной дозе 100 мкг побочные эффекты не существенны, но при увеличении дозы их риск увеличивается (В) [13]. Применение сальметерола 2 раза в день более эффективно, чем использование препаратов короткого действия 4 раза в течение дня (А) [7]. Назначение сальметерола у больных с недостаточным контролем за течением БА может быть столь же эффективно, как увеличение дозы ингаляционных ГКС в 2 раза [23].
Антагонисты лейкотриеновых рецепторов
Антагонисты лейкотриеновых рецепторов (АЛТ) являются альтернативой увеличения доз ингаляционных ГКС при недостаточном контроле за течением астмы. Эти лекарственные средства могут применяться совместно со средними и высокими дозами ингаляционных ГКС (А) [З]. Недостаточно данных, которые позволили бы отнести АЛТ к числу противовоспалительных препаратов первого выбора у больных бронхиальной астмой, однако у пациентов, которые не могут принимать ГКС, АЛТ являются препаратами выбора (D) [8]. Другим показанием к назначению АЛТ является аспириновый вариант бронхиальной астмы (D) [8].
Дополнительная терапия
Препараты хрома. Кромогликат натрия и недокромил могут применяться как альтернатива бета2-агонистам для предотвращения астмы физического усилия (А) [З]. Не существует свидетельств, на основании которых можно предпочесть недокромил хромогликату натрия или наоборот (А) [I]. Хотя недокромил более эффективен, чем плацебо, однако степень его эффективности не позволяет рекомендовать препарат в качестве средства первого ряда лечения БА (А), тем не менее у детей младше 12 лет и взрослых с легким течением астмы он может являться альтернативой низким дозам ингаляционных ГКС, не обладая нежелательными эффектами ГКС (А).
Теофиллин. Теофиллин не должен применяться при бронхиальной астме в качестве препарата первого ряда
(А) [З]. У пациентов с течением астмы, при котором средние дозы ингаляционных ГКС неэффективны, добавление к теофиллина лечению ГКС может улучшить контроль за течением астмы и сократить потребность в ГКС (В) [I]. Дозу теофиллина следует увеличивать постепенно путем титрации (С) [I].
Антихолинэргические средства. Препараты этой группы не рекомендуются в качестве препаратов первого ряда для лечения бронхиальной астмы, за исключением случаев толерантности к действию бета2-агонистов (С) [8].
Кетотифен не рекомендуется для лечения бронхиальной астмы (В) [8].
Средства доставки
При лечении бронхиальной астмы ингаляционный путь доставки бронхолитиков и противовоспалительных препаратов является более предпочтительным, чем назначение этих лекарственных средств перорально или парентерально (А) [З]. В последние годы существенно расширился арсенал средств доставки ингаляционных препаратов. Условно принято выделять аэрозольный дозированный ингалятор (применяются со спейсером или без него), порошковые ингаляторы (турбухайлер, дискхайлер, циклохайлер и т.д.) и небулайзер. Существует алгоритм подбора больному адекватного средства доставки (С) [8]. Согласно этому алгоритму, первоначально больным астмой следует назначать лекарственные препараты в виде дозированных аэрозольных ингаляторов. Если при употреблении дозированных ингаляторов у больного возникают трудности, следует дополнительно применять спейсер большого объема (объем > 0,75 л). Если же и при использовании дозированного ингалятора со спейсером больной не справляется с техникой ингаляций или не может применять их в течение всего дня, то ему показано назначение препарата в виде порошкового ингалятора наиболее дешевой модели или дозированного аэрозольного ингалятора «легкое дыхание».
Аэрозольный ингалятор со спейсером показан для всех возрастных групп, у пожилых больных и детей можно применять аэрозольный ингалятор со спейсером, оснащенным лицевой маской (В). При использовании любой системы доставки ингаляционных препаратов необходимо периодически оценивать технику ингаляции и проводить обучение больных (А) [З].
Применение ингаляционных ГКС через спейсер позволяет уменьшить риск кандидоза полости рта (А) [б]. При обострении бронхиальной астмы использование спейсера большого объема является эффективной альтернативой применению небулайзера, при этом удается в несколько (до 7-14) раз уменьшить дозы бронхо-литических средств (А) [7]. Аэрозольные ингаляторы со
спейсером большого объема (>0,75 л) можно рекомендовать и при тяжелых обострениях астмы (А) [7].
Дозированные аэрозольные ингаляторы столь же эффективны, как порошковые ингаляторы (А), в том числе аутохаллер (А) [3, 21].
Лечение бронхиальной астмы в условиях стационара
Признаком нестабильного течения БА на всех ее стадиях является увеличение потребности в ингаляционных бета2-агонистах (С), более частое, чем обычно, появление симптомов бронхообструкции и уменьшение величины ПСВ (А) [2, 8].
Пациенты, у которых величины ОФВ1 и ПСВ, измеренные до начала лечения, меньше 40% от индивидуального лучшего показателя (ИЛП) или должных величин (ПСВ<100 л/мин и ОФВ,<1,0 л) нуждаются в госпитализации в стационар (А) [7].
КУПИРОВАНИЕ ОБОСТРЕНИЯ БРОНХИАЛЬНОЙ АСТМЫ В УСЛОВИЯХ ОТДЕЛЕНИЯ ИНТЕНСИВНОЙ ТЕРАПИИ.
- Дополнительная терапия кислородом показана больным с обострением бронхиальной астмы и должна проводиться до тех пор, пока уровень сатурации не превысит 94% (D). Измерение газов артериальной крови показано больным в критическом состоянии с признаками гиперкапнии и при снижении сатурации < 90% (D) [16].
- Бета2-агонисты короткого действия относятся к препаратам первого ряда для лечения обострении бронхиальной астмы. Эти препараты назначаются в виде ингаляций, а титрация дозы производится с учетом объективных и клинических признаков бронхообструкции (А). Бета2-агонисты не должны применятся внутривенно вместо ингаляций при лечении обострения БА (А), так как ингаляции сальбутамола более эффективны, чем его внутривенное назначение (А) [24]. Бронхолитики могут применяться парентерально в тех случаях обострении БА, когда назначение ингаляционных средств проблематично (например, при выраженном кашле) (С) [18].
- Выбор средства доставки (дозированный ингалятор, спейсер, небулайзер) зависит от характера проводимой терапии, доступности этих устройств и индивидуальных особенностей пациента (А). Применение аэрозольного ингалятора со спейсером большого объема более предпочтительно, чем использование небулайзера, независимо от возраста и тяжести состояния больного (А) [3, 21].
- Системные ГКС. Все больные, поступившие в стационар по скорой медицинской помощи с обострением БА, являются вероятными кандидатами для назначения системных глюкокортикостероидов (А) (см. также показания к назначению системных ГКС; табл. 2). При тяжелом обострении БА внутривенное и пероральное назначение ГКС демонстрирует одинаковую эффективность (А), поэтому при обострениях бронхиальной астмы следует использовать пероральные ГКС (А) [З]. Преднизолон назначается перорально в дозе 30-60 мг ежедневно до тех пор, пока не купируется обострение и течение астмы не становится контролируемым, а показатели функции внешнего дыхания не возвращаются к исходным. Обычно бывает достаточным применение преднизолона в течение 7-14 дней, хотя лечение может быть продолжено до трех недель (С) [17]. Наибольший риск желудочно-кишечного кровотечения имеет место у больных, уже имевших в анамнезе кровотечения или применявших антикоагулянты (С) [25]. В том случае, если продолжительность лечения пероральными ГКС не превышала 2 нед., отменять их прием следует одномоментно (С) [8].
- Применение холинолитиков в сочетании с бета2-агонистами можно рекомендовать при обострениях астмы средней тяжести, они также могут оказаться эффективными при тяжелых обострениях БА (А) [9].
- Назначение теофиллина не показано в первые 4 часа пребывания пациента в стационаре (А) [7]. При лечении обострении бронхиальной астмы, резистентных к лечению, можно применять адреналин (внутримышечно и внутривенно) (В) [3, 18], сальбутамол (внутривенно), магния сульфат внутривенно (А), гелиокс (С) [16]. При экстренной интубации следует применять кетамин и сукцинилхолин (А) [16].
Таблица 2
Рекомендации Британского торакального общества по назначению системных ГКС при обострениях астмы (D) [25]
|
ЛЕЧЕНИЕ ОБОСТРЕНИЯ БРОНХИАЛЬНОЙ АСТМЫ В УСЛОВИЯХ СТАЦИОНАРА.
- Все больные, поступившие в стационар по скорой медицинской помощи с обострением БА, должны получать системные глюкокортикостероиды (А) [8, 25] (табл. 2). Всем пациентам показано назначение ингаляционных ГКС в дополнение к терапии системными ГКС (D) [7].
- Бета2-агонисты короткого действия должны назначаться в ингаляционной форме, выбор средства доставки (дозированный ингалятор, спейсер, небулайзер) зависит от характера проводимой терапии, доступности этих устройств и индивидуальных особенностей пациента (А) [3]. Применение аэрозольного ингалятора со спейсером большого объема более предпочтительно, чем использование небулайзера, благодаря быстрому ответу на лечение, простоте в титрации дозы и более эффективному использованию госпитального штата (А) [7].
- Холинолитики можно применять в сочетании с бета2-агонистами в течение 24-48 ч при тяжелых обострениях астмы и, возможно, при обострениях средней тяжести (А) [18].
- Оценка ответа на лечение и критерии выписки пациента из стационара должны базироваться на результатах серии исследований ФВД и уровне контроля за симптомами (С) [8].
- Пациенты с величиной ОФВ1 и ПСВ < 40% от индивидуального лучшего показателя, больные с гиперкапнией, отсутствием ответа на лечение или отрицательной динамикой состояния должны продолжать лечение в условиях отделения интенсивной терапии (D) [8].
- Обучение пациента, включая составление индивидуального плана лечения, должно происходить уже в период госпитализации (А) [8].
- После выписки из стационара пациенты должны продолжить прием системных ГКС (30-60 мг/сут) по крайней мере в течение 7-10 дней (А) (примечание: на Западе, как правило, продолжительность госпитализации не велика) [7].
- Пациенты, перенесшие тяжелое обострение бронхиальной астмы, должны быть осмотрены специалистом в период пребывания в стационаре или наблюдаться в амбулаторных условиях после выписки (D) [З].
- Пациенты, у которых уровень достиг ОФВ1 > 70% от должного, имеющие доступ к необходимым медикаментам, обладающие адекватной техникой ингаляции и получившие индивидуальный лечебный план, могут быть выписаны из стационара (D) [8].
Abstract
Asthma is an illness with many variations in cause and severity. Many treatment options are available to control and reverse asthma symptoms. What's the best treatment? It is important to provide more effective care for asthma from the point of view of evidence-based medicine. While the situations and outcomes varied-to some degree, the morbidity and resource utilization attributable to asthma can be strikingly reduced if moderate and severe asthmatics receive expert care
ЛИТЕРАТУРА
Комментарии
ПРАКТИКА ПЕДИАТРА
