Рандомизированное проспективное исследование лекарственного препарата Кудевита (коэнзима Q) в лечении пациентов с ишемической болезнью сердца с сердечной недостаточностью II—III функционального класса
СтатьиОпубликовано в журнале:
CONSILIUM MEDICUM | ТОМ 14 | № 1 | стр. 55-60
Д.М.Аронов1, Д.Г.Иоселиани2, В.Б.Красницкий1, Е.В.Ярных2, Т.В.Ковтун2 'ФГВУ ГНИЦ ПМ Минздравсоцразвития РФ
2Московский научно-практический центр интервенционной кардиоангиологии
Хроническая сердечная недостаточность (XCH), особенно у больных ишемической болезнью сердца (ИБС), является одной из основных причин инвалидизации и смерти. Лекарственная терапия препаратами основных групп с доказанной эффективностью, включающая |3-адреноблокаторы (БАБ), ингибиторы ангиотензинпревращающего фермента (ИАПФ), блокаторы рецепторов ангиотензина II (БРА) и диуретики, не позволяет решить эту проблему полностью или настолько, насколько ее хотелось бы решить нехирургическими методами. Поэтому в мире продолжается поиск новых лекарственных возможностей помощи таким больным.
Коэнзим Q10 - эндогенно образуемый субстрат, действующий как переносчик электронов в транспортной цепи митохондрий. Основная функция коэнзима Q10 в организме заключается в обеспечении достаточного энергообразования (аденозинтрифосфата) в митохондриях клеток для их нормального функционирования. Он является незаменимой частью дыхательного процесса в митохондриях [1]. Установлено, что при ХСН по мере снижения сократительной способности миокарда соответственно снижается уровень коэнзи-ма Q10. Степень тяжести сердечной недостаточности (СН) достоверно коррелирует со степенью снижения уровня коэнзима Q10 [2]. В то же время его концентрация в организме снижается с возрастом [1, 3]. У пожилых больных ИБС и ХСН суммация убыли коэнзима Q10 приводит к усугублению тяжести СН. В связи с этим логично предположить, что экзогенный коэнзим Q10, введенный извне, может оказаться полезным при лечении ХСН.
Настоящее исследование предпринято для изучения этого вопроса.
Исследование открытое рандомизированное контролируемое с формированием основной (исследуемой) и контрольной групп. Цель исследования - изучение клинической эффективности и безопасности применения препарата Кудевита у больных ИБС с СН II-III функциональных классов (ФК).
Задачи исследования:
1. Изучение терапевтическую эффективность Кудевиты у пациентов с СН, страдающих ИБС.
2. Изучить переносимость и возможные побочные эффекты исследуемого препарата;
3. Сравнить результаты лечения, полученные в основной и контрольной группах и оценить статистическую достоверность различий.
Материалы и методы
В исследование включены 40 пациентов, рандомизированных в основную (18 человек) и контрольную (20 человек) группы. Больные страдали ИБС и имели в анамнезе документированный инфаркт миокарда (ИМ), а также ХСН II—III ФК с фракцией выброса (ФВ) левого желудочка (ЛЖ) сердца менее 45% по данным ультразвукового исследования.
Демографическая и клиническая характеристики пациентов, включенных в исследование, представлены в табл. 1.
Таблица 1. Исходные данные: демографические и анамнестические данные, клинические характеристики и основные гемодинамические показатели пациентов, включенных в исследование
|
Показатель |
Основная группа (n=18) |
Контрольная группа(n=20) |
|
Число пациентов |
||
|
Пол м/ж |
14/4 |
18/2 |
|
Возраст, лет |
59,7±7,4 |
58,1±10,5 |
|
Индекс массы тела |
27,5±2,3 |
28,0±4,0 |
|
ИМ перенесенный |
17 (94,4%) |
20 (100%) |
|
QS-ИМ |
14 (77,8%) |
16 (80%) |
|
не трансмуральный Q-ИМ |
3 |
1 |
|
не Q-ИМ |
0 |
3 |
|
Артериальная гипертония |
10 (55,6%) |
14 (70%) |
|
Стенокардия стабильная |
10 (55,6%) |
8 (40%) |
|
ФК стенокардии |
2,3±0,5 |
2,1±0,3 |
|
II |
13 |
18 |
|
III |
5 |
2 |
|
САД ДАД ЧСС |
119±14 76±8 64±7 |
124±15 80±8 69±9 |
|
ФВ ЛЖ |
42±5 |
42,1±4,7 |
Примечание. В данной таблице все различия между группами оказались недостоверными. САД - систолическое артериальное давление; ДАД - диастолическое артериальное давление; ЧСС - частота сердечных сокращений.
Как видно из таблицы, группы исследуемых были идентичными.
Всем пациентам, включенным в исследование, в начале и в конце наблюдения были проведены электрокардиография (ЭКГ), эхокардиография (ЭхоКГ), 6-минутный нагрузочный тест, измерение АД и ЧСС, анализ крови и биохимические анализы крови на: аспартата-минотрансферазу, аланинаминотрансферазу, креати-нинкиназу, фракции липидов, глюкозу, мочевую кислоту, электролиты (натрий, калий, кальций), С-реактив-ный белок, церулоплазмин, натрийуретический пептид, коэнзим Q10, а также общую антиоксидантную активность. Проводилось анкетирование с целью оценки клинического состояния пациента (по шкале ШОКС) [4], качества жизни [5], а также опрос в процессе врачебного обследования по клинической симптоматике и поддерживающей терапии по основному заболеванию.
Пациенты основной группы принимали исследуемый препарат Кудевита в дозе 150 мг/сут: по 2 капсулы (60 мг) утром и 3 капсулы (90 мг) вечером для амбулаторного приема, пациенты контрольной группы, как и пациенты основной группы, получали стандартную терапию, показанную при данном заболевании. Длительность наблюдения составила 3 мес.
В процессе исследования не назначали препараты, влияющие на метаболизм миокарда, кардиопротекто-ры и антиоксиданты: (триметазидин, мельдоний, окси-метилэтилпиридина сукцинат, рибоксин, аденозин-трифосфат, кокарбоксилаза, витаминные и иные метаболические средства).
Статистические методы обработки результатов исследования
Анализ результатов настоящего исследования проведен с помощью пакета прикладных программ SAS (Statistical Analysis Systems, SAS Institute. USA). Для каждого показателя, измеряемого по количественной шкале, определяли интервал вариации (минимум и максимум), среднее групповое значение, среднее квадратичное отклонение, а также стандартную ошибку среднего. Для всех показателей, измеряемых по номинальной или ранговой шкале, оценивали соответствующие частоты выявления различных градаций в процентах. Изменение значений показателя или его динамику во времени рассчитывали попарно для каждого пациента в отдельности, затем вычисляли среднее значение в процентах по группе. Связи между количественными показателями оценивали по величине коэффициентов корреляции Пирсона, а достоверность корреляционных показателей - по соответствующим формулам для t-критерия Стьюдента для независимых выборок, а ранговых показателей - по х2 критерию Фишера.
Схема медикаментозной терапии больных представлена в табл. 2.
Таблица 2. Распределение медикаментозной терапии
|
Показатель |
В начале исследования |
Через 3 мес |
||||
|
Основная |
Контрольная |
Различия между группами |
Основная |
Контрольная |
Различия между группами |
|
|
Нитраты, % |
38,9 |
25 |
нд |
33,3 |
25 |
нд |
|
Изосорбида динитрат, % (мг/сут) |
16,7 (40) |
10 (60) |
нд |
11,1 (40) |
10 (30) |
нд |
|
Изосорбида мононитрат, % (мг/сут) |
22,2 (30) |
15 (57) |
нд |
22,2 (35) |
15 (60) |
нд |
|
БАБ, % |
94,1 |
100 |
нд |
100 |
100 |
нд |
|
Метопролол, % (мг/сут) |
11,8 (75) |
10 (50) |
нд |
11,8 (75) |
10 (50) |
нд |
|
Бисопролол, % (мг/сут) |
47,1 (4,4) |
50 (4,5) |
нд |
58,8 (4,3) |
50 (4,5) |
нд |
|
Карведилол, % (мг/сут) |
29,4 (15) |
30 (20,8) |
нд |
23,5 (12,5) |
25 (20) |
нд |
|
ИАПФ, % |
88,2 |
100 |
нд |
100 |
100 |
нд |
|
Эналаприл, % (мг/сут) |
11,8 (7,5) |
35 (8,2) |
нд |
17,6 (7,5) |
35 (9,6) |
нд |
|
Периндоприл, % (мг/сут) |
70,6 (3,7) |
60 (4,4) |
нд |
76,5 (3,7) |
60 (4,4) |
нд |
|
Фозиноприл, % (мг/сут) |
5,9 (2,5) |
5 (10) |
нд |
5,9 (2,5) |
5 (10) |
нд |
|
Антиагреганты, % |
100 |
100 |
нд |
100 |
100 |
нд |
|
АСК, % (мг/сут) |
93,8 (101,7) |
100 (95) |
нд |
93,8 (101,7) |
100 (95) |
нд |
|
Клопидогрел, % (мг/сут) |
6,3 (75) |
10 (75) |
нд |
6,3 (75) |
10 (75) |
нд |
|
Тиклопидин, % (мг/сут) |
6,3 (500) |
0 |
нд |
6,3 (500) |
0 |
нд |
|
Статины, % |
100 |
90 |
нд |
100 |
100 |
нд |
|
Симвастатин, % (мг/сут) |
43,8 (14,3) |
45 (15,6) |
нд |
43,8 (14,3) |
55 (14,5) |
нд |
|
Аторвастатин, % (мг/сут) |
56,3 (16,7) |
45 (13,3) |
нд |
56,3 (16,7) |
45 (13,3) |
нд |
Примечание. АСК - ацетилсалициловая кислота; здесь и в табл. 3-7: нд - недостоверно. Значение суточной дозы (мг/сут) представлено каксреднее значение по группе.
Как видно из таблицы, проводимая медикаментозная терапия в двух группах была одинаковой и полноценной.
Результаты исследований
При анализе динамики объективных показателей были выявлены следующие изменения. Амплитудные и временные параметры ЭКГ в обеих группах не изменились, за исключением числа отведений, в которых был зафиксирован отрицательный зубец Т (табл. 3). Этот показатель достоверно (р<0,05) уменьшился в основной группе, причем разница в динамике этого показателя оказалась в такой же мере достоверной и при межгрупповом сравнении. Интерпретировать этот результат можно как возможное следствие положительного влияния лечения исследуемым препаратом на метаболизм миокарда и функционирование дыхательной цепи митохондрий кардиомиоцитов, в частности.
Таблица 3. Параметры электрокардиограммы
|
Показатель |
В начале исследования |
Через 3 мес |
||||
|
Основная M±a |
Контрольная M±a |
Различия между группами |
Основная M±a (Д; р) |
Контрольная M± a (Д; р) |
Различия между группами (Д; р) |
|
|
Длительность P-QR, с |
0,15±0,03 |
0,16±0,02 |
нд |
0,16±0,03 |
0,16±0,03 |
нд |
|
Длительность QRS, с |
0,08±0,02 |
0,08±0,02 |
нд |
0,08±0,02 |
0,08±0,02 |
нд |
|
Длительность Q-T, с |
0,38±0,04 |
0,39±0,04 |
нд |
0,38±0,04 |
0,38±0,03 |
нд |
|
Длительность Q-Ткорр., с |
0,38±0,04 |
0,39±0,03 |
нд |
0,39±0,03 |
0,39±0,03 |
нд |
|
ЧСС, уд/мин |
65±11 |
68±14 |
нд |
65±11 |
68±8 |
нд |
|
Патологический Q, число отведений* |
2,9±1,4 |
2,5±1,4 |
нд |
3,0±1,6 |
2,5±1,5 |
нд |
|
Элевация ST, мм* |
0,6±1,0 |
1,0±1,3 |
нд |
0,5±0,9 |
1,0±1,5 |
нд |
|
Элевация ST, число отведений* |
1,1±1,6 |
1,6±2,0 |
нд |
1,0±1,5 |
1,3±1,7 |
нд |
|
Депрессия ST, мм* |
0,3±0,5 |
0,2±0,4 |
нд |
0,1±0,4 |
0,2±0,4 |
нд |
|
Депрессия ST, число отведений* |
0,5±1,2 |
0,4±0,8 |
нд |
0,4±1,2 |
0,3±0,6 |
нд |
|
Отрицательный зубец T, число отведений* |
3,0±2,2 |
3,1±2,2 |
нд |
2,4±2,0 (-0,6; *) |
3,2±2,2 |
<0,05 |
|
Блокада ножек пучка Гиса, общее число случаев* |
0,18±0,4 |
0,15±0,4 |
нд |
0,18±0,4 |
0,2±0,4 |
нд |
Примечание. Здесь и далее в табл. 4-7: р<0,05; *- в среднем по группе, в том числе, если признак отсутствует (0).
Очень важным функциональным параметром организма является физическая работоспособность. По результатам пробы с 6-минутной ходьбой в основной группе наблюдался достоверный прирост пройденного расстояния на 14%, хотя при межгрупповом сравнении и не достигший степени достоверности (табл. 4). При качественном анализе пробы (увеличение/уменьшение пройденного расстояния) через 3 мес достоверная разница в пользу основной группы была выявлена как при межгрупповом сравнении, так и при раздельном подсчете: увеличение пройденного расстояния в основной и контрольной группах произошло, соответственно, у 89% против 55% пациентов, и уменьшение -у 5,6% против 40% (р<0,05) (см. рисунок). По результатам пробы в динамике в основной группе в отличие от контрольной достоверно уменьшилась доля пациентов, у которых в конце нагрузки наблюдалась выраженная одышка: с 56 до 33% (р<0,05), и эта динамика также была достоверной при межгрупповом сравнении. Примечательно, что в основной группе через 3 мес лечения на старте (в покое) достоверно уменьшился показатель гемодинамической нагрузки: ЧСС - на 4% (р<0,05). В конце пробы выявлено снижение ДАД на 7 мм рт. ст. (р<0,05) по сравнению с контрольной группой. Таким образом, в целом по результату 6-минутного теста работоспособность в основной группе улучшилась.
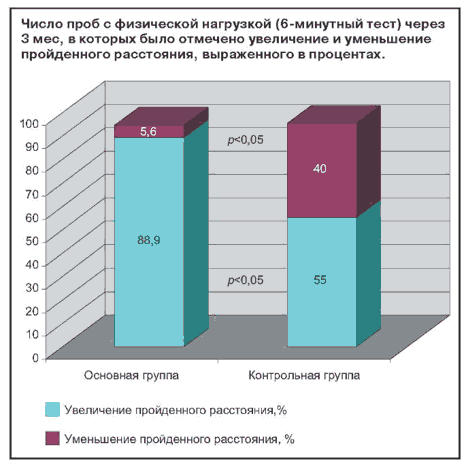
Таблица 4. Изменения показателей 6-минутного теста ходьбы
|
|
В начале исследования |
Через 3 мес |
||||
|
Показатель |
Основная M±a |
Контрольная M±a |
Различия между группами |
Основная M±a (Д%; р) |
Контрольная M±a (Д%; р) |
Различия между группами (по Д; р) |
|
Пройденное расстояние, м |
394±98 |
438±98 |
нд |
428±69 (13,9; *) |
452±85 |
нд |
|
Индекс пройденного расстояния (увеличение/уменьшение) в динамике |
- |
- |
- |
0,83±0,51 |
0,15±0,99 |
<0,05 |
|
Увеличение пройденного расстояния, % больных |
- |
- |
- |
88,9 |
55,0 |
<0,05 |
|
Уменьшение пройденного расстояния, % больных |
- |
- |
- |
5,6 |
40,0 |
<0,05 |
|
Появление выраженной усталости в конце пробы, % больных |
55,6 |
21,1 |
- |
33,3 (-40,1; *) |
31,6 |
<0,05 |
|
ЧСС на старте, уд/мин |
65±9 |
68±11 |
нд |
62±9 (-4,0; *) |
66±5 |
нд |
|
ДАД в конце пробы, мм рт. ст. |
84±13 |
84±6 |
нд |
79±7 |
86±5 |
<0,05 |
Таблица 5. Изменения ЭхоКГ-показателей
|
Показатель |
В начале исследования |
Через 3 мес |
||||
|
Основная M±a |
Контрольная M±a |
Различия между группами |
Основная M±a (Д%; р) |
Контрольная M±a (Д%; р) |
Различия между группами (по А; р) |
|
|
КСР ЛЖ, см |
4,7±0,6 |
4,7±0,4 |
нд |
4,6±0,7 (-1,9; *) |
4,7±0,4 |
нд |
|
КСО ЛЖ, мл |
107±35 |
105±21 |
нд |
102±38 (-4,3; *) |
101±19 |
нд |
|
ФВ ЛЖ, % |
42±5 |
42,1±4,7 |
нд |
43,5±5,5 (3,7; *) |
43,2±4,2 |
нд |
|
Градиент давления на уровне ПЖ/ПП, мм рт. ст. |
22,4±4,2 |
23,5±5 |
нд |
21,6±4,5 (-3,8; *) |
24±5,8 |
нд |
Примечание. КСО - конечный систолический объем; КСР - конечный систолический размер; ПЖ - правый желудочек; ПП - правое предсердие.
Данные лабораторных анализов в динамике представлены в табл. 6.
Таблица 6. Изменения лабораторных показателей
|
Показатель |
В начале исследования |
Через 3 мес |
||||
|
Основная M±a |
Контрольная M±a |
Различия между группами |
Основная M±a (Д%; р) |
Контрольная M±a (Д%; р) |
Различия между группами (по Д; р) |
|
|
ОХС/ХС ЛПВП |
5,2±1,5 |
4,3±1,4 |
нд |
4,5±1,5 (-11,7; *) |
4,4±1,5 |
р<0,05 |
|
Коэнзим Q10, нг/мл |
648±243 |
523±133 |
нд |
1749±1080 (193; **) |
684±464 |
р<0,05 |
|
Церулоплазмин, г/л |
42,7±5,5 |
41,3±4,3 |
нд |
39,6±6,3 (-7,1; *) |
39,9±9,9 |
нд |
**- р<0,001 при сравнении внутри группы.
Анализируя их, в первую очередь следует отметить достоверное увеличение концентрации коэнзима Q10 на 193% (р<0,001). Этот факт имеет важное клиническое значение, поскольку эффекты этого препарата связаны с его концентрацией в крови, подтверждает и достаточную приверженность пациентов лечению. В основной группе отмечена также достоверно лучшая динамика атерогенных фракций липидов крови по показателю коэффициента атерогенности: общего холестерина (ОХС) и холестерина липопротеидов высокой плотности (ХС ЛПВП). Его снижение составило 11,7% (р<0,05),в том числе при сравнении с контрольной группой (на фоне практически одинакового лечения статинами (см. табл. 2). Неоднозначной оказалась картина по динамике лабораторных критериев активности воспаления или повреждения клеток в основной группе, видимо, в связи с тем, что исходные их значения были низкими. Концентрация церуло-плазмина в группе леченных препаратом достоверно снизилась (на 7%; р<0,05). По данным лабораторных анализов можно утверждать, что в основной группе было зафиксировано улучшение липидного профиля, значительное повышение концентрации коэнзима Q10, снижение интенсивности перекисного окисления липидов. Кроме того, следует обратить внимание на то, что не возникло негативных изменений основных биохимических показателей, что объективно подтверждает безопасность исследуемого препарата.
По данным анкетирования (шкала ШОКС и вопросник по качеству жизни) в обеих группах не было выявлено изменений (табл. 7). Клинический опрос, наоборот, выявил положительную динамику в основной группе по частоте приступов боли в груди, в том числе при физической нагрузке, по ее выраженности, а также по частоте приема таблеток нитроглицерина. Исходно боли в груди у больных основной группы возникали достоверно чаще, а в конце лечения по частоте их возникновения группы сравнялись. При этом снижение частоты болей в груди в основной группе было достоверным, а также - при сравнении с таковым показателем контрольной группы.
Таблица 7. Данные анкетирования и опроса
|
|
В начале исследования |
Через 3 мес |
||||
|
Показатель |
Основная M±a |
Контрольная M±a |
Различия между группами |
Основная M±a (Д%; р) |
Контрольная M±a^%; р) |
Различия между группами (по Д; р) |
|
Шкала ШОКС |
2,3±0,8 |
3,0±1,2 |
нд |
2,2±0,6 |
2,9±1,2 |
нд |
|
Качество жизни (по Д.М.Аронову), ед |
-5,7±4,6 |
-7,5±4,2 |
нд |
-5,6±4,5 |
-7,5±4,5 |
нд |
|
Количество приступов боли в груди в неделю |
4,9±6,9 |
1,3±2,3 |
р<0,05 |
1,1±2,2 (-77,4;*) |
0,9±1,9 |
р<0,05 |
|
Количество приступов боли в груди при физической нагрузке в неделю |
3,4±5,8 |
1,2±2,0 |
нд |
0,8±1,6 (-73,5;*) |
0,7±1,6 |
нд |
|
Через сколько метров при ходьбе возникает боль |
537±279 |
317±207 |
нд |
677±333 (28,3;*) |
400±324 |
нд |
|
Количество таблеток нитроглицерина, принимаемых в неделю |
3,3±3,8 |
1,1±1,6 |
нд |
0,8±1,7 (-75,8;*) |
0,7±1,3 |
нд |
Переносимость препарата Кудевита оценивали на основании субъективных жалоб пациента и объективных данных, полученных в процессе лечения. Учитывалась динамика лабораторных показателей, а также частота возникновения и характер побочных явлений.
Факт хорошей приверженности лечению исследуемым препаратом подтверждался данными лабораторного анализа крови - увеличением концентрации коэнзима Q10. Переносимость препарата оценивали по объективным и субъективным данным.
У пациентов основной группы по воздействию препарата Кудевита на показатели периферической крови, включая число эозинофилов, печеночные ферменты и креатинфосфокиназу, а также на уровни глюкозы крови, мочевой кислоты, электролиты крови не отмечалось нежелательных побочных эффектов, а переносимость его была хорошей. Двое пациентов из основной группы выбыли из исследования по немедицинским причинам.
Обсуждение
Как видно из представленных данных, лечение больных ХСН на фоне ИБС и перенесенного ИМ оказало за относительно небольшой отрезок времени (3 мес) существенное влияние на состояние сердечно-сосудистой системы. Речь идет о лечении больных, которые находятся на поликлиническом наблюдении и, как это видно из табл. 2, получают полноценную терапию, соответствующую современным рекомендациям по лечению ХСН. Напомним, что больные обеих групп наблюдения получали интенсивную медикаментозную терапию по поводу ХСН и ИБС. Так, 94,1% больных основной группы и все больные контрольной группы получали БАБ, 88,2 и 100% больных соответственно ИАПФ. В обеих группах почти все получали АСК, 6,3 и 10% больных в соответствующих группах принимали кло-пидогрел; 39 и 25% больных в соответствующих группах - пролонгированные нитраты. На фоне такой комплексной и современной терапии, казалось бы, остается мало возможностей для дальнейшего улучшения состояния больных. Тем более что у больных были идеальные значения содержания С-реактивного белка (0,3±0,3 мг/л в 1-й и 0,4±0,8 мг/л во 2-й группе). И, тем не менее, улучшение состояния оказалось возможным. Оно выразилось в первую очередь в улучшении показателей физической работоспособности и результатов повторной пробы с 6-минутной ходьбой. Подобные результаты при применении коэнзима Q10 у больных СН отмечали авторы ранее опубликованных работ [6-8]. Увеличение расстояния, проходимого больными через 3 мес приема коэнзима Q10, сопровождалось значительным уменьшением числа приступов стенокардии и вынужденно принимаемых таблеток нитроглицерина. Можно полагать, что снижение приступов стенокардии связано с улучшением функции эндотелия, как это было выявлено в исследовании G.Watts [9].
Следует обратить внимание и на достаточно выраженное снижение ДАД (на 5 мм. рт. ст.). Гипотензивный эффект под влиянием коэнзима Q10 наблюдали и другие авторы [10, 11]. Следует обратить внимание и на признаки обратного развития моделирования сердца, выразившиеся в слабом, но достоверном уменьшении КСР и КСО ЛЖ, повышении ФВ ЛЖ сердца.
И, наконец, необходимо отметить улучшение окислительно-восстановительного статуса больных. Концентрация коэнзима Q10 - самого активного и естественного антиоксиданта возросла у больных на 193%, что сопровождалось достоверным снижением уровня прооксиданта церулоплазмина. Коэнзим Q10 является признанным антиоксидантом, содержание которого снижается в организме с возрастом [1, 3], с нарастанием явлений ХСН [2, 6, 8] и при приеме статинов [13, 14].
Следует отметить хорошую переносимость и безопасность препарата Кудевита, подтвержденную и другими исследователями [6-8], в том числе при назначении добровольцам значительно больших доз - 600 и
900 мг/сут [15].
Выводы
- Препарат Кудевита (ООО «ПИК-ФАРМА») при применении в составе комплексной терапии у больных ИБС с сердечной недостаточностью II-III ФК способствует достоверному улучшению:
- - физической работоспособности;
- сократительной функции сердца и гемодинамики по данным УЗИ, улучшению картины ЭКГ, указывающей на положительные сдвиги в метаболизме миокарда;
- липидного профиля плазмы крови;
- уменьшению количества и выраженности приступов боли в груди, уменьшению частоты приема нитроглицерина. - Кудевита достоверно снижает ДАД.
- Лечение препаратом Кудевита в течение 3 мес больных с данной патологией не сопровождалось негативными сдвигами параметров ЭКГ, а также биохимических маркеров активности воспаления и повреждения клеток по данным лабораторных анализов.
- Препарат Кудевита может быть рекомендован для применения в терапии больных c СН II-III ФК, страдающих ИБС.
Литература
1. Lenaz G, D'Aurelio M, Merlo PM et al. Mitochondrial bioener-getics in aging Biochim. Biophys. Acta 2000; 1459 (2-3): 3997-4042.
2. Mortensen SA Overview of coenzyme Q10as adjunctive therapy in chronic heart failure. Rationale, design and end-points of Q-symbio- a multinational trial. Biofactors 2003; 18: 79-89.
3. Ishii N, Senoo-Matsuda N, Miyake K et al. Coenzyme Q10 can prolong C. elegans lifespan by lowering oxidative stress. Mech AgeingDev 2004; 125 (l): 41-6.
4. Беленков ЮН, Мареев ВЮ, Агеев Ф.Т. Медикаментозные пути улучшения прогноза больных хронической сердечной недостаточностью. М.: Инсайт, 19975. Аронов ДМ, Зайцев ВП. Методика оценки качества жизни больных с сердечно-сосудистъми заболеваниями. Кардиология. 2002; 5:92-5.
6. Rosenfeldt F, Hilton D, Pepe S, Krum H. Systematic review of effect of coenzyme Q10inphysical exercise, hypertension and heart failure. Biofactors 2003; 18 (1-4): 91-100.
7. Baggio E, Gandini R et al Italian multicenter study on the safety and efficacy of coenzyme Q10 as adjunctive therapy in heart failure. CoQ10 Drug Surveillance Investigators. Mol Aspects Med 1994; 15:287-94.
8. Morisco C, Trimarco B, Condorelli M. Effect of coenzyme Q10 therapy in patients with congestive heart failure: a long-term multicenter randomized study. Clin Investig 1993; 71 (8): 134-6.
9. Watts GF, Playford DA, Croft KD et al. Coenzyme Q10 improves endothelial dysfunction of the brachial artery in Type II diabetes mellitus. Diabetologia 2002; 45 (3): 420-6.
10. Singh RB, Niaz MA, Rastogi SS et al. Effect of hydrosoluble coenzyme Q10 on blood pressures and insulin resistance in hypertensive patients with coronary artery disease. J Hum Hyper-tens 1999; 13 (3): 203-8.
I1. Hadgson JM, Watts GF et al. Coenzyme Q10 improves blood pressure and glycaemic control: a controlled trial in subjects with type 2 diabetes. Eur Clin Nutr 2002; 56 (11): 1137-42.
12. Ланкин ВЗ, Тихазе АК, Беленков ЮН. Антиоксиданты в комплексной терапии атеросклероза: pro et contra. Кардиология. 2004; 2: 72-81.
13. Strey CH, YoungJM, Molyneux SL et al. Endothelium-amelio-rating effects of statin therapy and coenzyme Q10 reductions in chronic heart failure. Atherosclerosis 2005; 179 (1): 201-6.Epub 2004 Dec 29.
14. PKivKH, Thelen KM, Van Coster R et al. High-dose statins and skeletal muscle metabolism in humans: a randomized, controlled trial. Clin Pharmacol Ther 2005; 78 (1): 60-8. 15. Ikematsu H, Nakamura K, Harashima S et al Safety assessment of coenzyme Q10 (Kaneka Q10) in healthy subjects: a double-blind, randomized, placebo-controlled trial. Regul Toxicol Pharmacol 2006; 44 (3): 212 -8. Epub 2006.
