Терапевтический эффект и профилактика острых респираторных инфекций при использовании повторных курсов индукторов эндогенного интерферона у детей
СтатьиОпубликовано в журнале:
«Педиатрия», 2009, Том 88, № 6, с. 111-115
А.Л. Заплатников1, Е.И. Бурцева2, Л.М. Шамрай3, Т.Н. Носкова3, Е.С. Шевченко2
1 ГУ ДПО Российская медицинская академия последипломного образования, Москва, 2 ГУ НИИ вирусологии им. Д.И. Ивановского РАМН, Москва , 3 МУЗ ГДП № 4 г. Подольск
В открытом проспективном сравнительном исследовании показана лечебно-профилактическая эффективность и хорошая переносимость повторного курса Анаферона у 68 детей в возрасте 1–5 лет, посещающих детские дошкольные учреждения. Установлено, что профилактическое применение Анаферона в течение 3 месяцев позволяет существенно снизить заболеваемость острыми респираторными инфекциями (ОРИ), как при первичном – в 1,75 раза (р Ключевые слова: дети, индукторы интерферона, анаферон, острые респираторные инфекции .
Therapeutic and prophylactic efficacy and good safety of Anaferon repeated courses were proved in open prospective comparative study performed in 68 children aged 1–5 years from different kindergartens. The study showed that Anaferon usage during 3 months permitted to decrease rate of acute respiratory infections (ARI) in 1,75 times after initial course (pKey words: children, interferon inductors, Anaferon, acute respiratory infections.
Острые респираторные вирусные инфекции (ОРВИ) являются наиболее распространенной инфекционной патологией человека с максимальным уровнем заболеваемости в детском возрасте. Учитывая медицинское, экономическое и социальное значение ОРВИ и гриппа у детей, вопросам профилактики и лечения этих заболеваний уделяется особое внимание [1–4]. При этом подчеркивается, что снижение уровня заболеваемости острыми респираторными инфекциями (ОРИ) и гриппом можно добиться только при выполнении целого комплекса мероприятий, среди которых строгое соблюдение противоэпидемических мероприятий, рациональный режим дня, полноценная диета, санация очагов хронической инфекции, регулярные занятия физкультурой, закаливание, а также комбинация специфических и неспецифических методов иммунопрофилактики [1–3, 5]. При этом следует обратить внимание на тот факт, что в последние годы имеет место учащение случаев нерационального использования иммуномодуляторов (ИМ), как в профилактических, так и в лечебных целях. Так, по данным В.А. Иванова, частое, бесконтрольное и необоснованное применение ИМ отмечено у 31,8% детей с рекуррентными респираторными инфекциями (РРИ). Подчеркивается, что часто болеющие дети нередко получают сразу несколько иммуномодулирующих средств [5]. При этом в ряде случаев имеет место одновременное назначение препаратов с одинаковым механизмом действия либо их комбинация с ИМ других классов. Установлено также, что на практике нередко используют шаблонное назначение ИМ в виде схем, предусматривающих последовательное применение препаратов, характеризующихся аналогичной фармакодинамикой. Кроме этого отмечено, что зачастую детям, планово получающим неспецифические иммунопрофилактические препараты, в период развития очередного эпизода ОРИ дополнительно назначают ИМ. В то же время результаты проведенного нами ранее исследования свидетельствуют о возможности снижения полипрагмазии за счет адекватного использования одного и того же ИМ, но в различных режимах его дозирования [6]. Так, было установлено, что профилактическое назначение Анаферона способствовало предотвращению ОРИ (у 23,2% детей) или снижению заболеваемости ОРИ (у 49,5% детей). В случае же развития очередного эпизода ОРИ была показана клиническая эффективность трансформации режима дозирования препарата с превентивного на лечебный, что существенно снижало необходимость использования других противовирусных и иммуномодулирующих лекарственных средств [6]. В целом следует отметить, что клинико-иммунологическая эффективность и безопасность Анаферона при лечении и профилактике ОРИ у детей была доказана в работах целого ряда авторов [5–11]. Однако профилактическая эффективность повторных курсов Анаферона до настоящего времени остается предметом научных дискуссий, что и определило необходимость проведения данного клинического исследования.
В осенне-зимний период сезона 2008–2009 гг. (ноябрь 2008 – январь 2009) проведено открытое, проспективное, сравнительное исследование по изучению эффективности повторных курсов Анаферона, который использовали для профилактики и лечения ОРИ у детей, посещающих детские дошкольные учреждения (ДДУ). Протокол исследования полностью соответствовал принципам GCP (1994) и этическим нормам «Хельсинкской декларации» (WMA, 1964). В исследование, согласно дизайну, включали детей в возрасте от 1 года до 5 лет 11 месяцев, посещавших ДДУ не менее 5 дней в неделю и не получавших ИМ и/или противовирусные лекарственные средства в течение не менее 1 мес до начала наблюдения. Обязательным условием включения в исследования являлось наличие добровольного информированного согласия родителей. В случае нарушений протокола, а также при отказе от продолжения наблюдения пациенты исключались из исследования.
В исследование были включены 68 детей. При этом в основную группу вошли дети (n=17), которым Анаферон был назначен повторно – через 8 месяцев после окончания первичного курса (первичный 3-месячный курс препарата для профилактики ОРИ дети получали с декабря 2008 до марта 2009 гг.). 35 детей получали Анаферон впервые (группа сравнения). Группу контроля составили дети, которым ИМ назначены не были (n=16). Группы были сопоставимы по возрасту (средний возраст детей основной группы – 3,88±0,14 лет, группы сравнения – 3,31±0,14 лет, группы контроля – 3,44±0,24 лет), полу и состоянию здоровья. Все дети были из одного ДДУ.
Режим дозирования и способ применения Анаферона (регистрационный номер 000372/01 от 06.10.09) соответствовал официальным рекомендациям и назначался для профилактики ОРИ по 1 табл. 1 раз в день (5 раз в неделю) в течение 3 месяцев [12]. Согласно дизайну исследования при развитии ОРИ дети основной и сравнительной групп переводились на лечебный режим дозирования препарата, предусматривающего прием 8 табл. в течение первых суток (в первые 2 ч – по 1 табл. каждые 30 мин, а затем – по 1 табл. 3 раза через равные промежутки времени), а начиная со 2-го дня – по 1 табл. 3 раза в сутки в течение 5–7 дней [12]. После выздоровления дети вновь переводились на профилактический прием Анаферона. При развитии ОРВИ у детей из группы контроля ИМ не использовались, а объем симптоматической терапии определялся особенностями клинических проявлений заболевания и в целом не отличался во всех исследуемых группах. Оценку профилактической и лечебной эффективности Анаферона проводили на основании следующих показателей: частота ОРИ в течение периода наблюдения, средняя продолжительность эпизодов ОРИ, длительность лихорадочного периода, частота бактериальных осложнений и количество курсов антибиотиков. Особое внимание уделяли анализу переносимости препарата.
Лечебно-профилактическая эффективность повторного курса Анаферона у детей в возрасте 1–5 лет, посещающих ДДУ
У 43 из 68 детей, включенных в исследование, изучали также иммунологическую эффективность противогриппозной вакцинации, проводимую в соответствие с Национальным календарем прививок.
Состояние исходного иммунитета к актуальным для 2008-2009 гг. штаммам сезонных вирусов гриппа (А/Brisbane/59/2007(Н1N1), А/Brisbane/10/2007 (Н3N2), В/Florida/4/06) определяли на основании результатов серологического обследования в предэпидемический период. Иммунологическую эффективность вакцинации оценивали по формируемому среди привитых уровню серопротекции и по частоте сероконверсий к гемагглю-тининам (ГА) вакцинных штаммов вирусов гриппа в парных сыворотках (до- и через 1 мес после прививки). Специфические антитела к ГА (анти-ГА) в сыворотке крови определяли при стандартной постановке РТГА с 0,75% взвесью эритроцитов человека 0 (I) группы крови. Защитными считали титры анти-ГА 1:40 и выше. Изменение эпидемической ситуации по гриппу в связи с началом пандемии (2009 г.) потребовало внести в дизайн исследования дополнение, согласно которому изучали серологические кросс-реакции к пандемическому вирусу гриппа А/California/04/2009 (H1N1) у детей, привитых против сезонного гриппа. Для этого, используя стандартную методику РТГА, в сыворотке крови привитых детей с защитными титрами анти-ГА к вакцинному штамму вируса гриппа А/Brisbane/59/2007 (Н1N1) определяли специфические антитела к вирусу гриппа А/IIV-Moscow/01/2009 (H1N1)-swl, подобный А/California/04/ 2009 (H1N1) и А/California/07/2009 (H1N1).
Статистическую обработку полученных результатов исследования проводили на персональном компьютере с использованием программы БИОСТАТИСТИКА (ver. 3.03 McGraw-Hill, Inc., 1993). Полученные данные обрабатывали методом вариационной статистики путем вычисления средней арифметической величины (М), стандартной ошибки средней арифметической (m). Сравнение показателей в малочисленных группах проводили с использованием U-критерия Манна–Уитни, сравнение долей в группах с малой выборкой – точного критерия Фишера. Результаты считали статистически достоверными при рАнализ результатов проведенного исследования убедительно показал, что при повторном применении Анаферона у детей, посещающих ДДУ, удается предупреждать развитие ОРИ также эффективно, как и при первичном курсе профилактики (см. таблицу). При этом отмечено, что если в основной группе подавляющее большинство детей (70,6%) ни разу не заболели в течение периода наблюдения, то в группе контроля оставался здоровым только 1 из 4 детей (р
| Показатели | Основная группа (n=17) | Группа сравнения (n=35) | Группа контроля (n=16) |
| Удельный вес детей, ни разу не заболевших ОРИ (абс/ %) | 12 (70,6%) 1 | 9 (25,7%) 2 | 2 (12,5%) |
| Продолжительность ОРИ, дни | 9,0±0,7 1 | 9,2±1,8 2 | 14,6±1,18 |
| Число эпизодов ОРИ с лихорадкой (абс/ %) | 1 (20%) 1 | 10 (28,6%) 2 | 16 (87,5%) |
| Частота бактериальных осложнений и назначений антибиотиков (абс/ %) | 01 | 8 (22,8%) 2 | 7 (43,8%) |
Достоверность различия: 1при сравнении показателей у детей основной и контрольной групп, 2при сравнении показателей у детей группы сравнения и контрольной группы.
Особый интерес представлял анализ эффективности Анаферона в зависимости от возраста наблюдаемых детей. При этом были выделены 2 возрастные группы – 1–2 года и 3–5 лет. Учитывая, что повторный курс препарата получали только дети 3–5 лет жизни, группы сравнения (n=22) и контроля (n=9) также были сформированы по указанному возрастному принципу. Анализ полученных результатов показал высокую лечебно- профилактическую эффективность первичных и повторных курсов Анаферона у детей данной возрастной группы. Так, заболеваемость ОРИ в основной и сравнительной группах была существенно ниже, чем в группе контроля (29,4%, 81,8% и 211,1% соответственно, рРисунок. Профилактическая эффективность Анаферона у детей в возрасте 3-5 лет, посещающих ДДУ.
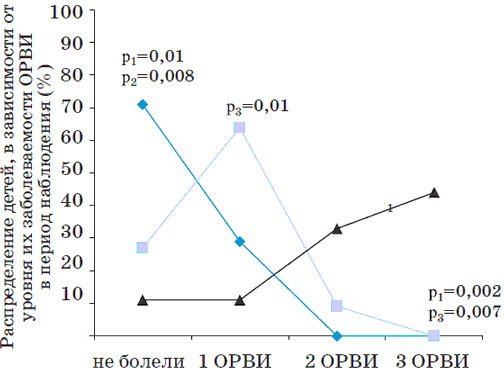
р1 - степень достоверности различий показателей основной группы и группы сравнения р2 - степень достоверности различий показателей основной группы и группы контроля р3 - степень достоверности различий показателей группы сравнения и группы контроля. ♦ - повторный курс Анаферона (n=22), ■ - первичный курс Анаферона (n=17), ▲ - контроль (n=9).
Учитывая, что среди наблюдаемых детей практически каждый 3-й ребенок, включенный в исследование, был в возрасте младше 3 лет (13 из них получали первый курс Анаферона, а 7 – были из группы контроля), отдельно анализировали эффективность Анаферона у данной категории пациентов. При этом установлено, что в целом дети, получавшие Анаферон, болели ОРИ в 1,54 раза реже по сравнению с контролем. Отмечена также отчетливо более низкая частота РРИ в основной группе. Так, среди детей, получавших Анаферон, практически каждый 4-й вообще не имел эпизодов ОРИ, а среди заболевших преобладали дети с 1 или 2 случаями заболевания, в то время как в контрольной группе только один ребенок из 7 оставался здоровым на протяжении всего периода наблюдения, а остальные дети (85,7%) имели 2 и более эпизодов ОРИ (рОтмечено, что благодаря профилактическому курсу Анаферона большая часть детей (82,3%), подлежащих иммунизации против гриппа, к моменту планируемой вакцинации были здоровы, что позволило их привить. Учитывая, что протокол исследования предусматривал также оценку эффективности гриппозной вакцинации, у 43 из 68 детей, включенных в исследование, был проведен серологический мониторинг, направленный на выявление специфических антител к вакцинным штаммам вируса гриппа до и после прививки. При этом обследование детей в предэпидемический период (ноябрь 2008 г.) показало низкие уровни исходной серопротекции к актуальным вирусам гриппа. Так, защитные титры анти-ГА были обнаружены у 25% детей к вирусу гриппа А/Brisbane/59/2007 (H1N1) и у 31,3% обследованных к вирусам гриппа А/Brisbane/10/2007 (H3N2) и В/Florida/4/2006. Через 1 месяц после введения одной дозы инактивированной вакцины 4-кратная сероконверсия к вирусу гриппа A (H1N1) была отмечена у 62,5% привитых, к вирусу гриппа А (Н3N2) у 18,7%, и к вирусу гриппа В - у 37,5% детей. При этом число детей с защитными титрами анти-ГА после иммунизации составило 68,7% к вирусу гриппа А (H1N1) и лишь 37,5% к вирусам гриппа А (Н3N2) и В. Следует особо отметить, что в апреле 2009 г., принимая во внимание изменение эпидемической ситуации по гриппу в связи с началом пандемии [13], дизайн исследования был дополнен изучением возможных перекрестных реакции антител к сезонному вирусу гриппа А/Brisbane/59/2007 (H1N1) и к пандемическому вирусу гриппа А/California/04/2009 (H1N1). Для этого в сыворотке крови привитых детей, у которых в результате прививки был сформирован протективный уровень антител к вакцинному штамму вируса гриппа А/Brisbane/59/2007 (Н1N1) (27 человек), определяли специфические анти-ГА к вирусу гриппа А/IIV-Moscow/01/2009 (H1N1)-swl, подобный А/California/04/2009 (H1N1) и А/California/07/2009 (H1N1). Анализ проведенного исследования показал отсутствие серологических кросс-реакций к пандемическому вирусу гриппа А/California/04/2009 (H1N1) у детей, адекватно ответивших на прививку против сезонного гриппа. Полученные данные полностью соответствуют результатам исследований других авторов и являются основанием к проведению дополнительной вакцинации против пандемического вируса гриппа у детей, иммунизированных против сезонного гриппа [4, 13–15].
Таким образом, результаты проведенного исследования показали, что повторный профилактический курс Анаферона у детей характеризуется высокой клинико-профилактической эффективностью, достоверно снижая заболеваемость ОРИ и благоприятно влияя на их течение. Особо следует отметить, что Анаферон хорошо переносился, побочных и нежелательных эффектов при его применении отмечено не было.
Выводы
1. Повторное применение 3-месячного профилактического курса Анаферона у детей характеризуется высокой клинико-профилактической эффективностью и хорошей переносимостью.
2. Использование Анаферона позволяет существенно снизить заболеваемость ОРИ у детей, посещающих ДДУ (при повторном курсе – в 5,9 раза (р3. Применение Анаферона сопровождается более благоприятным течением ОРИ – достоверно сокращается частота лихорадки, риск развития бактериальных осложнений и использование антибиотиков, а также продолжительность заболевания.
4. Вакцинация детей против сезонного гриппа не сопровождается формированием иммунитета к вирусу гриппа А/California/04/2009 (H1N1), что определяет необходимость проведения дополнительной иммунизации против пандемического (2009 г.) вируса гриппа А(H1N1).
ЛИТЕРАТУРА
1. Коровина Н.А., Заплатников А.Л. Острые респираторные вирусные инфекции в амбулаторной практике врача-педиатра. М.: Медпрактика, 2004.
2. Острые респираторные заболевания у детей: лечение и профилактика. Научно-практическая программа Союза педиатров России. М.: Международный Фонд охраны здоровья матери и ребенка, 2002.
3. Современные подходы к лечению и реабилитации часто болеющих детей: Пособие для врачей. Под ред Л.С. Балевой, Н.А. Коровиной, В.К. Таточенко. М.: Агентство Медицинского Маркетинга, 2006.
4. Policy Statement – Recommendations for the Prevention and Treatment of Influenza in Children 2009–2010. Pediatrics. 2009: 124 (4).
5. Иванов В.А. Состояние здоровья часто болеющих детей и дифференцированный выбор методов их оздоровления в условиях специализированного санатория. Автореф. дисс. канд. мед. наук. М., 2007.
6. Заплатников А.Л., Коровина Н.А. Бурцева Е.И. и др. Современные препараты, содержащие сверхмалые дозы действующего вещества, и традиционные гомеопатические средства в профилактике и лечении ОРВИ и гриппа у детей. Педиатрия, 2009; 1: 95–100.
7. Афанасьева О.И., Осидак Л.В., Головачева Е.Г. и др. Результаты изучения лечебной эффективности препарата «Анаферон детский» при гриппе у детей. Детские инфекции, 2003;2: 48–53.
8. Дондурей Е.А., Осидак Л.В., Головачева Е.Г. и др. Эффективность Анаферона детского при смешанных инфекциях у детей. Детские инфекции. 2006; 1: 55–60.
9. Перевощикова Н.К., Басманова Е.Д., Казанская Т.В. Анаферон детский в программе реабилитации детей, часто болеющих ОРВИ на фоне патологии лимфоглоточного кольца. Педиатрия, 2006; 6: 65–69.
10. Петров В.А., Бобров М.В. Применение Анаферона детского для лечения острых респираторных вирусных инфекций у детей в амбулаторно-поликлинических условиях. Медлайн экспресс, 2004; 11–12: 37–38.
11. Самсыгина Г.А., Казюкова Т.В., Дудина Т.А. и др. Новые технологии в профилактике острых респираторных инфекций и гриппа у детей младшего возраста. Педиатрия, 2008; 5: 102–107.
12. Государственный реестр лекарственных средств. М.: МЗиСР РФ (интернет-версия www/drugreg.ru, обновление 12.08. 2009).
13. WHO Weekly Epidemiological Record № 30, 24.7.2009.
14. Katz J. Serum cross-reactive antibody response to a novel influenza A (H1N1) virus after vaccination with seasonal influenza vaccine. MMWR 2009; 58: 521–524.
15. Surveillance for Pediatric Deaths Associated with 2009 Pandemik Influenza A (H1N1) Virus Infections – United State, April-August 2009. MMWR 2009; 58; 34.
