Некоторые аспекты эффективности и безопасности терапии острых респираторных заболеваний у детей
Статьи Опубликовано в журнале:педиатрия №2 | 2008 | приложение consilium medicum
О.В.Зайцева
Кафедра педиатрии МГМСУ, Москва
Острые респираторные заболевания (ОРЗ) являются самыми распространенными в детском возрасте, на их долю приходится до 90% всех регистрируемых заболеваний. Существует ошибочное мнение, что ОРЗ можно не лечить - болезнь "пройдет" самостоятельно. Респираторные инфекции без адекватного лечения часто принимают тяжелое, а порою и осложненное течение. ОРЗ могут вызвать обострение хронических заболеваний, таких как бронхиальная астма, гломерулонефрит, заболевания сердца и др. ОРЗ - полиэтиологичная группа заболеваний, имеющих сходную клиническую картину. У детей ОРЗ достаточно часто протекают с высокой лихорадкой, выраженным токсикозом, головной болью, мышечной ломотой. Легкий насморк у ребенка может закончиться тяжелой пневмонией, синуситом или отитом с выраженным болевым синдромом. Своевременная терапия ОРЗ способствует более быстрому выздоровлению и предупреждает развитие осложнений. Безусловно, лечение ОРЗ у детей должно быть не только эффективным, но и максимально безопасным. В особом внимании нуждаются дети раннего возраста.
Повышение температуры тела является наиболее частым и одним из самых важных симптомов заболеваний детского возраста. Лихорадочные состояния у детей -наиболее распространенный повод обращений к врачу, хотя нередко многие родители пытаются снизить повышенную температуру тела у детей самостоятельно, применяя жаропонижающие лекарственные средства (ЛС). Лечение безрецептурными препаратами, безусловно, также требует контроля, особенно с точки зрения безопасности терапии [8, 10]. Поэтому вопросы терапии лихорадочных состояний до настоящего времени являются актуальными проблемами педиатрии.
В ответ на воздействие патогенных раздражителей происходит перестройка температурного гомеостаза, направленная на повышение температуры тела с целью повышения естественной реактивности организма. Такое повышение температуры называют лихорадкой. Лихорадка рассматривается как защитно-приспособительная реакция организма, возникающая в ответ на воздействие патогенных раздражителей и характеризующаяся перестройкой процессов терморегуляции, приводящих к повышению температуры тела и стимулирующих естественную реактивность организма. Биологическое значение лихорадки заключается в повышении иммунологической защиты. Повышение температуры тела приводит к повышению фагоцитоза, увеличению синтеза интерферонов, активации и дифференцировке лимфоцитов и стимуляции антителогенеза. Повышенная температура тела препятствует размножению вирусов, кокков и других микроорганизмов. Однако защитно-приспособительный характер лихорадки сохраняется только при относительно небольшом повышении температуры. Гипертермия может стать одним из неблагоприятных патогенетических факторов течения болезни, а порою и причиной фатального исхода.
Особо следует отметить, что даже при одинаковом уровне гипертермии лихорадка у детей может протекать по-разному. Так, если теплоотдача соответствует теплопродукции, это свидетельствует об адекватном течении лихорадки и клинически проявляется относительно нормальным самочувствием ребенка, розовой или умеренно гиперемированной окраской кожи, влажной и теплой на ощупь ("розовая лихорадка"). Этот тип лихорадки часто не требует применения жаропонижающих средств.
В случае, когда при повышенной теплопродукции теплоотдача неадекватна из-за нарушения периферического кровообращения, течение лихорадки прогностически неблагоприятно. Клинически при этом отмечаются выраженный озноб, бледность кожных покровов, акроцианоз, холодные стопы и ладони ("бледная лихорадка"). Эти дети, как правило, нуждаются в назначении жаропонижающих препаратов в сочетании с сосудорасширяющими и антигистаминными средствами (или нейролептиками).
Одним из клинических вариантов неблагоприятного течения лихорадки является гипертермическое состояние, которое у детей раннего возраста в большинстве случаев обусловлено инфекционным воспалением и сопровождается выраженным токсикозом. При этом отмечается стойкое (6 ч и более) и значительное (выше 40,0°С) повышение температуры тела, сопровождающееся нарушением микроциркуляции, метаболическими расстройствами и прогрессивно нарастающей дисфункцией жизненно важных органов и систем [5, 8]. Развитие лихорадки на фоне острых микроциркуляторных обменных нарушений, лежащих в основе токсикоза, приводит к декомпенсации терморегуляции с резким нарастанием теплопродукции, неадекватно сниженной теплоотдачей. Все это связано с высоким риском развития метаболических нарушений и отека мозга и требует срочного применения комплексной неотложной терапии.
В соответствии с рекомендациями ВОЗ "Лечение лихорадки при острых респираторных инфекциях у детей" (WHO, 1993) и отечественными рекомендациями жаропонижающие препараты следует назначать, когда температура у ребенка превышает 39,0°С (измеренная ректально) или 38,5°С (измеренная субаксиллярно). Исключение составляют дети с риском развития фебрильных судорог, дети с тяжелым заболеванием легочной или сердечно-сосудистой системы и дети первых 2 мес жизни.
При выборе анальгетиков-антипиретиков для детей особенно важно ориентироваться на высокоэффективные препараты с наименьшим риском возникновения побочных реакций. В настоящее время только ибупрофен и парацетамол полностью отвечают критериям высокой эффективности и безопасности и официально рекомендуются Всемирной организацией здравоохранения и национальными программами в педиатрической практике в качестве жаропонижающих средств.
Необходимо отметить, что неопиоидные анальгетики (анальгетики-антипиретики) до настоящего времени остаются одними из наиболее применяемых ЛС, в том числе и в педиатрии. Эта группа препаратов обладает уникальным сочетанием жаропонижающего, противовоспалительного, анальгезирующего, а также антитромботического механизмов действия, которые потенциально позволяют контролировать основные симптомы многих заболеваний. Одновременное присутствие такого спектра положительных эффектов не наблюдается ни у одной другой группы ЛС [1-3, 11]. Однако несмотря на некоторые общие свойства, препараты из группы анальгетиков-антипиретиков различаются как по эффективности, широте терапевтического спектра, так и по степени вероятности развития нежелательных реакций. В настоящее время наиважнейшим условием применения ЛС у детей является отсутствие значимых (серьезных) побочных реакций, доказанных проведенными крупномасштабными клиническими исследованиями.
Первое научное сообщение о жаропонижающем действии препарата, полученного из ивовой коры, было сделано в середине XVIII в. Позже было установлено, что активным началом этого препарата является салицин. Постепенно синтетические аналоги салицина (салицилат натрия и ацетилсалициловая кислота) полностью заменили в терапевтической практике природные соединения. В дальнейшем изучение роли биологически активных эндогенных соединений в развитии воспаления, начатое в 1930-х годах, привело к созданию нескольких фармакологических групп неопиоидных анальгетиков, которые подразделяют на нестероидные противовоспалительные препараты (НПВП) и "простые анальгетики" (парацетамол). Парацетамол не входит в группу НПВП, поскольку практически не обладает противовоспалительным действием [4].
Основной механизм действия анальгетиков-антипиретиков, определяющий их эффективность, - подавление активности циклооксигеназы (ЦОГ) - фермента, регулирующего превращение арахидоновой кислоты в простагландины (ПГ), простациклин и тромбоксан. Установлено, что существует два изофермента ЦОГ. Так, ЦОГ-1 направляет процессы метаболизма арахидоновой кислоты на осуществление физиологических функций: образование ПГ, оказывающих цитопротективное действие на слизистую оболочку желудка, на регуляцию функции тромбоцитов, микроциркуляторного кровотока и др. ЦОГ-2 образуется только при воспалительных процессах под влиянием цитокинов. При воспалении метаболизм арахидоновой кислоты значительно активизируется, повышается синтез ПГ, лейкотриенов, высвобождение биогенных аминов, свободных радикалов, NO и др., что обусловливает развитие ранней стадии воспаления. Блокада анальгетиками-антипиретиками ЦОГ в центральной нервной системе (ЦНС) приводит к жаропонижающему и аналгезирующему эффекту (центральное действие ЛС), а снижение содержания ПГ в месте воспаления - к противовоспалительному действию и за счет уменьшения болевой рецепции к обезболивающему (периферическое действие ЛС) [2, 3, 5].
Анальгетическая, противовоспалительная и жаропонижающая активность неопиоидных анальгетиков доказана в многочисленных контролируемых испытаниях, соответствующих стандартам доказательной медицины (уровень А) [9]. В мире ежегодно НПВП потребляют более 300 млн человек. Их широко применяют при лихорадочных состояниях, острых и хронических болях, ревматических заболеваниях и многих других. Большинство пациентов используют безрецептурные лекарственные формы.
Несмотря на высокую эффективность анальгетиков-антипиретиков, использование их у детей не всегда безопасно. Так в 1970-е годы появились убедительные данные, свидетельствующие о том, что применение ацетилсалициловой кислоты (аспирин) при вирусных инфекциях у детей может сопровождаться синдромом Рея (Reye), характеризующимся токсической энцефалопатией и жировой дегенерацией внутренних органов, преимущественно печени и головного мозга. Ограничения, введенные в США на применение ацетилсалициловой кислоты у детей, привели к значительному снижению синдрома Рея с 555 в 1980 г. до 36 в 1987 и 2 - в 1997 г. [27]. Кроме того, ацетилсалициловая кислота повышает риск развития воспалительных изменений со стороны желудочно-кишечного тракта (ЖКТ), нарушает свертываемость крови, повышает ломкость сосудов, у новорожденных может вытеснять билирубин из его связи с альбуминами и тем самым способствовать развитию билирубиновой энцефалопатии. Эксперты ВОЗ не рекомендуют применение ацетилсалициловой кислоты как жаропонижающего средства у детей до 12 лет, что нашло отражение в национальном Формуляре (2000 г.) [11, 24]. Приказом Фармкомитета РФ от 25.03.1999 назначение ацетилсалициловой кислоты при острых вирусных инфекциях разрешено с 15-летнего возраста. Вместе с тем под строгим контролем врача ацетилсалициловая кислота может применяться при ревматических заболеваниях.
Одновременно накапливались данные о побочных эффектах и других антипиретиков. Так, амидопирин из-за своей высокой токсичности был исключен из номенклатуры лекарственных препаратов [4]. Метамизол может угнетать кроветворение вплоть до развития фатального агранулоцитоза, что способствовало резкому ограничению его использования во многих странах мира (International Agranulocytosis and Aplastic Anaemiа Study Group, 1986 г.). Однако в ургентных ситуациях, таких как гипертермический синдром, острые боли в послеоперационном периоде и др., не поддающихся иной терапии, допустимо парентеральное использование анальгина и метамизолсодержащих препаратов.
Предполагают, что угнетение ЦОГ-2 является одним из важных механизмов клинической эффективности анальгетиков, а ЦОГ-1 - их токсичности (прежде всего в отношении ЖКТ). В связи с этим, наряду со "стандартными" (неселективными) НПВП, которые в одинаковой степени подавляют активность обеих изоформ ЦОГ, были созданы селективные ингибиторы ЦОГ-2. Однако и эти препараты оказались не лишены побочных эффектов. Установлено, что селективный НПВП нимесулид обладает значительно более высокой частотой развития серьезных побочных эффектов при сравнении с ибупрофеном и парацетамолом в средних терапевтических дозах. Использование нимесулида для лечения лихорадочного и болевого синдромов в педиатрической практике недопустимо, так как риск развития возможных побочных реакций намного выше, чем у ибупрофена и парацетамола. В европейских странах (в том числе в Швейцарии, Италии, Франции, Португалии, Греции, Ирландии) нимесулид не разрешен для использования у детей моложе 12 лет. Применение нимесулида в России возможно по рекомендации врача (регламентируется рецептурный отпуск препарата) у детей старше 2 лет, но назначение целесообразно только при необходимости осуществления длительной противовоспалительной терапии, что обычно имеет место в ревматологии.
Обсуждая безопасность ЛС, необходимо помнить, что широкомасштабные исследования по эффективности и безопасности ЛС проводятся, как правило, с оригинальным препаратом, а не с его "копиями" ( генериками). Профиль безопасности оригинальных препаратов хорошо изучен и достаточно высокий, однако это не всегда относится к генерикам. Так, например, из всех препаратов ибупрофена у детей с 3-месячного возраста без рецепта можно использовать только Нурофен для детей, в то время как Ибуфен разрешен только у детей старше года.
Таким образом, при выборе анальгетиков-антипиретиков для детей необходимо ориентироваться на препараты с наименьшим риском возникновения побочных реакций. Только ибупрофен и парацетамол полностью отвечают критериям высокой эффективности и безопасности. Парацетамол и ибупрофен могут назначаться детям с первых месяцев жизни (с 3-месячного возраста -без рецепта). Рекомендованные разовые дозы: парацетамол - 15 мг/кг, ибупрофен - 7,5-10 мг/кг (в лекарственных формах, предназначенных для детей). Повторное использование антипиретиков возможно не ранее чем через 4-5 ч (Нурофен суспензия для детей действует до 8 ч), но не более 4 раз в сутки [4, 11, 24].
Следует отметить, что механизм действия ибупрофена и парацетамола различен. Парацетамол обладает выраженным жаропонижающим, но очень незначительным аналгезирующим и противовоспалительным действием, так как блокирует ЦОГ преимущественно в ЦНС и не обладает периферической активностью. Имеются качественные изменения метаболизма парацетамола в зависимости от возраста ребенка, которые связаны со зрелостью системы цитохрома Р-450. Кроме того, задержка выведения препарата и его метаболитов может отмечаться при нарушении функций печени и почек. Рекомендуемая суточная доза 50 мг/кг у детей является безопасной, но при ее увеличении может наблюдаться гепатотоксиче-ское действие препарата. Так, компанией "ГлаксоСмитКляйн Консьюмер Хелскер", строго контролирующей безопасность парацетамола, в течение 2003 г. зарегистрировано 106 случаев побочных эффектов парацетамола у взрослых (примерно 1 случай на 1 млн употреблявших препарат), из них серьезных - 34 (20%). У детей побочные эффекты было зарегистрированы в 107 случаях (примерно 1 случай на 127,1 тыс. получивших препарат детей), из них серьезных - 8 (7%). Побочные эффекты чаще всего обусловлены неправильным дозированием препарата или передозировкой (иногда преднамеренной) и связаны с поражением печени. Риск серьезных осложнений может значительно повыситься лишь при 10-кратной передозировке парацетамола. Описан случай фульминантной печеночной недостаточности с гипогликемией, коагулопатией при хроническом превышении родителями дозы парацетамола (150 мг/кг) в течение нескольких дней [17]. При наличии у ребенка недостаточности глюкозо-6-фосфатдегидрогеназы и редуктазы глутатиона парацетамол может вызвать гемолиз эритроцитов, лекарственную гемолитическую анемию. Однако терапевтические дозы парацетамола, как правило, безопасны, что позволяет широко использовать его в педиатрической практике в качестве жаропонижающего средства.
Ибупрофен - НПВП, обладающий выраженным жаропонижающим, аналгезирующим и противовоспалительным действием. Ибупрофен синтезирован в конце 50-х годов группой ученых под руководством д-ра Стюарта Адамса. Создание препарата было результатом упорного поиска ЛС для лечения хронических воспалительных заболеваний, которое обладало бы, помимо выраженных терапевтических эффектов, низким риском желудочно-кишечной токсичности. Впервые ибупрофен стал использоваться в 1969 г. как средство для лечения ревматоидного артрита. В дальнейшем акцент в его применении сместился на терапию лихорадки и острой боли. Хорошая переносимость, предсказуемость побочных эффектов, низкий риск развития серьезных осложнений при возможных передозировках в сочетании с выраженным противовоспалительным, анальгетическим и жаропонижающим эффектом явились причиной его широкого распространения в педиатрической практике.
Ибупрофен блокирует ЦОГ как в ЦНС, так и в очаге воспаления (периферический механизм), что и обусловливает его не только антипиретический, но и противовоспалительный эффект. В результате уменьшается фагоцитарная продукция медиаторов острой фазы, в том числе и ИЛ-1 (эндогенного пирогена). Снижение концентрации ИЛ-1 также способствует нормализации температуры тела. Ибупрофен проявляет двойное болеутоляющее действие - периферическое и центральное. Болеутоляющее действие проявляется уже в дозе 5 мг/кг и существенно более выражено, чем у парацетамола. Это позволяет эффективно использовать ибупрофен при слабой и умеренной боли в горле, боли при тонзиллитах, острых средних отитах, зубной боли, боли при прорезывании зубов у младенцев, а также для купирования поствакцинальных реакций [6, 14, 15].
В большинстве исследований продемонстрировано, что ибупрофен так же эффективен при лихорадке, как и парацетамол [12, 18, 19]. В других исследованиях показано, что жаропонижающий эффект ибупрофена в дозе 7,5 мг/кг выше, чем у парацетамола в дозе 10 мг/кг и ацетилсалициловой кислоты (10 мг/кг) [13]. Это проявлялось большим снижением температуры через 4 ч и у большего числа детей. Такие же данные были получены в двойном слепом исследовании в параллельных группах при повторном приеме ибупрофена 7 и 10 мг/кг и парацетамола 10 мг/кг у детей от 5 мес до 13 лет [23]. Однако следует отметить, что в настоящее время внесено изменение рекомендуемой дозы парацетамола с 10-15 мг/кг до 15 мг/кг не более 4 раз в сутки с интервалом не менее 4 ч, что обоснованно, поскольку эта доза является более эффективной при сохранении профиля безопасности препарата.
В многочисленных мультицентровых исследованиях показано, что среди всех анальгетиков-антипиретиков ибупрофен и парацетамол являются наиболее безопасными препаратами; даже при длительном их использовании частота неблагоприятных явлений оказалась сопоставимой и составила приблизительно 8-9% [13, 14, 16, 18, 20]. Частота развития побочных эффектов, не связанных с поражением ЖКТ, при кратковременном использовании ибупрофена у детей до 2 лет не отличается от таковой для парацетамола.
Известно, что побочные эффекты при приеме НПВП отмечаются преимущественно со стороны ЖКТ (абдоминальные боли, диспепсический синдром, НПВП-гастропатия), реже - в виде аллергических реакций, склонности к кровотечениям, крайне редко отмечается нарушение функции почек. Ибупрофен признан наиболее безопасным представителем класса НПВП при дозировке у взрослых до 1200 мг/сут. Важно, что при передозировке ибупрофена риск развития необратимых повреждений внутренних органов (в том числе печени) незначителен. Передозировка характеризуется гастроинтестинальными симптомами, нарушениями со стороны ЦНС, уменьшением почечной выделительной функции, судорогами и эпизодами апноэ. Из накопленного опыта ясно, что в случаях острой передозировки токсические эффекты были выражены слабо и не требовали специфической терапии. Несмотря на то что концентрация ибупрофена в крови напрямую не коррелирует со степенью выраженности симптомов интоксикации, развитие симптомов острого отравления у детей происходит при применении ибупрофена в дозе превышающей 400 мг/кг, т.е. в 10 раз превышающий максимальную суточную дозу.
Ибупрофену посвящены многочисленные большие рандомизированные сравнительные клинические испытания, в которых не было выявлено серьезных побочных явлений, в частности со стороны почек и печени [19, 20]. N.Moore и соавт., проводившие крупномасштабное исследование PAIN с использованием средней суточной дозы ипуброфена 1,2 г у взрослых, выявили, что частота развития нежелательных явлений при применении ибупрофена сопоставима с таковой плацебо (2,4 и 2,1% соответственно). Вместе с тем авторы подчеркнули, что при увеличении дозы препарата для создания противовоспалительного эффекта общая частота неблагоприятных явлений увеличивалась до 22%, преимущественно со стороны ЖКТ, однако серьезные побочные эффекты практически отсутствовали [27].
Аспирин и НПВП могут провоцировать бронхоспазм у лиц с аспириновой непереносимостью, так как угнетают синтез ПГЕ2, простациклина и тромбоксанов и способствуют увеличению синтеза лейкотриенов. Парацетамол не оказывает влияния на синтез этих медиаторов аллергического воспаления, однако бронхоконстрикция возможна и при приеме парацетамола, что связывают с истощением системы глутатиона в респираторном тракте и снижением антиоксидантной защиты. В то же время в крупном международном исследовании показано, что при использовании ибупрофена и парацетамола у 1879 детей с бронхиальной астмой были госпитализированы только 18, из них сходное число получали парацетамол и ибупрофен (19), что и свидетельствует об относительной безопасности этих ЛС у детей с бронхиальной астмой. При бронхиолите у детей первых 6 мес жизни ибупрофен и парацетамол также не оказывали бронхоспастического действия. Непереносимость аспирина у детей встречается довольно редко, но в этих случаях применение НПВП противопоказано.
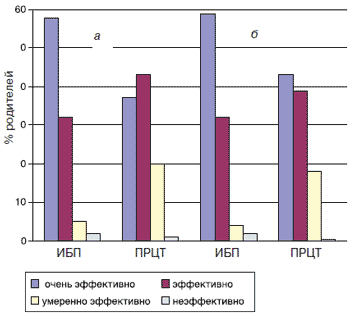
Таким образом, ибупрофен и парацетамол являются препаратами выбора в качестве жаропонижающих средств у детей, а ибупрофен также широко используется с противовоспалительной и анальгетической целью (при боли умеренной интенсивности). Очевидно, что педиатрам и родителям достаточно часто приходится решать вопрос, какой препарат предпочесть. В этой связи представляет интерес исследование DOVER, проведенное в Великобритании в 2006 г. DOVER - мультицентровое рандомизированное двойное слепое контролируемое сравнительное исследование по изучению эффективности и безопасности применения у детей базисных анальгетиков-антипиретиков - ибупрофена и парацетамола. В исследовании приняли участие 300 детей в возрасте от 3 мес до 12 лет с лихорадочными состояниями. Ибупрофен и парацетамол назначался в разовой дозе 10 мг и 15 мг/кг массы тела соответственно. Результаты данного исследования подтвердили эквивалентную жаропонижающую эффективность и высокую безопасность ибупрофена и парацетамола при применении их в указанных дозах (рис. 1). Однако родители детей оценили ибупрофен как более эффективный и предпочтительный для применения препарат, особенно при купировании болевых симптомов (рис. 2, 3). Авторы делают вывод, что ибупрофен является препаратом первого выбора у детей при коротком курсе терапии острой боли умеренной интенсивности, а также при сочетании лихорадки и боли. Допустимо применение и парацетамола (ацетаминофена), однако его обезболивающий эффект значительно ниже, даже при максимально высокой разовой дозе (15 мг/кг массы тела). Оптимальным в педиатрической практике является назначение оригинального препарата ибупрофена - Нурофен для детей [28].
Рис. 1. Эффективность ибупрофена и парацетамола.
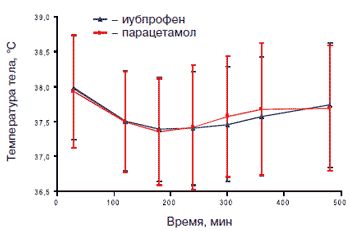
Рис. 2. Родители, которые предпочтут данный препарат при повторном назначении.
а - 1-я доза препарата (p≤0,05), б - конец клинического исследования (p≤0,01). ИБП - ибупрофен, ПРЦТ - парацетамол.
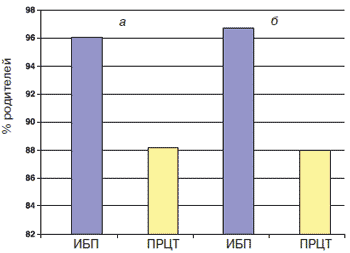
Рис. 3. Оценка эффективности препаратов родителями.
а - 1-я доза препарата (p≤0,05), б - конец клинического исследования (p≤0,01). ИБП - ибупрофен, ПРЦТ - парацетамол.
Ниже нами представлены некоторые особенности использования ибупрофена и парацетамола в практике педиатра широкого профиля (за исключением применения НПВП в детской ревматологии).
Аллергические заболевания у детей в настоящее время являются одними из самых распространенных, частота их постоянно увеличивается. Аллергия как премор-бидный фон у этой группы пациентов нередко определяет особенности течения состояний, протекающих с лихорадкой и, кроме того, повышает риск возникновения аллергических реакций на применяемые медикаменты.
Лихорадка у детей с аллергическими заболеваниями имеет свои особенности. Во-первых, у этих больных имеется склонность к выраженному и затяжному течению лихорадки, что обусловлено высоким уровнем интерлейкина-1 у пациентов с атопией и, следовательно, патологическим, "замкнутым" кругом его синтеза, особенно в острый период аллергической реакции. Во-вторых, дети, предрасположенные к атопии, имеют высокую вероятность развития лихорадки лекарственного генеза (так называемая аллергическая лихорадка). В-третьих, необходимо учитывать, что на фоне обострения аллергии может отмечаться повышение температуры неинфекционного характера. Назначение жаропонижающих препаратов (анальгетиков-антипиретиков) детям с аллергическими заболеваниями и реакциями требует строгого врачебного контроля. Целесообразно в комплексное лечение лихорадочных состояний детям с аллергическими заболеваниями, наряду с жаропонижающими, включать и антигистаминные препараты.
С проблемой терапии острой боли умеренной интенсивности врач-педиатр широкого профиля встречается достаточно часто. Боль у детей нередко сопровождает некоторые инфекционно-воспалительные заболевания (острый отит, ангину, фарингит, острые респираторные инфекции), возникает, наряду с лихорадкой, в раннем постпрививочном периоде. Боль беспокоит младенцев при прорезывании зубов, а детей более старшего возраста - после экстракции зуба. Болевой синдром, даже незначительной интенсивности, не только ухудшает самочувствие и настроение ребенка, но и замедляет репаративные процессы и как следствие выздоровление [1, 6, 15, 21]. Необходимо подчеркнуть главную роль этиотропного и патогенетического подхода в лечении заболеваний, сопровождающихся болью. Однако успешней результат терапии будет там, где наряду с патогенетическими методами лечения применяется адекватное обезболивание.
Механизм формирования боли достаточно сложен, но наиболее важную роль в нем играют вещества простагландинового и кининового ряда, которые являются прямыми нейрохимическими медиаторами боли. Уменьшение продукции медиаторов боли и/или снижение рецепторной чувствительности (например, за счет блокады болевых рецепторов) обусловливают анальгетические эффекты терапии. Кроме того, воспалительный отек, как правило, усиливает болевой синдром.
В практике педиатра общего профиля основными препаратами для купирования острой боли умеренной интенсивности являются неопиоидные анальгетики, в то время как опиоидные анальгетики остаются ведущей группой при лечении острой боли, обусловленной хирургическим вмешательством, тяжелой травмой. Блокада анальгетиками-антипиретиками ЦОГ в ЦНС приводит к аналгезирующему эффекту центрального генеза, а снижение содержания ПГ в месте воспаления - к противовоспалительному действию и, за счет уменьшения болевой рецепции, к обезболивающему периферическому действию [1, 3, 5].
Клинические исследования свидетельствуют о том, что ибупрофен и, в меньшей степени, парацетамол являются препаратами выбора при терапии острой боли умеренной интенсивности у детей [17, 22]. Своевременная и адекватная сопроводительная обезболивающая терапия приносит облегчение больному ребенку, улучшает его самочувствие и способствует более быстрому выздоровлению.
Профилактика и лечение поствакцинальных реакций у детей.
Поствакцинальные реакции - ожидаемые состояния, указанные в инструкциях по применению вакцин. Поствакцинальные реакции встречаются часто, их не следует путать с осложнениями вакцинации, развитие которых чаще всего непредсказуемо и отражает индивидуальную реакцию ребенка или нарушение техники вакцинации. Хорошо известной поствакцинальной реакцией у детей является гипертермия после иммунизации. Кроме того, на месте введения вакцины могут появляться гиперемия, припухлость, боль умеренной интенсивности в месте инъекции, что также иногда сопровождается повышением температуры, недомоганием и головной болью. Гипертермия и местные реакции после иммунизации рассматриваются как показание для назначения ибупрофена [25]. Так как поствакцинальные реакции предсказуемы, при проведении прививки АКДС уместно профилактически рекомендовать ребенку ибупрофен на 1-2 дня после вакцинации [10].
С целью изучения клинической эффективности ибупрофена у детей при некоторых инфекционно-воспалительных заболеваниях, сопровождающихся лихорадкой и/или болевым синдромом, нами проведено открытое неконтролируемое исследование, в котором мы применяли Нурофен для детей. Изучение клинического состояния включало оценку жаропонижающего и болеутоляющего действия, эффективность и длительность жаропонижающего и обезболивающего действия, продолжительность курса Нурофена, регистрацию нежелательных явлений.
Проведенное нами исследование показало, что Нурофен для детей (ибупрофен) оказывает выраженное и быстрое жаропонижающее, обезболивающее и противовосплительное действие у пациентов с острыми инфекционно-воспалительными заболеваниями дыхательных путей и ЛОР-органов. Применение препарата у наблюдаемых детей было эффективно и безопасно. Необходимо отметить, что Нурофен для детей обладает хорошими вкусовыми качествами и хорошо переносится детьми самого разного возраста. Побочных эффектов со стороны органов пищеварения, развития аллергических реакций, усиления или провокации бронхоспазма мы не отмечали. Ни у одного из пациентов прием Нурофена не был прекращен из-за развития нежелательных явлений. Наш опыт свидетельствует о том, что наряду с этиотропной и патогенетической терапией заболевания целесообразно проведение рациональной сопроводительной терапии. Своевременная и адекватная терапия анальгетиками-антипиретиками приносит облегчение больному ребенку, улучшает его самочувствие и способствует более быстрому выздоровлению.
Таким образом, ибупрофен и парацетамол являются одними из наиболее применяемых лекарственных средств в педиатрической практике. Это препараты выбора у детей в качестве жаропонижающих средств. Однако при наличии у ребенка боли умеренной интенсивности или сочетании лихорадки и болевого синдрома, а также при развитии поствакцинальных реакций предпочтение следует отдать ибупрофену. Оригинальный препарат Нурофен для детей может применяться у детей с 3-месячного возраста, а при необходимости назначения детям более раннего возраста - только под контролем врача. Однако при назначении любого анальгетика-антипиретика необходимо внимательно определять дозу, избегать использования комбинированных препаратов, содержащих более чем одно жаропонижающее средство. Недопустимо курсовое применение антипиретиков без уточнения причин лихорадки. Литература
1. Веин А.В., АвруцкийМ.Я. Боль и обезболивание. М.: Медицина, 1997.
2. ВетровВ.П., Длин В.В. и др. Рациональное применение антипиретиков у детей. Пособие для врачей. М., 2002.
3. Геппе Н.А., Зайцева О.В. Представления о механизмах лихорадки у детей и принципах жаропонижающей терапии. Рус. мед. журн. 2003; 11 (1): 31-7.
4. Государственный реестр лекарственных средств. М.: МЗ РФ, 2000.
5. Коровина Н.А., Заплатников А.Л. и др. Лихорадка у детей. Рациональный выбор жаропонижающих лекарственных средств. Руководство для врачей. М., 2000.
6. Лебедева Р.Н., Никода В.В. Фармакотерапия острой боли. М.: АИР-АРТ, 1998.
7. Лоурин М.И. Лихорадка у детей. Пер. с англ. М.: Медицина, 1985.
8. Острые респираторные заболевания у детей: лечение и профилактика. Научно-практическая программа М., 2002.
9. Рациональная фармакотерапия ревматических заболеваний. Руководство. Под ред. ВАНасонювойй, ЕЛ.Насонова. М., 2003.
10. Таточенко В.К Педиатру на каждый день. Справочник по лекарственной терапии. М., 2002.
11. Федеральное руководство для врачей по использованию лекарственных средств (формулярная система). Вып. 1. М.: ГЭО-ТАР-медицина, 2000.
12. Aksoylar S et al. Evaluation of sponging and antipyretic medication to reduce body temperature in febrile children. Acta Paediatrica Japon-ica 1997; 39:215-7.
13. Autret E et al. Evaluation of ibuprofen versus aspirin and paracetamol on efficacy and comfort in children with fever. Eur J Clin 1997; 51: 367-71.
14. Bertin L, Pons G et al. Randomized, double-blind, multicenler, controlled Trial of ibuprofen versus acetaminophen (paracetamol) and placebofor treatment of symptoms of tonsillitis and pharyngitis in children. J Pediatr 1991; 119 (5): 811-4.
15. Bosek V, MignerR. Year book of pain. 1995; 144-7.
16. Czaykowski D et al. Evaluation of the antipyretic efficacy of single dose ibuprofen suspension compared to acetaminophen elixir in febrile children. Ped Res 1994; 35 (4, Part 2): Abstr. 829
17. HenretigFM. Clinical safety of OTC analgesics. 1996. Special report: 68-74.
18. Kelley MT, Walson PD, Edge H et al. Pharmacokinetics and pharmacodynamics of ibuprofen isomers and acetaminophen in febrile children. Clin Pharmacol Ther 1992; 52: 181-9.
19. Lesko SM, Mitchell AA An assessment of the safety of pediatric ibuprofen: a practitioner-based randomized clinical trial. JAMA 1995; 273:929-33.
20. Lesko SM, Mitchell AA Renal function after short-term ibuprofen use in infants and children. Pediatrics 1997; 100: 954-7.
21. MacPherson RD. New directions in pain management. Drags Today 2002; 3 (2): 135-45.
22. McQuay Hj, Moore RA An evidence-based resource for pain relief. Oxford University Press, 1998.
23. Sidler J et al. A double-blind comparison of ibuprofen and paracetamol in juvenile pyrexia. Br J Clin Pract 1990; 44 (Suppl. 70): 22-5.
24. The management of fever in young children with acute respiratory infections in developing countries/WHO/ARl/93.90/, Geneva 1993.
25. Van der Walt JH, Roberton DM. Anaesthesia and recently vaccinated children. Paed Anaesth 1996; 6 (2): 135-41.
26. Center for Disease Control: National Reye syndrome Surveillance -United States. New England J Med 1999; 340: 1377.
27. Moore N et al. Исследование PAIN, Clin Drug Invest 1999;18 (2): 89-98.
28. Doder Stady "Ibuprofen versus paracetamol in pediatric fever-objective and subjective findings from a randomized, blinded study". UK Cur Med Res Opin 2007; 23 (9).
