Отсутствие симптомов отмены Вальдоксана (агомелатин) и развитие симптомов отмены пароксетина
СтатьиAbsence of discontinuation symptoms with agomelatine and occurrence of discontinuation symptoms with paroxetine: a randomized, double-blind, placebo-controlled discontinuation study
S.A. Montgomerya, S.H. Kennedyb, G.D. Burrowsc, M. Lejoyeuxd, I. Hindmarche
International Clinical Psychopharmacology 2004, 19:271-280
aImperial College University of London, London, UK,
bUniversity Health Network, Toronto, Canada,
cDepartment of Psychiatry, Austin и Repatriation Medical Centre, Victoria, Australia,
dCentre Hospitalier Universitaire Louis Mourier, Colombes, France,
eHPRU Medical Research Centre, University of Surrey, Guildford, UK.
Эффекты резкой отмены Вальдоксана (агомелатин), нового мелатонинергического/серотонинергического антидепрессанта, изучались в рамках двойного слепого плацебо-контролируемого исследования, в котором в качестве активного контроля использовался пароксетин. Через 12 недель двойной слепой терапии Вальдоксаном 25 мг/сут или пароксетином 20 мг/сут пациенты со стойкой ремиссией депрессии рандомизировались для 2-недельной двойной слепой терапии плацебо или продолжения приема предыдущего антидепрессанта. Симптомы отмены оценивали по завершении первой и второй недели после отмены с помощью списка связанных с отменой признаков и симптомов (Discontinuation Emergent Signs and Symptoms; DESS). Для 2-недельного периода отмены было рандомизировано 192 пациента в стойкой ремиссии. У пациентов с отменой Вальдоксана не обнаруживалось увеличения симптомов отмены в сравнении с пациентами, продолжавшими прием Вальдоксана. У пациентов, которые прекращали прием пароксетина и переходили на плацебо, отмечалось достоверно больше симптомов отмены по DESS на первой неделе после отмены в сравнении с пациентами, продолжившими прием пароксетина (соответствующие средние количества симптомов отмены составили 7,3±7,1 и 3,5±4,1; P < 0,001). На второй неделе достоверных различий между группами продолжавших прием антидепрессантов и группами с отменой не обнаруживалось. В отличие от пароксетина резкое прекращение приема Вальдоксана не сопровождается развитием симптомов отмены.
ВВЕДЕНИЕ
Сообщения о развитии симптомов отмены появились почти сразу после появления первого антидепрессанта. Первым препаратом с верифицированными антидепрессивными свойствами является имипрамин - работа Kuhn, опубликованная в 1957 г. А уже в 1958 г. Kristiansen и Andersen публикуют сообщение о развитии симптомов отмены у 15 из 85 пациентов после резкого или постепенного прекращения терапии имипрамином. В ряду симптомов отмены авторами указывается тошнота, рвота, головокружение, неусидчивость, эпизоды повышенного потоотделения и расстройства сна. Симптомы продолжались примерно 3 дня, в целом были легкими и не вызывали существенного дискомфорта (Andersen et al., 1959). Далее Kramer et al. (1961) сообщают о сходных проявлениях у 25 из 45 пациентов после прерывания терапии имипрамином: в течение 48 часов после отмены препарата пациенты страдали такими симптомами, как тошнота, рвота, головные боли, головокружение, острый ринит, озноб, слабость и костно-мышечные боли. Симптомы быстро купировались возобновлением приема имипрамина. Авторы указывают, что подобные симптомы отмены могут ошибочно интерпретироваться в качестве признаков рецидива депрессии.
В дальнейшем выяснилось, что подобные симптомы не являются специфичными для имипрамина, так как вскоре были обнаружены при отмене других трициклических антидепрессантов. Например Bialos et al. (1982) сообщают о сходных проблемах в случаях отмены амитриптилина: симптомы развивались непосредственно после прекращения приема препарата и продолжались в течение 2 недель. Этот феномен отмены дифференцируется от рецидива депрессии, который развивается позднее, примерно через 3-15 недель после прекращения терапии.
Сходные симптомы описывались и в отношении препаратов другого крупного фармакологического класса - бензодиазепинов. Такие явления, как инсомния, тошнота, утрата аппетита, ажитация, повышенное потоотделение, депрессия, обострение психоза и судорожные припадки, развивающиеся после резкой отмены хлордиазепоксида, впервые приводятся в работе Hollister et al. (1961), а затем указываются в большом числе публикаций, авторы которых наблюдали сходные симптомы после отмены других бензодиазепинов, включая диазепам, лоразепам, клобазам, нитразепам, оксазепам и флюразепам. В последующем данные этих исследований обощались в работах Hallstrom и Lader (1981), Lapierre (1981) и Barrows et al. (1990). Однако, как указывают в своей обзорной статье Noyes et al. (1987), необходимо соблюдать определенную осторожность при интерпретации этих данных в связи с существенными методологическими ограничениями исследований, которые были преимущественно открытыми и не предусматривали обеспечивающих надежность результатов методов, таких как двойная слепая терапия, рандомизация и плацебо-контроль.
Симптомы отмены не ограничиваются психотропными препаратами. Они развиваются, например, после остановки терапии гипотензивными средствами. Головная боль, сердцебиение, слабость, неусидчивость и расстройства сна могут развиваться вскоре после отмены терапии и редуцироваться при возобновлении приема препарата (O'Brien и MacKinnon, 1972; Geyskes et al., 1979; Reid et al., 1984).
Поэтому не вызывает удивления тот факт, что вскоре после внедрения в практику селективных ингибиторов обратного захвата серотонина (СИОЗС) появились сообщения о симптомах отмены, связанных с применением этих антидепрессантов. Опубликованные данные по симптомам отмены СИОЗС при большом депрессивном расстройстве стали предметом многостороннего анализа в работах целого ряда авторов (Lejoyeux et al., 1996; Therrien и Markowitz, 1997; Zajecka et al., 1997). Было показано, что симптомы отмены развиваются независимо от метода остановки терапии - быстрой или постепенной. Также имеются указания на определенные различия между препаратами класса СИОЗС по профилям симптомов отмены. Так, в исследовании, основанном на данных государственной системы фармакологической бдительности Великобритании, установлено, что симптомы отмены чаще развиваются при использовании пароксетина и флувоксамина в сравнении с флуоксетином (Price et al., 1996). Этих публикаций было достаточно, чтобы стимулировать внимание к проблеме и подтвердить необходимость проспективных исследований для более тщательного изучения феномена отмены.
В последующем было выполнено несколько клинических исследований, направленных на изучение симптомов отмены СИОЗС. Rosenbaum et al. (1998) изучали симптомы отмены в группе из 231 пациента в течение 5-8 дней после прекращения терапии флуоксетином 20-60 мг/сут, сертралином 50-150 мг/сут или пароксетином 20-60 мг/сут. Для измерений симптомов отмены использовалась шкала связанных с отменой признаков и симптомов (DESS; Discontinuation Emergent Signs and Symptoms). Показано, что симптомы отмены чаще возникали после прекращения приема пароксетина в сравнении с сертралином или флуоксетином. Хотя авторы указывают, что на момент оценки пациенты находились в ремиссии, нельзя исключить, что в исследовании также участвовали пациенты с сохраняющейся умеренной депрессивной симптоматикой, так как в критериях включения указывается до 25 баллов по Шкале депрессии Монтгомери-Асберг (MADRS; Montgomery-Asberg Depression Rating Scale; Montgomery, Asberg, 1979) - показатель, соответствующий уровню депрессии умеренной степени тяжести.
Соответственно, сохраняется вероятность искажения результатов оценки симптомов отмены за счет обострения депрессивной симптоматики. Авторы последующих исследований с применением сходной методологии и оценкой тех же СИОЗС предпринимали попытки решения этой проблемы путем установления максимального порогового балла Шкалы депрессии Гамильтона (Hamilton Depression scale) на уровне 10 баллов (Michelson et al., 2000) или максимального балла шкалы MADRS на уровне 12 баллов (Hindmarch et al., 2000; Judge et al., 2002), хотя стойкой ремиссии для включения в выборку не требовалось. В обоих исследованиях также установлена более высокая частота симптомов отмены при терапии пароксетином.
Применение стандартных критериев, несомненно, улучшило методологию, однако ценность цитированных выше исследований ограничивается чрезмерно короткими сроками наблюдения, в среднем 5 дней. Этого интервала недостаточно для сравнения препарата с коротким периодом полувыведения, такого как пароксетин, с сертралином или флуоксетином, которые образуют активные метаболиты и характеризуются более длительными периодами полувыведения. Данные о том, что после остановки терапии сертралином или флуоксетином симптомы отмены возникают реже, чем после прекращения приема пароксетина, подтверждают мнение о зависимости риска развития симптомов отмены с периодом полувыведения препарата. Однако в результате большого исследования (n=87) Hindmarch et al. (2000) выявили сопоставимые уровни симптомов отмены для циталопрама и флуоксетина, несмотря на существенные различия в длительности периодов полувыведения этих двух СИОЗС. Соответственно, информация о длительности периода полувыведения лишь частично объясняет феномен симптомов отмены.
Ни в одном из приведенных исследований не предусматривалось сравнительного двойного слепого рандомизированного метода сравнения пациентов с отменой антидепрессанта и пациентов с продолжением терапии тем же препаратом. Такой подход позволил бы исключить эффект ожидания симптомов отмены, как у пациентов, так и исследователей. Очевидно, что для уточнения столь сложных аспектов феномена отмены терапии необходимы дополнительные исследования с тщательно проработанной методологией оценок.
В настоящем исследовании потенциальные симптомы отмены антидепрессантов изучались с применением двойного слепого плацебо-контролируемого метода оценки у пациентов в состоянии стойкой ремиссии. Столь тщательная методологии использовалась для изучения нового антидепрессанта Вальдоксана (агомелатин). Вальдоксан обладает уникальным фармакологическим профилем, так как является агонистом рецепторов мелатонина и антагонистом 5-НТ2с-рецепторов. Показано, что в рамках 8-недельной терапии большой депрессии Вальдоксан превосходит плацебо в дозе 25 мг/сут, но не обнаруживает достоверных отличий от плацебо при назначении в дозах 1 и 5 мг/сут. Несмотря на короткий период полувыведения - менее 2 часов, Вальдоксан обнаруживает высокий антидепрессивный эффект при однократном суточном приеме в вечернее время (Loo et al., 2002).
МЕТОДЫ
Дизайн исследования
Данное мультицентровое исследование проводилось в условиях общемедицинской сети во Франции, Великобритании, Австралии и Канаде. Симптомы отмены оценивались по завершении 1 и 2 недель после двойной слепой резкой отмены активной терапии Вальдоксаном или пароксетином, полной или с заменой на плацебо. В исследовании предусматривались две независимые пары параллельных групп - с отменой Вальдоксана и с заменой Вальдоксана на плацебо, а также с отменой пароксетина и с заменой пароксетина на плацебо. Пароксетин назначался в минимальной эффективной дозе, в связи с чем резкая отмена препарата представлялась оправданной.
Одобрение протокола Исследовательским этическим комитетом каждого из участвовавших в исследовании центров было получено до начала исследования. Данное исследование проводилось в соответствии с Рекомендациями для качественной клинической практики (Good Clinical Practice).
Пациенты
В исследование включались амбулаторные больные с депрессией в возрасте 1 8 лет и старше, соответствующие критериям большого депрессивного расстройства по DSM-IV (American Psychiatric Association, 1994), единичный или рекуррентный эпизод. Диагнозы большого депрессивного эпизода и всех коморбидных психических расстройств верифицировались с помощью Краткого международного нейропсихиатрического опросника (Mini International Neuropsychiatry Interview) - полуструктурированное интервью диагностики основных психических расстройств по критериям DSM-IV оси I (Sheehan et al., 1998). Пациенты с другими психическими расстройствами по Оси I или Оси II DSM-IV не могли участвовать в исследовании. Из исследования исключались пациенты с любыми сопутствующими тяжелыми и/или нестабильными общемедицинскими заболеваниями, которые могли бы повлиять на проведение исследования.
С целью создания однородной выборки для включения пациента в исследование требовалось минимум 18 и максимум 27 баллов по шкале MADRS. В исследование отмены терапии включались пациенты, достигшие соответствия установленным критериям стойкой ремиссии по завершении 12 недель терапии исследования.
Процедура
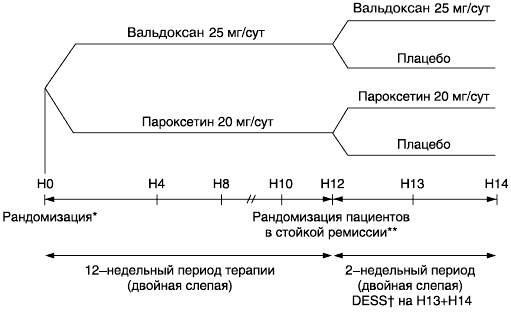
По истечении 3-5-дневного вводного периода без терапии пациентам методом рандомизации назначалась 12-недельная двойная слепая терапия Вальдоксаном 25 мг/сут или пароксетином 20 мг/сут. Пациенты, достигшие соответствия критерию стойкой ремиссии - суммарный балл MADRS < 12 на 8, 10 и 12-й неделе, подвергались повторной двойной слепой рандомизации, которая проводилась отдельно в двух группах активной терапии, для продолжения активной терапии или для приема плацебо в течение 2 недель (рис. 1). Комплаентность оценивалась подсчетом таблеток на каждом визите.
*Балл MADRS от 18 до 27 включительно.
**Балл MADRS † Список связанных с отменой признаков и симптомов.
Дизайн исследования. *Балл Шкалы депрессии Монтгомери-Асберг (MADRS) от 18 до 27 включительно. **Балл MADRS < 12 на неделе 8, 10 и 12. † Список связанных с отменой признаков и симптомов (Discontinuation Emergent Signs and Symptoms; DESS).
Сопутствующая терапия
В течение 8 недель до и 2 недель отмены терапии не разрешалось никакой сопутствующей психотропной терапии, особенно назначения бензодиазепинов в качестве гипнотиков или анксиолитиков.
Оценки
В 12-недельном периоде терапии оценки проводились на старте и на 8, 10 и 12-й неделе. Для оценки депрессивных симптомов использовалась шкала MADRS, для измерения тяжести тревожных симптомов - Шкала тревоги Гамильтона (HAM-A; Hamilton Rating Scale for Anxiety; Hamilton, 1959). Для оценки общего улучшения состояния пациентов использовалась 7-балльная Шкала общего клинического впечатления (CGI-тяжесть заболевания; Guy, 1976).
В периоде отмены терапии потенциальные симптомы отмены оценивались через 1 и 2 недели после замены на плацебо с помощью шкалы DESS (Rosenbaum et al., 1998). Шкала DESS предназначена для заполнения клиницистом и предусматривает оценку 43 признаков и симптомов, связанных с отменой или прерыванием терапии антидепрессантами.
Симптомы, возникавшие или усиливавшиеся в течение 7 дней до оценки, квалифицировались как связанные с терапией. Симптомы регистрировались как новые, если они впервые развивались в периоде отмены, или как обострившиеся, если во время оценки они оказывались тяжелее, чем были до периода отмены. Главным показателем было суммарное количество симптомов DESS, зарегистрированных на первой и второй неделе после отмены антидепрессантов. С целью обеспечения однородности оценок все исследователи прошли предварительное обучение. Для контроля исследователи регистрировали все спонтанные нежелательные явления, которые сообщались пациентами на каждом визите, с последующей их категоризацией в соответствии с терминологией Медицинского словаря для административных действий (Medical Dictionary for Regulatory Activities; MedDRA 3.3). На 1-й и 2-й неделе после отмены терапии состояние пациентов также оценивали по шкалам MADRS, HAM-A и CGI. Критерием частичного рецидива служило повышение суммарного балла MADRS до > 18, в качестве критерия рецидива использовалось увеличение балла MADRS до > 22, а признаком «синдрома отдачи» считалось увеличение балла MADRS до стартового показателя или выше по отношению к баллу на момент начала купирующей терапии исследования (Montgomery et al., 1993).
Статистический анализ
В выборку периода отмены включались пациенты из общей выборки терапии, которые прошли рандомизацию и получили минимум одну дозу препарата исследования после рандомизации.
Различия в суммарных количествах симптомов DESS между пациентами с отменой Вальдоксана и пациентами, продолжавшими прием Вальдоксана, на 1-й и 2-й неделе отмены анализировались с применением двустороннего t-теста Стьюдента для независимых выборок. Для оценки чувствительности исследования тот же метод анализа использовался для сравнений групп с отменой и продолжением терапии пароксетином. Учитывая вероятность того, что показатели DESS могли не иметь нормального распределения в каждой группе, для анализа надежности проводился U-тест Манна-Уитни. При выявлении достоверных различий по суммарным баллам DESS при сравнении групп Вальдоксана или пароксетина с их группами плацебо проводился дополнительный анализ по каждому пункту DESS с применением точного теста Фишера. В связи с тем что этот анализ был дополнительным, никаких коррекций для множественных анализов не предусматривалось. Изменения в депрессивной и тревожной симптоматике по показателям шкал MADRS, HAM-A и CGI анализировались с применением двустороннего t-теста Стьюдента для независимых выборок. Все эти анализы считались дополнительными. Для проведения статистических анализов использовался пакет программного обеспечения SAS версии 8.1 (SAS Institute Inc., Cary, NC, USA). Достоверность для общих статистических тестов устанавливалась на уровне 0,05.
РЕЗУЛЬТАТЫ
Демографические показатели
Выборка 12-недельной терапии
В фазу 12-недельной терапии исследования было включено 335 пациентов: 167 получали Вальдоксан 25 мг/сут и 168 - пароксетин 20 мг/сут. Различий в демографических показателях между группами не обнаружено. В 12-недельном периоде терапии, предшествовавшем рандомизированной отмене терапии исследования, зафиксирован высокий уровень комплаентности (по результатам подсчета таблеток) в обеих группах: Вальдоксан - 97%, пароксетин - 98%.
Выборка периода отмены
Рандомизацию для отмены терапии исследования прошли 192 пациента (88 на Вальдоксане и 104 на пароксетине), достигшие стойкой ремиссии. Из них 27 пациентов были переведены с Вальдоксана на плацебо, 61 пациент продолжил прием Вальдоксана; 43 пациента были переведены с пароксетина на плацебо и 61 пациент продолжил прием пароксетина. На момент начала периода отмены терапии исследования группы не обнаруживали достоверных различий ни по демографическим показателям, ни по средним баллам шкал MADRS, HAM-A и CGI (табл. 1). Одному пациенту после замены пароксетина на плацебо был назначен зопиклон и альпразолам в связи с тревогой, развившейся вследствие отмены пароксетина, однако данные этого пациента использовались в анализе. В периоде отмены комплаентность оставалась высокой во всех терапевтических группах (не менее 93,5%). Число пациентов в группах оставалось стабильным. Лишь один пациент (в группе продолжения приема Вальдоксана) был преждевременно исключен из исследования в периоде отмены; причина - редукция депрессивного расстройства.
Таблица 1. Демографические показатели и показатели тяжести в выборке повторной рандомизации для отмены терапии исследования
| Вальдоксан (n=88) | Пароксетин (n=104) | |
| Мужчины/женщины (%) | 30/70 | 35/65 |
| Возраст (среднее±SD) (годы) | 42,6±14,1 | 42,5±12,7 |
| Длительность текущего большого депрессивного эпизода (месяцы) | 7,2±13,1 | 5,9±6,9 |
| Число депрессивных эпизодов (включая текущий) | 2,5±1,9 | 2,4±1,4 |
| DSM-IV единичный эпизод | 35% | 36% |
| DSM-IV рекуррентный эпизод | 65% | 64% |
| DSM-IV меланхолический тип | 68% | 71% |
| Стартовый балл MADRS (среднее±SD) | 22,6±2,4 | 22,9±2,2 |
| Стартовый балл HAM-A (среднее±SD) | 19,6±7,6 | 19,9±6,9 |
| Стартовый балл CGI-тяжесть (среднее±SD) | 4,1±0,8 | 4,2±0,8 |
| Балл MADRS перед отменой (среднее±SD) | 6,±3,5 | 5,2±3,2 |
| Балл HAM-A перед отменой (среднее±SD) | 6,3±4,9 | 5,5±4,1 |
| Балл CGI-тяжесть перед отменой (среднее±SD) | 1,6±0,8 | 1,6±0,7 |
Результаты оценки по DESS через 1 неделю после отмены терапии
Через 1 неделю после отмены терапии не обнаружено статистически достоверных различий по количеству симптомов отмены между пациентами, прервавшими терапию Вальдоксаном и пациентами, продолжившими прием Вальдоксана (3,0±4,2 и 4,4±5,7 соответственно; P = 0,250) (рис. 2a). В то же время в группе пациентов с завершением терапии пароксетином выявлено достоверно больше симптомов, чем у пациентов, продолжавших прием пароксетина (7,3±7,1 и 3,5±4,1 соответственно; P < 0,001) (рис. 2б). Результаты сравнений подтверждены с помощью U-теста Манна-Уитни. В ходе дополнительного анализа отдельных пунктов выделено 8 симптомов, которые чаще встречались после отмены пароксетина в сравнении с пациентами, продолжившими терапию пароксетином. К этим симптомам относится инсомния, яркие сновидения, мышечные боли, головокружение, ринит, озноб, тошнота и диарея (P < 0,05) (рис. 3). Также установлены различия на уровне статистической тенденции (Р < 0,1) по нескольким другим симптомам, включая плаксивость, изменения сознания, забывчивость, одышку, рвоту, спазмы в желудке и неустойчивость походки, не достигавшим уровня статистической достоверности.
Результаты оценки по DESS через 2 недели после отмены терапии
Через 2 недели после отмены терапии не выявлено статистически достоверных различий между группой пациентов, переведенных с Вальдоксана на плацебо, и группой пациентов, продолжавших прием Вальдоксана (2,0±2,3 и 3,0±4,4 соответственно; P = 0,312), а также между пациентами, прервавшими прием пароксетина, и пациентами, продолжавшими терапию пароксетином (3,0±3,9 и 2,8±3,5 соответственно; P = 0,746). У пациентов с симптомами отмены на первой неделе после прекращения приема пароксетина на второй неделе обнаруживалось увеличение числа симптомов, которые оставались без изменений или ухудшались на второй неделе после отмены, в сравнении с пациентами, которые продолжали терапию пароксетином (среднее число симптомов: отмена пароксетина - 6,5 ± 6,1; продолжение приема пароксетина - 3,3±3,2; P = 0,004).
Рецидив и частичный рецидив
Все пациенты, соответствовавшие критерию рецидива (MADRS > 22), также соответствовали критерию отдачи симптомов - увеличение тяжести симптомов до уровня, зафиксированного перед началом купирующей терапии. Следовательно, результаты оценки рецидива и эффекта отдачи совпадают.
Рецидивы отмечались только у 2 из 70 (2,9%) пациентов в группах отмены терапии (оба из группы пароксетина) и у 5 из 1 22 (4,1 %) пациентов, продолживших прием активных препаратов (2 в группе Вальдоксана и 3 в группе пароксетина) (табл. 2).
В группах отмены терапии зафиксировано 4 случая частичного рецидива (балл MADRS > 18): 3 на первой неделе отмены пароксетина и 1 на первой неделе отмены Вальдоксана. В группах пациентов, продолжавших прием антидепрессантов, также установлено 4 случая частичного рецидива: 2 на первой неделе в группе Вальдоксана и 2 на второй неделе в группе пароксетина (табл. 2). Среди частичных и развернутых рецидивов в совокупности за 2-недельный период выявляется 6 случаев из 70 (8,6%) среди пациентов с отменой антидепрессантов и 9 случаев из 122 (7,4%) среди пациентов, продолживших прием антидепрессантов. Почти во всех выявленных случаях развернутые и частичные рецидивы депрессивной симптоматики были кратковременными - у 7 из 9 пациентов они редуцировались до завершения 1-й недели оценки и лишь у 2 пациентов продолжались на 2-й неделе.
Показатели MADRS, HAMA и CGI
Изменения баллов MADRS и CGI-тяжесть были достоверно более выраженными в группе пароксетин/плацебо в сравнении с группой продолжения терапии пароксетином на первой неделе отмены (P = 0,01 и P < 0,001 соответственно), однако на второй неделе эти различия нивелировались (P = 0,522 и P < 0,731 соответственно) (табл. 3 и 4). Достоверно более выраженные изменения в баллах HAM-A выявлялись в группе отмены пароксетина в сравнении с группой продолжения терапии пароксетином, как на 1-й неделе (P < 0,001) (табл. 3), так и на второй неделе после отмены (P < 0,034) (табл. 4). В результате дополнительного анализа отдельных пунктов шкалы HAM-A установлено, что на второй неделе отмены баллы тяжести соматической тревоги оставались высокими (P = 0,01), тогда как показатели психической тревоги редуцировались (Р = 0,159) (табл. 4).
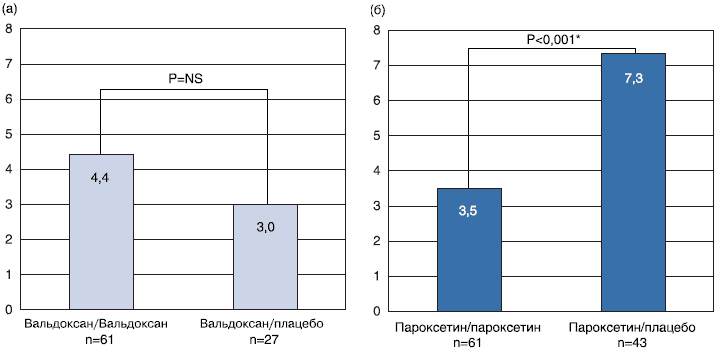
Среднее число связанных с отменой признаков и симптомов (DESS) после завершения 1-й недели отмены Вальдоксана или пароксетина: без достоверных различий между группами Вальдоксана и плацебо при достоверно большем числе симптомов в группе отмены пароксетина в сравнении с группой продолжения терапии пароксетином. Двусторонний t-тест Стьюдента (*P < 0,001).
В ходе анализа отдельных пунктов HAM-A на 1-й неделе отмены выявлены достоверно более высокие баллы показателей тревожного настроения, соматических мышечных, гастроинтестинальных, вегетативных симптомов и нарушений поведения (P < 0,05). Причем баллы тревожного настроения и соматических мышечных симптомов на 2-й неделе после отмены пароксетина (P < 0,05).
В показателях шкал MADRS, HAM-A и CGI не обнаружено достоверных различий между пациентами с отменой Вальдоксана и пациентами, продолжавшими прием Вальдоксана (табл. 3 и 4).
Нежелательные явления
Нежелательные явления в группах отмены терапии, которые оценивались исследователями как связанные с препаратами исследования, перечислены в табл. 5. За весь период отмены исследования не зафиксировано ни одного серьезного нежелательного явления.
ОБСУЖДЕНИЕ
Главным результатом проведенного исследования является подтверждение, что Вальдоксан не связан с симптомами отмены. Эти данные имеют очень большое значение, так как применение большинства антидепрессантов сопряжено с развитием симптомов отмены после прекращения их приема. Причем значимость результатов настоящего исследования еще более возрастает в связи с тем, что в этом исследовании, выполненном с тщательно проработанной методологией, доказана чувствительность использовавшихся методов оценки и показано развитие симптомов отмены после прекращения терапии пароксетином, что соответствует данным предыдущих исследований о повышенном уровне симптомов отмены при терапии пароксетином (Rosenbaum et al., 1998; Hindmarch et al., 2000; Michelson et al., 2000; Judge et al., 2002).
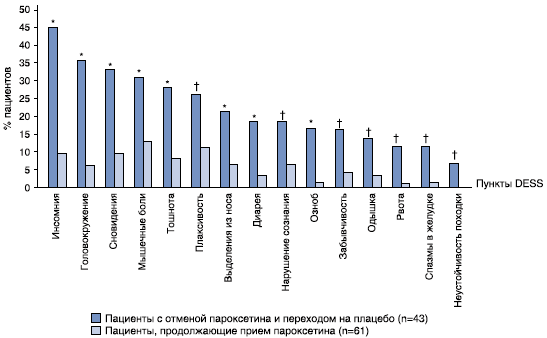
† P<0,1 Точный тест Фишера
*P<0,05 Точный тест Фишера
Список связанных с отменой признаков и симптомов. Более высокая частота новых симптомов или обострения предыдущих симптомов через 1 неделю после отмены терапии пароксетином - различия статистически достоверные или на уровне статистической тенденции. Точный тест Фишера.
Таблица 2. Число пациентов, достигших соответствия критериям рецидива или частичного рецидива, в группах Вальдоксана, пароксетина и соответствующих группах плацебо
| Вальдоксан/ Вальдоксан (n=61) |
Вальдоксан/ плацебо (n=27) |
Пароксетин/ пароксетин (n=61) |
Пароксетин/ плацебо (n=43) |
|
| Рецидив и отдача | ||||
| Первая неделя отмены | 1 | 0 | 1 | 1 |
| Вторая неделя отмены | 1 | 0 | 2+1a | 1 |
| Всего | 2 | 0 | 3 | 2 |
| Частичный рецидив | ||||
| Первая неделя отмены | 2 | 1 | 0 | 3 |
| Вторая неделя отмены | 0+1b | 0 | 2 | 0 |
| Всего | 2 | 1 | 2 | 3 |
bПациент с рецидивом на второй неделе отмены.
Таблица 3. Период отмены: изменения баллов MADRS, HAMA и CGI через 1 неделю после отмены терапии
| Вальдоксан/ Вальдоксан (n=61) |
Вальдоксан/ плацебо (n=27) |
Пароксетин/ пароксетин (n=61) |
Пароксетин/ плацебо (n=43) |
|
| Изменения в баллах MADRS | ||||
| Δ(W13-W12) | 1,6+4,8 P=0,677 |
1,2±4,3 | 3,0±5,4 P=0,01 |
0,6±3,8 |
| Изменения в суммарных баллах HAM-A | ||||
| Δ(W13-W12) | 1,1±3,4 P=0,842 |
1,3±4,8 | 4,0±6,0 P<0,001 |
0,5±4,2 |
| Изменения в баллах психической тревоги HAM-A | ||||
| Δ(W13-W12) | 1,4±2,6 P=0,372 |
0,8±2,8 | 1,8±3,4 P=0,016 |
0,3±2,5 |
| Изменения в баллах соматической тревоги HAM-A | ||||
| Δ(W13-W12) | -0,3±2,0 P=0,189 |
0,5±2,7 | 2,2±3,2 P<0,001 |
0,1±2,2 |
| Изменения в баллах CGI-тяжесть заболевания | ||||
| Δ(W13-W12) | 0,4+0,9 P=0,485 |
0,2+0,8 | 0,6±0,9 P<0,001 |
0,0±0,7 |
Многие из предыдущих сообщений о симптомах отмены были основаны на данных открытых исследований, в которых результаты оценки искажались под влиянием фактора непреднамеренного ожидания со стороны исследователей, и не подтвердились данными последующих плацебо-контролируемых исследований. Для редукции искажений, связанных с фаторами пациента и исследователя, в настоящем исследовании был использован метод рандомизированной двойной слепой и плацебо-заместительной отмены терапии. Перед включением в период отмены пациенты получали 1 2-недельную терапию Вальдоксаном 25 мг/сут или пароксетином 20 мг/сут. Далее в соответствии с двойным слепым методом, предусмотренным протоколом исследования, проводилась повторная рандомизация для замены на плацебо или продолжения приема антидепрессанта. Вероятность развития симптомов отмены при терапии Вальдоксаном подвергалась тщательному изучению с использованием повторной рандомизации и двойного слепого плацебо-контролируемого метода. В результате получены достоверные доказательства того, что в течение 2 недель после прекращения приема Вальдоксана никаких симптомов отмены не развивается. Хотя ранее сходные результаты были получены для флуоксетина, препарата с длительным периодом полувыведения, установленный для флуоксетина низкий уровень симптомов отмены объясняется медленным выведением активного метаболита - норфлуоксетина, плазменные концентрации которого снижаются наполовину только через 2 недели после прекращения приема флуоксетина (Rosenbaum et al., 1998). Сообщается о развитии симптомов отмены через 4-6 недель после прекращения приема флуоксетина (Zajecka et at, 1998), что соответствует показателям периода полувыведения этого антидепрессанта. Иными словами, наблюдается задержка развития симптомов отмены, которые скорее проявляются в частично редуцированной форме, чем предотвращаются полностью. В периоде задержки симптомов сохраняются клинически эффективные плазменные концентрации флуоксетина, в связи с чем сохраняется и риск серьезных неблагоприятных лекарственных взаимодействий. Например, после сообщений о летальных случаях при назначении ингибиторов моноаминоксидазы (ИМАО) в течение этого длительного периода «отмены» (Keltner, 1994), инструкция по применению флуоксетина была дополнена требованием 5-недельного периода отмывки между остановкой терапии флуоксетином и назначением ИМАО.
В соответствии с процедурой рандомизации, которая проводилась независимым агентством, предусматривались меньшие шансы замены Вальдоксана на плацебо в сравнении с шансами продолжения терапии Вальдоксаном. Однако представляется маловероятным, что указанный дисбаланс при рандомизации мог повлиять на результаты оценок. Ни добавление пациентов для равенства размеров групп, ни увеличение общего количества наблюдений не привело бы к появлению статистически достоверных различий между группами отмены и продолжения терапии.
Таблица 4. Период отмены: изменения баллов MADRS, HAMA и CGI через 2 недели после отмены терапии
| Вальдоксан/ Вальдоксан (n=61) |
Вальдоксан/ плацебо (n=27) |
Пароксетин/ пароксетин (n=61) |
Пароксетин/ плацебо (n=43) |
|
| Изменения в баллах MADRS | ||||
| Δ(W14-W12) | -0,4±4,0 P=0,162 |
1,2±5,0 | 2,2±5,0 P=0,522 |
1,6±5,2 |
| Изменения в суммарных баллах HAM-A | ||||
| Δ(W14-W12) | -0,1±3,2 P=0,425 |
0,7±4,7 | 3,2±5,9 P=0,034 |
0,9±4,9 |
| Изменения в баллах психической тревоги HAM-A | ||||
| Δ(W14-W12) | 0,3±2,5 P=0,537 |
0,7±2,9 | 1,6±3,4 P=0,159 |
0,7±3,1 |
| Изменения в баллах соматической тревоги HAM-A | ||||
| Δ(W14-W12) | -0,8±1,7 P= 0,467 |
-0,1±2,6 | 1,7±3,1 P= 0,010 |
0,3±2,3 |
| Δ(W14-W12) | 0,0±0,7 P=0,337 |
0,2±0,9 | 0,3±0,8 P=0,731 |
0,3±0,8 |
Таблица 5. Число и типы связанных с терапией нежелательных явлений в течение 2-недельного периода отмены в соответствии с терминологией словаря MedDRA
| Пациенты с отменой Вальдоксана (n=27) |
Пациенты с отменой пароксетина (n=43) |
|
| Легкие | Диспепсия (n=1) | Диарея (n=1) Гриппоподобные симптомы (n=1) |
| Умеренные | Нет | Рвота (n=1) Абдоминальная боль (n=1) Синдром отмены препарата (n=1) Повышенное потоотделение (n=1) Лабиринтит (n=1) |
| Тяжелые | Нет | Нет |
Клинические характеристики и сроки развития симптомов отмены пароксетина, установленные в настоящем исследовании, в целом совпадают с данными предыдущих исследований пароксетина. Значимые симптомы отмены, встречавшиеся у 10% или более пациентов на 1-й неделе отмены, включали инсомнию, головокружение, яркие сновидения, мышечные боли, тошноту, ринит, диарею и озноб. В целом идентичные сочетания симптомов выявлены в предыдущих исследованиях, за исключением выраженных депрессивных симптомов.
Методология настоящего исследования позволяла редуцировать потенциальные искажения в результатах, связанные с обострением депрессивных симптомов, вероятность которых высока при отмене терапии неадекватно леченного депрессивного эпизода. Показатели симптомов отмены были максимальными на 1-й неделе отмены и в последующем редуцировались - на 2-й неделе показатели приближались к уровню, предшествующему отмене терапии, не обнаруживая достоверных отличий от стартовых значений. В настоящем исследовании некоторые симптомы отмены, выявленные на 1 -й неделе, сохранялись и на 2-й неделе отмены. Однако это исследование не предусматривало оценки динамики симптомов отмены в сроки, превышающие 2 недели после прекращения терапии.
Длительность периода наблюдения потенциальных симптомов отмены является еще одним важным аспектом подобных исследований. В некоторых предыдущих двойных слепых исследованиях период наблюдения был слишком коротким для получения надежных результатов. Предполагается, что симптомы отмены связаны с периодом полувыведения препарата (Rosenbaum et al., 1998) и развиваются через 3-5 периодов полувыведения после остановки терапии (Montgomery и van Zwieten-Boot, 2002). В настоящем исследовании период наблюдения был рассчитан на основании периодов полувыведения оцениваемых антидепрессантов, что обеспечивало достаточную продолжительность оценок для выявления эффектов отмены. Период полувыведения пароксетина составляет 24 часа, Вальдоксана - 2 часа. Учитывая эти показатели, а также тот факт, что ни один из исследуемых антидепрессантов не образует активных метаболитов, можно прогнозировать, что симптомы отмены будут развиваться на 1-й неделе и редуцироваться на 2-й неделе после прекращения приема препаратов. Соответственно, 2-недельный период наблюдения считался достаточным для регистрации как ранних, так и отставленных симптомов отмены. Сопутствующая терапия, которая могла бы повлиять на результаты оценки симптомов отмены, была запрещена в данном исследовании.
Выбор инструмента для оценки потенциальных симптомов отмены также представляет собой определенную проблему. В настоящем исследовании для регистрации главных показателей использовался список симптомов DESS, который широко применяется в подобных исследованиях. Этот инструмент содержит длинный список симптомов, составленный на основании опубликованных данных по признакам и симптомам отмены антидепрессантов. DESS, как и все подобные списки симптомов, имеет важный недостаток - неточность оценок. Например, даже вне условий отмены терапии часто выявляется три или четыре из 43 перечисленных симптомов. Это вызывает сомнения в правомерности предложенного Rosenbaum et al. (1998) критерия синдрома отмены, предусматривающего минимум 4 симптома из списка DESS.
Оценка симптомов отмены антидепрессанта осложняется в связи с возможностью обострения депрессивной симптоматики. Если отмена терапии проводится у пациента с резидуальными симптомами депрессии - ситуация, сопряженная с высокой вероятностью обострения депрессии, возникают дополнительные затруднения в идентификации симптомов отмены. Наше исследование предусматривало оценку пациентов со стойкой ремиссией, соответствующих предопределенным критериям стойкой ремиссии - балл MADRS < 12 в интервале с 8 по 12 неделю терапии, так как пациенты в ремиссии характеризуются достоверно более низким риском возобновления депрессивной симптоматики (Montgomery et al., 1991). Такой подход позволяет эффективно дифференцировать рецидив симптомов депрессии от симптомов отмены. Депрессивные симптомы в нашем исследовании отмены были выражены в значительно меньшей степени, чем в других исследованиях, которые не предусматривали оценки пациентов в состоянии стойкой ремиссии.
Отмена пароксетина сопровождалась достоверным повышением показателей депрессивных симптомов по шкале MADRS на 1-й неделе, однако уже на 2-й неделе отмены достоверных различий между группами отмены и продолжения терапии пароксетином не выявлялось. Также установлено достоверное повышение баллов HAM-A на 1-й неделе отмены у пациентов, принимавших пароксетин, хотя на 2-й неделе достоверные различия были установлены только по показателям соматической тревоги. Эти данные позволяют предположить, что соматические симптомы более устойчивы и соответствуют результатам оценки по DESS. Достоверных различий между группами отмены и продолжения терапии Вальдоксаном не выявлено ни на первой, ни на второй неделе после отмены.
Значительная вариабельность симптомов депрессии требует двойных слепых сравнений по показателям отмены между пациентами с отменой терапии и пациентами, продолжавшими терапию тем же антидепрессантом. Во многих из предыдущих исследований не удавалось корректировать влияние естественной вариабельности депрессивной симптоматики на результаты оценки симптомов отмены применением адекватного контроля и квалификацией этих флюктуаций как признаков спровоцированного отменой рецидива депрессии. В нашем исследовании показано, что на 2-й неделе после отмены вероятность рецидива одинакова у пациентов с отменой пароксетина и пациентов, продолжавших прием пароксетина. В связи с этим представляется обоснованным предположить, что выявленные в нашем исследовании признаки обострения симптомов депрессии связаны, скорее, с естественными флюктуациями депрессивной симптоматики, чем с провоцированным отменой истинным рецидивом депрессии.
Мы не обнаружили никаких признаков повышения риска рецидива депрессии в связи с отменой Вальдоксана или пароксетина: отмена каждого из этих антидепрессантов у пациентов в стойкой ремиссии не провоцировала рецидива депрессии в течение 2 недель после прекращения терапии. Эти данные согласуются с результатами 2-недельной оценки вероятности рецидивов в других исследованиях, направленных на сравнительное изучение частоты рецидивов при отмене и продолжении терапии антидепрессантом у пациентов в стойкой ремиссии. В таких случаях значимые различия между антидепрессантами и плацебо появляются лишь через 1 месяц после отмены, а риск рецидива достигает максимального уровня через 2-3 месяца после отмены антидепрессанта. В нашем исследовании, напротив, симптомы развивались на 1-й неделе и редуцировались на 2-й неделе после отмены терапии.
Установленное в предыдущих исследованиях антидепрессантов повышение частоты рецидивов депрессии после отмены терапии (Rosehbaum et al., 1998; Hindmarch et al., 2000) также может быть связано с методологическими недостатками - в этих исследованиях не предусматривалось формирования выборок только из пациентов в стойкой ремиссии.
Симптомы отмены после резкого прекращения приема антидепрессантов вызывают значительный дискомфорт у пациентов и могут ошибочно интерпретироваться их врачами. В условиях клинической практики пациенты часто забывают принимать препараты или сознательно отказываются от их приема, в связи с чем проблема симптомов отмены имеет большое практическое значение. Предполагается, что отмена одних антидепрессантов чаще сопровождается развитием симптомов отмены, чем прекращение приема других антидепрессантов; например, сообщается, что пароксетин чаще вызывает симптомы отмены, чем флуоксетин (Rosenbaum et al., 1998; Hindmarch et al., 2000; Michelson et al., 2000; Judge et al., 2002). Антидепрессанты, не вызывающие или ограниченно вызывающие симптомы отмены, были бы крайне полезны для терапии пациентов, склонных к нерегулярному приему препаратов или характеризующихся повышенной чувствительностью к симптомам отмены других антидепрессантов. В нашем исследовании с применением тщательно проработанной методологии показано, что прекращение приема Вальдоксана не сопровождается развитием клинически значимых симптомов отмены. Отсутствие симптомов отмены при использовании Вальдоксана (агомелатин) является значительным клиническим преимуществом этого препарата в терапии депрессивных расстройств.
Список использованной литературы
